奥沙利铂一线治疗后再引入与雷替曲塞联合二线治疗晚期结直肠癌的临床观察*
2016-04-08赖林侯恩存陆运鑫陈柯帆朱文良莫苑君谭智威
赖林 侯恩存 陆运鑫 陈柯帆 朱文良 莫苑君 谭智威
奥沙利铂一线治疗后再引入与雷替曲塞联合二线治疗晚期结直肠癌的临床观察*
赖林侯恩存陆运鑫陈柯帆朱文良莫苑君谭智威
摘要目的:评估奥沙利铂一线用于治疗晚期结直肠癌后与雷替曲塞联合再引入二线治疗的疗效及安全性。方法:收集2010年5月至2014年12月广西中医药大学附属瑞康医院收治的48例晚期结直肠癌患者,根据一线应用奥沙利铂的情况分为两组:A组(一线使用不含奥沙利铂方案)20例;B组(一线使用含奥沙利铂方案)28例。二线治疗方案:雷替曲塞3 mg/m2,静脉滴注,d1;奥沙利铂100~130 mg/m2,静脉滴注,d1;每21天1次。结果:48例均可评价疗效,两组有效率分别为30.0%(6/20)、32.1%(9/28);疾病控制率分别为80.0%(16/20)、75.0%(21/28);中位无进展生存期分别为6.5个月、7.0个月;中位总生存期分别为10个月、13个月;两组有效率、疾病控制率、中位无进展生存期及中位总生存期比较差异均无统计学意义(P=0.264,0.514,0.713,0.788)。主要不良反应为骨髓抑制、转氨酶异常和胃肠道反应,以Ⅰ~Ⅱ级为主;两组感觉神经异常Ⅰ~Ⅱ级发生率相近。结论:奥沙利铂再引入联合雷替曲塞二线化疗对曾使用过奥沙利铂一线化疗的患者仍然有效,无耐药性,安全可行,对不能接受伊立替康二线治疗的晚期结直肠癌患者是较好选择。
关键词晚期结直肠癌奥沙利铂雷替曲塞回顾性分析
*本文课题受广西壮族自治区卫生和计划生育委员会自筹经费科研课题项目(编号:Z2015434)和广西中医药大学自然科学研究青年基金项目(编号:QN14011)资助
Clinical observation on oxaliplatin reintroduction combined with raltitrexed as secondline chemotherapy after the first-line oxaliplatin-based chemotherapy in advanced colorectal cancer patients
Lin LAI,Encun HOU,Yunxin LU,Kefan CHEN,Wenliang ZHU,Yuanjun MO,Zhiwei TAN
Correspondence to:Lin LAI;E-mail:1003671212@qq.com
The Second Department of Medical Oncology,Ruikang Hospital Affiliated to Guangxi University of Traditional Chinese Medicine,Nanning 530011,China
This work was supported by Guangxi Health and Family Planning Commission Self-funding Technology Project(No.Z2015434)and Guangxi University of Traditional Chinese Medicine Youth Foundation(No.QN14011)
Abstract Objective:To investigate the efficacy and toxicity of oxaliplatin reintroduction combined with raltitrexed as second-line chemotherapy after the first-line oxaliplatin-based chemotherapy in advanced colorectal cancer patients.Methods:The 48 evaluable patients with advanced colorectal cancer following disease progression prior to the first-line chemotherapy were treated with oxaliplatin and raltitrexed(raltitrexed 3 mg/m2ivgtt d1,oxaliplatin 100-130 mg/m2ivgtt d1,q21d).All 48 patients were divided into two groups:Group A,non-oxaliplatin-based regimens as the first-line chemotherapy,20 cases;Group B,oxaliplatin-based regimens as the first-line chemotherapy,28 cases.Each group was evaluated every two cycles.Results:The response rates(RR)of Groups A and B were 30.0%(6/20)and 32.1%(9/28),the disease control rates(DCR)were 80.0%(16/20)and 75.0%(21/28),the median progression free survival time(mPFS)was 6.5 and 7.0 months,and the median overall survival time(mOS)was 10 and 13 months,respectively.No statistical significance was observed between the two groups in their RR,CR,mPFS,and mOS(P=0.264,0.514,0.713,0.788),respectively.The most common adverse effects observed wereⅠ-Ⅱgrades of bone marrow suppression,aminotransferase abnormality,and digestive toxicities.The incidence of neurotoxicity(Ⅰ-Ⅱgrades)between the two groups was similar.Conclusion:Instead of irinotecan combined with raltitrexed,oxaliplatin reintroduction combined with raltitrexed for second-line chemotherapy after the first-line oxaliplatin-based chemotherapy in advanced colorectal cancer patients is feasible.
Keywords:advanced colorectal cancer,oxaliplatin,raltitrexed,retrospective studies
结直肠癌是世界范围内最常见的恶性肿瘤之一[1]。30%的患者就诊时已发生转移[2],因而化疗对晚期结直肠癌的作用日益受到关注。氟尿嘧啶(5-fluorouracil,5-FU)与奥沙利铂(oxaliplatin,L-OHP)或伊立替康(irinotecan,CPT-11)的联合方案FOLF⁃OX或FOLFIRI已成为晚期结直肠癌治疗公认的一线方案,且两者互为二线方案,对转移性结直肠癌患者的治疗取得了良好疗效[3],但在实际临床应用中仍存在一些亟需解决的问题。
目前,国际上公认的对于晚期结直肠癌化疗的策略有以下3种:1)持续化疗直至出现疾病进展或不可耐受的不良反应为止;2)采用化疗假期(chemother⁃apy holiday)或无化疗间歇期(chemotherapy-free inter⁃val,CFI),俗称“打打停停”[4-5];3)选用诱导化疗中的一种药物,或者是与诱导药物无交叉耐药的另一种药物维持治疗[6]。美国国立综合癌症网络(NCCN)指南对于已接受过奥沙利铂作为初始治疗的患者,二线治疗推荐改用伊立替康为基础的化疗方案。但由于伊立替康价格昂贵、具有慢性腹泻等禁忌证、不适于老年人及体质虚弱者应用等特点,部分患者不得不拒绝接受伊立替康治疗。de Gramont等[7]及Main⁃drault-goebel等[8]报道了奥沙利铂一线治疗转移性结直肠癌后二线或三线再重新启用的治疗结果,陈永昌等[9]亦报道了奥沙利铂辅助化疗失败后再引入治疗晚期结直肠癌的研究,但对于奥沙利铂再引入后联合雷替曲塞(raltitrexed)的研究国内外均未见报道。本研究回顾性分析48例接受雷替曲塞联合奥沙利铂二线治疗的晚期结直肠癌患者的临床病理特征及预后,旨在为中止奥沙利铂化疗的晚期结直肠癌患者二线是否能够使用奥沙利铂与雷替曲塞联合方案提供参考性依据。
1材料与方法
1.1材料
1.1.1病例选择收集2010年5月至2014年12月广西中医药大学附属瑞康医院收治的48例接受雷替曲塞联合奥沙利铂二线治疗的晚期结直肠癌患者,其中男性28例,女性20例。根据一线应用奥沙利铂的情况分为两组:A组(一线使用不含奥沙利铂方案)20例,其中男性9例,女性11例,平均年龄(58.00± 14.88)岁;B组(一线使用含奥沙利铂方案)28例,其中男性19例,女性9例,平均年龄(53.20±10.69)岁。两组患者在性别、平均年龄、组织学类型、PS评分、原发病灶、转移部位、既往手术情况、一线化疗使用方案等方面比较差异均无统计学意义(P>0.05,表1)。

表1 患者一般情况Table 1 Patients' characteristics at baseline

表1 患者一般情况(续表1)Table 1 Patients' characteristics at baseline
1.1.2入组条件1)经病理组织学或细胞学确诊的晚期结直肠癌患者,其转移病灶无法手术切除;2)对一线含奥沙利铂方案获益(疗效达SD、PR或CR),且化疗中止或结束6个月后出现病情进展;3)相关累积神经毒性恢复至≤1度(NCI-CTC 4.0);4)体力状态(performance status,PS)评分为0~2分,预计生存期≥3个月;5)有CT或者MRI可测量的病灶(至少1个病灶且直径>1 cm);6)一线化疗未使用过含雷替曲塞方案,均未行局部放疗者;7)未合并其它恶性肿瘤,未合并其它严重疾患或脏器功能障碍不适合化疗者;8)无严重药物过敏史。
1.2方法
1.2.1治疗治疗方法为雷替曲塞3 mg/m2,静脉滴注,第1天;奥沙利铂100~130 mg/m2,静脉滴注,第1天,每3周1次。每2个周期评价疗效,最多治疗6个周期。
1.2.2近期疗效评价按照RECIST 1.1[10]标准进行评价,分为完全缓解(complete response,CR)、部分缓解(partial response,PR)、稳定(stable disease,SD)、进展(progressive disease,PD),有效率(response rate,RR)=CR + PR,疾病控制率(disease control rate,DCR)=CR+PR+SD。不良反应按照《美国国家癌症研究所—通用毒性标准》(NCI-CTC)4.0版[11]的分级标准,分为Ⅰ~Ⅳ级。
1.2.3随访通过门诊或电话询问方式进行随访,随访开始时间为确诊晚期结直肠癌的时间,随访至患者死亡或截止日期至2015年7月,统计所有患者无进展生存时间和总生存时间。无失访病例。无进展生存期(progression free survival,PFS)定义为二线化疗第1天开始至患者肿瘤进展或死亡的时间。总生存期(overall survival,OS)定义为二线化疗第1天开始至患者死亡或随访截止的时间。
1.3统计学方法
采用SPSS 18.0统计软件进行分析。定量资料的统计描述采用x±s,定性资料的描述采用例数及百分比,组间差异的比较采用χ2检验。应用Kaplan-Meier法描述生存曲线,采用Log rank检验比较生存曲线差异。P<0.05为差异具有统计学意义。
2 结果
2.1近期疗效
2.1.1近期疗效分析48例患者均可评价近期疗效,其中CR 5例、PR 10例、SD 22例、PD 11例,总有效率为31.25%(15/48),总疾病控制率为77.10%(37/48)。
2.1.2两组近期疗效分析A组有效率为30.00%(6/20),疾病控制率为80.00%(16/20);B组有效率为32.10%(9/28),疾病控制率为75.00%(21/28);两组有效率、疾病控制率比较差异均无统计学意义(P>0.05,表2)。

表2 患者近期疗效比较 例(%)Table 2 Short-term efficacy of the two treatment groups n(%)
2.2远期疗效
2.2.1远期疗效分析48例患者予电话询问方式进行随访,随访至患者死亡或截止日期至2015年7月。无失访病例,均可评价远期疗效。中位PFS为6.5个月(95%CI:4.37~8.63),中位OS为13.0个月(95%CI:9.30~16.70)。
2.2.2两组远期疗效分析A组的中位PFS为6.5个月(95%CI:4.40~8.60),B组的中位PFS为7.0个月(95%CI:6.50~7.50)。A组的中位OS为10个月(95%CI:8.80~11.20),B组的中位OS为13个月(95%CI:9.20~16.80)。两组的中位PFS及中位OS比较差异均无统计学意义(P=0.713,P=0.788)(图1,2)。
2.3不良反应
血液学不良反应:以粒细胞减少、贫血较为明显,以Ⅰ~Ⅱ级为主;非血液学不良反应:以转氨酶异常、恶心呕吐、疲乏较为明显,以Ⅰ~Ⅱ级为主。两组感觉神经异常Ⅰ~Ⅱ级发生率相近,两组均无Ⅲ~Ⅳ级血小板减少、转氨酶异常、腹泻、感觉神经异常等不良反应发生,无肌酐异常、黏膜炎不良反应发生(表3)。

图1 两组中位无进展生存时间Figure 1 Median progression free survival of the two groups
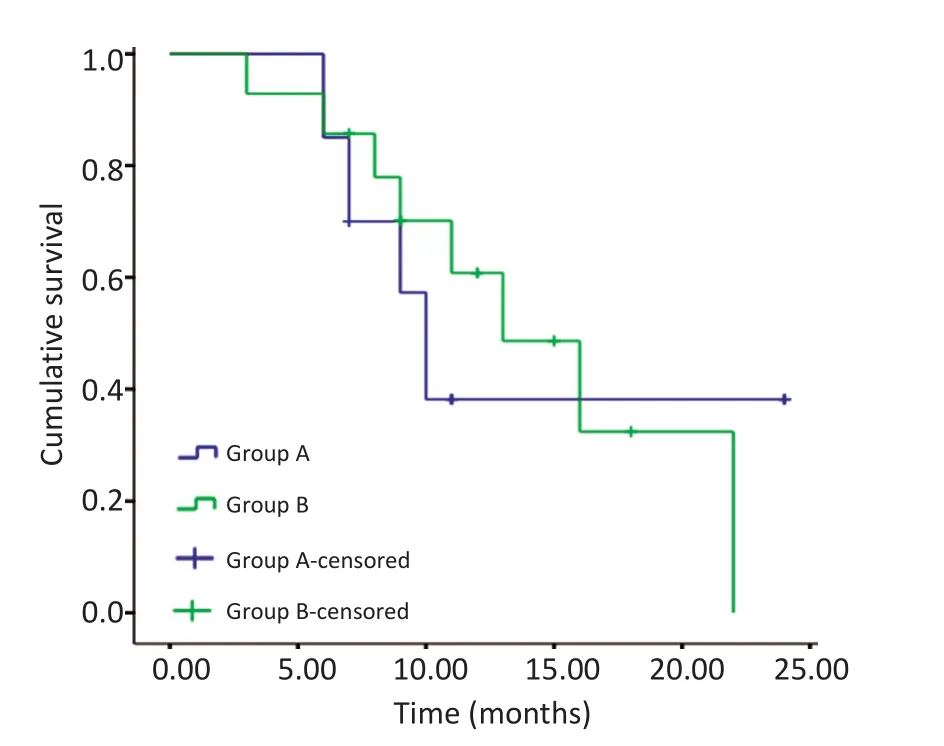
图2 两组中位总生存时间Figure 2 Median overall survival of the two groups
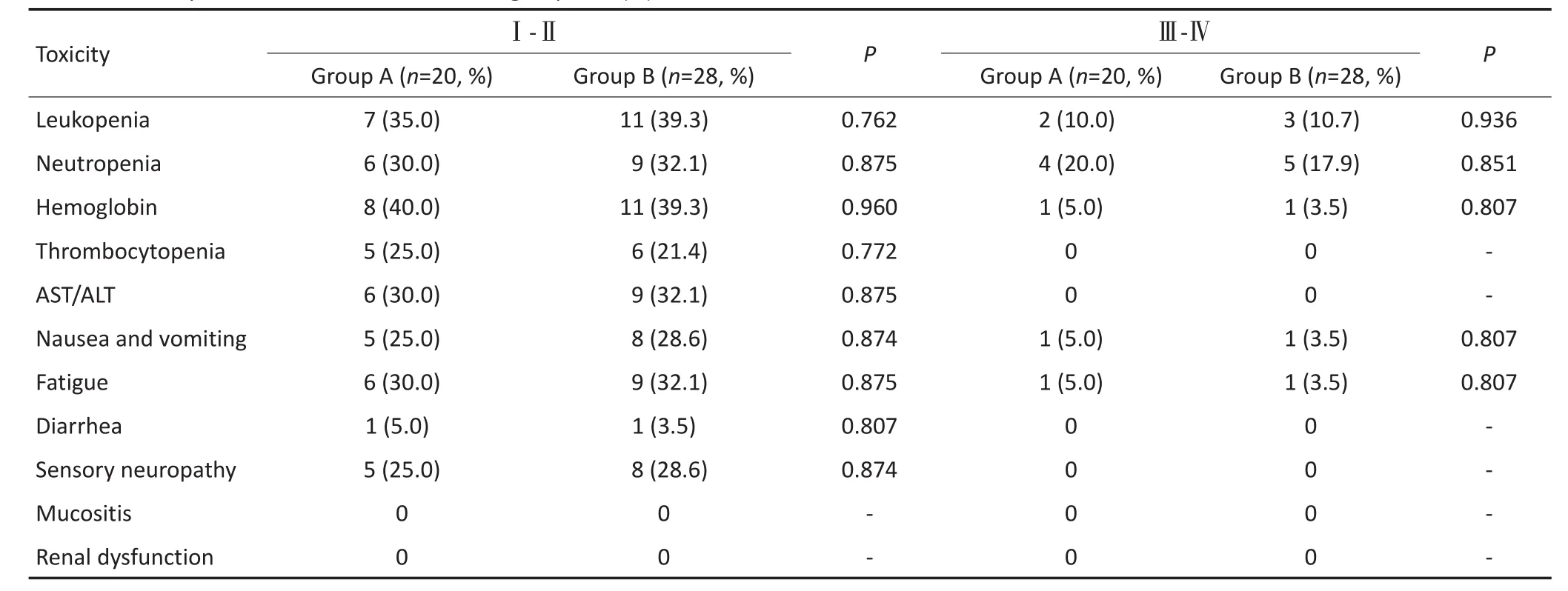
表3 两组患者不良反应 例(%)Table 3 Toxicity reaction of the two treatment groups n(%)
3 讨论
目前晚期结直肠癌的主要治疗手段仍是化疗,治疗的选择主要取决于治疗目标、既往治疗的类型和时限以及治疗方案构成中各种药物不同的不良作用谱。2007年美国Vanderbilt大学等[12]已提出将晚期结直肠癌的治疗视为一个连续统一的整体,各线治疗的界限是模糊的并非截然分开的。治疗的主要目的在于延长晚期患者的生存时间,改善患者的生存质量。在此背景下,用完全不同的药物组成的不同线别的化疗模式被扬弃了,而灵活运用多种活性药物相比严格遵循特定方案顺序能使患者有更多获益。
奥沙利铂与5-FU联合组成FOLFOX方案可作为晚期结直肠癌治疗的一线方案,但由于奥沙利铂的神经不良反应使其在临床的使用中受到了限制。据报道[13],分别有10%、25%、50%接受该方案化疗的患者在9、12、14个周期后会发生Ⅲ度神经不良反应,由于不良反应逐渐加重需减量甚至停用奥沙利铂。不同于顺铂,奥沙利铂的神经不良反应具有可逆性,因此许多研究者致力于探索更适合的给药方法。Ad⁃ams等[14]、Tournigand等[4]、Andre等[15]研究结果均表明,在接受FOLFOX作为一线治疗的转移性结直肠癌患者中采用间歇给予奥沙利铂的“打打停停”策略可以减少神经不良反应却并不影响总生存时间。Suenaga等[16]在该研究的基础上,进行了奥沙利铂在晚期结直肠癌治疗中再引入的Ⅱ期前瞻性研究,认为只要既往对含奥沙利铂方案敏感,且停用奥沙利铂超过6个月,无论是否曾对奥沙利铂耐药,都可从奥沙利铂再引入中获益,进而推测反复再引入治疗有可能是未来晚期结直肠癌化疗的新方向。有关奥沙利铂再引入的报道国内较少,对于其再引入后联合雷替曲塞的研究国内外均未见报道。本文首次探讨结束奥沙利铂为治疗基础方案且化疗超过6个月的晚期结直肠癌患者,二线使用奥沙利铂与雷替曲塞联合方案的疗效和安全性评价。
氟尿嘧啶是结直肠癌化疗的基石,它通过对胸苷酸合成酶(TS)非特异性抑制发挥细胞毒作用,氟尿嘧啶与该酶形成稳定的络合物从而影响了DNA、RNA的活性起到抗肿瘤作用[17]。雷替曲塞是一种更强的TS抑制剂,其组织/血浆药物浓度比在人体内较高,其代谢产物可以在细胞内长时间蓄积,从而延长了作用时间。雷替曲塞与氟尿嘧啶不存在交叉耐药,且疗效优越,甚至具有更强的抗人结肠癌肿瘤细胞活性,且使用方法便捷,无心脏不良事件出现,可作为5-FU耐药或者不适宜使用5-FU患者的有效替代药物[18-19]。
近年来,有许多研究者致力于雷替曲塞等全新的TS抑制剂与奥沙利铂联合的研究,证实了两药联合具有增效低毒的优势[20]。雷替曲塞联合奥沙利铂方案总有效率达到17.0%~33.3%,在一线治疗中mPFS达到8.7个月,在二线治疗中mPFS为4~6.5个月,mOS为9~13.6个月,疗效明显高于传统的FOLF⁃OX方案。本研究结果提示在一线化疗使用过及未使用过奥沙利铂的两组间分别在有效率、中位PFS、中位OS比较差异均无统计学意义(P>0.05)。两组的疗效结果与文献报道[20]基本相似或略好,而且感觉神经异常的发生率并未因奥沙利铂的再次使用而增加。提示在雷替曲塞联合奥沙利铂二线化疗,对曾使用过奥沙利铂一线化疗的患者仍然有效,无耐药性,不良反应并未明显增大。
Ⅰ~Ⅱ级不良反应与国内报道基本相似,神经异常Ⅰ~Ⅱ级发生率两组近似,但未出现国内外报道的Ⅲ~Ⅳ级感觉神经异常[20],考虑可能与本院使用中医疗法预防神经不良反应相关。均未出现化疗不良反应相关死亡病例,不良反应均为可逆性,患者总体耐受较好,均未出现氟尿嘧啶常见的黏膜炎。而且未发生心脏不良事件也与Ransom等[18]报道相符,可成为合并心脏基础疾病或使用氟尿嘧啶已发生心脏不良事件的安全替代和选择。
本研究结果提示,雷替曲塞联合奥沙利铂二线化疗对曾使用过奥沙利铂一线化疗的患者仍然有效,无耐药性,不良反应并未明显增大,对于不能进一步使用伊立替康的晚期结直肠癌患者是一个较好选择。但仍需大样本的前瞻性随机对照研究予以证实。
参考文献
[1]Brenner H,Kloor M,Pox CP.Colorectal cancer[J].Lancet,2014,383(9927):1490-1502.
[2]Liu JB,Zhang YR,Qu T,et al.Chemotherapy for metastatic colorectal cancer after failure of treatment with irinotecan and oxaliplatin[J].Chin J Clin Oncol,2013,40(23):1464-1467.[刘俊宝,张育荣,屈涛,等.奥沙利铂和伊立替康治疗失败后转移性结直肠癌的化疗选择[J].中国肿瘤临床,2013,40(23):1464-1467.
[3]Grothey A,Sargent D.Overall survival of patients with advanced colorectal cancer correlates with availability of fluorouracil,irinotecan,and oxaliplatin regardless of whether doublet or single-agent therapy is used first line[J].J Clin Oncol,2005,23(36):9441-9442.
[4]Tournigand C,Cervantes A,Figer A,et al.Optimox1:a randomized study of FOLFOX4 or FOLFOX7 with oxaliplatin in a stop-and-Go fashion in advanced colorectal cancer-a GERCOR study[J].J Clin Oncol,2006,24(3):394-400.
[5]Maughan TS,James RD,Kerr DJ,et al.Comparison of intermittent and continuous palliative chemotherapy for advanced colorectal cancer:a multicentre randomised trial[J].Lancet,2003,361(9356):457-464.
[6]Meng Y,Yang JW.Mantenance treatment of metastatic colorectal cancer[J].Int J Pathol Clin Med,2013,33(5):412-415.[蒙燕,杨建伟.转移性结直肠癌的维持治疗[J].国际病理科学与临床杂志,2013,33(5):412-415.]
[7]de Gramont A,Buyse M,Abrahantes JC,et al.Reintroduction of oxaliplatin is associated with improved survival in advanced colorectal cancer[J].J Clin Oncol,2007,25(22):3224-3229.
[8]Maindrault-goebel F,Gramont DA,Louvet C,et al.Evaluation of oxaliplatin dose intensity in bimonthly leucovorin and 48-hour 5-fluorouracil continuous infusion regimens(FOLFOX)in pretreated metastatic colorectal cancer.Oncology Multidisciplinary Research Group(GERCOR)[J].Ann Oncol,2000,11(11):1477-1483.
[9]Chen YC,An X,Zhang L,et al.Oxaliplatin reintroduction in colorectal cancer patients following disease progression after adjuvant oxaliplatin-based chemotherapy[J].Chin J Clin Oncol,2012,39(13):927-931.[陈永昌,安欣,张乐,等.奥沙利铂辅助化疗失败后一线再引入治疗晚期结直肠癌的研究[J].中国肿瘤临床,2012,39(13):927-931.]
[10]Eisenhauer EA,Therasse P,Bogaerts J,et al.New response evaluation criteria in solid tumours:revised RECIST guideline(version 1.1)[J].Euro J Cancer,2009,45(2):228-247.
[11]Chen AP,Setser A,Anadkat MJ,et al.Grading dermatologic adverse events of cancer treatments:the Common Terminology Criteria for Adverse Events Version 4.0[J].J Ame Aca Derm,2012,67(5):1025-1039.
[12]Goldber RM,Rothenberg ML,Cutsem VE,et al.The continuum of care:a paradigm for the management of metastatic colorectal cancer[J].Oncologist,2007,12(1):38-50.
[13]Chu M,Honda M,Tanaka C,et al.Multicenter randomized phase II clinical trial of oxaliplatin reintroduction as a third-or later-linetherapy for metastatic colorectal cancer—biweekly versus standard triweekly XELOX(The ORION Study)[J].Int J Clin Oncol,2015,20(1):1-7.
[14]Adams RA,Meade AM,Seymour MT,et al.Intermittent versus continuous oxaliplatin and fluoropyrimidine combination chemotherapy for first-line treatment of advanced colorectal cancer:results of the randomised phase 3 MRC COIN trial[J].Lancet Oncol,2011,12(7):642-653.
[15]Andre T,Tournigan C,Mineur L,et al.PhaseⅡstudy of an optimized 5-fluorouracil-oxaliplatin strategy(OPTIMOX2)with celecoxib in metastatic colorectal cancer:a GERCOR study[J].Ann Oncol,2007,18(1):77-81.
[16]Suenaga M,Mizunuma N,Matsusaka S,et al.A phaseⅡstudy of oxaliplatin reintroduction in patients pretreated with oxaliplatin and irinotecan for advanced colorectal cancer(RE-OPEN study):Reports of interim analysis[J].J Clin Oncol,2013,31(4):2403-2413.
[17]Benoist S,Nordlinger B.The role of preoperative chemotherapy in patients with resectable colorectal liver metastases[J].Ann Surg Oncol,2009,16(9):2385-2390.
[18]Ransom D,Wilson K,Fournier M,et al.Final results of Australasian Gastrointestinal Trials Group ARCTIC study:an audit of raltitrexed for patients with cardiac toxicity induced by fluoropyrimidines[J].Ann Oncol,2014,25(1):117-121.
[19]Claire K,Neel B,Mark H,et al.Use of raltitrexed as an alternative to 5-fluorouracil and capecitabine in cancer patients with cardiac history[J].Euro J Cancer,2013,49(10):2303-2310.
[20]Lai L,Hu XH,Hou EC.Clinical observation on raltitrexed alone versus raltitrexed in combination with oxaliplatin/irinotecan as second-line chemotherapy for advanced colorectal cancer:a comparative study[J].Guangxi Journal,2015(4):492-496.[赖林,胡晓桦,侯恩存.雷替曲塞单药与联合奥沙利铂或伊立替康二线治疗晚期结直肠癌的临床对比观察[J].广西医学,2015(4):492-496.]
(2016-01-08收稿)
(2016-02-03修回)
(编辑:孙喜佳校对:杨红欣)

赖林专业方向为消化道肿瘤的基础与临床研究。E-mail:1003671212@qq.com
·读者·作者·编者·
作者简介
通信作者:赖林1003671212@qq.com
doi:10.3969/j.issn.1000-8179.2016.05.037
作者单位:广西中医药大学附属瑞康医院肿瘤内科二病区(南宁市530011)
