Pt合金催化SO2电化学氧化反应的研究
2016-04-05邵志刚
穆 聪,侯 明,杜 超,梁 栋,邵志刚
(1.中国科学院大连化学物理研究所,辽宁大连116023;2.中国科学院大学,北京100049;3.新源动力股份有限公司,辽宁大连116023)
Pt合金催化SO2电化学氧化反应的研究
穆 聪1,2,侯 明1,杜 超3,梁 栋3,邵志刚1
(1.中国科学院大连化学物理研究所,辽宁大连116023;2.中国科学院大学,北京100049;3.新源动力股份有限公司,辽宁大连116023)
SO2电化学氧化反应一般用于工业废气脱硫、硫循环水电解制氢、硫氧化物检测等领域,随着SO2对质子交换膜燃料电池(PEMFC)毒化问题的出现,人们逐渐关注SO2电化学氧化的研究。电催化剂是SO2电化学氧化过程的关键材料之一。以PtRu/C、Pt3Pd/C和Pt/C作催化剂,采用循环伏安测试和极化曲线测试进行SO2电化学氧化研究。循环伏安测试结果显示,相同时间内PtRu/C催化剂表面SO2氧化量最高,Pt3Pd/C最低。极化曲线显示,PtRu/C催化剂上SO2电化学氧化的半波电位低于Pt3Pd/C和Pt/C催化剂,且PtRu/C催化剂上氧化峰电流最高。三种催化剂对SO2电化学氧化的活性高低为PtRu/C>Pt/C>Pt3Pd/C。
二氧化硫;电化学氧化;Pt合金催化剂
SO2电化学氧化反应一般用于工业废气脱硫[1]、硫循环水电解制氢[2]、硫氧化物检测[3]等领域,近年来,随着SO2对质子交换膜燃料电池(PEMFC)毒化问题的出现[4],人们逐渐关注SO2电化学氧化的研究。PEMFC具有清洁、高效、功率密度高且室温快速启动等优点,是21世纪最具前景的能源技术之一。然而空气中的SO2会毒化PEMFC阴极Pt催化剂,造成电池性能衰减[4]。采用外净化器是一种有效保护PEMFC的方法,现有外净化器多采用物理吸附或碱性物质吸附SO2达到净化效果,这些方法存在吸附饱和的问题。本课题组[5]提出了一种SO2电化学氧化脱除的外净化方法,能够有效保护PEMFC不受SO2毒化。
SO2电化学氧化反应是通过电化学过程将SO2氧化成SO42-,其反应过程如下:

该反应在热力学上可逆电势较低,然而受动力学上的限制,反应的过电位较高,实际不易发生[5]。SO2电化学氧化反应非常复杂,反应机理与电极材料密切相关[6],因此研究反应的电催化剂至关重要。
目前,科研工作者已对Pt、Pd、Au等金属,石墨、活性炭、过渡金属大环化物、PbO2等多种催化剂进行了筛选和研究,其中Pt催化剂因其良好的电化学活性和稳定性而最受关注[6-9]。SO2在Pt表面容易吸附,电化学分析和在线傅立叶红外光谱显示[10-12],当电位为0.65 V时,SO2以分子形式吸附于Pt表面;当电位高于0.65 V时,SO2发生氧化反应,当电位达到1.5 V时,SO2全部被氧化成SO42-;当电位低于0.65 V时,SO2发生还原反应生成S单质。虽然Pt催化剂体现出较好的SO2电化学氧化性能,但由于Pt的成本过高,限制了其使用。近年来,Pt合金催化剂在电化学领域已经有较多的研究和应用,由于合金的电子效应和几何效应,很多情况下Pt合金表现出优异于Pt催化剂的电化学性能,且合金能够减少Pt用量,降低成本。但是关于将Pt合金催化剂用于SO2电化学氧化方面的研究报道仍然很少。Lee等[13]采用高温热处理法制备了不同比例的Pt-Al/C双金属催化剂,结果显示有Al掺杂的双催化剂比Pt/C具有更高的SO2电化学氧化活性。Garsany等[14]研究发现,Pt3Co/C对SO2电化学氧化速率快于Pt/C。由此看来,Pt合金催化剂用于SO2电化学氧化反应具有研究价值。
在众多Pt合金催化剂中,Pt3Pd/C是在PEMFC中应用研究较多的合金催化剂,PtRu/C在直接醇类燃料电池抗CO中毒方面有较多应用。本文中,选用商业化50%(质量分数) Pt3Pd/C和45%PtRu/C进行SO2电化学氧化研究,作为对比,50%Pt/C的测试结果也在文中给出。
1 实验
电化学测试在配有旋转圆盘电极系统的电化学分析仪(CHI 630D或CHI 730D)上进行。采用传统三电极体系,工作电极为催化剂薄膜电极,具体制备过程如下:称取5 mg催化剂,加入1 mL异丙醇和50 μL质量分数为5%的Nafion溶液,超声分散,配制成催化剂浆料。量取适量催化剂浆料,滴涂于事先抛光处理好的直径为4 mm的玻碳电极上,自然晾干。参比电极为饱和甘汞电极,对电极为Pt片电极。电解质溶液为N2饱和的0.5mol/L H2SO4溶液。含SO2的电解质溶液由无水Na2SO3和 N2饱和的 0.5mol/L H2SO4溶液配制,为 0.001mol/L Na2SO3+0.5mol/L H2SO4溶液或0.005mol/L Na2SO3+0.5mol/L H2SO4溶液。本文中,所有实验均在室温常压下进行,所给电势值均已换算为相对于标准氢电极的电势(.SHE)。
1.1 SO2电化学氧化的循环伏安测试
(1)催化剂的活化:在N2饱和的0.5mol/L H2SO4溶液中,采用循环伏安(CV)扫描进行催化剂的活化,直至得到稳定重复的CV曲线。扫描电压为0~1.4 V,扫速为100 mV/s。
(2)催化剂CV曲线测定:在N2饱和的0.5mol/L H2SO4溶液中测定催化剂的初始CV曲线,扫描电压为0~1.4 V,扫速为50 mV/s。
(3)SO2恒电位吸附:在 0.001mol/L Na2SO3+0.5mol/L H2SO4溶液中,工作电极在0.65 V恒电位条件下吸附SO2,吸附时间为30、60、120、240和420 s。
(4)SO2电化学氧化的CV测试:将上述吸附SO2的工作电极用足量去离子水冲洗,之后在N2饱和的0.5mol/L H2SO4溶液中进行CV测试,扫描电压为0~1.4 V,扫速为50 mV/s,扫描7圈。
1.2 SO2电化学氧化的极化曲线测试
将活化处理好的工作电极置于0.005mol/L Na2SO3+0.5mol/L H2SO4溶液中,采用线性伏安扫描(LSV)技术测定SO2电化学氧化的极化曲线。扫描电压为0.5~1.4 V,扫速为5 mV/s,正向扫描,旋转圆盘电极(RDE)转速为1 600 r/min。
2 结果与讨论
2.1 SO2电化学氧化循环伏安测试分析
图1为Pt/C、PtRu/C和Pt3Pd/C三种催化剂对SO2电化学氧化的CV曲线以及催化剂初始CV曲线。在催化剂初始CV曲线中,0~0.4 V的氧化还原峰为H的脱附峰和吸附峰,0.75~1.4 V的氧化峰为Pt氧化峰,0.4~1.0 V的还原峰为氧还原峰。从吸附SO2后的CV1曲线中可以观察到,0~0.4 V的H脱附峰和吸附峰减小,表明在0.65 V恒电位条件下有SO2吸附到催化剂表面,占据了催化剂的活性位点,导致H吸脱附峰面积减小;正向1.0~1.4 V之间出现额外氧化电流,说明催化剂表面吸附的SO2在高电位下被氧化;反向0.2~0.6 V可以观察到少许额外还原电流,可能是催化剂表面吸附的SO2有少量在反向扫描至低电位时发生还原反应生成S单质[12]。在随后的CV扫描中(CV2~CV7),H吸脱附峰逐圈增强,正向1.0~1.4 V的额外氧化电流逐渐消失,氧还原峰增强。上述现象表明,随着CV扫描的进行,催化剂表面吸附的SO2逐渐被氧化成SO42-,并从催化剂表面脱除。图1中,三种催化剂的CV6和CV7曲线几乎重合,说明经过7圈CV扫描催化剂表面吸附的SO2可以完全被氧化脱除。CV7曲线与催化剂初始CV曲线有轻微偏差,可能是由于CV扫描电位范围较大,导致催化剂部分流失,活性下降[12]。

图1 三种催化剂表面恒电位吸附SO2后的CV曲线(相同催化剂担载量,恒电位为0.65 V,吸附时间为30 s)
上述现象与文献报道的SO2在Pt催化剂表面吸附后的电化学氧化现象类似[12,15]。在SO2电化学氧化CV曲线(CV1~CV7)中,总的电量由双电层电量、H的吸脱附电量、Pt的氧化还原电量以及SO2的氧化电量组成。由于在每一圈CV曲线中,Pt的氧化还原电量、H的吸脱附电量以及双电层电量可以相互抵消,故第圈CV曲线中的正向氧化电量与反向还原电量之差为SO2的氧化电量[12],即:

催化剂表面SO2的氧化电量计算结果如表1所示(相同催化剂担载量,恒电位为0.65 V,吸附时间为30 s)。可以看出,随着CV1~CV7的逐圈扫描,三种催化剂上的均逐渐减小。催化剂表面SO2氧化电量为CV1~CV7的氧化电量之和,分别为1.09×10-4C(PtRu/C)>8.84×10-5C(Pt/C)>5.61×10-5C (Pt3Pd/C)。由此,对SO2电化学氧化活性为PtRu/C>Pt/C>Pt3Pd/C。
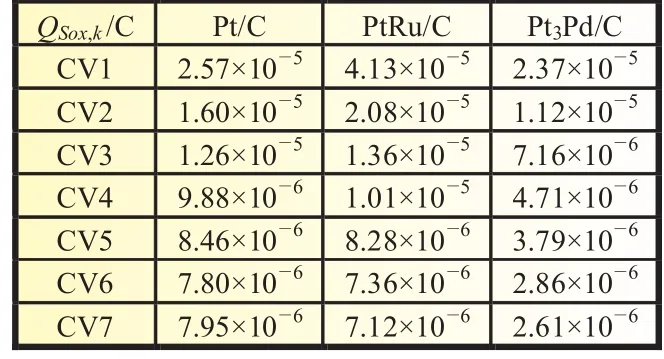
表1 三种催化剂表面SO2的氧化电量
2.2 不同吸附时间的SO2电化学氧化分析
图2为0.65 V恒电位吸附SO2时间分别为30、60、120、240和420 s之后测试得到的Pt/C、Pt3Pd/C和PtRu/C催化剂的CV曲线。可见,随着恒电位吸附时间的延长,三种催化剂的CV曲线中H脱附峰面积逐渐减小,推测SO2在催化剂表面的吸附量逐渐增大。按公式(2)计算不同恒电位时间对应的催化剂表面SO2氧化电量如表2所示(相同催化剂担载量,恒电位0.65 V,吸附时间为30、60、120、240、420 s)。随着恒电位吸附时间的延长,催化剂表面的SO2氧化电量逐渐增大。恒电位420 s后,Pt3Pd/C催化剂表面SO2氧化电量略有减小,推测是由于在恒电位240 s时Pt3Pd/C催化剂表面SO2吸附已达到饱和,继续延长恒电位时间不会增加SO2的吸附量。将三种催化剂进行比较可以发现,PtRu/C催化剂表面的SO2氧化电量始终最大,而Pt3Pd/C催化剂始终最小,说明三种催化剂对SO2电化学氧化反应的催化剂活性为PtRu/C>Pt/C>Pt3Pd/C。
2.3 SO2电化学氧化的极化曲线分析
Pt/C、Pt3Pd/C和PtRu/C催化剂上的SO2电化学氧化极化曲线如图3所示。三种催化剂上,SO2电化学氧化极化曲线均呈火山型,氧化电流随电压的增大而先增大后减小,在1.1 V左右出现氧化电流峰。这是由于SO2与含氧基团在催化剂表面存在竞争吸附,高电位下含氧基团的吸附占主导地位,因而会在一定程度上抑制SO2电化学氧化,出现氧化电流在高电位下随电压增大而减小的现象。三种催化剂对SO2电化学氧
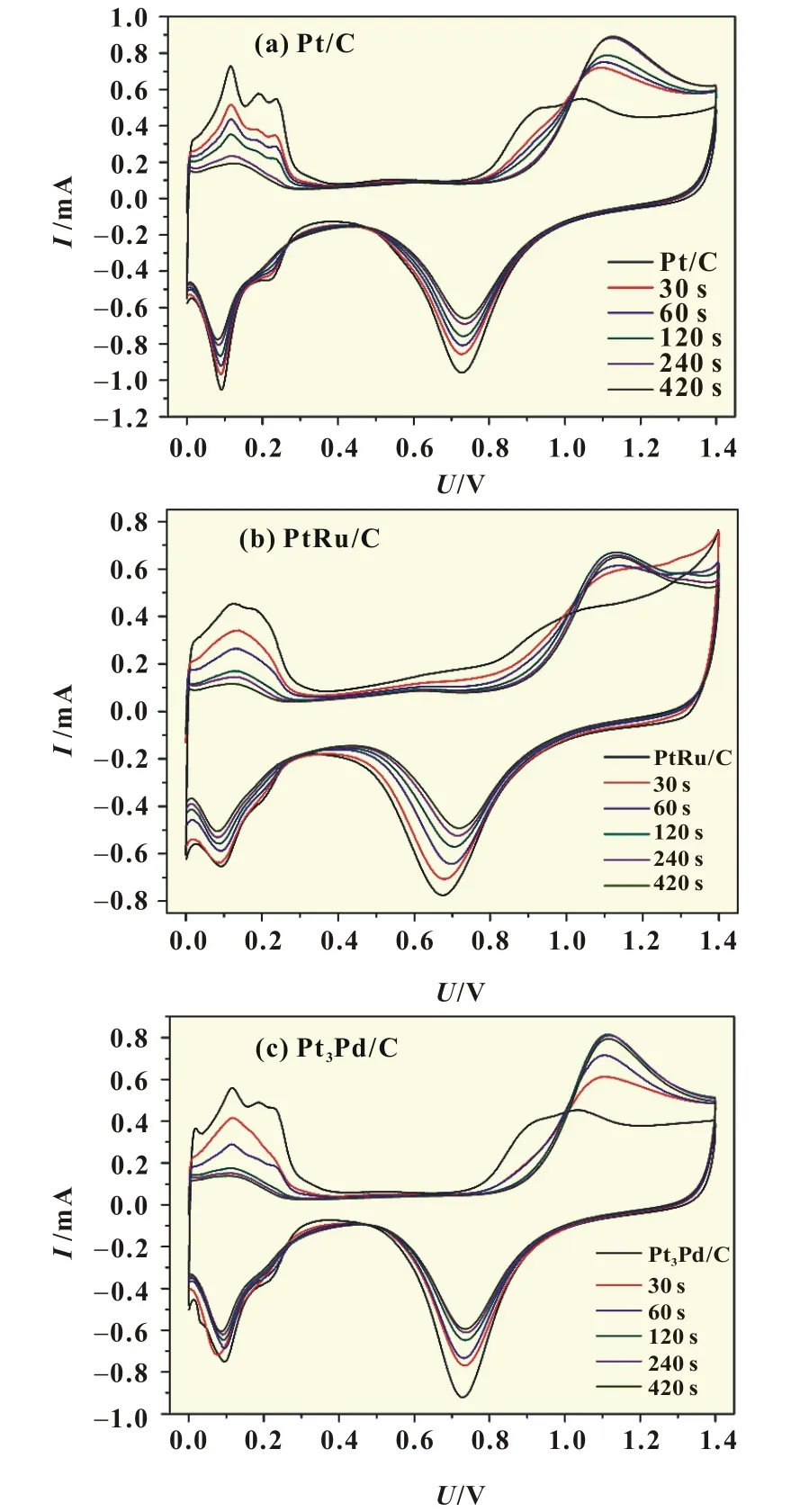
图2 三种催化剂表面恒电位吸附SO2后的CV曲线(相同催化剂担载量,恒电位0.65 V,吸附时间为30、60、120、240、420 s)

表2 不同恒电位时间的三种催化剂表面的SO2氧化电量

图3 三种催化剂表面SO2电化学氧化极化曲线(相同Pt担量,电解质溶液为0.005mol/L Na2SO3+0.5mol/L H2SO4溶液,RDE转速为1 600 r/min)
化的半波电位大小关系为PtRu/C<Pt/C<Pt3Pd/C,峰电流大小关系为PtRu/C>Pt/C>Pt3Pd/C。上述现象表明,三种催化剂对 SO2电化学氧化反应的催化活性为 PtRu/C>Pt/C>Pt3Pd/C。
3 结论
PtRu/C、Pt3Pd/C和Pt/C催化剂表面的SO2吸附和电化学氧化体现出相似的特征。在0.65 V恒电位条件下,三种催化剂表面均能吸附SO2,随后进行CV扫描能够将催化剂表面吸附的SO2氧化脱除。在恒电位吸附和CV扫描条件相同的情况下,三种催化剂表面SO2氧化电量为PtRu/C>Pt/C>Pt3Pd/C。极化曲线显示,SO2电化学氧化的半波电位为 PtRu/C<Pt3Pd/C<Pt/C,氧化峰电流为PtRu/C>Pt/C>Pt3Pd/C。综上,三种催化剂对 SO2电化学氧化的活性为 PtRu/C>Pt/C>Pt3Pd/C。
[1]UN U T,KOPARAL A S,OGUTVEREN U B.Electrochemical desulfurization of waste gases in a batch reactor[J].Journal of Environmental Engineering-Asce,2007,133:13-19.
[2]ALLEN J A,ROWE G,HINKLY J T,et al.Electrochemical aspects of the hybrid sulfur cycle for large scale hydrogen production [J].Int J Hydrog Energy,2014,39:11376-11389.
[3]SHANARAN D R,UEHERA N,KATO T.Determination of sulfur dioxide based on a silver dispersed functional self-assembled electrochemical sensor[J].Sensors and Actuators B-Chemical,2002,87: 442-447.
[4]FU J,HOU M,DU C,et al.Potential dependence of sulfur dioxide poisoning and oxidation at the cathode of proton exchange membrane fuel cells[J].Journal of Power Sources,2009,187:32-38.
[5]ZHAI J,HOU M,LIANG D,et al.Investigation on the electrochemical removal of SO2in ambient air for proton exchange membrane fuel cells[J].Electrochem Commun,2012,18:131-134.
[6]O'BRIEN J A,HINKLEY J T,DONNE S W,et al.The electrochemical oxidation of aqueous sulfur dioxide:a critical review of work with respect to the hybrid sulfur cycle[J].Electrochim Acta, 2010,55:573-591.
[7]SCOTT K,TAAMA W M.An investigation of anode materials in the anodic oxidation of sulphur dioxide in sulphuric acid solutions [J].Electrochim Acta,1999,44:3421-3427.
[8]BELANGER G.Determination of sulfur dioxide by anodic oxidation on lead dioxide electrodes[J].Analytical Chemistry,1974,46: 1576-1577.
[9]AGBOOLA B,NYOKONG T.Comparative electrooxidation of sulphite by self-assembled monolayers(SAMs)of Co(II),Fe(II),Ni (II)and Mn(III)tetrakis benzylmercapto and dodecylmercapto met allophthalocyanines complexes on gold electrodes[J].Talanta, 2007,72:691-698.
[10]MATVEEVA E S,SHEPELIN V A,KASATKIN E V.A coulometric study of sulfurous acid adsorption on the platinum-electrode[J].Soviet Electrochemistry,1982,18:560-562.
[11]QUIJADA C,RODES A,HUERTA F,et al.In situ FT-IRRAS study of SO2adlayers formed on Pt(111)electrodes from open-circuit adsorption in acidic media[J].Electrochim Acta,1998,44: 1091-1096.
[12]GARSANY Y,BATURINA O A,SWIDER-LYONS K E.Impact of sulfur dioxide on the oxygen reduction reaction at Pt/Vulcan carbon electrocatalysts[J].J Electrochem Soc,2007,154:B670-B675.
[13]LEE J,LANGER S H.Electrochemical sulphur dioxide oxidation with platinum-aluminum electrocatalysts[J].Journal of Applied Electrochemistry,1995,25:353-357.
[14]GARSANY Y,BATURINA O A,SWIDER-LYONS K E.Oxygen reduction reaction kinetics of SO2-contaminated Pt3Co and Pt/Vulcan carbon electrocatalysts[J].J Electrochem Soc,2009, 156:B848-B855.
[15]FORAL M J,LANGER S H.Charactrization of sulfur layers from reduced sulfur-dioxide on porous platinum black teflon electrodes [J].Journal of Electroanalytical Chemistry,1988,246:193-205.
Study on electrochemical oxidation of SO2with platinum alloy catalysts
The electrochemical oxidation of SO2is widely applied for flue gas desulfurization, water splitting for hydrogen production(hybrid sulfur process)and electrochemical sensing of sulfur oxides.The reaction has been of interest recently due to its poisoning effect on the proton exchange membrane fuel cell(PEMFC).The electrocatalyst is one of the key materials for this reaction.PtRu/C,Pt3Pd/C and Pt/C were investigated as the electrocatalysts for the electrochemical oxidation of SO2by cyclic voltammetry measurement and polarization curve measurement.Cyclic voltammetry measurements reveal that the charge of sulfur dioxide oxidation on PtRu/C is the maximum whileminimum on Pt3Pd/C.Polarization curves show that the half-wave of PtRu/C is much more negative than that of Pt/C and Pt3Pd/C.Meanwhile,the peak current of PtRu/C is the largest among them.Consequently,the activity for the electrochemical oxidation of SO2is in the order of PtRu/C>Pt/C>Pt3Pd/C.
sulfur dioxide;electrochemical oxidation;platinum alloy catalysts
TM 911
A
1002-087 X(2016)06-1199-03

2015-12-09
国家“973”项目(2012CB215500)
穆聪(1989—),女,辽宁省人,硕士,主要研究方向为SO2电化学氧化催化剂。
侯明,E-mail:houming@dicp.ac.cn;邵志刚,E-mail:zhgshao@dicp.ac.cn
