大豆分离蛋白-乙二胺接枝物的合成及性质
2016-03-30袁明昆,许楚,周景辉
袁 明 昆, 许 楚, 周 景 辉
( 大连工业大学 轻工与化学工程学院, 辽宁 大连 116034 )
大豆分离蛋白-乙二胺接枝物的合成及性质
袁 明 昆,许 楚,周 景 辉
( 大连工业大学 轻工与化学工程学院, 辽宁 大连116034 )
摘要:探讨了以1-(3-二甲氨基丙基-3)-乙基碳二亚胺盐酸盐(EDC)和N-羟基琥珀酰亚胺(NHS)催化大豆分离蛋白(SPI)的羧基和乙二胺(EDA)的氨基进行接枝反应制备大豆分离蛋白-乙二胺接枝物(SPI-EDA)的最佳条件。利用激光粒度/Zeta电位仪、FT-IR、HPLC、PCD等对SPI-EDA接枝物进行结构与性质表征。确定适宜的合成条件:反应温度为室温,时间4 h, SPI、EDC、EDA与 NHS摩尔比1.0∶0.5∶0.6∶0.125。检测结果表明,EDA成功的接枝到SPI羧基基团上,与SPI相比,SPI-EDA的电荷密度、相对分子质量等都有所改善,接枝物SPI-EDA聚集体粒径增大且分布均一。
关键词:大豆分离蛋白(SPI);1-(3-二甲氨基丙基-3)-乙基碳二亚胺盐酸盐(EDC);乙二胺(EDA);大豆分离蛋白-乙二胺接枝物(SPI-EDA)

0引言
目前造纸助剂大多数都是化石基产品,由于其不可再生和不可降解性,造纸助剂的发展趋势是转向可再生生物基资源的产品,如淀粉[1]、瓜尔胶[2]、纤维素[3]、壳聚糖[4]等。大豆分离蛋白(SPI)是大豆生产油料等产品后的副产物,来源集中、产量较大、成本低,属于可降解可再生资源。SPI大量用于饲料,也有用其作为食品添加剂、膜材料、胶黏剂等原料[5]。
由于SPI上的谷氨酸和天门冬氨酸等氨基酸都含有自由羧基,两者约占总的氨基酸单元的35%[6],导致SPI在浆料中带负电,不符合造纸助剂带正电荷的要求,因此如要把SPI用作造纸助剂,有必要对其进行化学改性。如能在SPI羧基端接枝上氨基基团使之具有类似聚乙烯亚胺(PEI)的结构,就可以满足造纸助留助滤剂所要求的高分子和正电性,从而可以将其用作造纸助剂[7]。
碳二亚胺类催化剂(EDC)催化反应具有高效、低温、水性等优点,常被用于催化羧酸和伯胺间的接枝反应,很适合大分子的温和改性。EDC催化接枝反应还可以被用于多肽[8]、纤维素[9]和明胶[10]等大分子的改性等。其反应机理是:EDC通过酰胺结合与SPI结构中的谷氨酸和天门冬氨酸残基上的羧基形成活泼的共价偶联物O-异酰基脲中间体,随后乙二胺(EDA)上的伯胺通过亲核攻击,最终与SPI上的羧基形成酰胺交联[11-12]。
本实验利用EDC和NHS催化SPI上的羧基和EDA上的氨基进行接枝反应,探索了SPI-EDA接枝物的最佳制备条件,并通过激光粒度/Zeta电位仪、FT-IR、HPLC、PCD等对SPI-EDA接枝物进行结构与性质表征,旨在扩大SPI的用途,开发新的造纸助剂品种。
1实验
1.1原料与仪器
原料:大豆分离蛋白(SPI,w(分离蛋白)≥90%),山东东营万德福公司;乙二胺(EDA),上海晶纯生化科技股份有限公司,纯度为99%;1-(3-二甲氨基丙基-3)-乙基碳二亚胺盐酸盐(EDC),阿达玛斯试剂有限公司,纯度为99%;N-羟基琥珀酰亚胺 (NHS),国药化学试剂有限公司,纯度均为99%;2-(N-吗啡林)乙撑磺酸(MES),北京索莱宝科技有限公司,纯度为90%。
仪器:Nano-ZS90 Zeta电位仪,英国Malvern公司;PCD-04颗粒电荷滴定仪,德国BTG公司;Frontier傅里叶变换红外光谱仪,PerkinElmer公司;SCL-10AVP高效液相色谱,日本岛津公司。
1.2实验方法
1.2.1SPI-EDA的合成
在圆底烧瓶中分别加入不同摩尔比例的SPI、EDC、NHS、EDA,以MES为缓冲液调pH至5.5,升温至反应温度,保温一段时间后,取出冷却到室温。反应后溶液产物用丙酮沉淀、水溶,重复水溶/丙酮沉析的纯化过程3次,最后在冷冻干燥至完全脱水。
1.2.2反应产物Zeta电位和粒径的测定
称取一定量的绝干改性样品配制成质量分数为0.1%溶液(pH=7),用Nano-ZS90仪器测Zeta 电位,测定温度25 ℃,重复测定6次以上,取平均值。反应产物的粒径同样用Nano-ZS90仪器测定,测定范围5 nm~10 μm。
1.2.3反应产物FT-IR测定
取少量绝干样品与KBr晶体按质量比约1∶100进行研磨,用傅里叶红外光谱仪进行FT-IR测定,测定波段为4 000~400 cm-1,扫描次数为32次。
1.2.4反应产物电荷密度的测定
称取一定量的绝干改性样品配制成质量分数为0.01%溶液,取10 mL改性样品溶液于PCD-04颗粒电荷分析仪中,用阳离子聚电解质或阴离子聚电解质标准滴定液进行滴定,测定改性样品的电荷密度。电荷密度计算公式:
CD=cV/m
(1)
式中:CD为反应产物电荷密度,mmol/g;c为阳离子聚电解质溶液或阴离子聚电解质的浓度1.0 mmol/L;V为消耗的标准阳离子聚电解质或阴离子聚电解质的体积,mL;m为用于滴定溶液中样品质量,g。
1.2.5反应产物相对分子质量的测定
SPI、SPI-EDA的相对分子质量分布范围采用高效液相色谱结合TSK-gel G4000-SWxl(7.8 mm×30.0 cm)凝胶过滤色谱柱测定。进样量:20 μL;进样质量浓度:0.5 mg/mL;检测波长:220 nm。流动相:0.01 mol/L NaH2PO4,0.1 mol/L Na2SO4缓冲溶液(含0.1%SDS)。洗脱体积流量:0.7 mL/min。相对分子质量标准品分别选用肌球蛋白(200 ku)、β半乳糖苷酶(116 ku)、磷酸酶b(97.2 ku)、牛血清蛋白(66.4 ku)、卵清蛋白(43 ku)。对凝胶过滤色谱而言,相对分子质量的对数与保留时间呈线性相关,经过计算所得相对分子质量标准曲线为lgMw=-0.099 1t+6.140 2,R2=0.929。
2结果与讨论
2.1SPI-EDA合成结果与分析
2.1.1EDC用量对SPI-EDA合成的影响
Zeta电位是指带电颗粒表面剪切层的电位,可作为表征粒子表面静电荷的一个重要参数[13]。SPI是典型的两性聚电解质,在其多肽链上有许多极性基团和非极性基团,在水溶液中亲水性的极性基团暴露在SPI表面,使SPI表面带电。所以当EDA接在SPI上,其表面的电荷也会发生变化,因此可用Zeta电位来表征其不同接枝条件的表面电荷变化情况。
在反应温度30 ℃,反应时间为4 h,SPI、EDA、NHS摩尔比为1.0∶1.0∶1.0时,考察EDC用量对SPI-DEA合成反应的影响。由图1中可以看出,随着EDC用量的增加,改性产物的Zeta电位急剧增加,当SPI与EDC摩尔比超过2∶1后,Zeta电位则增加缓慢。这是因为SPI多肽链上的自由羧基被EDC活化生成共价偶联物O-异酰基脲中间体,这种中间体能够迅速与EDA上的氨基发生反应,从而消耗了SPI多肽链上一定量的羧基。继续增加EDC用量,羧基已基本全部被活化参与了反应,反应慢慢达到了平衡。因此适宜的SPI与EDC摩尔比为2∶1。

图1 EDC用量对SPI-EDA的Zeta电位的影响
2.1.2EDA用量对SPI-EDA合成的影响
在反应温度30 ℃,反应时间为4 h,SPI、EDC、NHS摩尔比为1.0∶0.5∶1.0时,考察EDA用量对SPI-DEA合成反应的影响。由图2中可以看出,随着EDA用量的增加,改性产物的Zeta电位逐渐增加,但SPI与EDA摩尔比超过5∶3后,Zeta电位基本不变。这是因为随着EDA用量的增加,EDA与中间体接触的概率增加,SPI多肽链上自由羧基与EDA上的氨基反应生成酰胺从而使SPI表面电荷发生转变。而当SPI与EDA用量之比超过5∶3之后,Zeta电位增加趋于平缓。这是因为此时SPI羧基基本被氨基取代。因此适宜的SPI与EDA摩尔比为5∶3。

图2 EDA用量对SPI-EDA的Zeta电位的影响
2.1.3NHS用量对SPI-EDA合成的影响
由在反应温度30 ℃,反应时间为4 h,SPI、EDC、EDA摩尔比为1.0∶0.5∶0.6时,考察NHS用量对SPI-DEA合成反应的影响。由图3可以看出,随着NHS用量的减少,Zeta电位基本不变,但是当EDC与HNS摩尔比小于4∶1时,Zeta电位开始降低。这是因为EDC与SPI多肽链上的羧基生成的是一种不稳定的中间体,这种中间体如不与氨基立即反应,就会很快水解并重新释放出羧基基团。一定量的NHS存在,可以将O-异酰基脲中间体转化为氨基反应活性的NHS酯,与氨基反应的速度相比,NHS酯的水解要缓慢得多,从而大大提高了EDC主导的接枝反应的效率[14]。因此EDC与NHS最适宜的摩尔比为4∶1。

图3 NHS用量对SPI-EDA 的Zeta电位的影响
2.1.4反应时间对SPI-EDA合成的影响
在反应温度30 ℃,SPI、EDC、EDA、NHS摩尔比为1∶0.5∶0.6∶0.125时,考察反应时间对SPI-DEA合成反应的影响。由图4可以看出,随着反应时间的增加,Zeta电位开始急剧增加,这是因为反应之初,SPI多肽链上有大量未参与反应的羧基。而随着反应时间的增加,Zeta电位开始缓慢增加。这是因为在反应体系中羧基与氨基含量是一定的,随着反应时间的增加,羧基和氨基会不断地被消耗掉,当反应时间超过4 h后,Zeta电位基本保持恒定,据此可以认为羧基和氨基基本被耗尽。因此最适宜的反应时间为4 h。

图4 反应时间对SPI-EDA Zeta电位的影响
2.1.5反应温度对SPI-EDA合成的影响
在反应时间为4 h,SPI、EDC、EDA、NHS摩尔比为1∶0.5∶0.6∶0.125时,考察反应温度对SPI-DEA合成的影响。由图5可见,随着温度的增加,Zeta电位变化不大。这是因为EDC催化剂具有高效、低温等优点,在较大的温度范围都可以发挥良好的催化效果。因此为节约成本,无须刻意控制温度,合成反应在室温下进行即可。

图5 反应温度对SPI-EDA Zeta电位的影响
2.2SPI-EDA 红外表征

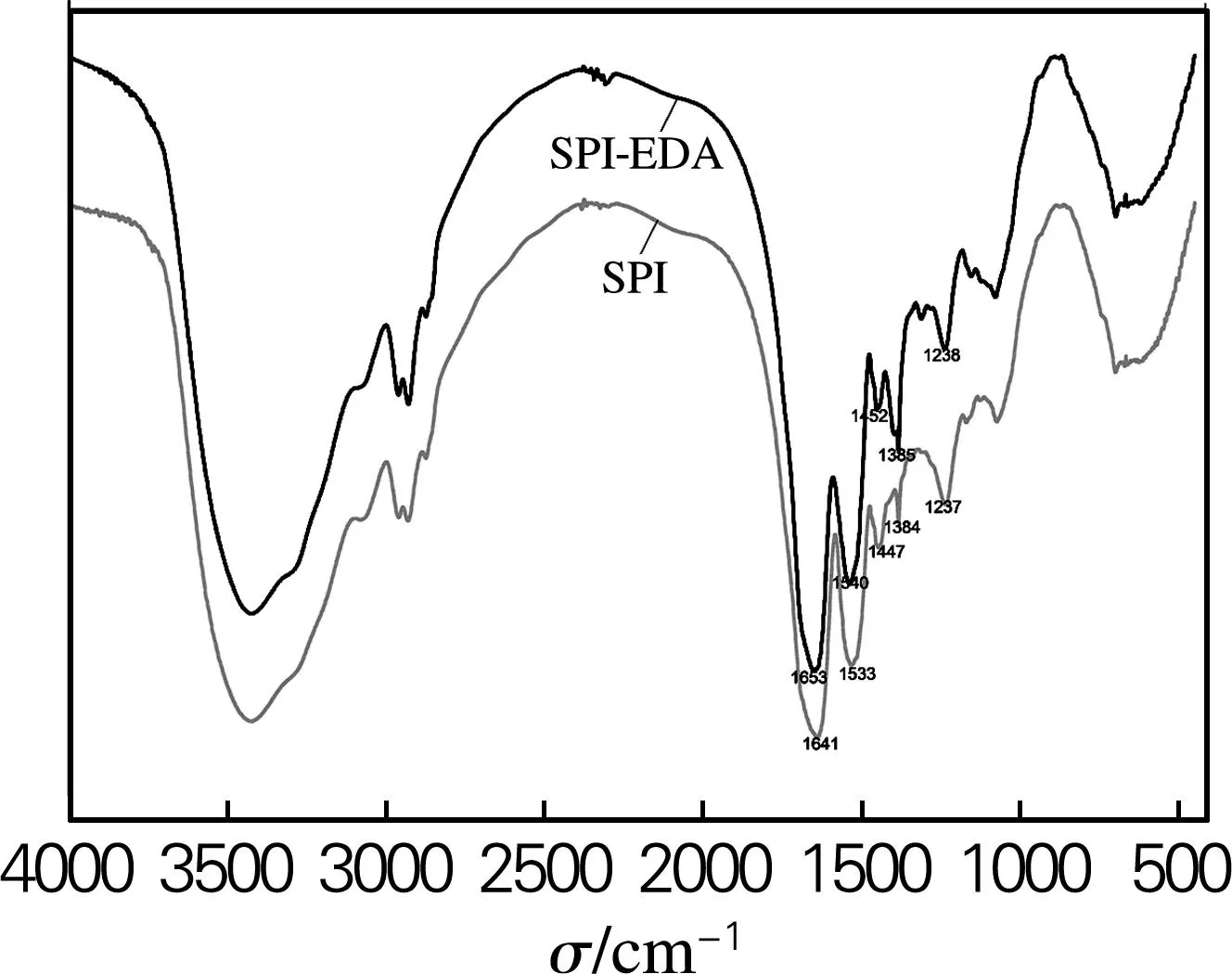
图6 SPI和SPI-EDA的红外谱图
图7(a)和图7(b)分别是SPI和SPI-EDA结合去卷积化和二阶导数对酰胺I带进行拟合的图谱。酰胺I 带对于研究蛋白质二级结构最有价值,它是由蛋白质不同二级结构的谱峰分量叠加形成的,通过拟合可以研究改性前后酰胺Ⅰ带中α-螺旋、β-折叠、β-转角等二级结构的比例。一般认为1 650~1 658 cm-1为α-螺旋,1 610~1 640 cm-1为β-折叠,1 660~1 700 cm-1为β-转角,1 650~1 640 cm-1为无规卷曲[16]。通过拟合结果可以发现,SPI-EDA相对于SPI,α-螺旋比例增加了6.48%,β-折叠比例减少了17.38%,β-转角比例减少了1.52%,无规卷曲比例增加了12.42%。这是因为SPI中谷氨酸和天门冬氨酸在SPI中主要是β-折叠形式存在的[17-18],EDA接枝到这两个氨基酸羧基基团上,改变了SPI原本的空间结构,导致二级结构β-折叠比例减少。这些二级结构比例的变化,可以间接地说明EDA成功地接枝到谷氨酸和天门冬氨酸羧基基团上。

(a) SPI

(b) SPI-EDA
图7SPI和SPI-EDA 酰胺Ⅰ带的拟合曲线
Fig.7FTIR curve fitting of SPI-EDA and SPI-EDA
in amideⅠ
2.3SPI-EDA电荷密度的表征
表1为SPI、SPI-EDA的电荷密度。从表中可以看出,未改性的SPI电荷密度为-0.319 mmol/g,而SPI接枝EDA后电荷由负转正为0.070 mmol/g。因为在水溶液中SPI表面暴有大量的羧基基团,羧基在水溶液中电离主要以 —COO— 形式存在[19]。而EDA接枝SPI多肽链上不仅消耗了羧基基团,还增加了SPI表面的氨基基团的数量,从而可以提高SPI接枝后的电荷密度。


表1 SPI和SPI-EDA 的电荷密度
2.4SPI-EDA聚集体的表征
由图8是SPI和SPI-EDA粒径分布图,可以看出 SPI平均流体力学半径为143 nm,这与文献中提到的结果相近[20],而SPI-EDA平均流体力学半径为251 nm,且SPI-EDA较SPI粒径分布较为均一。这是因为大豆分离蛋白多肽链上接上了含有氨基(—NH2)的EDA,接上的氨基与SPI本身的氨基基团发生相互排斥,使得SPI-EDA聚集体变得松散,聚集体的平均流体力学半径增大。
2.5SPI-EDA相对分子质量的表征
图9为SPI和SPI-EDA的高效液相色谱图,表2为SPI和SPI-EDA的各成分保留时间与质量分数对照表。从图10中可以看出,SPI和SPI-EDA分子质量的出峰时间为7.51、17.63、18.73 min,由此根据分子质量标准曲线lgMw=-0.099 1t+6.140 2可计算出两者的分子质量主要为248.8、24.7、19.1 ku。从表2中可以看出,SPI中不同分子质量组分所占的比例分别为8.45%、19.39%、72.16%,而SPI-EDA不同分子质量的组分比例为8.6%、74.86%、16.51%。通过对比可以发现分子质量为248.8 ku的组分比例基本不变,而分子质量为24.7和19.1 ku的组分变化明显,两者比例分别由19.39%增加到74.86% 和72.16%减小到16.51%。从中不难发现SPI接枝EDA后,主要是分子质量为19.1 ku组分与EDA发生了接枝。很可能这3种分子质量类型的聚集体是SPI中能够保持较为稳定的状态的组分。可能是分子质量较大的组分与小分子EDA(相对分子质量为60.10)接触的空间位阻大于分子质量较小的组分。


(a) SPI

(b) SPI-EDA
图8SPI和SPI-EDA 粒径分布图
Fig.8Particle size distribution of SPI-EDA
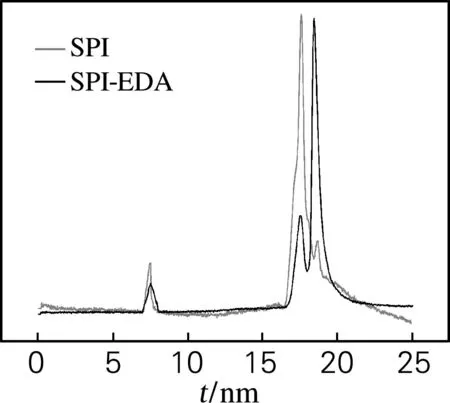
图9 SPI和SPI-EDA的高效液相色谱图

表2SPI和SPI-EDA各成分保留时间与百分含量对照表
Tab.2TheretentiontimeandthepercentageofthecontentsoftheSPIandSPI-EDA

样品t/min分子质量/kuw/%7.51248.88.45SPI17.6324.719.3918.7519.172.167.51248.88.60SPI-EDA17.6324.774.8618.7519.116.51
3结论
(1)SPI接枝EDA的最佳实验条件:反应温度为室温,反应时间4 h,大豆分离蛋白(SPI)、1-(3-二甲氨基丙基-3)-乙基碳二亚胺盐酸盐(EDC)、乙二胺(EDA)与N-羟基琥珀酰亚胺(NHS)用量摩尔比为1.0∶0.5∶0.6∶0.125。
(2)红外光谱分析证明EDA与SPI形成了化学连接。在二级结构中,接枝物SPI-EDA相对于SPI,α-螺旋增加了6.48%,β-折叠减少了17.38%,β-转角减少了1.53%,无规卷曲增加了12.42%。
(3)与SPI相比,SPI-EDA接枝物的电荷密度从-0.319 mmol/g增加到+0.070 mmol/g,聚集体的平均粒径从143 nm增加到251 nm左右。
(4)SPI-EDA与SPI对比可以发现分子质量为248.8 ku的组分比例基本不变,而分子质量为24.7和19.1 ku的组分变化明显。两者比例分别由19.39%增加到74.86%和72.16%减小到16.51%。
参考文献:
[1] PAL S, MAL D, SINGH R P. Cationic starch: an effective flocculating agent[J]. Carbohydrate Polymers, 2005, 59(4): 417-423.
[2] PAL S, MAL D, SINGH R P. Synthesis and characterization of cationic guar gum: a high performance flocculating agent[J]. Journal of Applied Polymer Science, 2007, 105(6): 3240-3245.
[3] SANG Y Z, XIAO H N. Preparation and application of cationic cellulose fibers modified by in situ grafting of cationic PVA[J]. Colloids and Surfaces A: Physicochemical and Engineering Aspects, 2009, 335(1): 121-127.
[4] LI H B, DU Y M, XU Y M. Adsorption and complexation of chitosan wet-end additives in papermaking systems[J]. Journal of Applied Polymer Science, 2004, 91(4): 2642-2648.
[5] JIN H Y, LUCIA L A, ROJIA O J, et al. Survey of soy protein flour as a novel dry strength agent for papermaking furnishes[J]. Journal of Agricultural and Food Chemistry, 2012, 60(39): 9828-9833.
[6] 刘晓亚,姜鹏,周华,等.大豆分离蛋白接枝氨基封端聚 2-丙烯酰胺基-2-甲基丙磺酸的合成及溶液性质[J].高分子学报,2009(5):430-436.
[7] 高党鸽,侯雪艳,吕斌,等.阳离子聚丙烯酸酯无皂乳液的合成与性能研究[J].功能材料,2013,44(2):187-190.
[8] 薛凤丽,卢大儒,郭佳,等.多肽Tat与CdTe量子点共价偶联后的跨膜转运[J].复旦学报(自然科学版),2006,45(3):298-302.
[9] 孔谦,柯渔,卢建波,等.含酚基羧甲基纤维素的合成及单分散微胶囊的制备[J].纤维素科学与技术,2011,19(2):10-15.
[10] 周名兵,胡盼,龚梅,等.双交联明胶-壳聚糖复合人工真皮支架的制备及其性能研究[J].功能材料,2012,43(11):1465-1468.
[11] 王迎军,杨春蓉,汪凌云.EDC/NHS交联对胶原物理化学性能的影响[J].华南理工大学学报(自然科学版),2007,35(12):66-70.
[12] 明津法,刘蓉,张焕相,等.EDC/NHS交联改性再生桑蚕丝素纳米纤维[J].高分子材料科学与工程,2012,28(10):162-165.
[13] 吴刚,沈玉华,谢安建,等.N,O-羧甲基壳聚糖的合成和性质研究[J].化学物理学报,2004,16(6):499-503.
[14]朱寿进,刘法谦,王璟朝,等.新型羧甲基壳聚糖水凝胶的合成与表征[J].高等学校化学学报,2014,35(4):863-868.
[15] DONG A, MATSUURA J, ALLISON S D, et al. Infrared and circular dichroism spectroscopic characterization of structural differences between β-lactoglobulin A and B[J]. Biochemistry, 1996, 35(5): 1450-1457.
[16] 任国栋,郭爱玲,耿放,等.二维红外相关光谱研究温度对卵转铁蛋白构象的影响[J].光谱学与光谱分析,2012,32(7):1780-1784.
[17] 孙冰玉,刘琳琳,张光,等.高温高湿对大豆分离蛋白二级结构及乳化性的影响[J].大豆科技,2014(4):26-31.
[18] HOU D H, ChANG S K C. Structural characteristics of purified glycinin from soybeans stored under various conditions[J]. Journal of Agricultural and Food Chemistry, 2004, 52(12): 3792-3800.
[19] 任俊莉,邱化玉,付丽红.胶原蛋白及其在造纸工业中的应用[J].中国造纸学报,2003,18(2):106-110.
[20] 周华,姜鹏,杨成,等.原子转移自由基聚合法合成大豆分离蛋白-g-聚甲基丙烯酸2-羟乙酯[J].高分子学报,2008(5):424-429.
Synthesis and properties of grafted copolymers based on soy protein isolated with ethylenediamine
YUANMingkun,XUChu,ZHOUJinghui
( School of Light Industry and Chemical Engineering, Dalian Polytechnic University, Dalian 116034, China )
Abstract:Grafted copolymer (SPI-EDA) was prepared by grafting reaction between the free carboxylic acid groups of soy protein isolate (SPI) and the amino groups of ethylenediamine (EDA) using 1-(3-(dimethylamino)propyl)-3-ethyl-carbodiimide hydrochloride (EDC) and N-hydroxysuccinimide (NHS) as the condensing agents. The optimal condition for synthesis of SPI-EDA was as follows: room temperature of reaction temperature, 4 h of reaction time, 1∶0.5∶0.6∶0.125 molar ratio of SPI, EDC, EDA and NHS. The chemical structure and physical property of SPI-EDA was analyzed by laser particle size/Zeta potential, FT-IR, HPLC and PCD, respectively. The results revealed that EDA was grafted onto the carboxyl group of SPI. The charge density and molecular weight of SPI-EDA were improved compared with SPI, and the size of SPI-EDA aggregates was increased and the distribution was uniform.
Key words:soy-protein-isolate; 1-(3-(dimethylamino)propyl)-3-ethyl-carbodiimidehydrochloride; ethylenediamine, soy protein isolate-ethylenediamine graft copolymer(SPI-EDA)
作者简介:袁明昆(1991-),男,硕士研究生;通信作者:周景辉 (1957-),男,教授.
基金项目:国家科技支撑计划项目(2013BAC01B03).
收稿日期:2015-09-07.
中图分类号:TS727
文献标志码:A
文章编号:1674-1404(2016)01-0023-06
