溢油分散剂中吐温80对石油中多环芳烃在海水中光降解的影响
2016-03-17陈启宁谢晴
陈启宁,谢晴
1. 大连理工大学化工学院,大连 116024;2. 工业生态与环境工程教育部重点实验室,大连理工大学环境学院,大连 116024
溢油分散剂中吐温80对石油中多环芳烃在海水中光降解的影响
陈启宁1,谢晴2,*
1. 大连理工大学化工学院,大连 116024;2. 工业生态与环境工程教育部重点实验室,大连理工大学环境学院,大连 116024
溢油事故发生后喷洒溢油分散剂是常用的应急措施之一,这使得溢油分散剂中的表面活性剂与石油中的重要污染物多环芳烃(PAHs)在海水中共存。光化学转化是水中PAHs的重要转化途径,这些共存表面活性剂如何影响PAHs在海水中的光化学消减还有待阐明。本研究选取溢油分散剂的重要活性成分吐温80和石油中2种不同类型的PAHs(菲和二苯并噻吩),通过光化学实验考察不同浓度吐温80对菲(PHE)和二苯并噻吩(DBT)在海水中的光降解速率常数和光解量子产率的影响,并通过量子化学计算的手段研究其影响机制。研究发现:吐温80可以使PHE和DBT的阳离子自由基回到稳定的基态,降低PHE和DBT的光解量子产率,从而抑制PHE和DBT的光降解。该结果表明,在评价溢油分散剂的风险性时不可忽视其对PAHs环境转化行为的影响。
溢油分散剂;表面活性剂;多环芳烃;光降解;海水
近年来,海洋溢油事故频发,造成了巨大经济损失,严重污染海洋环境,影响海洋生态系统健康,并通过食物链影响人体健康[1]。喷洒溢油分散剂是最常见的溢油应急处理方法之一,溢油分散剂的主要活性组分是表面活性剂,通过减小水和油间的表面张力,分散海面上的油膜[2]。2010年6月26日墨西哥湾输油管道爆炸后,超过3.7×1012t的溢油分散剂投入墨西哥湾。吐温80是多种溢油分散剂的共有成分[3]。
石油的主要成分为烷烃和芳烃,其中多环芳烃(PAHs)是联合国环境规划署提出的持久性有毒物质(PTS)。溢油是海洋/海湾中PAHs的重要来源[4]。据Pérez等[5]研究,2002年西班牙海域“威望号”轮船漏油事件17个月后,漏油海域海鸟血液中PAHs的浓度比非漏油区海鸟体内的浓度高30%。以往研究[6-12]表明,光化学转化是环境中PAHs的主要降解方式,其主要降解途径为:PAHs吸光后生成激发态的分子(PAHs*),PAHs*具有较高的活性,可以通过2种反应途径进一步降解:(1) PAHs*把氧气(O2)敏化成具有反应活性的单线态氧(1O2),1O2把PAHs氧化降解;(2) PAHs*发生自离子化,失去一个电子,生成阳离子自由基,再生成降解产物[7-8]。
PAHs的光化学转化动力学受其所在的介质及其中共存组分的影响。例如,PAHs在炭黑表面的光降解远远慢于在水中和松针表面的光降解[6-7,10];此外,水中存在的溶解性有机质(DOM)在光照时也能产生一些具有高活性的自由基,进而加快PAHs的降解;DOM也可能通过与PAHs竞争吸收光或淬灭自由基,从而抑制PAHs的光解[11-12]。肖翔和张勇[13]的研究表明,表面活性剂可以影响蒽在纯水中的光解,且不同表面活性剂的影响不同,推测其与蒽存在于表面活性剂胶束的内壳或外壳有关,但具体的影响机制还有待进一步揭示。鉴于此,本研究选取溢油分散剂的重要成分吐温80,以及2种代表性PAHs—菲(PHE)和二苯并噻吩(DBT)开展研究(图1),通过光化学实验和量子化学计算相结合的方法,探讨吐温80对这2种不同PAHs在海水中光降解速率和量子产率的影响及其内在机制,为阐明溢油分散剂对PAHs在海水中光降解的影响奠定基础。该研究有助于评价PAHs类污染物在海水中的光降解行为。

图1 吐温80、菲和二苯并噻吩的结构式Fig. 1 Structures of Tween 80, phenanthrene and dibenzothiophene
1 材料与方法(Materials and methods)
1.1 实验材料
吐温80购自美国Sigma-Aldrich公司,PHE(纯度97%)和DBT(纯度97%)购自日本TCI公司。采用二元化学露光剂“对硝基苯甲醚/吡啶”(PNA/pyr)测定PHE和DBT的光解量子产率[14],其中对硝基苯甲醚(纯度97%)购自美国Alfa Aesar公司,吡啶(色谱纯)购自天津科密欧化学试剂有限公司。海水取自大连星海湾(E 121°33'49.19", N 38°52'34.83"),水样过0.22 μm滤膜,pH值为8.1,冷冻保存备用。
1.2 光化学实验
光解实验在旋转式光化学反应仪(XPA-1型,南京胥江机电厂)中进行,以500 W汞灯为光源,采用290 nm滤光片模拟到达地面的太阳光。灯的发射光谱采用分光辐射光谱仪(SP-300i,美国Acton Research公司)测定,滤光片的透过光谱采用紫外-可见分光光度计(U2800,日本Hitachi公司)测定。
光解液以大连星海湾海水为溶剂,乙腈为助溶剂(乙腈的体积比为0.5%),PAHs的浓度为0.05 mg·L-1。由于吐温80的临界胶束浓度为13~15 mg·L-1[15],本研究考虑了小于和大于临界胶束浓度的情况,设置其浓度梯度为:0、5、10、15和20 mg·L-1,光解液置于石英试管中,反应仪内保持通风,以控制温度为(25 ± 1) ℃。每组实验重复3次,同时实验中设置暗对照以验证光解是否为目标物的唯一降解途径。选用化学露光剂PNA/pyr为参比测定PHE和DBT的量子产率,其中,对硝基苯甲醚和吡啶的浓度分别为10和100 μmol·L-1,此时硝基苯甲醚的光解量子产率ΦPNA= 0.000324[14]。
1.3 仪器分析方法
采用高效液相色谱(Agilent 1100-HPLC)的荧光检测器分析PHE和DBT的浓度,激发波长和检测波长分别为250 nm和360 nm,色谱柱选用Zorbax XDB-C18色谱柱(长15 cm,内径3 mm,填料粒径为3.5 μm),进样量为20 μL,流动相为乙腈和水(V∶V=8∶2),流速为0.4 mL·min-1。
对硝基苯甲醚的分析采用高效液相色谱二极管阵列检测器进行,色谱条件为:Zorbax XDB-C18色谱柱,进样量为20 μL,流动性相为乙腈和水(V∶V =1∶1),流速为0.4 mL·min-1,检测波长为300 nm。
1.4 量子化学计算
量子化学计算采用Gaussian 09软件[16]实现。选用B3LYP密度泛函中的3-21+G(d,p)基组进行吐温80以及2种PAHs的分子结构优化、频率分析及能量的计算。所有的能量计算都基于经过频率分析确认的最优结构进行。基于含时的密度泛函理论(TD-DFT)进行吐温80和PAHs激发单线态(S1)和激发三线态(T1)的计算。
2 结果与讨论(Results and discussion)
2.1 吐温80对PHE和DBT光解速率和光解量子产率的影响
PHE、DBT和吐温80的紫外可见吸收光谱以及实验光源的相对发射光谱如图2所示。可以看出290 nm以上PHE和DBT均有一定的光吸收。暗对照实验表明,在无光照时,420 min内PHE和DBT
均未发生可观测到的降解。在实验光源照射下,PHE和DBT均发生明显的光降解。对不同吐温80浓度下PHE和DBT的光降解进行动力学拟合,发现其均遵循准一级反应动力学,即ln(c/c0) (c0和c分别为PHE或DBT的初始浓度和在t时刻的浓度)与光照时间t呈线性关系,相关系数r > 0.97。2种PAHs的光解速率常数、半减期和光解量子产率列于表1。
由表1可以看出,PHE和DBT的光解半减期分别在(4.79 ± 0.57) h ~ (2.95 ± 0.18) h和(4.25 ± 0.31) h~ (2.60 ± 0.08) h之间,光解量子产率分别在(0.66 ± 0.08) × 10-3~ (1.13 ± 0.07) × 10-3和(1.68 ± 0.13) × 10-3~ (2.74 ± 0.08) × 10-3之间。未加吐温80的海水中PHE的光解量子产率比文献中报道的纯水中的量子产率数值(3.5 ± 0.5) × 10-3略低[8],海水中DBT的光解量子产率比PHE高1 ~ 2倍,与文献中报道的DBT在纯水中的光解量子产率(2.1 × 10-3)相近[18]。肖翔[19]对蒽和芘在纯水和模拟海水中光解的研究表明,盐度影响PAHs的光解动力学,蒽和芘在海水中的光解速率快于在纯水中。
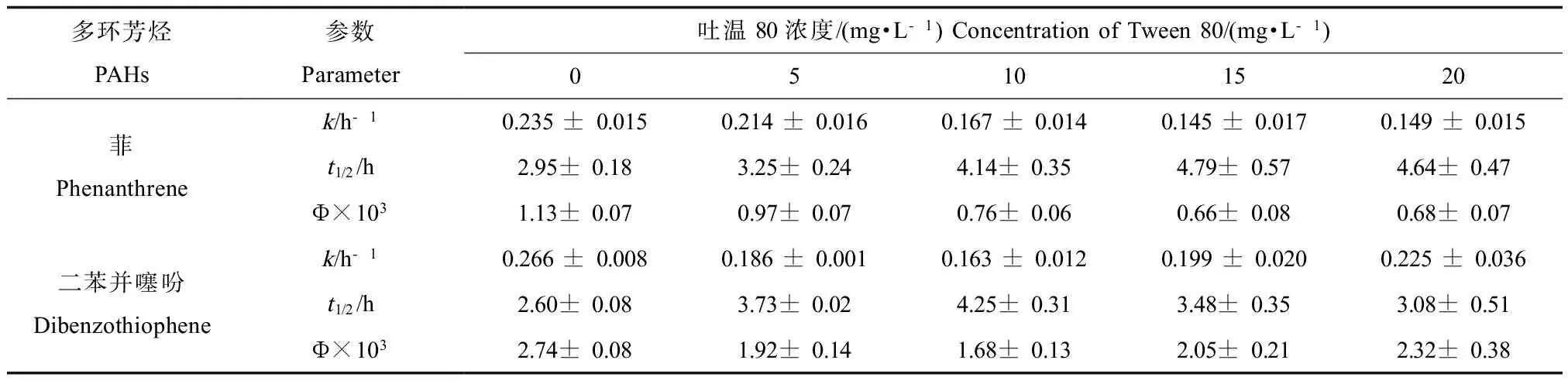
表1 不同浓度吐温80共存下,菲和二苯并噻吩在海水中的光解速率常数(k)、光解半减期(t1/2)和光解量子产率(Φ)Table 1 Photodegradation rate constants (k), half-lives (t1/2) and quantum yields (Φ) of phenanthrene and dibenzothiophene in seawater under different Tween 80 concentrations
注:k和t1/2的误差为3次重复实验的标准偏差;Φ的误差根据Boreen等[17]描述的灵敏度分析得到。
Note: Reported error of k and t1/2represents the standard deviation from the mean of three experiments, and the errors of Φ were estimated through a sensitivity analysis method described by Boreen et al.[17].
吐温80抑制了PHE的光降解速率,加入5、10、15、20 mg·L-1的吐温80对PHE光解速率的抑制率分别为9%、29%、38%和36%。特别是吐温80的浓度≤10 mg·L-1时,对PHE光解速率的抑制效应明显。随着吐温80浓度继续增大,PHE光解速率不再有显著变化。对DBT的光降解,吐温80的抑制作用先增大,后减小。吐温80的加入也降低了PHE和DBT的光解量子产率,并且其量子产率随浓度的变化趋势与其光解速率常数的变化趋势相同。这说明,吐温80的加入影响了PHE和DBT对光子的利用效率,从而影响着2种PAHs的光解半减期。Sigman等[20]也发现,在纯水中加入非离子型表面活性剂Brij 35,减小了芘的光解量子产率,推测其原因是表面活性剂抑制了芘光解过程中的电荷分离。本研究将进一步以PHE和DBT为例探讨吐温80抑制其光解量子产率的原因。
2.2 吐温80影响PHE和DBT光解的内在机制2.2.1 吐温80的光屏蔽效应
由图2可以看出,吐温80和2种PAHs的紫外-可见吸收光谱以及实验光源的光谱,在290 ~ 305 nm范围内有重合,说明吐温80与2种PAHs存在竞争光吸收。根据Zhang等[21]的评价腐殖酸光屏蔽因子方法(式1)计算了不同浓度吐温80的光屏蔽因子Sλ,并进一步根据式(2)和式(3)计算了不同吐温80浓度下,2种PAHs的相对光吸收(以不添加吐温80时的光吸收为基准),计算结果列于表2中。由表2可以看出,吐温80对PAHs的光屏蔽效应很小,可以忽略。
(1)

(2)
(3)

2.2.2 吐温80对PHE和DBT光解量子产率的影响机制
根据PHE和DBT的直接光解机理[7-8],分析吐温80减弱这2种PAHs量子产率的原因有:(1)吐温80把吸收光子后跃迁到激发态PAHs的分子(PAHs*)淬灭到基态PAHs;(2)吐温80把PAHs光解离生成的阳离子自由基(PAHs·+)淬灭到PAHs;(3)吐温80和1O2反应,阻碍了PAHs和1O2的反应。其中,吐温80和PAHs*的反应分2种:与激发单线态(S1)反应和与激发三线态(T1)反应。由于吐温80的化学性质较为稳定,并且1O2的氧化活性相对较弱,因此1O2很难氧化吐温80。对于原因(1)和(2)是否成立,可以通过下面3个反应的吉布斯自由能变(△G)进行判断[21],若反应1和反应2均可以发生或有一个可以发生,则原因1成立,若反应3可以发生,则原因2成立。
吐温80 + PAHs(S1)*→ 吐温80(S1)*+ PAHs
(反应1)
吐温80 +PAHs(T1)*→ 吐温80(T1)*+PAHs
(反应2)
吐温80 +PAHs·+→ 吐温80·++PAHs
(反应3)
根据Kavarnos和Turro的研究[22],对于电子转移反应和激发态的反应,在反应的瞬间分子结构变化很小,体系的熵变可以不考虑;对于在溶液里的反应,体积及压力的变化可以忽略;因此,常用反应体系能量(E)的变化来衡量△G。3个反应的△G可根据下面的公式计算:
反应(1):△G = E吐温80(S1)+ EPAHs- E吐温80- EPAHs(S1)
= (E吐温80(S1)- E吐温80) - (EPAHs(S1)- EPAHs)
=VE吐温80(S1)- VEPAHs(S1)

表2 菲和二苯并噻吩在含有不同浓度吐温80的海水中的相对光吸收Table 2 Relative light absorption of phenanthrene and dibenzothiophene in seawater with different concentration of Tween 80
反应(2):△G = E吐温80(T1)+ EPAHs- E吐温80- EPAHs(T1)
= (E吐温80(T1)- E吐温80) - (EPAHs(T1)- EPAHs)
=VE吐温80(T1)- VEPAHs(T1)
反应(3):△G = E吐温80·++ EPAHs- E吐温80- EPAHs·+
= (E吐温80·+- E吐温80) - (EPAHs·+- EPAHs)
=VIE吐温80- VIEPAHs
其中,VE吐温80(S1)和VEPAHs(S1)分别为吐温80和PAHs到达S1态的垂直激发能、VE吐温80(T1)和VEPAHS(T1)分别为吐温80和PAHs到达T1态的垂直激发能,VIE吐温80和VIEPAHs分别为吐温80和PAHs的垂直电离能。通过量子化学计算,得到以上参数的数值,结果列于表3中。根据这些参数值计算得到:对于PHE,反应(1~3)的△G分别为131.4 kJ·mol-1、126.2 kJ·mol-1和-15.6 kJ·mol-1;对于DBT,反应(1~3)的△G分别为121.1 kJ·mol-1、86.7 kJ·mol-1和-21.2 kJ·mol-1。这说明,对于PHE和DBT,反应(1)和(2)均不能自发进行,即吐温80不能将PAHs*淬灭到PAHs,反应(3)在热力学上是可以自发进行的,即吐温80可以与PHE和DBT的阳离子自由基反应,将其淬灭到初始形态,从而减小其光解量子产率(图3)。
本研究面向海洋溢油事故发生后喷洒溢油分散剂带来的环境问题,结合量子化学计算和模拟光照实验,考察了溢油分散剂的重要成分对2种PAHs在海水中光化学行为的影响机制,发现表面活性剂吐温80可以淬灭PHE和DBT的阳离子自由基,使其返回基态,进而降低PHE和DBT的光解量子产率。这些结果表明溢油分散剂的一些表面活性剂可能抑制溢油中PAHs类污染物在海水环境中的光降解。由于溢油中PAHs的种类很多,用于海洋溢油事故应急处理的表面活性剂种类也很多,仍有必要针对其他表面活性剂及商品化溢油分散剂对多种PAHs光化学行为的影响开展进一步的研究,以探明溢油分散剂对PAHs在海水中光化学行为的影响规律。
[1] 杨昊炜, 柴田. 浅谈溢油污染对海洋环境的危害[J]. 天津航海, 2007(4): 13-15
[2] 徐玲玲. 海洋溢油污染的应急处理[J]. 海洋环境保护, 2011(3): 17-19
[3] Judson R S, Martin M T, Reif D M, et al. Analysis of eight oil spill dispersants using rapid, in vitro test for endocrine and other biological activity [J]. Environmental Science & Technology, 2010, 44(15): 5979-5985
[4] Wells P G. Oil and seabirds: The imperative for preventing and reducing the continued illegal oiling of the sea by ships [J]. Marine Pollution Bulletin, 2001, 42(4): 251-252
[5] Pérez C, Velando A, Munilla I, et al. Monitoring polycyclic aromatic hydrocarbon pollution in the marine environment after the Prestige oil spill by means of seabird blood analysis [J]. Environmental Science & Technology, 2008, 42(2): 707-713
[6] Behymer T D, Hites R A. Photolysis of polycyclic aromatic hydrocarbons adsorbed on simulated atmospheric particulates [J]. Environmental Science and Technology, 1985, 19(10): 1004-1006
[7] Barbas J T, Sigman M E, Dabestani R. Photochemical oxidation of phenanthrene sorbed on silica gel [J]. Environmental Science & Technology, 1996, 30(5): 1776-1780
[8] Fasnacht M P, Blough N V. Aqueous photodegradation of polycyclic aromatic hydrocarbons [J]. Environmental Science & Technology, 2002, 36(20): 4364-4369
[9] Niu J F, Chen J W, Martens D, et al. Photolysis of polycyclic aromatic hydrocarbons adsorbed on spruce [Picea abies (L.) Karst.] needles under sunlight irradiation [J]. Environmental Pollution, 2003, 123(1): 39-45
[10] Wang D G, Chen J W, Xu Z, et al. Disappearance of polycyclic aromatic hydrocarbons sorbed on surfaces of pine [Pinua thunbergii] needles under irradiation of sunlight: Volatilization and photolysis [J]. Atmospheric Environment, 2005, 39(25): 4583-4591
[11] 李恭臣, 夏星辉, 周追, 等. 富里酸在水体多环芳烃光化学降解中的作用[J]. 环境科学学报, 2008, 28(8): 1604-1611
Li G C, Xia X H, Zhou Z, et al. Effects of fulvic acid on photolysis of polycyclic aromatic hydrocarbons in aqueous solution [J]. Acta Scientiae Circumstantiae, 2008, 28(8): 1604-1611 (in Chinese)
[12] Sanches S, Leitão C, Penetra A, et al. Direct photolysis of polycyclic aromatic hydrocarbons in drinking water sources [J]. Journal of Hazardous Materials, 2011, 192(3): 1458-1465
[13] 肖翔, 张勇. 表面活性剂存在下水溶液中溶解态蒽的光降解[J]. 环境化学, 2009, 28(5): 687-690
Xiao X, Zhang Y. Effects of surfactants onphotodegradation of dissolved anthracene [J]. Environmental Chemistry, 2009, 28(5): 687-690 (in Chinese)
[14] Dulin D, Mill T. Development and evaluation of sunlight actinometers [J]. Environmental Science & Technology, 1982, 16(11): 815-820
[15] 李隋, 赵永胜, 徐巍, 等. 吐温80对硝基苯的增溶作用和无机电解质作用机理研究[J]. 环境科学, 2008, 29(4): 920-924
Li S, Zhao Y S, Xu W, et al. Solubilization of nitrobenzene in micellar solutions of Tween 80 and inorganic salts [J]. Environmental Science, 2008, 29(4): 920-924 (in Chinese)
[16] Frisch M J, Trucks G W, Schlegel H B, et al. Gaussian 09 [CP]. Revision A.02. Wallingford, CT: Gaussian, Inc., 2009
[17] Boreen A L, Arnold W A, McNeill K. Photochemical fate of sulfa drugs in the aquatic environment: Sulfa drugs containing five-membered heterocyclic groups [J]. Environmental Science & Technology, 2004, 38(14): 3933-3940
[18] Shemer H, Linden K G. Aqueous photodegradation and toxicity of the polycyclic aromatic hydrocarbons fluorine, dibenzofuran, and dibenzothiophene [J]. Water Research, 2007, 41(4): 853-861
[19] 肖翔. 溶解态混合组分蒽和芘的光降解及表面活性剂对蒽或芘光降解的影响[D]. 厦门: 厦门大学, 2009: 25-28
Xiao X. Photodegradation of dissolved anthracene and pyrene in a mixture and the effect of surfactant on the photodegradation of dissolved anthracene or pyrene [D]. Xiamen: Xiamen University, 2009: 25-28 (in Chinese)
[20] Sigman M E, Schuler P F, Ghosh M M, et al. Mechanism of pyrene photochemical oxidation in aqueous and surfactant solutions [J]. Environmental Science & Technology, 1998, 32(24): 3980-3985
[21] Zhang S Y, Chen J W, Qiao X L, et al. Quantum chemical investigation and experimental verification on the aquatic photochemistry of the sunscreen 2-phenylbenzimidazole-5-sulfonic acid [J]. Environmental Science & Technology, 2010, 44(19): 7484-7490
[22] Kavarnos G J, Turro N J. Photosensitization by reversible electron transfer: Theories, experimental evidence, and examples [J]. Chemical Reviews, 1986, 86(2): 401-449
◆
Effects of Tween 80 in Oil Spill Dispersants on Photodegradation of PAHs from Spilled Oil in Seawater
Chen Qining1, Xie Qing2,*
1. School of Chemical Engineering, Dalian University of Technology, Dalian 116024, China 2. Key Laboratory of Industrial Ecology and Environmental Engineering (MOE), School of Environmental Science and Technology, Dalian University of Technology, Dalian 116024, China
Received 31 August 2016 accepted 9 October 2016
Spraying a large amount of oil spill dispersants is one of the most common ways to deal with oil spill accidents, which lead to the coexistence of surfactants and polycyclic aromatic hydrocarbon (PAHs) pollutants from spilled oil. Photodegradation is a main transformation pathway of PAHs in sea water. However, effects of the surfactants on the photodegradation of PAHs in sea water are still need further clarification. In this study, a common surfactant in oil spill dispersants, Tween 80, was selected to investigate its effects on the photodegradation rates and quantum yields of two typical PAHs in oil, i.e., phenanthrene (PHE) and dibenzothiophene (DBT). The influence mechanism of Tween 80 was probed by the quantum calculation. The results showed that Tween 80 decreased the photodegradation rates of PHE and DBT, due to decreasing the quantum yields of PHE and DBT by reacting with the PAH cation radicals. It is indicated that the effects of the oil spill dispersants on the environmental transformation of PAHs should be considered when assessing its environmental risks.
oil spill dispersants; surfactants; PAHs; photodegradation; seawater
国家自然科学基金(21207013);大学生创新训练计划项目(201410141354)
陈启宁(1995-),女,本科生,专业为化学工程与工艺,E-mail: qnchen@mail.dlut.edu.cn;
*通讯作者(Corresponding author), E-mail: qingxie@dlut.edu.cn
10.7524/AJE.1673-5897.20160831002
2016-08-31 录用日期:2016-10-09
1673-5897(2016)6-061-06
X171.5
A
谢晴(1983—),女,环境工程博士,工程师,主要研究方向为有机污染物的分离分析及环境转化,近五年发表学术论文20余篇。

图3 吐温80(T80)淬灭菲和二苯并噻吩(PAHs)光转化过程中瞬态物种的可能反应途径
注:*代表激发态,△G、S1和T1分别为反应吉布斯自由能、第一激发单线态和第一激发三线态。
Fig. 3 Possible reactions for Tween 80 (T80) to quench the transient species of phenanthrene and dibenzothiophene (PAHs) formed during the phototransformation
Note: * represents the excitation state. △G, S1 and T1 are Gibbs free energy change, first singlet excitation state and triplet excitation state, respectively.
表3 菲(PHE)、二苯并噻吩(DBT)和吐温80(Tween 80)到达第一激发单线态和三线态的
垂直激发能(VES1, VET1)和垂直电离能(VIE)
Table 3 The lowest singlet and triplet vertical excitation energy (VES1, VET1), and vertical ionization energy (VIE) for phenanthrene (PHE), dibenzothiophene (DBT) and Tween 80
化合物CompoundsVES1/(kJ·mol-1)VET1/(kJ·mol-1)VIE/(kJ·mol-1)PHE390.7237.2752.0DBT401.1312.6757.6Tween80522.1399.4736.4
陈启宁, 谢晴. 溢油分散剂中吐温80对石油中多环芳烃在海水中光降解的影响[J]. 生态毒理学报,2016, 11(6): 61-66
Chen Q N, Xie Q. Effects of Tween 80 in oil spill dispersants on photodegradation of PAHs from spilled oil in seawater [J]. Asian Journal of Ecotoxicology, 2016, 11(6): 61-66 (in Chinese)
