含银微纳米复合材料在生物医学应用的研究进展
2016-03-04李明熹
丁 琪,李明熹,杨 芳,2,顾 宁,2
(1.东南大学生物科学与医学工程学院 江苏省生物材料与器件重点实验室生物电子学国家重点实验室,江苏 南京210096)(2.苏州纳米科技协同创新中心纳米药物与生物材料专业中心,江苏 苏州 221009)

含银微纳米复合材料在生物医学应用的研究进展
丁琪1,李明熹1,杨芳1,2,顾宁1,2
(1.东南大学生物科学与医学工程学院 江苏省生物材料与器件重点实验室生物电子学国家重点实验室,江苏 南京210096)(2.苏州纳米科技协同创新中心纳米药物与生物材料专业中心,江苏 苏州 221009)
摘要:近些年来,微纳米复合材料发展十分迅速。微纳米复合材料通常由两种或以上的不同材料组成在一个单元结构里,藉此具有多功能的、功能增强或协同增强的特性。含银微纳米复合材料是其中重要的研究分支,在当前生物医学应用中取得了众多的功能集成或功能增强等研究成果。主要综述了银/聚合物和银/氧化铁两类微纳复合材料,首先总结了银/聚合物和银/氧化铁微纳复合材料的制备方法,包括乳液聚合法、原位生成/还原法、空穴法、离子交换法、一锅法、种子法、静电作用法以及胶束法等;其次,总结了银/聚合物和银/氧化铁复合材料在表面增强拉曼散射、光学成像、抗菌抗癌、免疫检测、电化学检测、催化降解等生物医学领域的应用,以及对未来发展趋势的展望。
关键词:银/聚合物微纳米复合材料;银/氧化铁微纳米复合材料;生物医学应用
1前言
纳米复合材料近些年吸引了众多研究者的关注,发展十分迅速。纳米复合材料通常由两种或以上的不同材料组成在一个单元结构里,藉此具有多功能的、功能增强或协同增强的特性[1-3]。在纳米尺度下,作为单一成分材料,贵金属银因其拥有独特的光学、电学和生物学特性,而被广泛深入地研究其在生物医学领域的应用,比如表面增强拉曼散射(SERS)、光学成像、抗菌抗癌、免疫检测、电化学检测、催化降解等[4]。近年来,为了进一步拓展纳米银的应用前景,将其与聚合物材料、纳米氧化铁、纳米金等其它的有机或无机材料组装在一起而得到的含银微纳米复合材料逐渐成为研究热点,并在生物医学应用中彰显出众多的功能集成或功能增强等优势。
以银纳米颗粒填充聚合物合成功能性银/聚合物微纳米复合材料已经取得很大进展,已报道的聚合物有聚乙烯醇、聚吡咯、聚苯乙烯、聚甲基丙烯酸甲酯等。银/聚合物复合材料的优势在于材料的总体接触面积非常大,所以纳米尺度的材料往往具有与宏观材料非常不同的性质,当分散颗粒(银纳米颗粒)与基底材料(聚合物)的性质充分结合起来时,将对基体的物理和化学性质产生特殊的作用。银/聚合物复合材料同时具有了纳米银和聚合物材料的优良特性,并赋予该类型复合材料一些特异或新的功能,从而使其在光子学、电子学、生物医学和信息材料学等诸多领域具有广阔的应用前景。
此外,银/氧化铁微纳米复合材料也是含银微纳米复合材料的重要分支。氧化铁因其丰富的磁学特性和良好的生物相容性,在生物医学领域里亦有着广泛的应用。目前已有一些研究者们成功地将纳米银和氧化铁构建在一个纳米单元结构中,并赋予了银/氧化铁微纳米复合材料具有彼此的磁性、光学、等离子体共振、磁光等特性,应用于生物医学领域中获得了很多集成银和氧化铁材料功能于一体或增强的研究数据。
本文就近年来银/聚合物和银/氧化铁微纳米复合材料的制备方法进行了概要的总结,综述了这些复合材料在表面增强拉曼散射、光学成像、抗菌抗癌、免疫检测、电化学检测、催化降解等生物医学领域的应用前景。
2含银微纳米复合材料的制备方法
2.1银/聚合物微纳米复合材料的制备方法
银/聚合物复合材料有多种制备方法,其中比较常见的有:乳液聚合法、原位生成法、空穴法、离子交换法和自组装法等等[5]。
2.1.1乳液聚合法
乳液聚合法是通过聚合物对银纳米颗粒的直接包覆,直接将纳米颗粒加入水中,通过物理的方法使聚合物在形成微囊结构过程中包裹银纳米颗粒,使银纳米颗粒嵌入膜壳内。Yang Fang等[6]在文章中提到了银纳米颗粒嵌入式微气泡的制备方法。简单说来该方法为,聚乳酸(PLA)溶解于10 mL二氯甲烷中,25 ℃,初次搅匀;有机溶液中加入1 mL二次水和0.05 mL司班80,高速搅拌。之后将这个乳液加入到49 mL的聚乙烯醇(PVA, MW 31000)和1 mL包埋有银纳米颗粒的的PVA (MW 110000)的共混液中,机械搅拌2 h,之后形成稳定的乳液。为了去除多余的PVA和银纳米颗粒,通过离心的方法得到微囊沉淀,之后用pH=7.4的PBS溶液进行洗涤3次,之后纯化的银-聚合物微囊用甘露醇保护并且冻干,之后充入氮气并且密封保存。
2.1.2原位生成法
原位生成法是用制备银纳米颗粒的前体、或化合物与聚合物生成复合物质,使其与银离子形成络合物,然后使用还原剂反应,使银纳米颗粒直接在聚合物结构中生成,但这种方法银纳米颗粒在聚合物中的分散较差,难以形成均匀的银/聚合物复合结构。安静等[7]在离子液体1-丁基-3-甲基米唑氟硼酸盐中制备出稳定的Ag胶体,通过原位法制备出银-聚苯乙烯纳米核壳复合粒子。
2.1.3空穴法
该方法首先将聚合物材料制成具有特定结构的多孔材料,这些多孔结构可以看作一个个空穴而将银纳米颗粒嵌入到这些空穴中,或者使用银的化合物在这些空穴中均匀分散而后通过一系列方法生成银纳米颗粒。Zhang等[8]使用1,2-二氯乙烯在溶胀的聚苯乙烯胶体表面刻蚀出空穴,然后将银离子包覆在空穴中,通过银离子的还原使银纳米颗粒直接在空穴中生成。
2.1.4自组装法
自组装法主要是在一定条件下,分子与分子依赖非共价键分子间作用力自发连接成结构稳定的分子聚集体,得到具有新颖特性的自组装材料[9-10]。Lun Li等[11]报道了以対巯基苯胺(PATP)为介质,约1 nm银纳米颗粒自组装成薄层的银纳米叶片的研究。实验中,作者首先利用PATP将约4 nm银纳米颗粒刻蚀至1 nm纳米晶簇Ag25。然后PATP所含有的-SH/-NH2通过静电或共价作用与Ag25形成醌型Ag25-PATP-Ag25中间体,最后通过PATP邻近苯骨架的较强的偶极-偶极相互作用和π-π堆积作用,引发Ag25-PATP-Ag25有序自组装成Ag纳米叶片。该方法将来可被应用于制备均匀可控的银纳米颗粒与聚合物的复合材料。
2.2银/氧化铁微纳米复合材料的制备方法
众所周知,纳米氧化铁(Fe3O4和Fe2O3)和纳米银(Ag)晶格失配,因此设计专门的湿化学合成(Wet-Chemical Synthesis)路线制备银/氧化铁微纳米复合材料极具挑战性。异质外延的氧化铁/银纳米复合结构已报道有同中心或偏心的核壳结构[12-15]、相分离的核-卫星式(Core-Satellite)结构[16-19]和异聚体结构[20-21](图1)。

图1 氧化铁/银纳米复合结构TEM照片:(a) 核壳结构,(b)异聚体结构,(c) 核-卫星式结构Fig.1 TEM images of iron oxide/silver nanocomposites: (a) core-shell nanostructure, (b) heteromer nanostructure, (c) core-satellite nanostructure
2.2.1一锅法
在有机相和高温条件下,共混的有机或无机的铁和银前驱体经过一锅热分解(One-pot Thermal Decomposition)过程,从而获得银/氧化铁复合纳米粒子。该类一锅法合成实例获得的大多是异聚体纳米复合结构。Zhai Yueming等[22]以硝酸银和硝酸铁为前驱体,在乙二醇、二甘醇和聚乙烯吡咯烷酮(PVP)按比例混合为有机相条件下,采用一锅溶剂热法(One-pot Solvothermal Procedure),在200 ℃下维持10 h,即获得花瓣状Ag-Fe3O4纳米复合粒子。Chen Yingjie等[23]在十二烷醇有机相中,以油酸和油胺为封端剂,在220 ℃时注入乙酸银后维持1 h,后再降温至160 ℃注入乙酰丙酮铁反应2 h,得到核壳结构的Ag@Fe3O4纳米复合粒子,进而继续升温至220 ℃反应30 min,制备出异聚体结构的Ag-Fe3O4纳米复合粒子。
2.2.2原位还原法
该合成策略是在预制成的纳米粒子上设计可接受目标前驱体或种子的无机结合位点,藉此克服高界面能壁垒,然后进行原位还原或种子进一步生长,从而获得核壳、核-卫星式或异聚体结构的银/氧化铁纳米复合纳米粒子。通常预制成的纳米粒子的表面是形成以氨基、巯基、羧基等为端基的聚合物层、二氧化硅层、硅烷层、碳层。Bian Longchun等[24]将丙烯酸和苯胺(PANI)接枝共聚到共沉淀法制备的Fe3O4纳米粒子的表面,利用-NH2端基结合硝酸银中Ag+离子去建立异质成核中心,然后原位还原而获得Ag/PANI/Fe3O4纳米粒子。Xie Yijun等[25]用多巴胺(PDA)作为Fe3O4微球的修饰剂、锚固银氨离子的模板以及还原剂,制备得到Fe3O4@PDA-Ag微球。Jun Bong-Hyun等[18]热解油酸铁得18 nm的Fe3O4纳米粒子,通过反相微乳液法包覆上16 nm厚SiO2层,再用(3-巯基丙基)三甲氧基硅烷改性,利用-SH基结合Ag+离子,再用乙二醇还原即得到嵌入式的Fe3O4-Ag纳米粒子。Wang Hui等[26]将戊二铁、丙酮和双氧水共混置于高温高压反应釜中,经过24 h、200 ℃后制得Fe3O4@C纳米粒子,然后作为模版吸附和原位还原低浓度和高浓度Ag+,分别得到哑铃型和核-卫星式Fe3O4@C-Ag纳米粒子。
2.2.3种子法
该类方法通常预制成某一材料,然后目标材料的离子源化合物再以其为种子生长,得以将异质材料结合在一起。该类方法通常是发生在有机相,且多以异聚体形式结合。Matthew R. Buck等[21]在190 ℃下,通过氧还原反应,用痕量五羰基铁还原乙酰丙酮铂,制得约5 nm Pt纳米粒子。Pt纳米粒子作为种子的条件下,以十八烯为溶剂,油胺为稳定剂,热解五羰基铁,获得Pt-Fe3O4异质二聚体纳米粒子。又将Pt-Fe3O4纳米粒子作为种子,仍以油胺为稳定剂,乙酸银为银源,进一步生长即获得Ag-Pt-Fe3O4异质三聚体纳米粒子。
2.2.4静电作用法
该类方法通常将不同种纳米材料预先分别制备好,并修饰上目标聚电解质而携带正/负电荷,从而通过静电作用将不同种材料结合在一起。Zheng Tingting等[16]首先在200 ℃下,以六水合三氯化铁为铁前驱体,聚丙烯酸(PAA)为修饰剂,乙二醇为溶剂,采用溶剂热法制备得到了端基为羧基的亚微米级的Fe3O4磁珠,随后通过微波辅助在其表面再组装上一层强阳离子聚电解质聚二烯基丙二甲基氯化铵(PDDA)。利用电偶置换反应(Galvanic Replacement Reaction),以纳米立方银为牺牲模板而制备获得Ag-Pd双金属纳米笼。最后Ag-Pd 双金属纳米笼通过静电吸附方式附着在Fe3O4磁珠表面,获得Fe3O4@Ag-Pd 核-卫星式纳米粒子。
2.2.5胶束法
该类方法通常将预制成的某一纳米材料处于含有目标材料离子源的正相或反相胶束中,在液-液界面进行反应得到纳米复合材料。Gu Hongwei等[27]将热解法制得Fe3O4纳米粒子分散在正己烷中,与AgNO3溶液混合,50 ℃下超声乳化30 min,获得异二聚体Fe3O4-Ag纳米粒子。超声有助于将油相和水相充分混合,形成微乳液。液-液界面处,部分暴露在水相的Fe3O4纳米粒子的Fe2+离子作为自催化还原的Ag+离子的活性中心和成核点。
3含银微纳米复合材料在生物医学领域的应用前景
纳米银材料因其拥有独特的光学、电学和生物学特性,在表面增强拉曼散射、光学成像、抗菌抗癌、免疫检测、电化学检测、催化降解等生物医学领域有着广泛深入的研究。当纳米银与聚合物材料、纳米氧化铁、纳米金等其它的有机或无机材料组装在一起而得到含银微纳米复合材料,使得其集合了更多其它的力学、磁光等特性,在生物医学应用中彰显出众多的功能集成或功能增强等研究成果。
3.1抗菌抗癌性能
银离子的抗菌作用在历史上很早就有发现,从古代的各种银质器皿可以长时间保存食物或有益健康即可见一斑。银离子抗菌剂可能的作用机理概括为以下几个方面:干扰细胞壁的合成;损伤细胞膜;抑制蛋白质的合成;阻碍遗传信息的复制,包括DNA、RNA和mRNA的合成。然而,出于银离子生物安全性的争议,银的化合物及其离子作为抗菌剂却逐渐淡出了人们的视线。不过近年来由于人体对抗生素产生的耐药性问题,使人们聚焦于比普通银更具优异性能的纳米银材料。一些证据表明,纳米银产生的杀菌活性有可能是通过银离子的释放[28-29]。
虽然纳米银性质活泼,容易氧化变性,但是可通过制备银/聚合物复合物的方法去控制银纳米颗粒的银离子产生与释放来克服。银/聚合物复合材料的抗菌作用是通过银纳米颗粒与细菌等微生物细胞发生反应,对微生物产生不良的影响,这些不良影响和后果,最集中的表现就是影响微生物的生长、繁殖以致死亡。Varun Sambhy等[5]制备了一种高效双重抗菌的双组分复合材料,以聚(4-乙烯基-N-己基溴化吡啶鎓)阳离子聚合物为基底,嵌入溴化银纳米颗粒。该复合材料对革兰氏阳性菌和革兰氏阴性菌有较强的抑菌活性,同时对生物体无毒,可以作为一种很好的银离子杀菌剂。
相比纳米银,当纳米银与纳米氧化铁组装在一起,使得银/氧化铁微纳米复合材料的生物相容性得到提高,同时具有光学和磁学特性。Panagiotis Dallas等[30]将纳米银嵌入到包封有γ-Fe2O3纳米粒子的1,4-苯二胺/含磷三嗪环低聚物表面,这导致该纳米复合材料对一系列的细菌和酵母菌都具有高抗菌和抗真菌效果,最小抑制浓度低于100 mg Ag/mL,同时又能通过外加磁场从样品中分离出来。Morteza Mahmoudi等[31]在Fe3O4纳米粒子表面包裹上一层纳米Ag环,将其作为一种新型抗耐药的抗菌剂,作为可取代抗生素的候选用剂。该纳米Ag环包裹的Fe3O4纳米复合材料对HepG2细胞没有表现出细胞毒性作用,具有极好的生物相容性。该纳米复合材料增强了银的抗菌活性,对金黄色葡萄球菌感染和表皮葡萄球菌感染有着高的治疗指数,其主要机制不仅是源自Ag环促进细菌中活性氧上调,而且在外加磁场刺激下该纳米复合材料能够渗透入细菌生物膜。
3.2光学性能
贵金属银纳米结构独特的光场增强光学特性,是源自其自由电子的共振响应,即局域的表面等离子体共振。等离子体共振能够辐射发光(米氏散射),能够被运用于表面增强拉曼散射(SERS)、光学成像等生物医学领域。而含银微纳米复合材料却被给予了更多的特性,拓宽和增强了它们的应用。
3.2.1表面增强拉曼散射
吸附在粗糙化金属表面的化合物由于表面局域等离子激元被激发引起电磁增强(即物理增强),以及粗糙表面上的原子簇及吸附其上的分子构成拉曼增强的活性点(即化学增强),这两者的作用使被测定物的拉曼散射产生极大的增强效应,其增强因子可达103~7数量级。已发现能产生SERS的金属有Ag,Au,Cu和Pt等少数金属,以Ag的增强效应为最佳,最为常用。
朱双美、范春珍等[32]研究了自组装银纳米颗粒以及其拉曼增强效应,硅烷化的玻片上的聚合物与银纳米颗粒结合,形成聚合物-银纳米颗粒复合物,能够获得强度较高的SERS效应。Jun Bong-Hyun等[18]构建了具有SERS活性和靶向性的Fe3O4@Ag@SiO2纳米粒子。相比银纳米粒子,该纳米复合粒子通过磁富集将邻氯苯硫酚和3,4-二氯苯硫酚的SERS信号增强了100倍。在该纳米复合粒子表面偶联上抗体(HER2 Ab或CD10 Ab),可靶向乳腺癌细胞(SKBR3)和白血病细胞(SP2/O),可通过磁分离与未靶向的细胞分离,且可被检测出拉曼信号。Clement Yuen等[14]亦以Fe3O4@Ag作为可磁富集的SERS的基底,用于早期疟疾诊断。Melisew Tadele Alula等[33]用Fe3O4@ZnO@Ag纳米复合粒子作为SERS基底来检测尿液中的肌酐酸。肌酐酸浓度高达1 μM,其SERS强度仍呈线性关系;肌酐酸浓度低至0.1 μM,仍可检测出其SERS信号。
3.2.2光学成像
近年来对于多模态造影复合材料的研究迅速发展。微气泡在诊断超声频率下具有良好的超声回波反射信号,是目前常用的超声造影剂。Yang等[6]通过对微气泡进行改进,使之膜壳带有银纳米颗粒,使微气泡同时可以进行超声和暗场等多模态的显影增强(图2)。携带银纳米颗粒的聚合物膜壳微气泡的超声显影增强平均灰度值(103.74±3.19)比无银纳米颗粒的微气泡平均灰度(60.56±4.05)显著提高。同时装载了银纳米颗粒的微气泡可以进行暗场成像监控。同时,超声照射后释放出的银纳米颗粒可进入特异性细胞,随后进行活细胞层面的暗场和SERS信号追踪。
另外,Chen Jian等[34]充分开发了载药Fe3O4@C@Ag纳米粒子的应用潜力。利用Ag纳米粒子在近红外(NIR)区的SPR效应和Fe3O4的超顺磁特性,可控制荷载在Fe3O4@C@Ag纳米粒子上的阿霉素的缓释性能,进而提高阿霉素药物的治疗效果,同时可进行磁共振成像(MRI)和双光子荧光(TPF)双模态成像,以实现药物输运过程中的实时监控。Wang Hui等[26]也报告了一种介孔碳保护的Fe3O4@C-Ag核-卫星式纳米粒子作为可循环催化剂和光致发光细胞成像的多功能用途。
3.3电化学性能
发展高性能电化学催化剂的一个关键点是对电化学传感器的优化。就已有的研究成果而言,纳米复合结构已经展现出极高的电化学催化活性,在电化学生物传感应用中能够提高检测灵敏度。Zheng Tingting等[16]报道一个重大发现:在没有过氧化氢的存在下,Fe3O4磁珠对小分子染料的电化学还原有着固有的催化活性,并且通过组装在其表面上的Ag-Pd金属纳米笼(Nanocage),使其催化电化学信号进一步放大。考察Fe3O4@Ag-Pd复合纳米粒子对电化学还原硫堇的催化活性后,研究者认为:相比于常用的过氧化物酶/H2O2的酶催化体系,Fe3O4@Ag-Pd复合纳米粒子具有更强的电化学催化稳定性。以乳腺癌细胞系为模型,将这一复合纳米催化粒子进一步用于循环肿瘤细胞(CTC)的传感,可检测低至4~5个细胞,且具有良好的选择性(图3)。该项成果为癌症的早期诊断、治疗以及愈后评估提供了帮助。
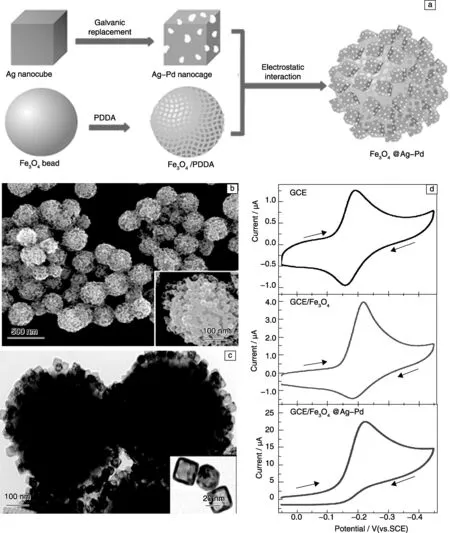
图3 构建Fe3O4@Ag-Pd复合纳米粒子过程示意图(a); Fe3O4@Ag-Pd复合纳米粒子的SEM照片((b),右下方插图为单个Fe3O4@Ag-Pd复合纳米粒子; Fe3O4@Ag-Pd复合纳米粒子的TEM照片(c),右下方插图为Ag-Pd纳米笼; GCE(裸玻碳电极)、GCE /Fe3O4、GCE /Fe3O4@Ag-Pd在含硫堇的PBS缓冲液(pH=7.0)的循环伏安曲线(d),扫描速率=50 mV·s-1Fig.3 Schematic illustration of the fabrication process of Fe3O4@Ag-Pd hybrid NPs(a); SEM image of Fe3O4@Ag-Pd hybrid NPs(b), the inset highlights one Fe3O4@Ag-Pd hybrid particle; TEM image of Fe3O4@Ag-Pd hybrid NPs(c), the inset shows a TEM image of Ag-Pd nanocages; CVs of a bare GCE, GCE/Fe3O4, and GCE/Fe3O4@Ag-Pd in 0.01 M PBS buffer (pH 7.0) containing 25μM thionine(d), scan rate = 50 mV·s-1
4结语
近年来,随着纳米科技的日益发展和生物医学应用的要求,研究者们不再局限于对单一组分的纳米材料的研究,而开始致力于构建多组分的纳米复合材料及拓展其应用。相比各自单一组分的纳米银材料,纳米银/聚合物、氧化铁/银纳米等复合材料的构建和发展,在生物医学领域的应用中给出了多功能或者功能增强的精彩表现。这将激励研究者们将更为深入地探索其合成方法和应用前景。
参考文献References
[1]Costi R, Saunders A E, Banin U.AngewChemIntEd[J], 2010, 49(29): 4 878.
[2]Cozzoli P D, Pellegrino T, Manna L.ChemSocRev[J], 2006, 35(11): 1 195.
[3]Sanchez C, Belleville P, Popall M,etal.ChemSocRev[J], 2011, 40(2): 696.
[4]Jain P K, Huang X, El-Sayed I H,etal.AccChemRes[J], 2008, 41(12): 1 578.
[5]Sambhy V, MacBride M M, Peterson B R,etal.JAmChemSoc[J], 2006, 128(30): 9 798.
[6]Yang F, Wang Q, Gu Z,etal.AcsApplMaterInter[J], 2013, 5(18): 9 217.
[8]An Jing(安 静),Wang Desong(王德松),Luo Qingzhi(罗青枝),etal.ProgressinChemistry(化学进展)[J],2008, 20(6): 859.
[8]Zhang J, Liu H, Wang Z,etal.MaterLett[J], 2007, 61(23-24): 4 579.
[9]Leininger S, Olenyuk B, Stang P J.ChemRev[J], 2000, 100(3): 853.
[10]Zhang S.NatBiotech[J], 2003, 21(10): 1 171.
[11]Li L, Wang Q.ACSNano[J], 2013, 7(4): 3 053.
[12]Shen J, Zhu Y, Yang X,etal.Langmuir[J], 2012, 29(2): 690.
[13]Xu Z, Hou Y, Sun S.JAmChemSoc[J], 2007, 129(28): 8 698.
[14]Yuen C, Liu Q.Analyst[J], 2013, 138(21): 6 494.
[15]Joshi P, Zhou Y, Ahmadov T O,etal.JMaterChemC[J], 2014, 2(46): 9 964.
[16]Zheng T, Zhang Q, Feng S,etal.JAmChemSoc[J], 2014, 136(6): 2 288.
[17]Han X X, Schmidt A M, Marten G,etal.ACSNano[J], 2013, 7(4): 3 212.
[18]Jun B-H, Noh M S, Kim J,etal.Small[J], 2010, 6(1): 119.
[19]Liu B, Zhang W, Yang F,etal.JPhysChemC[J], 2011, 115(32): 15 875.
[20]Gu H, Yang Z, Gao J,etal.JAmChemSoc[J], 2004, 127(1): 34.
[21]Buck M R, Bondi J F, Schaak R E.NatChem[J], 2012, 4(1): 37.
[22]Zhai Y, Han L, Wang P,etal.ACSNano[J], 2011, 5(11): 8 562.
[23]Chen Y, Gao N, Jiang J.Small[J], 2013, 9(19): 3 242.
[24]Bian L, Bao L, Wang J,etal.NanoscaleResLett[J], 2013, 8(1): 1.
[25]Xie Y, Yan B, Xu H,etal.AcsApplMaterInter[J], 2014, 6(11): 8 845.
[26]Wang H, Shen J, Li Y,etal.AcsApplMaterInter[J], 2013, 5(19): 9 446.
[27]Gu H, Yang Z, Gao J,etal.JAmChemSoc[J], 2005, 127(1): 34.
[28]Li L, Sun J, Li X,etal.Biomaterials[J], 2012, 33(6): 1 714.
[29]Guo D, Zhu L, Huang Z,etal.Biomaterials[J], 2013, 34(32): 7 884.
[30]Dallas P, Tucek J, Jancik D,etal.AdvFunctMater[J], 2010, 20(14): 2 347.
[31]Mahmoudi M, Serpooshan V.ACSNano[J], 2012, 6(3): 2 656.
[32]Zhu Shuangmei(朱双美),Fan Chunzhen(范春珍), Wang Junqiao(王俊俏),etal.JournalofLightScattering(光散射学报)[J], 2012, 24(3): 240.
[33]Tadele Alula M, Yang J.Talanta[J], 2014, 130: 55.
[34]Chen J, Guo Z, Wang H-B,etal.Biomaterials[J], 2013, 34(2): 571.
(编辑惠琼)
Current Status and Development of BiomedicalNanosilver-contained Composites
DING Qi1, LI Mingxi1, YANG Fang1,2, GU Ning1,2
(1.Jiangsu Key Laboratory for Biomaterials and Devices, State Key Laboratory of Bioeletronics,School of Biological Sciences & Medical Engineering, Southeast University, Nanjing 210096, China)(2.Collaborative Innovation Center of Suzhou Nano-Science and Technology, Suzhou 221009, China)
Abstract:In recent years, micro- or nano-composite materials have been rapidly developed. Usually, composite materials are composed of two or more different agents in one micro- or nano-unit structure, which realizes the characteristics of multifunction or synergistic functions enhancement. Silver nanoparticle containing micro- or nano-composite materials are one of the most important research branches in the field of biomedical applications. In this review, firstly, the preparation methods of silver/ polymer and silver/ iron oxide composites were summarized, which include emulsion polymerization method, in-situ formation/ reduction method, hole method, ion exchange method, one pot method, seed method, electrostatic interaction method as well as micelle method. Then, their applications have been reviewed. The promising applications on surface enhanced raman scattering, optical imaging, antibacterial, immune detection, electrochemical detection, catalytic degradation and so on have been described in detail.
Key words:silver/ polymer composites; silver/ iron oxide nano composite; biomedical applications
中图分类号:R114
文献标识码:A
文章编号:1674-3962(2016)01-0010-07
DOI:10.7502/j.issn.1674-3962.2016.01.02
通讯作者:顾宁,男,1964年生,教授,博士生导师,Email: guning@seu.edu.cn
基金项目:国家重大科学研究计划项目(2011CB933503);苏州市纳米科技专项(ZXG2012016)
收稿日期:2015-08-27
第一作者:丁琪,女,1976年生,博士研究生
