CsA联合泼尼松对小儿IgA肾病的疗效及对IL-18、ICAM-1的影响
2016-03-01唐筠
唐筠
CsA联合泼尼松对小儿IgA肾病的疗效及对IL-18、ICAM-1的影响
唐筠
目的探讨环孢素A(CsA)联合糖皮质激素治疗小儿IgA肾病的临床疗效及对其白细胞介素18(IL-18)、细胞间黏附分子-1(ICAM-1)的影响。方法选择60例在我院治疗的IgA肾病患儿,随机分为观察组和对照组,观察组(n=30)给予口服环孢素A联合泼尼松治疗,对照组(n=30)仅给予泼尼松治疗。对比两组临床疗效,及治疗前后血清IL-18、ICAM-1水平变化和不良反应。结果观察组的治疗总有效率显著高于对照组(P<0.05);观察组Lee氏Ⅲ级完全缓解率显著高于对照组(P< 0.05),但两组总有效率比较,差异无统计学意义(P>0.05)。两组Lee氏Ⅳ级及Ⅴ级临床疗效比较,也无统计学差异(P>0.05)。治疗后两组IL-18及ICAM-1均显著低于治疗前(P<0.05),且观察组均显著低于对照组(P<0.05)。两组不良反应比较,差异无统计学意义(P>0.05)。结论环孢素A联合泼尼松治疗小儿IgA肾病能更有效地缓解肾病进展;血清IL-18及ICAM-1水平可作为评价小儿IgA肾病病情程度及临床治疗效果的重要指标。
小儿;IgA肾病;环孢素A;泼尼松;IL-18;ICAM-1;疗效
IgA肾病是世界上最常见的原发性肾小球疾病,是导致肾功能衰竭的主要原因之一,约占终末期肾衰竭的10%~30%[1],而针对IgA肾病的治疗目前却无统一的参照标准。现有的治疗主要是通过减少尿蛋白、降低血尿酸,进而延缓肾功能减退,最终使患者获益[2]。目前我国儿童IgA的治疗主要是根据临床类型不同,结合病理情况选择治疗方法[3]。糖皮质激素可降低尿蛋白,保护肾功能,延缓肾功能进展。但是,很多肾病患儿对单用糖皮质激素治疗并不敏感[4]。环孢素A(CsA)属于新型的淋巴细胞调节剂,可选择性地作用于淋巴细胞,却不影响骨髓中的粒系和红系细胞[5]。本研究旨在探讨环孢素A联合糖皮质激素治疗小儿IgA肾病的临床疗效和安全性。
1 资料与方法
1.1 病例资料 选取2013年1月~2015年12月在本科就诊的IgA肾病患儿60例,所有患儿监护人均签署知情同意书,并经医院医学伦理委员会批准。按照入院时间顺序编号,采用奇偶数法随机分为观察组和对照组。观察组(n=30)给予口服环孢素A联合泼尼松,对照组(n=30)仅给予泼尼松。其中观察组男:女=18:12,年龄最小2 d,最大13岁,平均(8.21±2.11)岁;对照组男:女=16:14,年龄最小1 d,最大14岁,平均(9.12±1.98)岁。两组一般资料比较差异无统计学意义(P>0.05),具有可比性。
1.2 纳入和排除标准 (1)纳入标准:经肾穿刺活检病理证实为IgA肾病;病理分型Lee氏分级Ⅲ~Ⅴ级;血肌酐<150 μmol/L或eGFR>60 ml/min;24 h尿蛋白定量在25~50 mg/(kg·d);患者监护人签署知情同意书。 (2)排除标准:合并感染性疾病、肝脏疾病、系统性疾病、糖尿病及肿瘤;过敏性紫癜、强直性脊柱炎、系统性红斑狼掩、干燥综合征、银屑病等继发性IgA肾病;有糖皮质激素或免疫抑制剂禁忌者;合并其他严重肾脏疾病者,血肌酐>150 μmol/L或eGFR<60 ml/min;近1个月内曾接受糖皮质激素或细胞毒性药物等免疫抑制剂治疗者;HBsAg阳性、HCV阳性者或肝功能检测转氧酶超过正常值上限一倍;依从性差或对环孢素A过敏者。
1.3 治疗方法 对照组口服泼尼松(兰州佛慈制药股份有限公司,国药准字H62020884),起始剂量为0.6~0.8 mg/(kg·d),最大量≤40 mg/d,晨起顿服。6~8 w后逐渐减量,每2 w减2.5 mg,减至10 mg/d时维持治疗。观察组在对照组治疗基础上,加用环孢素A(华北制药集团新药研究开发有限责任公司,国药准字H10960009)治疗:第1~3个月口服环孢素A 3 mg/(kg·d);之后减量为2 mg/(kg·d),维持治疗9个月,维持环孢素A血药浓度在100~150 ng/ml。两组均治疗1年后观察疗效。
1.4 检测指标 所有患儿入院后第2 d抽取空腹静脉血3 ml,离心分离血清,采用ELISA法测定血清IL-18及ICAM-1水平。试剂盒由深圳晶美生物技术有限公司提供。
1.5 疗效判定标准 完全缓解(CR):24 h尿蛋白定量<0.15 g,血清白蛋白>35 g/L,肾功能正常;部分缓解(PR):24 h尿蛋白定量较治疗前减少>50%,但仍>0.15 g,同时肾功能好转或血肌酐升高<原基础值 15%;无效:24 h尿蛋白定量较治疗前减少< 25%,或尿蛋白较前增多,或肾功能较前恶化。总有效=CR+PR。
1.6 统计学方法 应用SPSS 20.0统计软件进行数据分析,计数资料以例和百分比表示,采用χ2检验,计量资料以±s表示,组间比较采用t检验,P<0.05为差异有统计学意义。
2 结果
2.1 两组临床疗效比较 观察组CR率和总有效率均显著高于对照组(P<0.05,表1)。
2.2 不同Lee氏分级患者之间临床疗效比较 观察组Lee氏Ⅲ级CR率显著高于对照组(P<0.05),但两组总有效率比较,差异无统计学意义 (P> 0.05);两组Lee氏Ⅳ级及Ⅴ级临床疗效比较,也无统计学差异(P>0.05)。见表2。
2.3 治疗前后两组血清IL-18及ICAM-1的变化治疗前两组血清IL-18及ICAM-1比较,无统计学差异(P>0.05);治疗后两组血清IL-18及ICAM-1均显著低于治疗前,且观察组显著低于对照组 (P< 0.05)。见表3。
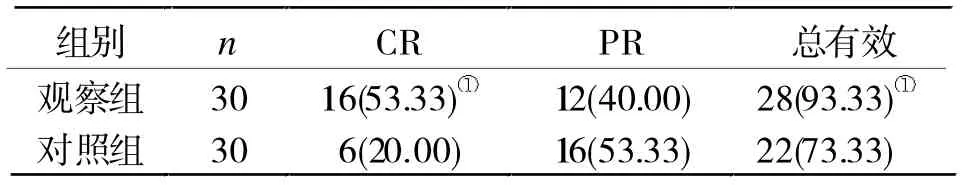
表1 两组临床疗效比较[n(%)]

表2 不同Lee氏分级患者之间临床疗效比较[n(%)]

表3 治疗前后两组血清lL-18及lCAM-1的比较(n=30)
2.4 两组不良反应比较 观察组2例出现肝功能异常,给予保肝药物及调整环孢素A剂量后,肝功能恢复正常;对照组5例出现感染,经相应治疗后不良反应均消失。两组不良反应比较,差异无统计学意义(P>0.05)。
3 讨论
由于原发性IgA肾病的临床表现多样,病理类型及肾小球受损程度的差异较大,目前世界范围内尚无统一有效、达成广泛共识的治疗方案[6]。环孢素A属于钙调磷酸酶抑制剂,通过作用于离子依赖的信号途径,选择性抑制淋巴细胞活性[7]。本研究中观察组的治疗总有效率显著高于对照组 (P<0.05),表明环孢素A联合泼尼松治疗小儿IgA肾病效果优于单独应用泼尼松治疗。本研究中观察组Lee氏Ⅲ级完全缓解率显著高于对照组(P<0.05),但两组总有效率比较,差异无统计学意义(P>0.05);两组Lee氏Ⅳ级及Ⅴ级临床疗效比较,也无统计学差异(P>0.05)。。说明Lee氏Ⅲ级患儿较Ⅳ级及Ⅴ级患儿更易获得临床缓解。
炎症因子和免疫活性物质参与IgA肾病的致病损伤过程[8]。IL-18主要是在感染、应激等诱发因素的作用下,由激活的单核巨噬细胞、NK细胞等产生,进而促进Th1细胞的增殖和免疫应答,刺激机体产生IL-8、肿瘤坏死因子-a(TNF-a)、一氧化氮(NO)等多种炎症因子,而这些炎症因子直接参与免疫性肾损伤的发生[9]。IL-18通过干扰素-r(IFN-r)间接造成肾脏损害[10]。本研究中治疗前两组血清IL-8及ICAM-1比较,差异不显著(P>0.05);治疗后两组血清IL-18及ICAM-1均显著低于治疗前,且观察组显著低于对照组(P<0.05),提示血清IL-18及ICAM-1可作为评价小儿IgA肾病临床疗效的指标。本研究中两组不良反应比较,差异无统计学意义(P>0.05),提示环孢素A联合泼尼松对小儿IgA肾病不会显著增加不良反应,安全性好。
综上所述,环孢素A联合泼尼松治疗小儿IgA肾病能更有效的缓解肾病进展;血清 IL-18及ICAM-1水平可作为评价小儿IgA肾病病情程度及临床治疗效果的重要指标。
[1]马宏.IgA肾病发病机制的研究进展 [J].实用儿科临床杂志, 2012,27(5):313-315.
[2]樊均明,李甫罡,冯胜刚,等.IgA肾病免疫发病机制及免疫抑制治疗[J].西部医学,2013,25(2):161-163,168.
[3]贾晓媛,王伟铭.IgA肾病的治疗进展 [J].上海交通大学学报(医学版),2012,32(3):361-365.
[4]郭宏湘,张建江,史佩佩,等.儿童紫癜性肾炎和IgA肾病临床病理对比分析[J].中国当代儿科杂志,2012,14(7):506-509.
[5]许琳.环孢素A联合中/低剂量泼尼松治疗进展性IgA肾病疗效观察[D].济南:山东大学,2014.
[6]汤颖,马小琨,张俊,等.血清IgA、C-3及IgA/C-3与IgA肾病诊断及病理分级的关系[J].中华全科医学,2010,8(1):17-19.
[7]满利萍.环孢素A联合科素亚治疗IgA肾病的临床疗效观察[D].合肥:安徽医科大学,2014.
[8]崔专,王悦,范敏华.IgA肾病患者的肾脏存活及影响因素[J].北京医学,2011,33(2):149-152.
[9]樊平,戴双明,邹川,等.IgA肾病的临床表现与病理特征研究[J].西安交通大学学报(医学版),2015,36(2):241-244.
[10]张曼丽,陈卫东,杨萍,等.MCP-1、ICAM-1在糖尿病肾病大鼠肾脏损害中作用及厄贝沙坦干预的影响 [J].中国中西医结合肾病杂志,2013,14(12):1040-1043,9.
Efficacy of CsA combined with prednison on treatment of IgA nephropathy in children and the effects on IL-18 and ICAM-1
Tang Jun Department of Nephrology,Xi'an Children's Hospital,Xi'an,Shaanxi,710003,China
ObjectiveTo explore the efficacy of ciclosporin A(CsA)combined with prednison on treatment of IgA nephropathy in children and the effects on IL-18 and ICAM-1.MethodsA total of 60 children patients with IgA nephropathy admitted to our hospital were selected and randomly divided into an observation group and a control group(n=30,respectively).The observation group was treated with CsA combined with prednisone and the control group with prednisone only.The efficacy,changes in the levels of IL-18 and ICAM-1 before and after the treatment and adverse reactions in the two groups were compared.ResultsThe ORR in the observation group was significantly higher than that in the control group(P<0.05);the Lee's level-Ⅲ complete remission rate in the observation group was much higher than that in the control group (P<0.05).However,the difference in the ORR between the two groups had no statistical significance(P>0.05).There was no statistical difference in the Lee's level-Ⅳand level-V efficacy between the two groups(P>0.05).The levels of IL-18 and ICAM-1 in the two groups after the treatment were significantly lower than those before the treatment(P<0.05),and the levels in the observation group were much lower than those in the control group (P<0.05). The adverse reactions in the two groups had no significant difference (P>0.05).ConclusionCsA combined with prednisone in the treatment of IgA nephropathy in children can be more effective to alleviate the progression of kidney disease.The levels of serum IL-18 and ICAM-1 can not only be used as clinical indicators of severity evaluation of IgA nephropathy in children,but also as an important reference for evaluating the clinical effects of the treatment.
children;IgA nephropathy;CsA;prednisone;IL-18;ICAM-1;efficacy
R 726.9
A
1004-0188(2016)11-1239-03doi:10.3969/j.issn.1004-0188.2016.11.006
2016-05-06)
710003西安,西安市儿童医院肾脏科
