硅钼酸@石墨烯复合膜修饰电极及电化学行为
2016-02-24郭伟华杨国强黄德娟刘云海
郭伟华, 杨国强, 黄德娟, 刘云海
(1.东华理工大学核资源与环境省部共建国家重点实验室培育基地,江西 南昌 330013;2.东华理工大学化学生物与材料科学学院,江西 南昌 330013)
硅钼酸@石墨烯复合膜修饰电极及电化学行为
郭伟华1,2, 杨国强2, 黄德娟2, 刘云海1,2
(1.东华理工大学核资源与环境省部共建国家重点实验室培育基地,江西 南昌 330013;2.东华理工大学化学生物与材料科学学院,江西 南昌 330013)
以氧化石墨烯(GO)和硅钼杂多酸(SiMo12)为原料,用一步电沉积法构筑SiMo12@ERGO复合膜修饰的氧化铟锡(ITO)电极。采用扫描电镜和X-射线光电子能谱研究了电极的表面形貌和成分,通过循环伏安法对修饰电极的电化学性能进行了研究,并将构筑的修饰电极应用于亚硝酸根和抗坏血酸的测定。结果表明,与空白ITO和分步沉积法得到SiMo12/ERGO修饰电极相比,该方法得到的复合膜电极上SiMo12的负载量高,稳定性良好,同时对抗坏血酸具有良好的电催化能力。
硅钼杂多酸; 氧化石墨烯;一步电沉积;电催化
在各种定量检测技术中,电化学技术具有灵敏度高,操作方便快捷等优点,已成为最具潜在应用的方法之一。然而,很多污染物在裸电极上直接氧化或还原是不可逆的并且需要高的过电位。减小过电位的一个有效方法就是选用化学修饰电极。多金属氧酸盐(简称多酸,POMs)是一类具有明确结构的金属-氧簇化合物,其多步的、可逆的电子转移过程,使之非常适合作为修饰电极的材料和电催化剂,已引起了科学家的广泛关注(Liu et al., 2010; Ji et al., 2015)。目前,可以通过多种方法得到POMs修饰电极,如电化学沉积(Reybier et al., 2002),吸附(Ca et al., 2006),导电聚合物包裹(McCormac et al., 2001),单层、多层膜自组装法(Wang et al., 2003)以及碳糊法(Wang et al., 2000)等。其中,电化学沉积法具有快速、简单的优点,是一种理想的修饰方法,被广泛地应用于多酸修饰电极的制备。
提高修饰电极比表面积可有效地降低电极反应过电位,提高电极效率。利用纳米材料对电极表面进行修饰是提高电极比表面积的有效方法。石墨烯,作为一种新型的碳纳米材料,由于其独特的结构,超大的比表面积,良好的稳定性,高电子传导性,在电分析化学领域得到了广泛的应用(Shao et al., 2010)。目前,石墨烯修饰电极通常是采用滴涂或者吸附方法将化学还原的氧化石墨烯修饰到电极表面。然而,在制备化学还原氧化石墨烯过程中经常使用到有毒试剂如水合肼。最近,Guo等(2009)提出了以氧化石墨烯溶液为前驱体,电化学还原氧化石墨烯制备石墨烯的方法,该方法具操作简单、可控、绿色无污染等优点,是一种理想的制备石墨烯修饰电极方法。
目前,关于POM/石墨烯纳米复合材料的研究已有报道(Liu et al., 2012a,2012b; Kim et al., 2013)。然而,这些方法得到的多是粉末型POM/石墨烯纳米复合材料,需将粉末状的POM/石墨烯纳米复合分散到适合的溶剂中,利用滴涂法将其修饰到电极表面。通过这种制备方法很难得到均匀的薄膜。通过层层组装的方法,可以将多酸和氧化石墨烯组装到电极表面,在通过紫外光还原的方法到得到POM/石墨烯多层膜(Li et al., 2011)。该方法可以得到均匀的、稳定的薄膜修饰电极。然而,聚电解质的存在可能会影响修饰电极的电催化性能,且制备过程步骤复杂、耗时。因此,开发一种简单,有效且快速地制备多酸@石墨烯修饰电极的方法是十分有意义的。
本文以氧化石墨烯(GO)和硅钼杂多酸(SiMo12)为前驱体,采用一步电化学沉积法得到SiMo12@ERGO复合膜修饰的氧化铟锡(ITO)电极。采用扫描电镜研究了电极的表面形貌,通过循环伏安法对修饰电极的电化学性能和稳定性进行了研究,并对该电极的电催化活性进行了测试。实验结果表明,与空白ITO和分步沉积法得到SiMo12/ERGO修饰电极相比,该方法得到的复合膜电极上SiMo12的负载量高,灵敏度较高,稳定性良好且对抗坏血酸具有良好的催化能力。
1 实验部分
1.1 主要试剂与仪器
磷片石墨购于南京先丰纳米材料科技有限公司,其他所有试剂均购于国药集团化学试剂有限公司,均为分析纯,所用的水为二次蒸馏水。
所有电化学测试均在CHI660D型电化学工作站(上海辰华仪器有限公司)上进行。采用三电极体系,ITO导电玻璃为工作电极,铂丝电极为辅助电极,饱和甘汞电极为参比电极。采用 NavaNanoSEM450场发射扫描电子显微镜对修饰电极的微观形貌进行表征。采用Kratos XSAM 800 X射线光电子能谱(XPS)对修饰电极的化学成分进行表征。
1.2 实验过程
1.2.1 硅钼杂多酸及氧化石墨烯的制备
H4SiMo12O40·xH2O(简写SiMo12)按文献方法合成(Rocchiccioli-deltcheff et al., 1983)。采用修正Hummers法(Hummers et al., 1958)方法制备氧化石墨。再将所得氧化石墨加入适量水,并用超声分散,离心分离弃去底部较大的颗粒,得到氧化石墨烯(GO)分散液。
1.2.2 电极预处理
用肥皂水冲洗ITO电极片,再将其放入双氧水、氨水、蒸馏水的混合液(体积比为1∶1∶1)中加热15 min,取出后用蒸馏水冲洗并超声振荡15 min,氮气吹干后备用。
1.2.3 SiMo12@ERGO修饰电极的制备
首先配置0.5 mmol/L的SiMo12溶液,及浓度为1 mg/mL GO胶体分散液。SiMo12溶液与GO分散液等体积混合,并超声振荡5 min,待用。
采用一步法制备SiMo12@ERGO修饰电极。将三电极系统置于SiMo12与GO混合液中,调节电位范围为-0.8~0.35 V,扫描速度为50 mV/s,循环扫描5圈。将电极取出,冲洗干净,得到SiMo12@ERGO修饰的ITO电极。为观察GO的影响,用蒸馏水代替混合液中的GO胶体分散液,同样条件下制备SiMo12修饰的ITO电极。
1.2.4 SiMo12/ERGO修饰电极的制备
为比较,采用分步法制备SiMo12/ERGO修饰电极。具体过程如下:先将三电极置于GO溶液中,利用循环伏安法在-0.8~0.35 V的范围内以50 mV/s循环扫描5圈,GO被还原为石墨烯并沉积到ITO电极表面,记作ERGO/ITO。然后将三电极置于SiMo12溶液中,在-0.35~0.35 V的电位范围内循环扫描5圈,SiMo12分子即被吸附到了ERGO/ITO电极的表面,得到SiMo12/ERGO修饰的ITO电极。
2 结果与讨论
2.1 修饰电极表面形貌与成分分析
采用扫描电镜(SEM)对SiMo12@ERGO、SiMo12/ERGO、SiMo12修饰的ITO电极的微观形貌进行了表征。一般来说,ITO基底表面是非常光滑和均匀的。从图1A中可见,单纯的SiMo12薄膜表面比较平整,在大范围内是均匀有序的,膜表面变得粗糙且存在着许多球状组织,这些小球是可能由于SiMo12阴离子聚集造成的。图1B所示的是分步法制备的SiMo12/ERGO膜在ITO基底上的表面形貌。由图可见,电极表面变得更加粗糙并出现了石墨烯的褶皱状结构,说明通过电化学还原法可将氧化石墨烯还原并修饰在电极表面。同时,由SiMo12阴离子聚集形成的小球依然可以被观察到。图1C为一步法制备的SiMo12@ERGO膜的表面形貌。显然,该电极表面的粗糙度进一步增加,展现出更多的石墨烯的褶皱状结构,并形成了一定的孔。此外,粗糙的表面将提供更大的比表面积,从而增加SiMo12在电极表面的覆盖度。这在电化学实验中将得到进一步的证实。

图1 修饰电极的SEM图Fig.1 SEM images of SiMo12 (A), SiMo12/ERGO (B) and SiMo12@ERGO (C) on the surface of ITO corresponding to images at different locations and magnification.
为了确定修饰电极的物质组成,对SiMo12@ERGO复合膜进行了X-射线光电子能谱(XPS)的测试。图2A 所示为复合膜中C的特征键能峰。从图中可以看出,复合膜中含氧官能团的强度明显小于GO的(Jiang et al., 2014),这表明在复合膜的制备过程中GO表面的含氧基团被还原。此外,XPS光谱(图2B,C)也显示出复合膜中含有Mo和Si元素,这表明采用一步沉积法成功得到了SiMo12@ERGO复合膜修饰电极。
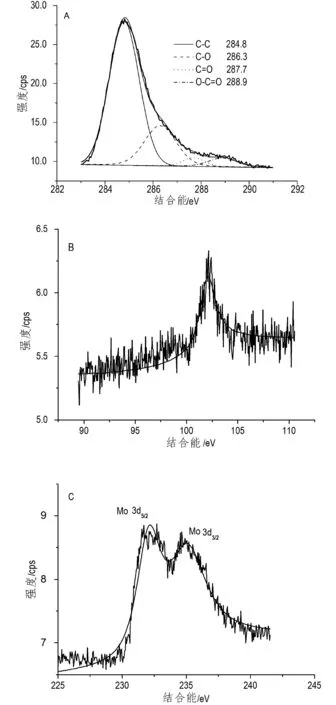
图2 SiMo12@ERGO修饰电极的XPS 光谱 Fig.2 XPS spectroscopy of SiMo12@ERGO filmA.C1s; B.Si2p; C.Mo3d
2.2 SiMo12@ERGO修饰电极的电化学行为
图3为不同修饰电极在0.1 mol/L的H2SO4溶液中,扫描速度为50 mV/s时的循环伏安曲线。图中曲线a,b分别为SiMo12@ERGO/ITO,SiMo12/ERGO/ITO的循环伏安曲线,插图为SiMo12/ITO的循环伏安曲线。
从图中可以看出,SiMo12/ITO在-0.18~0.35 V出现三对较弱的氧化还原峰,该三对峰为SiMo12的特征峰,说明被修饰到电极表面。而曲线a,b则出现了三对较强的氧化还原峰,其主要原因是石墨烯具有较大的比表面积,增加了杂多酸的负载量。此外,与曲线b相比,通过一步法得到的修饰电极(曲线a)的峰电流显著增大,其原因可能是在沉积过程中更多的SiMo12掺杂到石墨烯片层间,而分步沉积过程(曲线b)中SiMo12只沉积在石墨烯片表面或边缘。
另外,曲线a的峰电位向正电位方向偏移。SiMo12@ERGO/ITO、SiMo12/ERGO/ITO的平均峰电势(Ef=(Epa+ Epc)/2)、峰位差(ΔEp=Epa- Epc)和氧化峰II的峰电流(Ip)结果见表1。
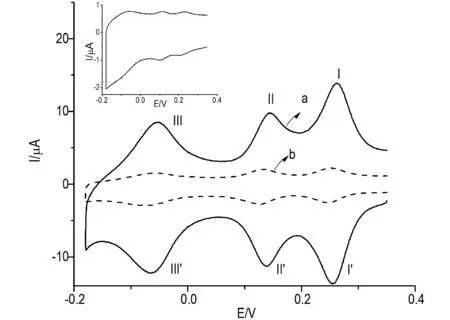
图3 (a)SiMo12@ERGO/ITO; (b)SiMo12/ERGO/ITO;插图为SiMo12/ITO在0.1 mol/L的H2SO4中的循环伏安曲线,扫描速率为50mV/sFig.3 CVs of (a)SiMo12@ERGO/ITO; (b)SiMo12/ERGO/ITO and SiMo12/ITO (inset) modified electrodes in 0.1 mol/L H2SO4solution at a scan rate of 50 mV/s.
Table 1 Reversible potentials (Ef), peak-to-peak separations (ΔEp) and peak current data for the reduction of SiMo12at the modified electrodes.

electrodeEf(mV)ΔEp(mV)IIIIIIIIIIIIIp(A)aSiMo12/ERGO248.5126.5-65.577131.163SiMo12@ERGO258142.5-57.587116.627
2.3 扫描速度对修饰电极电化学行为的影响
图4A中是SiMo12@ERGO/ITO电极在-0.18~0.35 V的电压范围内,0.1 mol/L H2SO4溶液体系中,不同扫描速度对修饰电极电化学行为的影响,扫描速度分别为10,20,30,50,80,100,200,300,500,800,1 000 mV/s。随着扫速的增加,氧化还原峰电流逐渐增大。以II氧化还原峰为例,给出了峰电流与扫速的关系图(图4B)。从图中可以看出,当扫速由10 mV/s逐渐增大至1 000 mV/s时,峰电流随着扫速呈现线性增长的趋势,这表明了该多层膜的氧化还原过程为表面控制过程。
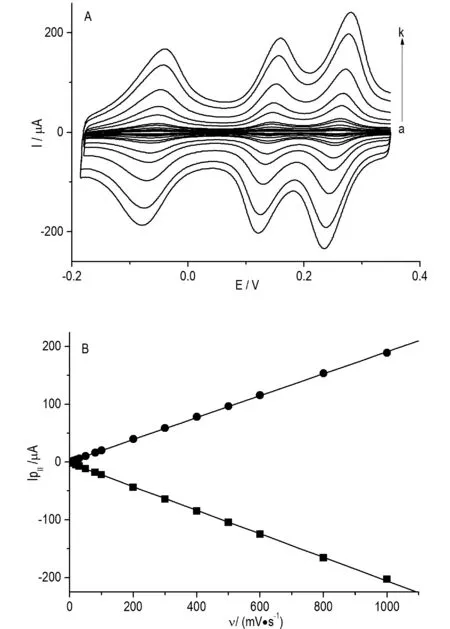
图4 (A)SiMo12@ERGO/ITO 在0.1 mol/L的H2SO4中在不同的扫描速率(从内到外依次为:10、20、30、50、80、100、200、300、500、800、1000mV/s)下的循环伏安曲线;(B)为峰电流[峰II-II’]随扫描速率变化的关系曲线Fig.4 (A)The CVs of theSiMo12@ERGO/ITO electrode in 0.1 mol/L H2SO4 aqueous solution at different scan rates (from 10、20、30、50、80、100、200、300、500、800 to1000 mV/s); (B) The plot of peak current vs. Scan rate.
2.4 不同pH环境对修饰电极的影响
图5A中所给的是SiMo12@ERGO/ITO电极在-0.18~0.35 V的电压范围内,扫描速度为50 mV/s,在不同pH缓冲溶液得到的循环伏安特性曲线。根据图5A中显示,随着酸度的减小,修饰电极的三个氧化还原峰向负电位方向偏移,并且峰电流在减小,其主要原因是复合膜中的杂多酸在电化学反应过程中,伴随的质子的转移,以尽快得到电中性,在酸度较低的情况下,质子的浓度下降,并且被其他体积较大、质量更重的阳离子所代替,由于空间位阻变大,阳离子扩散到电极表面的速率要更慢些,从而电化学反应速率降低,因此电流逐渐减小(Brett et al., 1993)。峰电位的负向移动可以根据能斯特方程(Wang, 1994)来解释。
由图5B可知,SiMo12@ERGO/ITO的氧化还原峰的平均峰电势Ef 与pH值呈现出良好的线性关系。I-I’,II-II’和III-III’的平均峰电势Ef 与pH值的直线斜率分别为-56 mV/pH,-72 mV/pH 和-60 mV/pH,这和2e/2H+过程的理论值-59 mV/pH很接近。因此,SiMo12@ERGO修饰电极的氧化还原过程可描述如下:
H6SiMo10VIMo2VO40
H8SiMo8VIMo4VO40
H10SiMo6VIMo6VO40
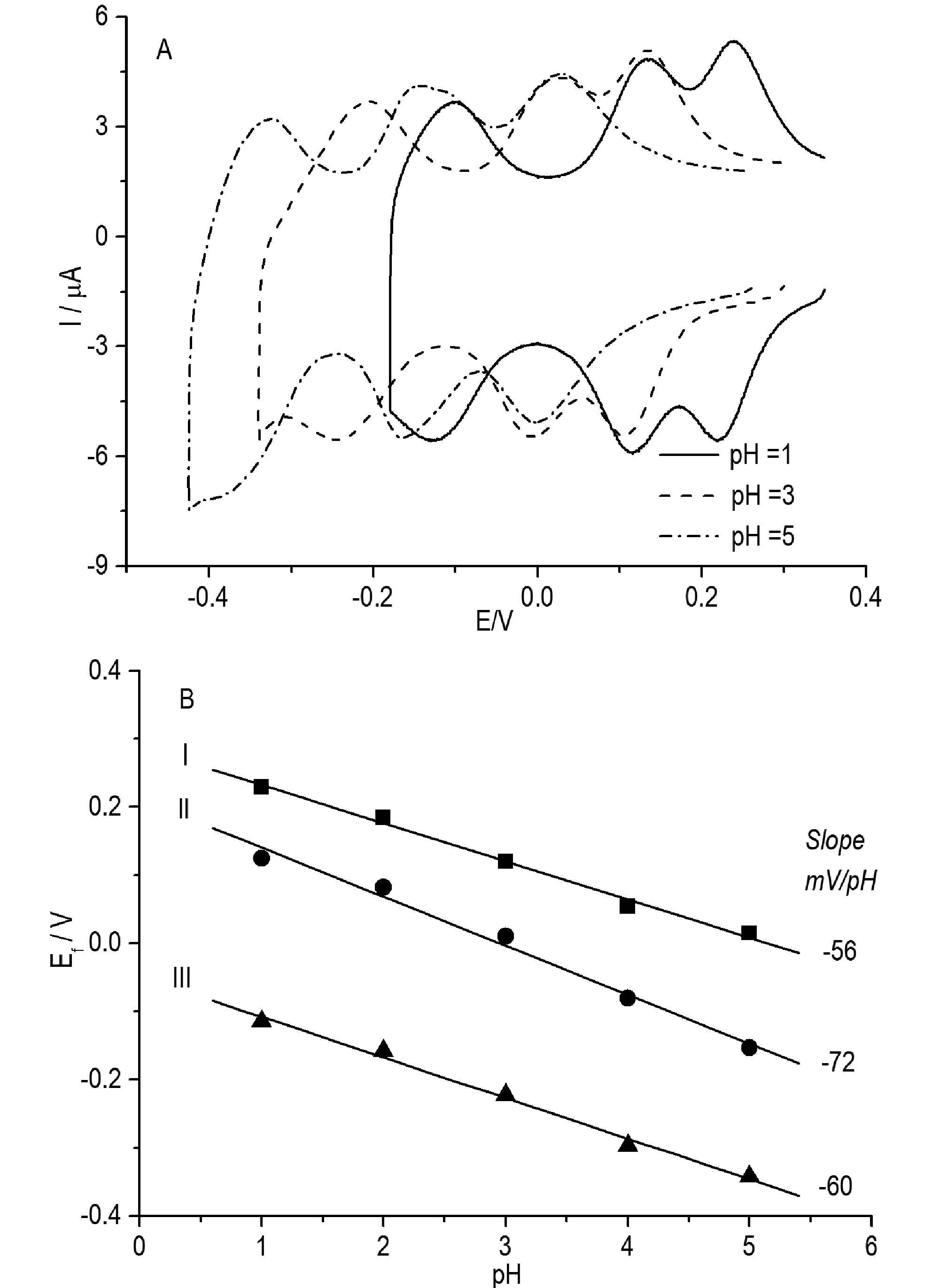
图5 (A) SiMo12@ERGO/ITO在不同pH缓冲溶液得到的循环伏安特性曲线,扫描速度为50 mV/s (B) Ef 与 pH 值的关系图Fig.5 (A) The CVs of SiMo12@ERGO/ITO electrode in aqueous solution at different pH Scan rate:50 mV/s. (B) Relationships of the formal potentials and the pH values.
2.5 SiMo12@ERGO修饰电极的电催化反应
主要考察了SiMo12@ERGO/ITO对抗坏血酸的催化活性。
图6中所示为修饰电极在不同浓度的抗坏血酸溶液中的循环伏安特性曲线图。根据图中显示,Ⅰ号氧化峰的峰电流随着抗坏血酸浓度的增大而增大,说明本实验所制备的修饰电极对抗坏血酸具有良好的催化氧化活性。由图6插图可知,在0.1~1 mmol/L 范围内,催化电流与抗坏血酸浓度成正比。
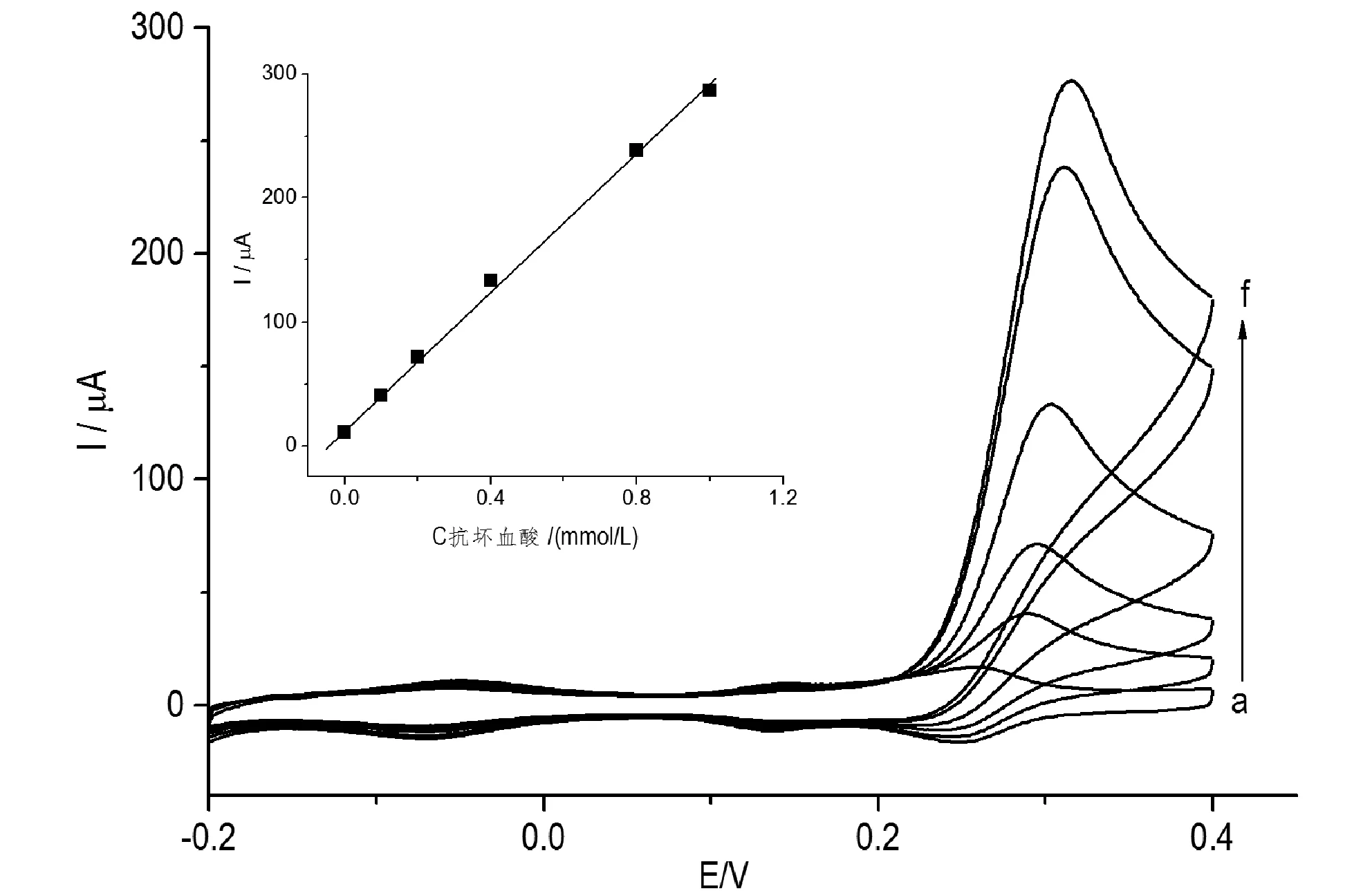
图6 SiMo12@ERGO/ITO对不同浓度抗坏血酸(a-f: 0, 0.1, 0.2, 0.4, 0.8, 1.0mmol/L)的循环伏安响应曲线, 扫描速率为50 mV/s. 插图为抗坏血酸的浓度与峰电流的关系图.Fig.6 CV curves of SiMo12@ERGO/ITO in 0.1 mol/LH2SO4 solutions at scan rate 50 mV/s in the presenceof different concentration of ascorbic acid. Inset plotofcatalytic current vs. Ascorbic acid concentration.
在含有0.4 mmol/L 的抗坏血酸溶液中测定了一些可能共存的无机离子和有机物对测定抗坏血酸的干扰。从图7中可以看出,等浓度的多巴胺和L-半胱氨酸以及10倍浓度的Cl-,Na+, PO43-均对抗坏血酸的测定不产生干扰。
2.6 化学修饰电极稳定性测试
图8中所显示的曲线是SiMo12@ERGO/ITO在0.1 mol/L的H2SO4溶液体系中,以50 mV/s的速率连续扫描50圈前后测试的循环伏安特性曲线。从图中可以看出,经过50圈得连续扫描后,I和II峰的峰电流略有下降,而III峰的峰电流几乎保持不变,且峰电位保持稳定说明修饰电极具有良好的稳定性。
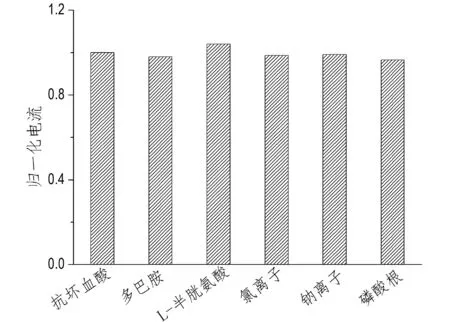
图7 SiMo12@ERGO/ITO电极在dopamine, L-cysteine, chloride, sodium, phosphate存在时的选择性分析Fig.7 Normalized amperometric current of SiMo12@ERGO/ITO for 0.4 mM Ascorbic acid in the presence of dopamine, L-cysteine, chloride, sodium, phosphate.
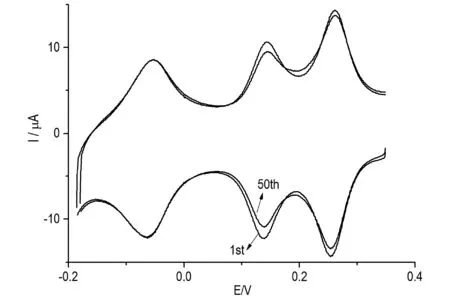
图8 SiMo12@ERGO/ITO在0.1 mol/LH2SO4中连续扫描50圈前后的循环伏安特性曲线,扫描速率50 mV/sFig.8 The 1st and 50th CVs of the SiMo12@ERGO/ITO in 0.1 mol/L H2SO4 solutions at scan rate 50 mV/s.
3 结论
本文中,采用一步循环伏安沉积法制备了SiMo12@ERGO修饰的ITO电极,研究了该电极的表面形貌和电化学性能,探讨了扫速和溶液酸度对其电化学行为的影响。研究结果表明,采用一步沉积法进行制备的SiMo12@ERGO复合膜修饰电极具有更高的多酸负载量。通过对抗坏血酸的催化性测试的实验,得出该电极具有良好催化氧化能力。
Liu S Q, Tang Z Y. 2010. Polyoxometalate-based functional nanostructured films: Current progress and future prospects [J]. Nano Today, 5(4): 267-281.
Ji Y C, Huang L J, Hu J, et al. 2015. Polyoxometalate-functionalized nanocarbon materials for energy conversion, energy storage and sensor systems [J]. Energy Environmental Science, 8(3): 776-789.
Reybier K, Malugani J P, Fantini S, et al. 2002. Electrodeposition of Keggin-type heteropolyanions on different electrode surfaces from nonaqueous media [J]. Journal of The Electrochemical Society, 149(3): E96-E101.
Ca D V, Sun L, Cox J A. 2006.Optimization of the dispersion of gold and platinum nanoparticles on indium tin oxide for the electrocatalytic oxidation of cysteine and arsenite [J]. Electrochim. Acta, 51(11): 2188-2194.
McCormac T, Farrell D, Drennan D, et al. 2001.Immobilization of a Series of Dawson Type Heteropolyanions [J]. Electroanalysis, 13(10): 836-842.
Wang S, Du D. 2003. Preparation and electrochemical properties of Keggin-type phosphomolybdic anions in electrostaticly linked L-cysteine self-assembled monolayers [J]. Sens. Actuators B, 94(3): 282-289.
Wang P, Wang X, Bi L, et al. 2000. Renewable-surface amperometric nitrite sensor based on sol-gel-derived silicomolybdate-methylsilicate-graphite composite material [J]. Analyst, 125(7): 1291-1294.
Shao Y Y, Wang J, Wu H, et al.2010. Graphene Based Electrochemical Sensors and Biosensors:A Review [J]. Electroanalysis, 22(10): 1027-1036.
Guo H L, Wang X F, Qian Q Y,et al. 2009. A green approach to the synthesis of graphene nanosheets [J]. ACS Nano 3(9): 2653-2659.
Liu R, Li S, Yu X, et al. 2012b. Facile synthesis of Au-nanoparticle/polyoxometalate/graphene tricomponent nanohybrids: An Enzyme-free electrochemical biosensor for hydrogen peroxide [J]. Small, 8(9): 1398-1406.
Liu R, Li S, Yu X, et al. 2012. A general green strategy for fabricating metal nanoparticles/polyoxometalate/graphene tri-component nanohybrids: enhanced electrocatalytic properties [J].Journal of Materials Chemistry, 22(8): 3319-3322.
Kim Y, Shanmugam S, 2013. Polyoxometalate-reduced graphene oxide hybrid catalyst: synthesis, structure, and electrochemical properties [J]. ACS Applied Materials Interfaces, 5(22): 12197-12204.
Li H, Pang S, Wu S,et al. 2011. Layer-by-layer assembly and UV photoreduction of graphene-polyoxometalate composite films for electronics [J]. Journal of the American Chemical Society, 133(24) 9423-9429.
Rocchiccioli-deltcheff C, Fournier M, Franck R,et al. 1983. Vibrational investigations of polyoxometalates. 2. Evidence for anion-anion interactions in molybdenum(VI) and tungsten(VI) compounds related to the Keggin structure [J]. Inorganic Chemistry, 22(2): 207-216.
Hummers W S, Offeman R E, 1958. Preparation of Graphitic Oxide [J]. Journal of the American Chemical Society, 80(6): 1339.
Jiang M, Zhu D D, Cai J J, et al. 2014. Electrocatalytic hydrogen evolution and oxygen reduction on polyoxotungstates/graphene nanocomposite multilayers [J]. J. Phys. Chem. C 118 (26) 14371-14378.
Brett M A, Brett A M O, 1993. Electrochemistry Principles, Methods, and Applications [M]. Oxford University Press:25.
Wang J. 1994. Analytical Electrochemistry [M]. VCH, New York.
Silicomolybdate/Graphene Composite Film Modified Electrode and Its Electrocatalytic Performance
GUO Wei-hua1,2, YANG Guo-qiang2, HUANG De-juan2, LIU Yun-hai1,2
(1. State Key Laboratory Breeding Base of Nuclear Resources and Environment,East China University of Technology, Nanchang, JX 330013, China; 2. Chemistry, Biological and Materials Sciences Department, East China University of Technology, Nanchang, JX 330013, China )
A nanocomposite film modified Indium tin oxide (ITO) electrode based on graphene oxide (GO) and silicomolybdenum heteropoly acid (SiMo12) was fabricated by one-step electrodeposition. SEM and XPS were used to characterize the surface morphology and chemical composition of the as-prepared modified electrode. Successful formation and the electrochemical behavior of SiMo12@ERGO modified electrode were confirmed by cyclic voltammetry. In comparison with the SiMo12/ITO and SiMo12/ERGO/ITO, the SiMo12@ERGO/ITO has the highest peak current for the redox of SiMo12. The SiMo12@ERGO modified electrode exhibited high electrocatalytic activities toward the oxidation of Ascorbic acid.
Silicomolybdate;graphene oxide;one-step electrodeposition;electrocatalysis
2016-04-08
国家自然科学基金(21401022);博士科研启动基金项目(DHBK1007);东华理工大学核资源与环境重点实验室开放基金项目NRE1511)
郭伟华(1983—),讲师,博士,主要从事电分析化学研究。E-mail:whguo@ecit.cn
10.3969/j.issn.1674-3504.2016.04.012
O646
A
1674-3504(2016)04-0379-07
郭伟华,杨国强,黄德娟,等.2016. 硅钼酸@石墨烯复合膜修饰电极及电化学行为[J].东华理工大学学报:自然科学版,39(4):379-385.
Guo Wei-hua, Yang Guo-qiang, Huang De-juan et al.2016. Silicomolybdate/Graphene composite film modified electrode and its electrocatalytic performance [J].Journal of East China University of Technology (Natural Science), 39(4):379-385.
