石墨烯/纳米纤维素/亚甲基蓝电极同时检测抗坏血酸和尿酸
2016-02-17窦砚鹏梁英彭俊军刘慧宏
窦砚鹏,梁英,彭俊军,刘慧宏
(1. 湖北文理学院化学工程与食品科学学院,湖北 襄阳 441053;
2. 武汉纺织大学化学与化工学院,湖北 武汉 430074)
石墨烯/纳米纤维素/亚甲基蓝电极同时检测抗坏血酸和尿酸
窦砚鹏1,2,梁英1,彭俊军2,刘慧宏2
(1. 湖北文理学院化学工程与食品科学学院,湖北 襄阳 441053;
2. 武汉纺织大学化学与化工学院,湖北 武汉 430074)
摘要:直接采用电化学还原法在玻碳电极上成功制备石墨烯( graphene,GN)修饰的电极和石墨烯/纳米纤维素/亚甲基蓝(graphene/nano-crystalline cellulose/methylene blue composite,GN/NCC/MB)复合材料修饰电极,并利用循环伏安法研究了这两种电极在PBS (phosphate buffered solution 0.1 mol·L-1,pH=7.0)溶液中的对抗坏血酸(ascorbic acid,AA)和尿酸(uric acid,UA)在该电极上的电化学行为.实验结果表明:在AA和UA共存体系中,GN/NCC/MB/GCE修饰的玻碳电极能够将AA和UA的氧化峰电位明显分开,峰电位相差300 mV.并且用两种形式,研究了AA和UA两种物质峰电流与其物质的量浓度的关系,发现AA、UA的氧化峰电流与其浓度分别在40.0~700.0 μmol·L-1、4.0~120.0 μmol·L-1范围内呈线性关系.在AA和UA共存时,两者的最低检测限度分别为17.644 2 μmol·L-1和3.251 1 μmol·L-1.GN/NCC/MB复合材料修饰的玻碳电极可以实现AA和UA共存时两种物质的定量检测.
关键词:石墨烯;纳米纤维素;亚甲基蓝;抗坏血酸;尿酸;修饰电极
0引言
抗坏血酸(AA)是维持机体正常生理功能的重要维生素之一,可预防和治疗不孕症、精神疾病及肿瘤[1].尿酸(UA)是人体内嘌呤核苷酸分解代谢过程的最终产物.体液尿酸含量的变化与人体新陈代谢、免疫等机能密切相关, 同时也可间接预示与嘌呤代谢有关的痛风、基因完全缺损症、高尿酸血等各种疾病[2].人体体液的UA和AA共存, 其浓度的同时测定具有重要实用价值[3].虽然UA和AA均可以应用电化学阳极氧化法予以测定,但二者在GN电极上的氧化峰电位非常接近,准确测定十分困难[4-5].因此制备一种能够将AA和UA氧化峰电位在循环伏安法上明显区分开,并建立同时测定AA和UA的电化学方法具有十分重要的理论和实际应用意义[6].
石墨烯(GN)是由单层碳原子紧密堆积成二维蜂窝状晶体结构的一种新型炭质材料,是自然界已知材料中最薄的一种材料.这种二维材料保持了近乎完美的晶体结构和优异的晶体学性质,蕴含了丰富而新奇的物理现象,具有重要的理论研究和应用价值[6].石墨烯良好的导电导热能力、超高的比表面积(2 630 m2/g),已作为电极材料在电催化、电传感、新能源领域受到研究者广泛关注[7].目前制备石墨烯的主要方法是通过化学还原法将氧化石墨烯还原成石墨烯.[8-9]该方法得到的石墨烯往往有团聚现象,难于分散溶液中,不宜直接作为电传感电极材料.近来,将氧化石墨烯通过电化学还原法制备成石墨烯(GN)被认为是一种环境友好型的石墨烯制备方法.如Guo等[11]通过恒电位还原法首次在玻碳电极(GCE)上直接制得电化学还原的石墨烯.该方法不需要使用其他还原剂,产物无杂质污染,具有比化学还原方法更高的纯度,所制备的石墨烯含有一些官能团,同时也容易现场在电极基底上成膜,适合作为电化学传感器修饰电极.[11-14]
亚甲基蓝(MB)属于阳离子吩噻嗪类染料,也是一种比较活泼的电子转移体,其在溶液中的氧化还原电位在0.1~-0.4 V(vs.SCE)之间,具有良好的电化学活性.其可在经过预处理的电极上,聚合成一层聚合物薄膜,用于电传感修饰电极的电子媒介体和协同催化材料[15].不过,研究者往往是通过聚合方法修饰在电极表面上,形成亚甲基蓝聚合物膜,与电极材料分层分布在修饰电极上[16-17].这样就可能导致亚甲基蓝协同作用不能完全发挥.为了克服此问题,在本研究工作中,我们首先制备氧化石墨烯、亚甲基蓝和纳米纤维素混合溶液,然后制成复合薄膜修饰在玻碳电极表面,再通过现场电化学还原作用形成石墨烯/纳米纤维素/亚甲基蓝复合物薄膜修饰的电极(GN/NCC/MB/GCE).其中纳米纤维素(NCC)由于具有较大的比表面积,优异的生物相容性,较强的吸附性能[13],可以让亚甲基蓝牢固地负载在电极表面,使亚甲基蓝与石墨烯能够均匀分散,从而最大限度地发挥其催化作用.
本文中主要通过现场电化学还原法制备了GN/NCC/MB复合材料,研究了GN/NCC/MB电极对UA和AA的电化学行为,并用循环伏安法对UA和AA的同时检测进行电化学定量分析.
1实验材料和方法
1.1主要仪器与实验试剂CHI660C电化学工作站(上海辰华仪器公司);KH-250DB型数控超声波清洗器 (昆山禾创超声仪器有限公司);微量进样器25 μL(上海安亭微量进样器厂).
氧化石墨烯(自制,0.25 mg/mL);亚甲基蓝(0.373 9 mg/mL,国药集团化学试剂有限公司);纳米纤维素(自制,0.66 mg/mL);抗坏血酸(176.13,天津市天新精细化工开发中心);尿酸(168.11,国药集团化学试剂有限公司).实验中使用的磷酸盐缓冲溶液PBS均为0.1 mol·L-1,pH=7.0,由0.1 mol·L-1NaH2PO4和0.1 mol·L-1K2HPO4配制而成.实验用水均为超纯水(18.30 mΩ·cm).
1.2修饰电极的制备
1.2.1GN/GCE电极的制备将玻碳电极用0.3 μm的Al2O3粉抛光至镜面,并用二次蒸馏水冲洗干净,然后分别在二次蒸馏水、无水乙醇、二次蒸馏水中各超声2 min,在室温下晾干待用.用微量进样器将10 μL氧化石墨烯滴加到经上述处理的玻碳电极表面,室温干燥.将晾干后的电极放入0.1 mol·L-1PBS中在电位-1.1 V下还原30 min,即得石墨烯修饰电极.
1.2.2GN/NCC/MB/GCE电极的制备玻碳电极的处理同1.2.1将氧化石墨烯、纳米纤维素、亚甲基蓝按体积比为5∶5∶1混合均匀.用微量进样器将氧化石墨烯、纳米纤维素和亚甲基蓝的均匀混合液体10 μL滴加到经上述处理的玻碳电极表面,室温干燥.将晾干后的电极放入0.1 mol·L-1PBS中在电位-1.1 V下还原30 min,即得石墨烯/纳米纤维素/亚甲基蓝修饰电极.
1.3电化学检测方法采用标准三电极体系:饱和甘汞电极(saturated calomel electrode,SCE)为参比电极,铂丝为对电极,玻碳电极(直径4 mm)或经过GN和GN/NCC/MB修饰的玻碳电极作为工作电极.以60.0 mL pH=7.0的 PBS溶液作为支持电解质溶液,(25±0.5) ℃的条件下进行循环伏安测试.
2实验结果与讨论
2.1AA、UA在GN/NCC/MB/GCE电极上的电化学行为图1表示GN修饰的玻碳电极和GN/NCC/MB复合材料修饰的电极分别在含有AA(0.4 mmol·L-1)和不含有AA的0.1 mol·L-1的PBS溶液中的循环伏安曲线.图1(a)为GN电极修饰的电极在不含有AA的PBS溶液中的循环伏安曲线,图1(b)为GN/NCC/MB复合材料修饰的玻碳电极在不含有AA的PBS溶液中的循环伏安曲线,从图中可以看出图1(b)在-0.4~-0.2 V(vs.SCE)之间有一对氧化还原峰,这是MB染料在PBS溶液当中的特征氧化还原峰.图1(c)为GN修饰的玻碳电极在含有AA(4.0 mmol·L-1)的PBS溶液中的循环伏安曲线,可以看出在电位为0.178 V(vs.SCE)处出现了一个氧化峰,这个氧化峰是AA的特征氧化峰[6],图1(d)为GN/NCC/MB修饰的玻碳电极在含有AA(4.0 mmol·L-1)的循环伏安曲线,从图中可以看出,在-0.4~-0.2 V(vs.SCE)处MB的氧化还原特征峰仍然存在,并且峰电位和峰电流与图1(b)变化不大,但与图1(c)相比AA的氧化特征峰峰电位由0.178 V(vs.SCE)负移至0 V(vs.SCE),峰电流由50 μA增加至70 μA,增加了近20 μA.这可能是由于石墨烯、纳米纤维素和亚甲基蓝三者形成的复合材料中三者协同作用使得该种复合材料修饰的电极对抗坏血酸有明显的催化作用所致.
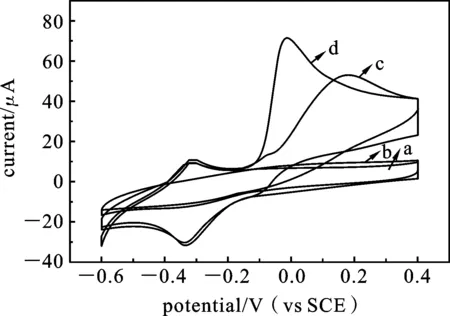
图1 GN电极(a,c)和GN/NCC/MB电极(b,d)在不含(a,b)和含有4.0mmol·L-1AA(c,d)的0.1mol·L-1PBS 中的循环伏安曲线扫描速率: 20 mV·s-1,pH = 7.0
图2为GN和GN/NCC/MB修饰的电极分别在含有UA(0.4 mmol·L-1)和不含有UA的两种PBS溶液中的循环伏安曲线.图2(a)为GN修饰玻碳电极在PBS溶液中的循环伏安曲线,图2(b)为GN/NCC/MB修饰的玻碳电极在PBS溶液中的循环伏安曲线,从图上可以看出在电位为-0.4~-0.2 V(vs.SCE)处有一对明显的氧化还原峰,这是MB的特征氧化还原峰.图2(c)为GN修饰的玻碳电极在含有UA(0.4 mmol·L-1)的PBS溶液(0.1 mol·L-1pH=7.0)中的循环伏安曲线,从图2(c)中可以看出在电位为0.334 V处出现了一个明显的氧化峰,峰电流约为20 μA,这是GN催化氧化UA的特征峰.图2(d)为GN/NCC/MB修饰的玻碳电极在含有UA(0.4 mmol·L-1)的PBS溶液(0.1 mol·L-1,pH=7.0)的循环伏安曲线,图中在-0.4~-0.2 V(vs.SCE)处的氧化还原峰为MB的特征氧化还原峰,与图2(b)相比,峰电位和峰电流变化不大,但在电位为0.301 V处出现了明显的氧化峰,峰电流约为50 μA,与图2(c)相比,峰电位负移至0.301 V,这是UA的特征氧化峰[6],减小了33.0 mV,峰电流由20 μA增加至50 μA,增加为原来的2.5倍.这是由于在GN/NCC/MB复合材料修饰的电极中,石墨烯、纳米纤维素和亚甲基蓝三者的协同作用对尿酸的电化学氧化起到了明显催化作用.
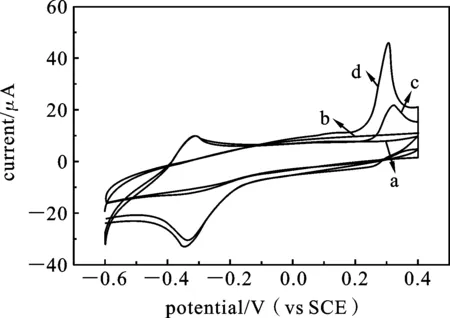
图2 GN电极(a,c)和GN/NCC/MB电极(b,d)在不含(a,b)和含有0.4mmol·L-1UA(c,d)的0.1mol·L-1PBS中的循环伏安曲线(扫描速率:20mV-1,pH=7.0)
2.2GN/NCC/MB/GCE电极上AA与UA共存的电化学响应图3为GN修饰的玻碳电极和GN/NCC/MB修饰的玻碳电极分别在PBS(0.1 mol·L-1,pH=7.0)和含有AA(4.0 mmol·L-1)+UA(0.4 mmol·L-1)的PBS溶液中两种溶液中的循环伏安曲线.图3(a)为GN修饰的玻碳电极在PBS(0.1 mol·L-1,pH=7.0)溶液中的循环伏安曲线,图3(b)为GN/NCC/MB复合材料修饰的玻碳电极,从图中可以看出在电位-0.4~-0.2 V(vs.SCE)出现的一对明显的氧化还原峰为MB的特征氧化还原峰.图3(c)为GN修饰的玻碳电极在含有AA(4.0 mmol·L-1)+UA(0.4 mmol·L-1)的PBS(0.1 mol·L-1,pH=7.0)的溶液中的循环伏安曲线,从图中可以看出在电位为0.35 V处出现了一个明显的氧化峰,而在0.20 V处出现了一个肩峰,这是由于电化学氧化AA和UA时相互干扰[3],两种物质的氧化峰电位很接近,相互杂糅在一起,电化学检测这两种物质产生困难,GN修饰的玻碳电极不能达到将两种物质氧化峰完全分开所致.图3(d)为GN/NCC/MB复合材料修饰的玻碳电极在含有AA(4.0 mmol·L-1)+UA(0.4 mmol·L-1)的PBS(0.1 mol·L-1, pH=7.0)溶液中的循环伏安曲线,从图中可以看出,在电位为-0.4~-0.2 V(vs.SCE)处出现的一对氧化还原峰为MB的氧化还原峰与图3(b)的氧化还原峰电位与电流相近,但在电位为0 V和0.3 V处分别出现了两个明显的氧化峰,并且区分非常明显(ΔEp=0.3 V),这两个氧化峰分别为AA(0 V)的氧化峰和UA(0.3V)的氧化峰,这说明石墨烯、纳米纤维素和亚甲基蓝制备的复合材料可以同时催化氧化UA和AA,并且可以很明显地区分这两种物质的氧化峰电位,有望实现同时进行这两种物质的电化学检测.
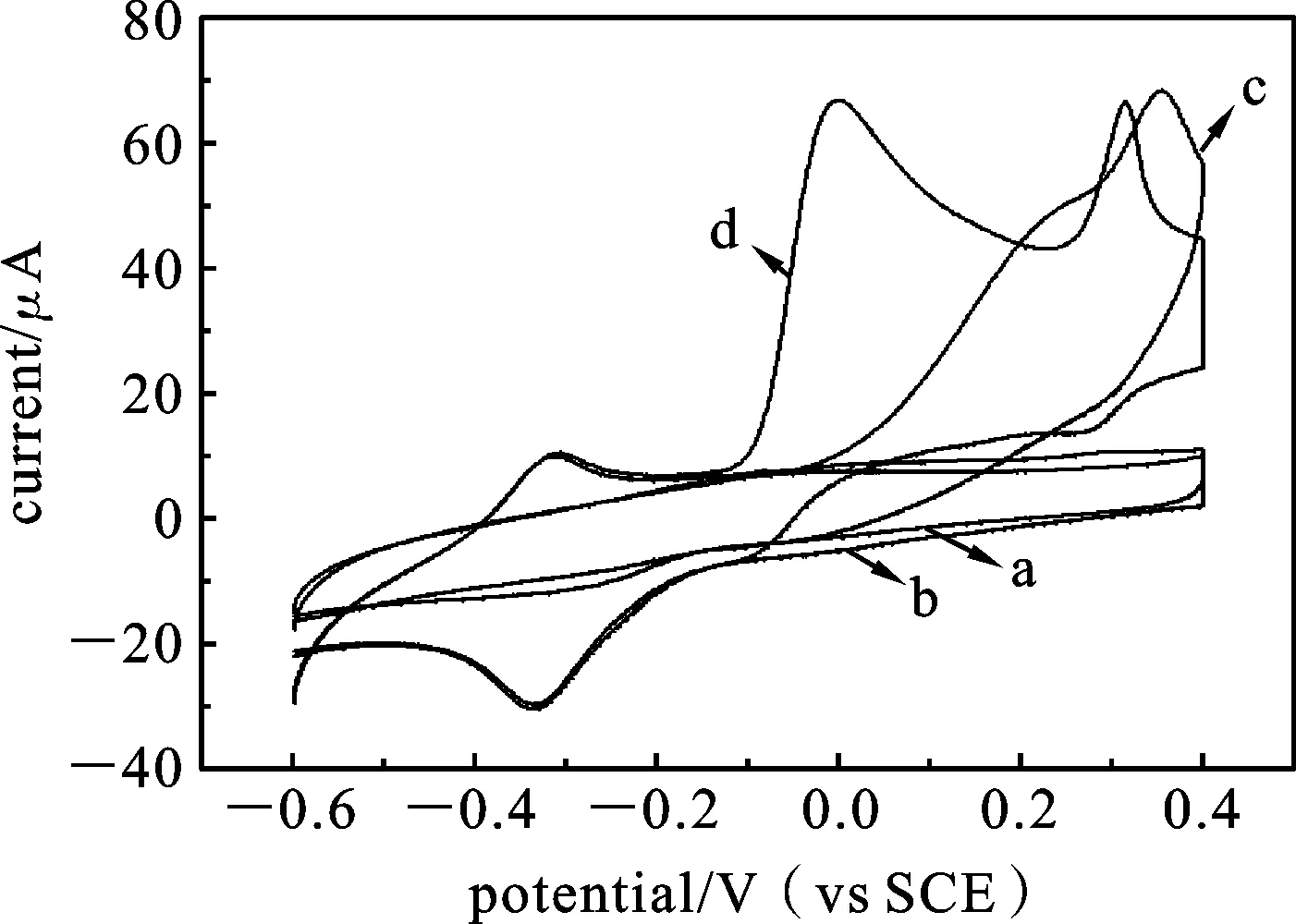
图3 GN电极(a,c)和GN/NCC/MB电极(b,d)在不含(a,b)和含有4.0mmol·L-1AA+0.4mmol·L-1UA(c,d)的0.1mol·L-1PBS中的循环伏安曲线(扫描速率:20mV-1,pH=7.0)
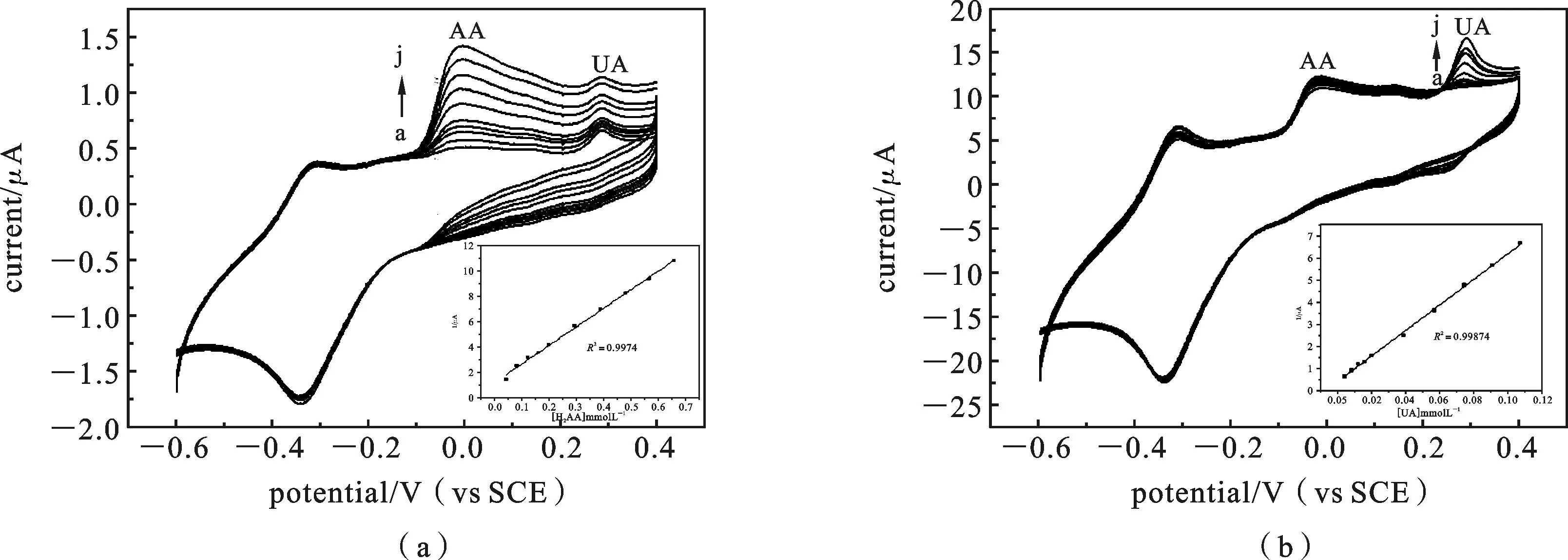
图4 不同浓度的AA(A)和UA(B)共存时GN/NCC/MB/GCE电极的循环伏安曲线扫描速率:20 mV·s-1,pH=7.0(a) CUA=20.0 μmol·L-1, CAA/μmol·L-1(a)~j)):40.0,80.0,120.0,160.0,200.0,300.0,400.0,500.0,600.0,700.0(b) CAA=40.0 μmol·L-1, CUA/μmol·L-1(a)~j)):4.0,8.0,12.0,16.0,20.0,40.0,60.0,80.0,100.0,120.0

图5 AA和UA在GN/NCC/MB/GCE上循环 伏安曲线及其峰电流随其浓度变化关系 (扫描速率:20 mV·s-1,pH=7.0) CAA(μmol·L-1),a)~j):40.0,80.0,120.0,160.0,200.0,300.0,400.0,500.0,600.0,700.0 CuA(μmol·L-1),a)~j):4.0,8.0,12.0,16.0,
2.3AA、UA的检测图4(a)和(b)为GN/NCC/MB修饰的玻碳电极对AA和UA同时存在时固定一种物质含量改变另外一种物质含量时的循环伏安曲线.从图中可以看出UA和AA同时存在时,UA和AA的氧化峰能够明显分开.图(A)为同时含有UA(20.0 μmol·L-1)+AA(40.0 μmol·L-1, 80.0 μmol·L-1, 120.0 μmol·L-1, 160.0 μmol·L-1,200.0 μmol·L-1,300.0 μmol·L-1,400.0 μmol·L-1,500.0 μmol·L-1,600.0 μmol·L-1,700.0 μmol·L-1)的PBS(0.1 mol·L-1, pH=7.0)的溶液中的循环伏安曲线,从图中可以看出保持UA的浓度不变,改变AA的浓度,UA的氧化峰电位不变峰电流变化不大,但随着AA浓度的不断提高,图4(A)插图可以看出AA的峰电流与其浓度在40.0~700.0 μmol·L-1范围内符合线性关系,通过线性拟合处的直线方程为:I(μA)=1.169 58+0.0146 95C:(AA)(μmol·L-1),线性相关系数为0.997,由线性回归方程得出AA的最低检测限度为19.599 μmol·L-1,据此得出一定量UA的存在并不影响AA的线性检测.图4(B)为同时含有AA(40.0 μmol·L-1)+UA(4.0 μmol·L-1,8.0 μmol·L-1,12.0 μmol·L-1,16.0 μmol·L-1,20.0 μmol·L-1,40.0 μmol·L-1,60.0 μmol·L-1,80.0 μmol·L-1,100.0 μmol·L-1,120.0 μmol·L-1)的PBS(0.1 mol·L-1,pH=7.0)溶液中的在电位窗口为-0.6~0.4 V(vs.SCE)中的循环伏安曲线,从图中可以看出保持AA的浓度不变,改变UA的浓度,AA的氧化峰电位和峰电流几乎不变,UA的氧化峰电位几乎不变,氧化峰电流在UA浓度为4.0~120.0 μmol·L-1范围内成线性关系,线性回归方程为:I(μA)=0.402 86+57.730C(UA)(C:μmol·L-1),线性相关系数为0.998,由线性回归方程计算出UA的最低检出限浓度为1.973 6 μmol·L-1,据此得出一定量的AA存在并不影响UA的线性检测.进一步证明了图3中的出的由GN/NCC/MB复合材料修饰电极实现AA和UA同时定量检测的可能性.
3结论
本实验成功制备出GN/NCC/MB复合物电极,并研究了该电极对UA和AA的电化学行为,研究表明,GN/NCC/MB/GCE 电极可同时催化氧化AA和UA.同时存在AA和UA时,两者的氧化峰电位差可达300 mV,相互之间不影响.在同一溶液中同时测定AA和UA的含量,AA与UA氧化峰电流与其浓度分别在40.0~700.0 μmol·L-1,4.0~120.0 μmol·L-1范围内呈线性关系,最低检测限度分别为17.6442 μmol·L-1和3.251 1 μmol·L-1,该种复合材料修饰的玻碳电极可以实现AA和UA共存时定量检测.
参考文献4
[1] Khaw K T ,Bingham S.Relation between plasma ascorbic acid and mortality in men and women in EPIC-Norfolk prospective study: a prospective population study,European prospective investigation into cancer and nutrition[J].Lancet,2001,357 (9257):657-663.
[2] Toncev G,Milicic B.Serum uric acid levels in multiple sclerosis patients correlate with activity of disease and blood-brain barrier dysfunction[J].European Journal of Neurology,2002,9(3):221-226.
[3] 范建凤,崔燕,王庆红,等.金纳米粒子-石墨烯修饰玻碳电极的制备及对多巴胺、抗坏血酸和尿酸的同时检测[J].分析化学学报,2015,3(31):367-371.
[4] 孙娜,王宗花. 聚对氨基苯磺酸/石墨烯复合修饰电极对尿酸的选择性灵敏测定[J].分析测试报,2012,31(7):853-857.
[5] 任旺,张英,丁杰.PCA/GC电极同时测定尿酸(UA)和抗坏血酸(AA)[J].电化学,2009,15(3):345-349.
[6] Yang L,Liu D,Huang J H,et al.Simultaneous determination of dopamine,ascorbic acid,and uric acid at electrochemically reduced grapheme oxide modified electrode[J].Sensors and Actuators B:Chemical,2014 (193):166-172.
[7] 杨勇辉,孙红娟.石墨烯的氧化还原法制备及结构表征[J].无机化学学报,2010,26(11):2083-2090.
[8] Graphene Geim K.Status and prospects[J].Science,2009,324(5934):1530-1534.
[9] 胡耀娟, 金娟, 张卉,等.石墨烯的制备、功能化及在化学中的应用[J].物理化学学报,2010,26(8):2073-2086.
[10] Shin H J,Kim K K,Benayad A,et al.Effcient reduction of graphite oxide by sodium borohydride and its effect on electrical conductance[J].advance functional materials,2009,19(12):1987-1992.
[11] Chen L Y,Tang Y H,Wang K,et al.Direct electrodeposition of reduced graphene oxide on glassy carbon electrode and its electrochemical application[J].Electrochemical Communication,2011(13):133-137.
[12] Liu C,Wang K,Luo S,et al.Direct electrodeposition of graphene enabling the one-step synthesis of graphene-metal nanocomposite films[J].Small,2011,7(9):1203-1206.
[13] Jiang Y Y, Lu Y Z, Li F H, et al.Facile electrochemical codeposition of “clean” graphene-Pd nanocomposite as an anode catalyst for formic acid electrooxidation[J].Electrochemical Communication.2012,19:21-24.
[14] 陈志华,葛玉卿,金庆辉,等.石墨烯复合修饰电极的电化学应用[J].化学传感器,2010,30(4):9-13.
[15] Mao K X,Wu D,Li Y.Lable-free electrochemical immunosensor based on graphene/methylene blue nanocomposite[J].Analytical Biochemistry,2012,422:22-27.
[16] 郭新美,王宗花,夏建飞,等.多巴胺在聚亚甲基蓝/石墨烯修饰电极上的电化学行为研究[J].分析测试学报,2012,31(4):464-469.
[17] 杨怀成, 魏万之, 曾金祥,等.烟酰胺腺嘌呤二核苷酸的聚亚甲基蓝/单壁碳纳米管修饰电极差分脉冲伏安法检测[J].分析测试学报,2008,27(2):135-138.
(责任编辑胡小洋)

Simultaneous determination of ascorbic acid and uric acid at GN/NCC/MB/GCE modified electrode
DOU Yanpeng1,2, LIANG Ying1, PENG Junjun2,LIU Huihong2
(1. School of Chemical Engineering & Food Science,Hubei University of Arts and Science ,Xiangyang 441053, China;
2. College of Chemistry & Chemical Engineering,Wuhan Textile University,Wuhan 430074,China)
Abstract:GN modified electrode and GN/NCC/MB composite modified electrode were prepared by direct electrochemical reduction method,and was used to study the electrochemical behavior of ascorbic acid and uric acid by cyclic voltammetry in PBS solution (0.1 mol·L-1,pH=7.0).The experiments results show that the oxidation peaks potential of AA and UA can be distinguished to 0 V and 0.3 V at a scan rate of 20 mV·s-1respectively,with a potential difference of 300 mV,which is large enough to determine UA and AA individually and simultaneously.In the mixed solution of AA and UA,two experimental modes were adopted to study the linear relationship between the oxidation peak current of AA (UA) and the concentration of AA(UA),the experiments shows that the catalytic peak current obtained is linearly dependent on the UA and AA concentration in the range of 40.0—700.0 μmol·L-1,4.0—120.0 μmol·L-1in 0.1 mol·L-1(pH=7.0),and the detection limit is 17.644 2 μmol·L-1and 3.251 1 μmol·L-1,respectively.GN/NCC/MB composite modified electrode can realize the quantitative determination of AA and UA in the mixed solution simultaneously.
Key words:graphene;nano-crystalline cellulose;methylene blue;ascorbic acid;uric acid;modified electrode
中图分类号:TQ32
文献标志码:ADOI:10.3969/j.issn.1000-2375.2016.01.014
文章编号:1000-2375(2016)01-0073-06
通信作者
作者简介:窦砚鹏(1989-),男,硕士生;彭俊军,,博士,副教授,E-mail:johnpeng@wtu.edu.cn;梁英,通信作者, 博士,教授,E-mail: xfliangy@163.com
基金项目:国家自然科学基金(51378183)资助
收稿日期:2015-09-04
