葡萄糖对共沉淀法制备Li2FeSiO4正极材料的影响
2016-02-15张宏皓
张宏皓,张 卿,任 冰
(1. 陕西应用物理化学研究所,陕西 西安,710061;2. 西安建筑科技大学,陕西 西安,710000)
葡萄糖对共沉淀法制备Li2FeSiO4正极材料的影响
张宏皓1,张 卿2,任 冰1
(1. 陕西应用物理化学研究所,陕西 西安,710061;2. 西安建筑科技大学,陕西 西安,710000)
采用两步沉淀工艺制备了锂离子电池正极材料Li2FeSiO4,通过加入不同含量的葡萄糖,研究了不同碳含量对Li2FeSiO4的结构及形貌的影响。结果表明:所有样品都是纯相的Li2FeSiO4;碳包覆后的颗粒粒径明显减小,尺寸在300~500nm之间;碳包覆可以有效提高锂离子电池正极材料Li2FeSiO4的电子电导率;6wt%碳含量下的样品0.1C下首次放电容量可达152.3mAh/g,0.5C下循环50次容量保持率为87.7%,具有良好的电化学性能。
正极材料;共沉淀法;硅酸铁锂;电化学性能
2005年Nyten等人[1]以硅酸锂、草酸亚铁和正硅酸乙酯为原料,通过高温固相法合成Li2FeSiO4正极材料。该材料以其资源丰富、环境友好、高安全性及循环稳定性好等优点受到了广泛的关注,但电子导电率和锂离子扩散速度低的缺点阻碍了其在商业中的应用[2]。目前对于材料的改善方法主要有颗粒尺寸及形貌的优化[3],导电剂的包覆[4]及阴阳导电离子的掺杂[5],其中碳包覆是一种常见的改性手段。葡萄糖的结构和成分稳定,杂质含量少,碳氢含量适中,裂解后成分稳定,成为制备Li2FeSiO4最常用的碳源。本文采用共沉淀法,选取葡萄糖为碳源,研究了不同含碳量对材料的形貌结构以及电化学性能的影响,确定了最佳的碳包覆条件。
1 实验方法
1.1 样品的制备
按摩尔比将分析纯的正硅酸乙酯(TEOS)与酒精混合均匀后,在碱性环境(氨水)下,TEOS水解缩聚生成SiO2白色沉淀,将一定计量比的抗坏血酸加入到悬浊液中,调节pH值至6;然后将硫酸亚铁溶入去离子水中,充分搅拌待其完全溶解后缓慢滴加到上述白色悬浊液中,常温常压下搅拌1h;二次沉淀得到浅黄色的悬浊液后,加入丙酮并放置于离心机中分散得到黄色沉淀物;分别加入质量百分比为0%、3%、6%、9%的葡萄糖溶液,加入一定化学计量比的锂源,放置于球磨罐中并抽真空处理,通入氮气以保证球磨罐中惰性气体保护。球磨后放置于真空干燥箱内并设置温度50℃,干燥2h后得到前驱体材料,在氩气气氛下进行热处理,进行不同热烧结温度和不同保温时间的热烧结工艺处理,合成目标产物Li2FeSiO4/C正极材料。
1.2 样品的表征
采用XRD-7000型X射线衍射仪进行物相分析,工作电压为40kV,电流为40mA,扫描角度为15~85°。选用Cu的Kα射线,用JSM-6700型场发射扫描电子显微镜对试样进行形貌分析,加速电压30kV。采用日本生产的JEM-2100F型透射电镜进行形貌观察。
1.3 实验电池的组装与测试
以NMP(N-甲基吡咯烷酮)为溶剂,按活性物质、乙炔黑、粘结剂(PVDF)质量比85∶5∶10混合研磨,涂于铝箔上,然后120℃真空干燥4h得正极涂片;以锂片为负极,1mol/L的LiPF6/EC(碳酸乙烯酯)+ DEC (碳酸二乙酯)(1∶1,V/V)为电解液,聚丙烯多孔膜(Celgard2400)为隔膜,在氩气手套箱中装配成扣式模拟电池,于BTS-5V/10mA电化学测试仪上恒流充放电测试,充放电电压为1.5~4.5V。于PAR2273电化学工作站测试样品的交流阻抗,频率范围1×10-2~1 ×106Hz。
2 结果与讨论
2.1 结构与形貌分析
图1为不同碳含量下Li2FeSiO4/C样品的XRD图。从图1中可以看出,4组样品的特征峰峰形与文献[6]报道的XRD谱一致,说明所制备的样品都是纯相。图谱中没有出现碳的衍射峰,分析其原因是由于碳以非晶态或无定形的形式存在,这也说明碳的加入并没有影响Li2FeSiO4的晶体结构。从图谱中可以看出随着碳含量的增加,样品的特征峰高度先增后减,各样品衍射峰峰型尖锐,强度较高,底背平坦,半峰宽较窄,表明各组Li2FeSiO4材料纯度较高、结晶度较好,晶粒发育较为完善。图2为不同碳含量下Li2FeSiO4/C样品的SEM照片。
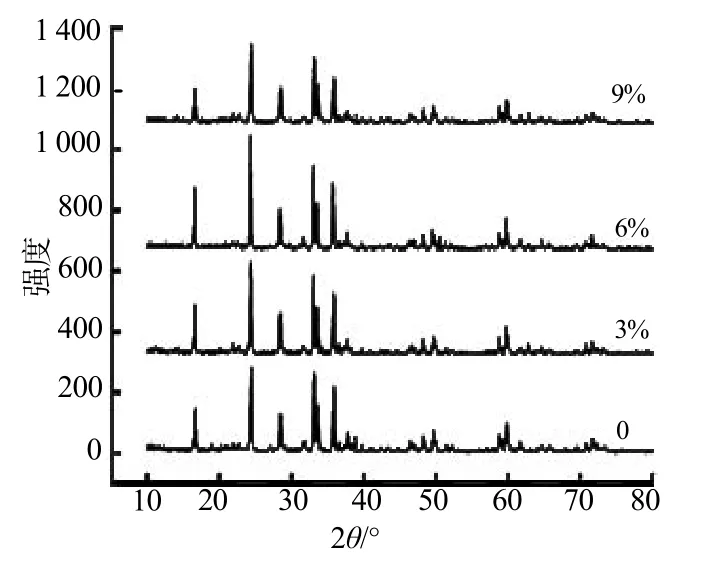
图1 不同碳含量下Li2FeSiO4/C样品的XRD图Fig.1 XRD patterns of Li2FeSiO4/C samples with different carbon contents

图2 不同碳含量下Li2FeSiO4/C样品的SEM照片Fig.2 SEM images of Li2FeSiO4/C samples with different carbon content
从图2中可以看出:葡萄糖量对样品颗粒形貌和样品分散性的影响较为严重。碳包覆少量时,图2(a)和图2(b)中的样品呈较为规则的类球形,一次粒径在600~800 nm之间,粒径分布较宽,且团聚现象较为明显。这是由于在烧结过程中,葡萄糖的含量较少而不能有效地分散在每个颗粒表面,造成颗粒与颗粒之间的粘结。随着碳包覆量的升高,颗粒粒径明显减小,一次粒径在300~500nm之间,颗粒分布的一致性更好,说明葡萄糖的加入可以拟制晶粒的生长,因此添加碳的样品颗粒细小,这也将大大增加材料的导电率。
图3为不同碳含量下Li2FeSiO4/C样品的TEM照片。观察图3可以看出,图3(a)样品表面的碳层并不明显,少量的碳层是由于在前驱体中添加的少量抗坏血酸高温下分解形成的。图3(b)、(c)和(d)中样品的碳层是由抗坏血酸与添加的葡萄糖共同作用的结果,从图3中明显可以看出,随着葡萄糖量的增加,颗粒表面的碳层厚度也逐渐增加,但图3(b)样品表面碳层分布很不均匀。

图3 不同碳含量下Li2FeSiO4/C样品的TEM照片Fig.3 TEM images of Li2FeSiO4/C samples with different carbon content
2.2 EDS分析
从TEM分析中可以看出碳层厚度随着葡萄糖量的增加而逐渐变厚。为了更好地研究碳含量的变化,对加入葡萄糖后的3组样品进行了EDS测试。表1中列举不同碳含量下的Li2FeSiO4/C样品的能谱测试数据。表1中b组样品中碳元素平均量为9.03%;c组样品中碳元素平均量为16.46%;d组样品中碳元素平均量为24.40%。可以看出随着葡萄糖加入量的上升,碳元素的平均重量百分比呈现上升趋势。
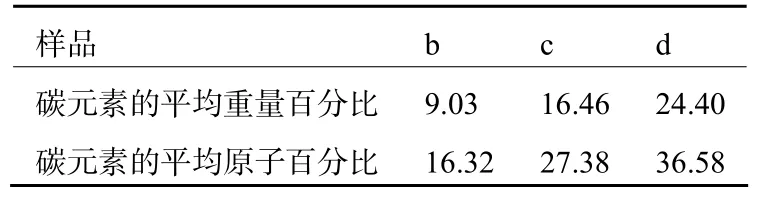
表1 不同碳含量的EDS测试数据Tab.1 EDS test data of Li2FeSiO4/C samples with different carbon content
2.3 电化学性能分析
为了研究葡萄糖添加量对Li2FeSiO4/C的电学性能影响,对各组样品进行了恒流充放电测试。图5为 4组样品室温下在0.1C下的首次充放电曲线图,测试过程中电压范围为1.5~4.0V。
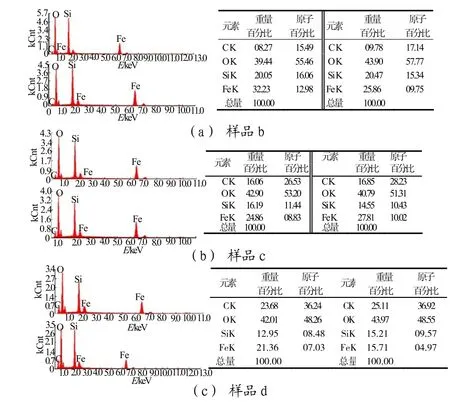
图4 不同含碳量下Li2FeSiO4/C样品的EDS分析图Fig.4 EDS analysis chart of Li2FeSiO4/C samples with different carbon content
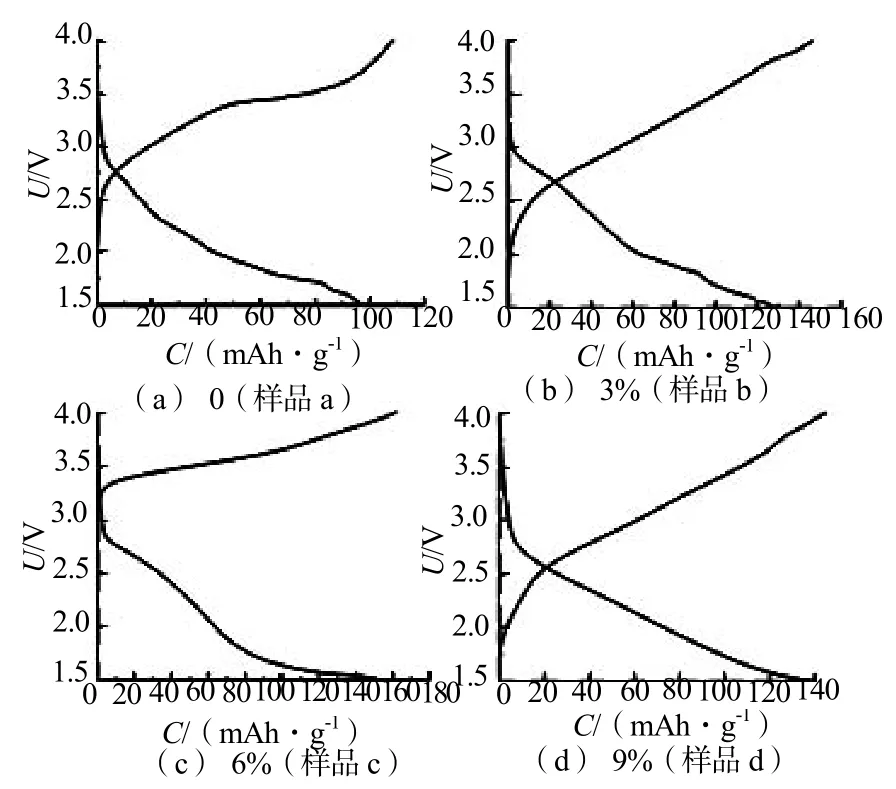
图5 不同含碳量下Li2FeSiO4/C样品的首次放电曲线Fig.5 Initial discharge curves of Li2FeSiO4/C samples with different carbon content
4组样品的首次充电容量分别为108.2mAh/g,146.4mAh/g,161.7mAh/g,144.7mAh/g。首次放电容量分别为96.7mAh/g,129.1mAh/g,152.3mAh/g,139.6mAh/g。充放电效率分别为89%,88%,94%,96%,其中样品c的放电比容量和库仑效率最高。观察可以发现,随着葡萄糖量的增加, 图5(b)、(c)、(d)样品的放电容量均大于未掺碳的图5(a)样品的放电容量。首次充放电结果说明一方面葡萄糖作为还原剂可以拟制Fe2+氧化为Fe3+,有效地减少杂质的产生,另一方面导电碳越来越均匀地包覆在Li2FeSiO4颗粒表面和分布颗粒之间,可以有效地提高材料的电导率,使得样品的放电比容量增大。但是当碳含量增加到9%时,样品容量反而相对减小,可能是因为葡萄糖添加过多导致Li2FeSiO4颗粒表面包覆的碳层过厚,反而会阻碍锂离子的脱出和嵌入,从而导致其电化学性能有所下降。
图6为各组Li2FeSiO4/C样品分别在0.2C、0.5C和1C下的放电曲线图,图6(a)样品的放电容量分别为79.5 mAh/g、66.2mAh/g、50.2mAh/g,图6(b)样品的放电容量分别为113.3 mAh/g、96.6 mAh/g、84.1mAh/g,图6(c)样品的放电容量分别为141.8 mAh/g、127.3 mAh/g、103.8mAh/g,图6(d)样品的放电容量分别为124.2 mAh/g、108.7 mAh/g、90.3mAh/g;其中图6(c)样品在较大倍率1C下的放电容量仍有103.1mAh/g,远远高于其他样品,说明适当的含碳量会有效地改善材料的倍率性能。而图6(d)样品由于过厚的碳层,使得该样品的倍率性能相比于图6(c)样品有所下降。
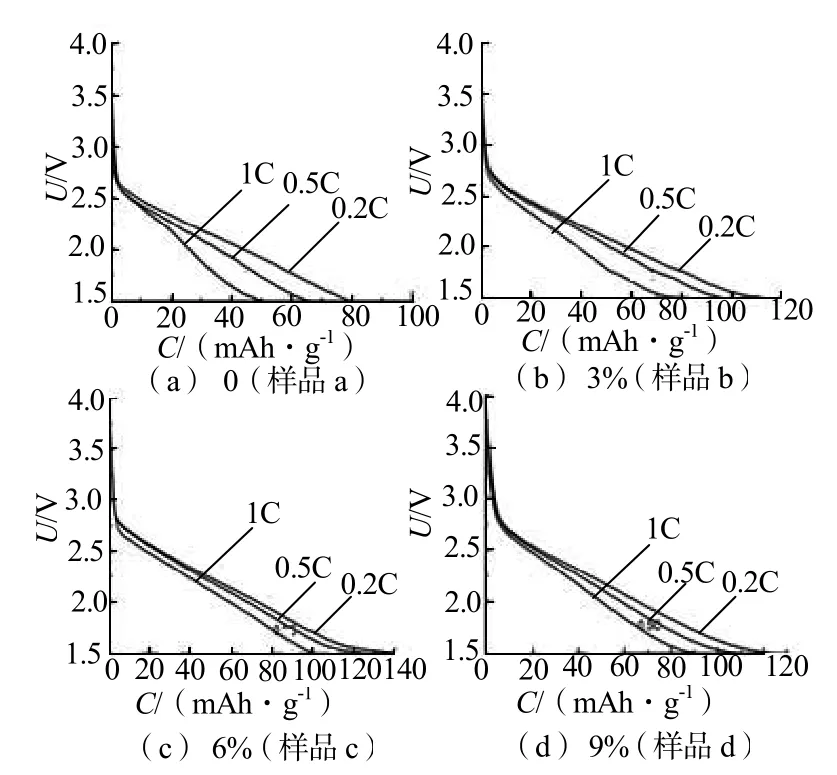
图6 不同含碳量下Li2FeSiO4/C样品的不同倍率放电曲线Fig.6 Rate capability of Li2FeSiO4/C samples with different carbon content
图7是各组Li2FeSiO4/C样品在0.5C下的循环50次放电曲线。由图7可以看出含碳量为0的Li2FeSiO4/C样品循环50次后容量为33.5mAh/g,保持在首次的50.6%;碳含量为6%的Li2FeSiO4/C循环50次后容量为111.7mAh/g,保持在首次的87.7%;碳含量为9%的Li2FeSiO4/C循环50次后容量为91.7mAh/g,保持在首次的84.4%。随着含碳量的增加,样品的容量保持率呈先增大后减小的趋势,说明适当的碳包覆对Li2FeSiO4/C材料的循环性能可以起到改善效果。同时相比图6样品,3组碳包覆样品容量的衰减更为缓慢,说明葡萄糖的添加对Li2FeSiO4/C材料容量的保持具有很重要的作用。
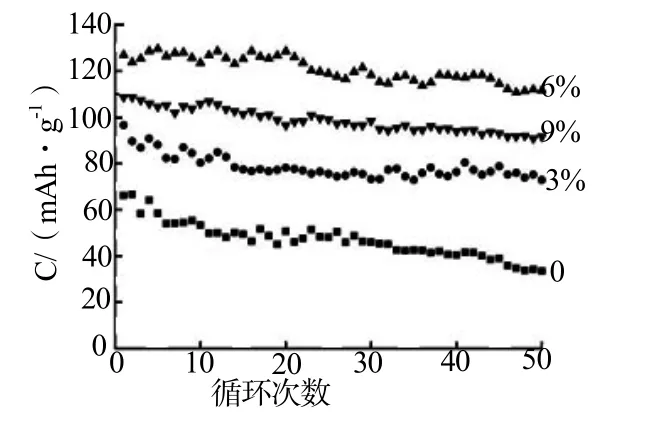
图7 不同含碳量下Li2FeSiO4/C样品的循环曲线Fig.7 Cycle behavior of Li2FeSiO4/C samples with different carbon content
为了研究葡萄糖的添加对Li2FeSiO4/C材料电导率的影响,进行了交流阻抗测试。图8为不同碳含量下Li2FeSiO4/C样品的交流阻抗测试图谱以及Z′——ω-1/2的关系曲线图,通过交流阻抗的计算可以得到不同碳含量下Li2FeSiO4/C样品的锂离子材料扩散速率,如表2所示。

表2 不同葡萄糖添加量制备的Li2FeSiO4/C样品的锂离子扩散速率Tab.2 Diffusion coefficient of Li2FeSiO4/C samples with different carbon content
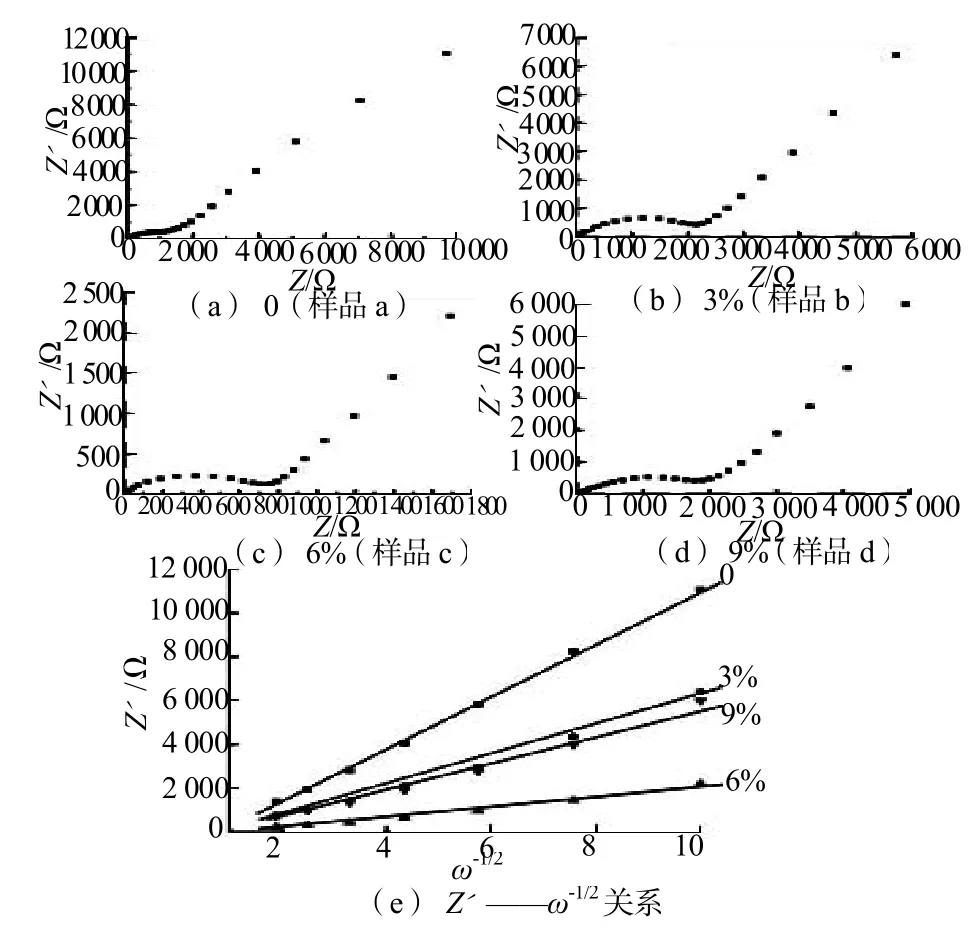
图8 不同含碳量下Li2FeSiO4/C样品的交流阻抗谱及Li2FeSiO4/C在低频区中Zre与ω-1/2的关系曲线图Fig.8 The EIS and the relationship between Z and ω-1/2of Li2FeSiO4/C samples with different carbon content
从交流阻抗的测试结果可以看出:样品c的锂离子扩散速率最大,较其他样品有了很大的改善,这主要归因于适当的含碳量在样品颗粒的表面形成了一层均匀的碳层,并在颗粒之间分散着有效的导电碳网络,有利于锂离子的迁移和扩散,提高Li2FeSiO4的动力学性能,有效地提高了材料的电导率,减小了材料的电化学极化现象。而样品d的锂离子扩散系数较样品c有所降低,原因可能是由于过厚的碳层会增加Li+在颗粒中的迁移距离,影响材料的离子电导率。所以,适当的碳含量有利于Li+的嵌入和脱出,有利于材料电化学性能的提高。结合交流阻抗测试结果可知,样品a和样品b中,碳层太薄或者不均匀对提高材料的电导率作用不大,而样品d中颗粒表面分布着约10nm厚的碳层,过厚的碳层会严重阻碍锂离子的嵌入和脱出,造成材料电导率的下降。只有样品c表面分布着4~6nm厚的碳层,适当厚度的碳层会有效地提高材料的电导率,增大材料的锂离子扩散速率,减小材料的极化现象,改善材料的电化学性能。
3 结论
(1)通过两步沉淀工艺得到了Li2FeSiO4/C前躯体材料,并在不同碳含量下成功合成了Li2FeSiO4/C正极材料,随着碳含量的增加,材料粒径呈变小趋势,且材料表面的碳层越来越均匀。
(2)通过电化学性能测试,结果表明含碳量在6%的Li2FeSiO4/C正极材料具有较高的锂离子扩散系数和良好的放电容量,在不同的放电倍率下表现出较高的容量保持率和稳定的循环性能。
[1]A, ABOUIMRANE A, ARMAND M, et al. Electrochemical performance of Li2FeSiO4as a new Li-battery cathode material[J]. Electrochemistry Communications, 2005, 7(2): 156-160.
[2]李云松,傅儒生,程璇,等.前驱体固相法制备硅酸铁锂正极材料[J].硅酸盐学报,2011,39(7):1 097-1 101.
[3]Zhang S, Deng C, Yang S. Preparation of nano-Li2FeSiO4as cathode material for lithium-ion batteries [J]. Electrochemical and Solid-State Letters, 2009, 12(7): A136-A139.
[4]Li L, Guo H, Li X, et al. Effects of roasting temperature and modification on properties of Li2FeSiO4/C cathode [J]. Journal of Power Sources, 2009, 189(1): 45-50.
[5]Deng C, Zhang S, Yang S Y. Effect of Mn substitution on the structural, morphological and electrochemical behaviors of Li2Fe1-xMnxSiO4synthesized via citric acid assisted sol-gel method [J]. Journal of Alloys and Compounds, 2009, 487(1): L18-L23.
[6]Zaghib K, Salah A A,Ravel N, et al. Structural magnetic and electrochemical properties of lithium iron orthosilicate [J]. Journal of Power Sources, 2006, 160(2): 1 381-1 386.
The Influence of Glucose on Li2FeSiO4Cathode Material Performance
ZHANG Hong-hao1,ZHANG Qing2,REN Bing1
(1. Shaanxi Applied Physics and Chemistry Research Institute, Xi’an, 710061;2.Xi’an University of Architecture and Technology, Xi’an, 710000)
The cathode material of Li2FeSiO4for lithium-ion battery was prepared via two steps precipitation method. The influence of different carbon content on the structure and morphology of the Li2FeSiO4were analyzed via the addition of different content of glucose. The test results show that all samples are pure Li2FeSiO4, the particle size of samples (300~500nm) decreases after the carbon coating. The electronic conductivity of the Li2FeSiO4is improved after carbon coating, the first discharge capacity of 152.3mAh/g could be obtained at 0.1C rate, when the carbon content is 6wt%, the capacity was maintained at 87.7% after 50 cycles at 0.5C, which explained it has a better electrochemical performance.
Cathode material;Co-precipitation method;Lithium iron silicate;Electro-chemical property
TM911
A
1003-1480(2016)06-0053-05
2016-09-17
张宏皓(1985 -),男,助理工程师,主要从事锂电池产品研发。
