从高砷铜烟尘中综合回收有价金属的研究
2016-02-11聂颖
聂 颖
(中国恩菲工程技术有限公司, 北京 100038)
从高砷铜烟尘中综合回收有价金属的研究
聂 颖
(中国恩菲工程技术有限公司, 北京 100038)
本文介绍了高砷白烟灰的湿法处理工艺,并通过试验得到各工序的最佳技术条件,最终确定“纯硫酸浸出- 氧化除铁砷- 沉铜- 沉锌”的工艺流程,白烟灰中有价金属分别以海绵铜、铅渣、碱式硫酸锌的形式回收利用,而砷与铁共同沉淀并以稳定的砷酸铁的形式从系统开路。研究结果表明:采用此工艺流程,白烟灰中铜的回收率可达到~85%,锌的回收率可达到~84%,铅的回收率大于98%。
高砷烟尘; 湿法冶金; 砷酸铁
铜冶炼过程中,经熔炼和吹炼后大部分易挥发元素(砷、铅、锌、锑等)进入烟气,最后以氧化物或硫酸盐的形态存在于烟尘中,该烟尘一般俗称白烟灰。铜冶炼过程产生的白烟灰化学成分十分复杂,其中不但含有Cu、Zn、Pb、Sb、Cd及In、Ge有价金属元素,同时含有砷等有害元素,若直接返回铜冶炼系统,会大大增加入炉原料的杂质含量,恶化炉况,降低炉子处理能力,同时砷、锑、铋等杂质的循环累积将直接影响电铜质量[1]。此外,砷还将影响制酸触媒使用寿命进而降低二氧化硫转化率和硫酸质量[2]。因此,将白烟灰中有害元素开路并综合回收其中的有价金属十分必要。
本文以我国某铜冶炼企业冶炼过程中产生的高砷白烟灰为原料,并结合该企业现有生产工艺流程,系统地研究了白烟灰中有价金属元素的浸出、分离及回收工艺。
1 试验原料
试验选用高砷白烟灰的主要成分见表1、白烟灰物相见表2。

表1 高砷白烟灰主要成分 %
表2白烟灰物相表
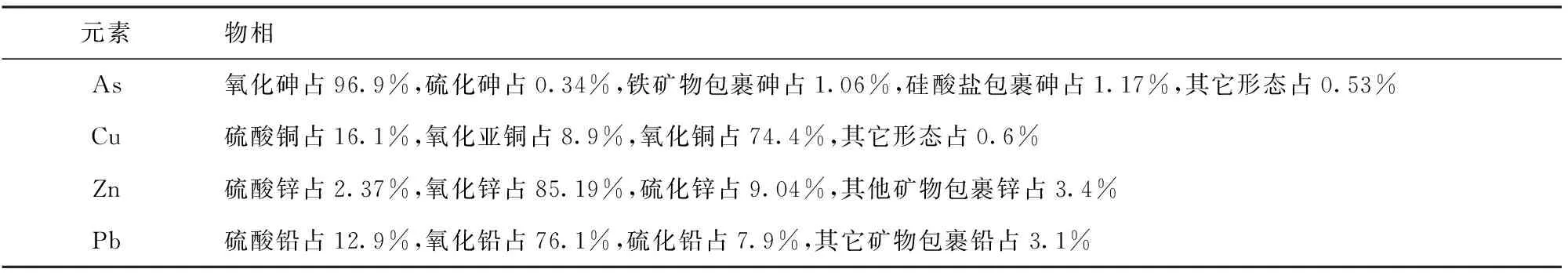
元素物相As氧化砷占96.9%,硫化砷占0.34%,铁矿物包裹砷占1.06%,硅酸盐包裹砷占1.17%,其它形态占0.53%Cu硫酸铜占16.1%,氧化亚铜占8.9%,氧化铜占74.4%,其它形态占0.6%Zn硫酸锌占2.37%,氧化锌占85.19%,硫化锌占9.04%,其他矿物包裹锌占3.4%Pb硫酸铅占12.9%,氧化铅占76.1%,硫化铅占7.9%,其它矿物包裹铅占3.1%
试验辅助材料主要有:
浓硫酸:分析纯试剂,含H2SO498%;
双氧水:分析纯试剂,含H2O230%;
二氧化锰:工业试剂,含MnO270%;
石灰乳:分析纯试剂氧化钙,配制浓度20%;
铁粉:工业用,含Fe 95%;
硫酸高铁:分析纯试剂,含Fe3+22%。
2 工艺流程
目前国内大部分铜冶炼厂采用的湿法工艺流程为“白烟尘- 浸出(水浸或稀硫酸浸出)- 沉铜- 除铁砷- 沉镉- 蒸发结晶沉锌(产品为七水硫酸锌)”,浸出渣即铅渣送火法处理,海绵铜送铜系统,铁砷渣堆存,海绵镉及七水硫酸锌外售[3]。由于该企业原料中As含量高(9%~15%),出于安全考虑,浸出后液先除砷后除铜。该企业自有铅系统及锌系统,浸出渣即铅渣送自有铅系统处理以进一步回收其中的铅,后续沉锌直接生产碱式硫酸锌送自有锌系统作为中和剂使用。最终确定采用硫酸浸出- 除砷- 除铜- 沉锌工艺,工艺流程如图1所示。
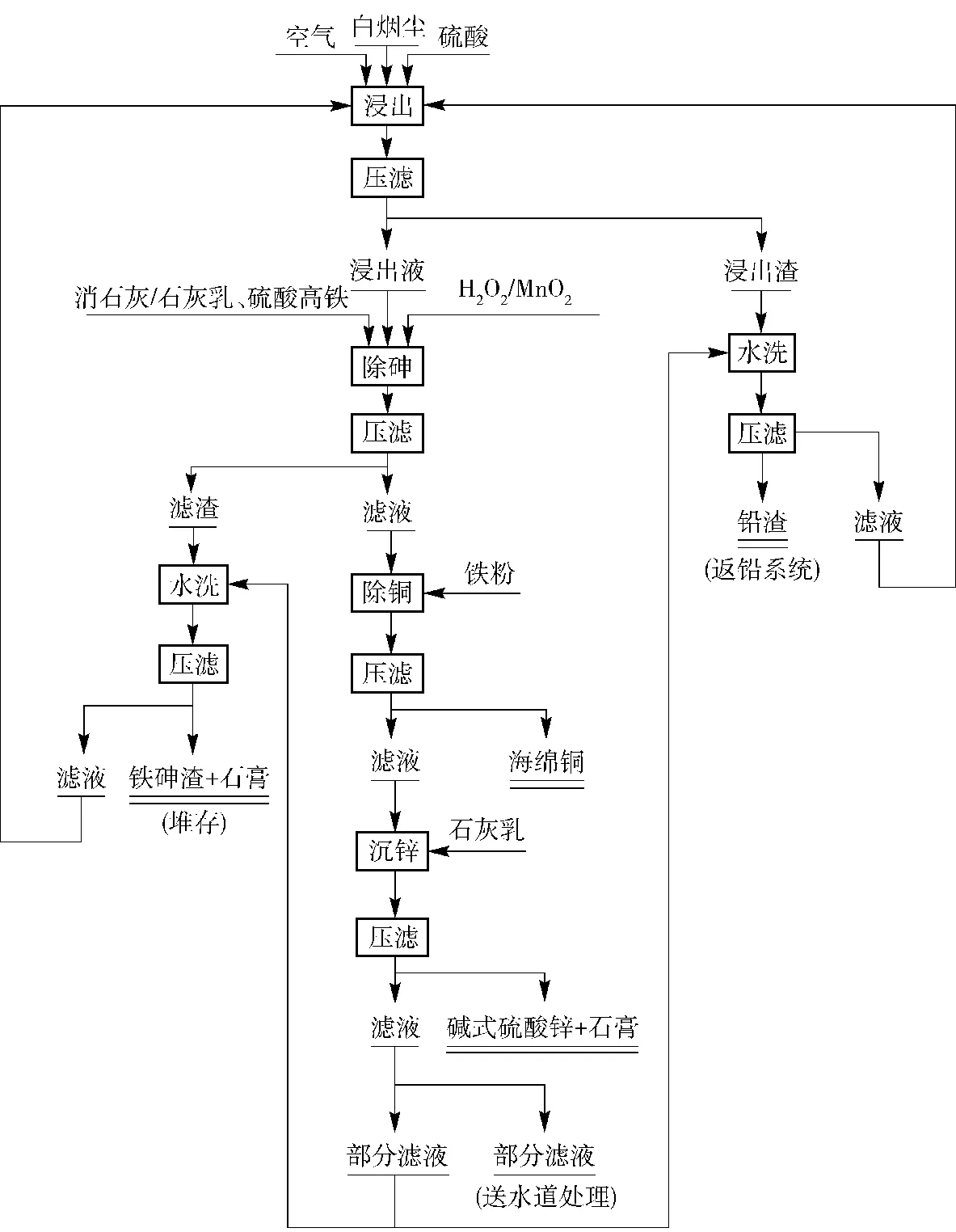
图1 工艺流程图
3 工艺原理
3.1 浸出
浸出过程,就是以稀硫酸溶液作溶剂,将白烟灰中Cu、Zn等有价金属溶解进入溶液的过程。其主要化学反应方程式如下:
3.2 除砷
加入硫酸高铁和氧化剂(本试验最终选用双氧水),同时通入石灰乳以控制反应终点的pH值,使铁和砷以稳定的砷酸铁形式沉淀。其主要化学反应方程式如下:
2FeAsO4·2H2O↓+3H2SO4
3.3 除铜
利用铁、铜两种金属的电极电位不同,采用加铁粉的办法,使浸出溶液中的铜被置换出来,得到海绵铜。其主要化学反应方程式为:
3.4 沉锌
加入石灰乳,控制溶液的pH值,用化学沉淀法使锌以碱式硫酸锌形式沉淀。其主要化学反应方程式为:
ZnSO4·3Zn(OH)2·4H2O↓+3CaSO4·2H2O↓
4 试验结果与讨论
4.1 浸出
浸出时,首先将白烟灰浆化,同时加入一定量的硫酸进行预酸化,之后在浸出烧杯补充需要的水,升温,搅拌。浸出条件为:浸出液初始酸度1 mol/L,温度85~90 ℃,浸出时间2 h,终酸0.3~0.4 mol/L。浸出矿浆进行过滤,滤渣经洗涤过滤得到铅渣。得到金属平均浸出率分别为:Cu 88.67%,Zn 85.81%,Fe 40.40%,As 63.79%;平均渣率46%~47%,浸出渣成分:Cu 1.07%,Zn 4.95%,Fe 3.10%,As 6.00%,Pb 25.5%。
本文做了纯硫酸浸出及硫酸+氧化剂的氧化浸出,关于氧化剂的选择,出于经济性考虑,工厂一般选择二氧化锰作为氧化剂,但系统中引入了锰离子需要在后续工序中考虑脱除,本试验还考虑了双氧水作为氧化剂,加入双氧水系统不带入其他杂质,于后续工序有利。
4.1.1 不同氧化剂的选择对浸出率的影响
本试验研究了液固比3.5∶1条件下纯硫酸浸出、硫酸+二氧化锰的氧化浸出、硫酸+双氧水的氧化浸出,三种条件下各金属元素的浸出率见表3。

表3 不同氧化剂条件下各元素的浸出率%
从表3可以看出:
在液固比为3.5∶1条件下,H2SO4+MnO2(Ⅰ,Ⅱ,Ⅲ)浸出效果较差,各元素浸出率均较低。对于Cu和Zn的浸出效果而言,H2SO4+H2O2(Ⅱ)以及H2SO4(Ⅱ)的效果最佳,Cu的浸出率可达到将近90%,而Zn的浸出液也接近87%。但相比纯硫酸浸出,H2SO4+H2O2(Ⅱ)浸出时其As的浸出率仅略高于60%,Fe的浸出率约为25%,而H2SO4(Ⅱ)浸出时As的浸出率最高可到约74%,Fe的浸出率也能达到约34%。由此可见,纯硫酸浸出效果好于氧化浸出,浸出工艺最终选择纯硫酸浸出。分析氧化浸出效果不好的原因,可能是已浸出的三价铁和五价砷提前生成砷酸铁沉淀而进入铅渣。
4.1.2 液固比对浸出率的影响
针对纯硫酸浸出,做了三组3.5∶1和4∶1的对比试验,试验结果见表4。

表4 纯硫酸浸出不同液固比条件下各元素的浸出率 %
从表4可以看出,液固比3.5∶1与4∶1时浸出率相差不大,结合该企业现有生产流程,选择液固比4∶1。
4.2 除砷
在浸出后液中加入硫酸高铁,搅拌。反应条件为:温度85~90℃,硫酸高铁加入量保持铁砷摩尔比(1~1.05)∶1,反应时间4 h,加入石灰乳控制终酸pH=1.0~1.2。反应后矿浆进行过滤,滤渣经洗涤过滤得到铁砷渣,铁砷渣成分:Cu 0.28%,Zn 0.25%,Fe 5.42%,As 7.50%。
4.2.1 不加氧化剂直接脱砷
本试验先研究了不加氧化剂情况下的脱砷率,得到试验结果见表5。
从结果可以看出,不加氧化剂直接用高铁脱砷,两组脱砷率均在50%上下,说明大部分的砷并不是以五价砷的形式存在于浸出后液,无法直接用高铁脱除,考虑溶液中砷部分为三价砷,需要同时加入氧化剂。氧化剂仍选用二氧化锰和双氧水。

表5 不加氧化剂条件下的脱砷率 %
4.2.2 不同摩尔比对除砷率的影响
本试验考察二氧化锰和双氧水两种氧化剂按照不同摩尔比加入对脱砷率的影响,试验结果见表6。
表6两种氧化剂在不同摩尔比条件下的脱砷率

摩尔比脱砷率/%CuZnAs终点pH13.492.8783.221.05Mn∶As1.511.6110.2492.231.2522.051.5645.290.9246.445.6176.471.1012.241.8085.791.09H2O2∶As1.56.935.6794.101.2128.617.6571.851.1045.765.7793.111.04
单从MnO2和H2O2两种氧化剂的脱砷结果对比可以看出,两者用量与砷的摩尔比相同时,其脱砷效果基本相近;对比Mn∶As=1和H2O2∶As=1两组试验结果可以看出,两者在脱砷率、铜损失率以及锌损失率上基本一致,且经计算双氧水的利用率~85%,较二氧化锰的利用率~83%略高。同时从后面逐渐增大Mn和H2O2与As的摩尔比可以看出,过量的两种氧化剂并未使脱砷率得到明显提升,本试验选择双氧水作为氧化剂同时确定H2O2∶As=1接着做后续试验。
4.2.3 不同终点pH值对除砷率的影响
在双氧水作为氧化剂同时H2O2∶As摩尔比=1的条件下,补充两组试验,试验结果见表7。
表7H2O2∶As=1摩尔比条件下的脱砷率
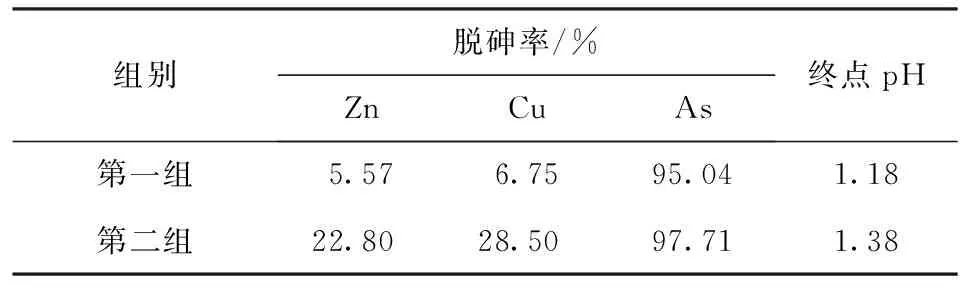
组别脱砷率/%ZnCuAs终点pH第一组5.576.7595.041.18第二组22.8028.5097.711.38
从表6和表7同时可以看出,脱砷率也受终点pH值影响。pH值低于1.0时,脱砷率较低;而当pH值高于1.0时,pH值越高脱砷率越大,脱砷效果越好,但同时铜和锌的损失越多。为保证较高的脱砷率同时考虑铜和锌适当高的回收率,本试验选择控制终点pH=1.05~1.10。
4.3 除铜
在除砷后液中加入铁粉,搅拌。反应条件为:温度75~85 ℃,铁粉加入量保持铁铜摩尔比(1~1.05)∶1,反应时间2 h。反应后矿浆进行过滤,滤渣经洗涤过滤得到含铜74%的海绵铜。
本试验考察Fe∶Cu=1.05∶1,1.25∶1两种情况下的脱铜率及铁粉的利用率,得到试验结果见表8。
表8不同摩尔比条件下的脱铜率及铁粉的利用率

摩尔比置换率/%CuZnFeAs终点pHFe∶Cu=1.05∶178.941.4299.2242.711.17Fe∶Cu=1.25∶199.720.1399.3327.801.2899.100.2995.7032.811.30
从试验的结果可以看出,控制脱砷终点pH在1左右,脱砷后液仍然含有一定量的氢离子,当加入铁粉后,铁粉先与余酸发生反应生成硫酸亚铁,过量铁粉才会与铜离子发生置换将铜离子置换成金属铜;故若不考虑与余酸反应所需铁粉量,直接加入置换铜所需铁粉量(Fe∶Cu=1.05∶1),铜的置换率仅能达到78%;若考虑了与余酸反应所需铁粉量(Fe∶Cu=1.25∶1),有充足的铁粉用于置换铜离子,铜的置换率可达到99%以上,铁粉的利用率也能达到95%以上。
4.4 沉锌
在除铜后液中加入石灰乳,搅拌。反应条件为:温度75~85 ℃,反应时间2 h,终点酸度pH=6.5~7.0。反应后矿浆进行过滤,滤液作为洗渣水返回浸出,滤渣经洗涤过滤得到含锌18%~20%的碱式硫酸锌。
5 结论
根据上述试验结果,最终确定工艺流程为“纯硫酸浸出- 氧化除铁砷- 沉铜- 沉锌”,采用此流程,铜的回收率达到~85%,锌的回收率达到~84%,铅的回收率大于98%,浸出渣即铅渣可以送自有铅系统进一步回收铅,碱式硫酸锌送自有锌系统作为中和剂,海绵铜外售,铁砷渣堆存。采用此工艺流程对高砷白烟尘进行处理,解决了该企业现存白烟灰堆存的难题,既解决了生产中废酸处理的问题,又开路了冶炼过程中有害杂质元素,避免其富集,同时砷转化为无毒稳定的砷酸铁弃渣,具有一定的经济与环保优势,可为其它高砷白烟灰的处理提供参考。
[1] 张荣良,丘克强,谢永金等.铜冶炼闪速炉烟尘氧化浸出与中和脱砷[J].中南大学学报:自然科学版,2006,37(1):73-78.
[2] 阮胜寿,路永锁.浅议从炼铜电收尘烟灰中综合回收有价金属[J].有色冶炼,2003,32(6):41-44.
[3] 李涛.高砷白烟尘湿法处理工艺与实践[J].中国有色冶金,2015,10(5):11-14.
Research of valuable metals recovery from high-arsenic copper dust
NIE Ying
In this paper the hydrometallurgical treatment of high-arsenic copper dust was introduced and the optimum technical condition of each process was obtained by experiments, the process flow of “sulfuric acid leaching- oxidation of iron and arsenic-copper deposition-zinc deposition” was finally determined. By using this process, the valuable metals in high-arsenic copper dust were recoveried in the form of sponge copper,lead residue and basic zinc sulfate, arsenic and ferric co-precipitated with the form of stability ferric arsenate from the system. The results showed that if this process was adopted, the recovery rate of copper in high-arsenic copper dust is ~85%, the recovery rate of zinc is ~84%, and the recovery of lead is more than 98%.
high-arsenic copper dust; hydrometallurgy; ferric arsenate
聂颖(1984—),女,湖北荆门人,硕士学位,工程师,从事有色冶金工程设计工作。
2016-02-22
TF811
B
1672-6103(2016)05-0068-05
