基于自发呈报系统177例脑脊液分流管不良事件预警分析
2016-02-09郑思维
赵 瑛,史 琛,黄 晖,赵 丽,郑思维,黄 璞
1 华中科技大学同济医学院附属协和医院药剂科,武汉市,430022 2 湖北省药品(医疗器械)不良反应监测中心,武汉市,430071
基于自发呈报系统177例脑脊液分流管不良事件预警分析
【作者】赵 瑛1,史 琛1,黄 晖2,赵 丽2,郑思维1,黄 璞1
1 华中科技大学同济医学院附属协和医院药剂科,武汉市,430022 2 湖北省药品(医疗器械)不良反应监测中心,武汉市,430071
目的通过自发呈报系统(SRS)进行脑脊液分流管不良事件监测并分析,为安全用械、合理用械提供参考依据。方法回顾分析177份脑脊液分流器不良事件报告,进行数据挖掘分析和预警。结果177例中170例不良事件明确或可能与脑脊液分流管的使用有关;脑室扩大和感染是最为常见的不良事件表现,分别占21.2%和19.4%;不良事件的发生与产品质量、手术操作、患者病理状态和使用情况等风险因素有关。结论应进一步加强脑脊液分流管不良事件监测,加强风险控制,降低脑脊液分流管不良事件发生率,维护公众用械安全。
自发呈报系统;脑脊液分流管;脑积水;医疗器械;不良事件
自发呈报系统( Spontaneous Reporting System,SRS)是指医务人员、其他专业人员或消费者在临床实践中将可疑的不良反应/事件报告给生产、经营企业、ADR监测专业机构、药品监督管理部门[1-3]。该方法具有易于实施、监测范围广、不受时间与空间的限制以及可对病例进行追踪等优点,是目前世界上进行不良反应监测、发现不良反应信号最基本的方法,也是目前上市后不良反应/事件信号的主要来源[4-5]。
脑积水(Hydrocephalus)是神经外科的多发病、常见病,是由多种原因导致脑脊液在脑室系统积聚过多,引起脑室扩大,进而压迫脑组织而产生脑部症状和体征的一组疾病[6-9]。在患者病情允许的情况下,脑脊液分流术是目前治疗脑积水的首选方法之一[10],是通过脑脊液分流管(CSF Flow Control Shunts)将脑脊液从脑室转移至适当引流区(如腹腔)吸收[11]。脑脊液分流管及其附件属于第三类医疗器械,目前还没有其安全性监测的相关报道。医疗器械不良事件(Medical Device Administration Events, MDAEs)监测是确保上市后医疗器械安全有效的重要手段[12,13],本研究以对脑脊液分流管为监测对象,基于2010~2015年SRS的大样本数据,开展对脑脊液分流管不良事件特征探索和不良反应信号预警,为提升上市后医疗器械的安全监测预警水平,为完善医疗器械推荐使用方案提供依据和奠定基础。
1 资料与方法
1.1 资料来源
2010年1月1日至2015年6月30日国家药品不良反应监测中心收集的全国所有与脑脊液分流管及附件相关的医疗器械不良事件报告,共177例。
1.2 数据清理与标准化
由于自发呈报系统中不同人员填写信息内容和质量不一致,因此要实现对SRS数据的挖掘和信号监测,需要先对脑脊液分流管不良事件报告进行清理与标准化。本研究对不良事件报告信息中出现的疾病名称采用国际通用疾病分类“ICD-10”分类标准,对报告中出现的不良反应名称严格按照“WHO 药品不良反应术语集”进行统一的编码。
1.3 评价方法与内容
采用描述性方法,对收集的脑脊液分流管不良事件报告进行统计分析。对所有收集报告的构成情况、上报单位情况进行统计分析;对与使用相关或可能相关的不良事件分析其生产企业分布情况、患者人群基本信息、不良事件主要表现、严重程度分级、发生原因以及处理转归,全面系统的找出风险因素并提出相关控制建议。
2 结果
2.1 报告构成情况分析
177例报告中,明确与使用脑脊液分流管及附件相关的不良事件为130例,7例明确与脑脊液分流管及附件的使用不相关,40例未明确不良事件发生是否与使用具有脑脊液分流管及附件相关性。
2.2 上报单位构成比
177报告中,涉及的上报单位有27家,其中器械生产经营企业3家,上报144例(占81.4%);医疗机构20家,上报26例(占14.7%);经营企业2家,上报4例(占2.3%)、ADR中心2家,涉及3例(占1.7%)。
2.3 生产企业分布情况分析
170例相关或可能相关的不良事件中,168例明确记录了生产企业,2例产品信息不详(表1)。所有脑脊液分流管均为进口产品,包括美国美敦力、美国强生和法国索菲萨,其中美敦力和强生公司占95.29%。因无生产厂家销售数量的背景数据,无法判定产品不良事件发生率。
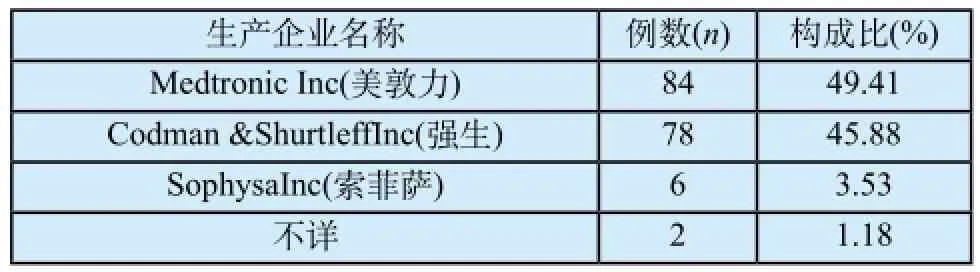
表1 不良事件生产企业分布情况Tab.1 Composition of different manufacturers which have occurred adverse events
2.4 不良事件患者人群基本情况分析
全部170相关或可能相关不良事件中,女性患者52例,男性104例,性别不详14例,男女比例为1:2。157人注明患者年龄,年龄不详13人,年龄最小的4月龄,最大为80岁,平均年龄38.32岁。具体年龄分布如图1所示。
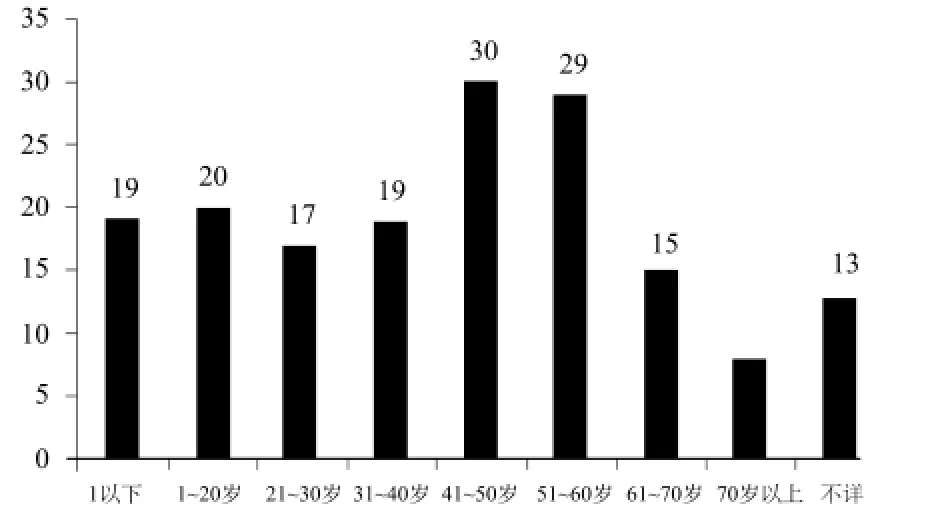
图1 年龄构成情况Fig.1 Age composition of users
2.5 不良事件表现及严重程度分级
170例相关或不相关不良事件中,脑室扩大和感染是最为常见的不良事件,分别占21.2%和19.4%。具体不良反应表现与发生率见表2。根据不良事件严重程度进行分级[6],分级标准分为一级(致命)、二级(严重)、三级(一般)、四级(轻微)、五级(无伤害)。对170份病例进行分级,死亡率是1.8%,严重率是98.2%。
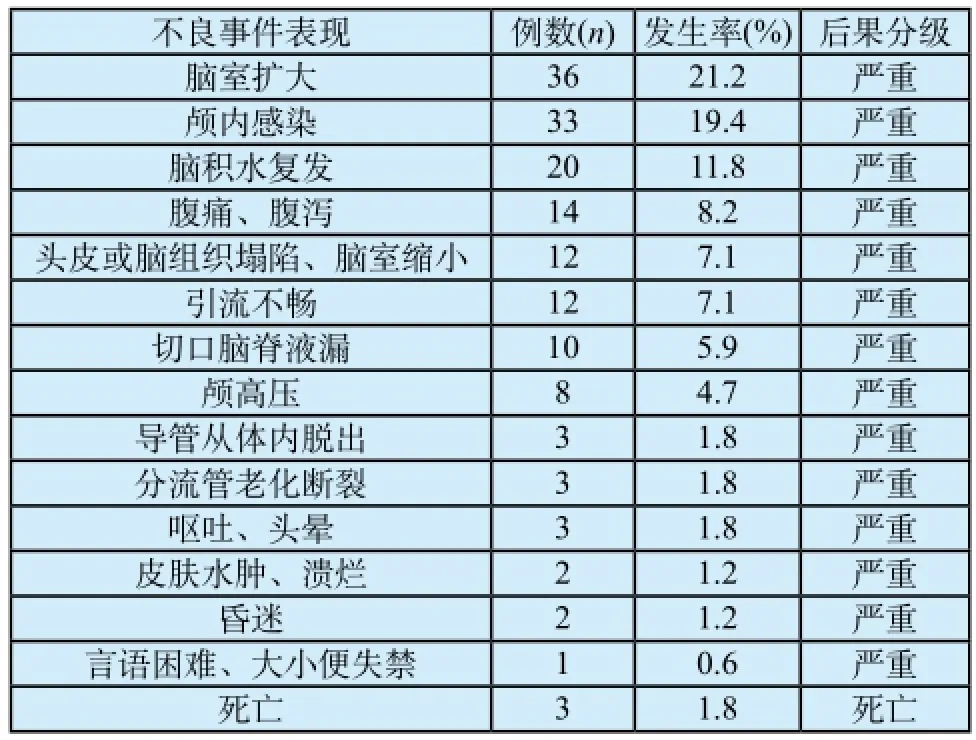
表2 不良事件表现和严重程度分级Tab.2 Clinical symptoms and severity gradation of adverse events
2.6 不良事件发生原因分析
全部170例相关或可能相关不良事件中,可能原因分为质量因素、操作因素、患者因素三类。质量因素包括分流管堵管、阀门失效、储液囊漏水、断管、接口处松动等;操作因素包括分流管植入位置不当、压力值设定不合理、操作引起断管操作污染、手术间环境等;患者因素包括脑脊液成分不正常、自身排异所致、免疫力低下、未注意使用禁忌、未定期调压、患者病情变化等;但由于绝大部分不良事件可能涉及一个或多个因素,无法准确判断或以此统计每个事件的具体原因。
2.7 不良事件的处理
处理方法主要包括抗感染、调节压力、植入新管、体外引流、对症治疗、保守治疗等。根据不良事件发生情况,同一病例可能同时采取以上多个处理方法。
3 讨论
3.1 应加强药械不良事件上报培训
177例脑脊液分流管不良事件报告中,医疗机构上报26例,仅占14.7%。医疗机构作为使用单位在不良事件上报工作中起着重要作用,医生、护士和药师往往是不良事件最先发现的人员,应是不良事件/反应报告的主体。但由于对药械不良事件的主动上报意识不足,不良事件的实际发生率往往被低估,不利于药械质量和使用安全的管理和持续改进。应建立药械相关监测制度与监管措施,加强医务人员上报流程的培训和技术指导,提高医务人员对药械不良事件的认知和上报意愿。
3.2 预防和控制术后感染
感染是分流术后最为严重和常见的并发症, 从一定程度上影响脑积水的治疗。对分流术后感染的患者进行及时有效的预防和治疗是减少后遗症, 提高患者生活质量的关键。患者出现感染的原因复杂,术前乃至手术中各个环节都有可能导致感染的发生,通常与患者存在免疫力低下、手术操作中无菌条件、围手术期处理等因素有关。应加强手术操作规范和手术条件要求、慎重选择病例,术中采取无菌操作、术后注意感染的预防,也可选择有抗生素涂层或经抗生素溶液浸泡的导管。一旦感染发生,应立即给予对症治疗,同时视情况将导管从患者体内取出。
3.3 分流管堵塞的处理
分流管堵塞是较为常见的患者伤害,其发生与分流管植入位置,局部有无感染、组织粘连,脑脊液成分改变等情况有关。若为远端堵塞,可考虑减掉堵塞导管。近端堵塞,需通过手术取出原植入的分流管和导管,植入新的分流管和导管。对于脑脊液成分改变引起的反复堵管,则考虑使用体外引流。
4 风险管理建议
4.1 质量因素
①企业应主动提高分流管质量标准,减少因质量问题引起的不良反应,如分流管的折断,漏液,调压失败等。②提高分流管材料的抗剪切力和抗拉伸力,提高产品的可靠性。③为了降低感染风险,应尽量简化器械装置,减少植入操作时间。④温度对引流管硅胶材质有影响,建议说明书中注明运输贮存条件。
4.2 操作因素
①应由有资质、经过培训的专业技术人员进行操作。提高手术熟练程度,减少操作时间。②应建立手术操作规范,减少术后感染的风险。③分流管植入手术应在层流洁净手术室进行,严格消毒,降低感染的发生,做好手术室洁净度监测。④对患者的颅内压有正确的估计,必要时行腰椎穿刺测压,选择合理的阈值分流,防止分流过度。
4.3 患者因素
①行分流术前,应对患者脑脊液成分进行评估。②注意使用禁忌,进行详细病情评估,包括近期发热、脑部炎症、免疫力等情况,③对于带有调压阀的分流系统,勿靠近强磁场。④加强患者健康教育,密切关注患者的病情变化。
[1] 卢鹏飞, 向永洋, 谢雁鸣, 等. 基于自发呈报系统丹参多酚酸盐安全信号预警分析[J]. 中国中药杂志, 2013, 38(18): 3003-3007.
[2] 李苑雅, 张艳, 沈爱宗. 基于自发呈报系统药品不良反应信号监测方法的研究进展[J]. 安徽医药, 2015, 19(7): 1233-1236.
[3] 江静, 候永芳, 刘秀娟, 等. 不同信号监测方法在我国药品不良反应自发呈报系统中的应用[J].中国药物警戒, 2010, 7(3): 154-155.
[4] Huang YL , Moon J , Segal JB. A comparison of active adverse event surveillance systems worldwide[J]. Drug Saf, 2014, 37(8): 581-596.
[5] Clark JA , Humphries JE , Crean S , et al. Topical bovine thrombin: a 21-year review of topical bovine thrombin spontaneous case safety reports submitted to FDA's Adverse Event Reporting System [J]. Pharmacoepidemiol Drug Saf, 2010, 19(12): 107-114.
[6] Konstantelias AA , Vardakas KZ , Polyzos KA , et al. Antimicrobialimpregnated and -coated shunt catheters for prevention of infections in patients with hydrocephalus: a systematic review and meta-analysis[J]. J Neurosurg, 2015, 122(5): 1096-1112.
[7] 汤华, 吴全理. 脑积水手术治疗进展[J].医学综述, 2008, 14(13): 2021-2022.
[8] 吴中华, 王斌, 李明, 等. 脑室镜下第三脑室造瘘术与脑室-腹腔分流术治疗脑积水的疗效观察[J]. 中国实用神经疾病杂志, 2014, 19(19): 112-113.
[9] Spector R , Robert Snodgrass S , Johanson CE.A balanced view of the cerebrospinal fluid composition and functions: Focus on adult humans[J]. Exp Neurol, 2014, 273: 57-68.
[10] 陈德忠, 邓元央. 脑室-腹腔分流术治疗慢性继发性脑积水的临床分析[J]. 中国当代医药, 2014, 6(6): 169-171.
[11] 张素敏. 我国医疗器械不良事件报告的影响因素探讨[J].中国药物警戒, 2008, 5(4): 205-207.
[12] 曲婷婷, 崔昊. 影响医疗器械不良事件监测在医疗机构中开展的因素探讨[J].中国医疗器械信息, 2010, 16(9): 47-66.
[13] 吕英伟, 刘志诚, 孟刚.医疗器械不良事件监测方法学的探讨[J].中国药物警戒, 2007, 4(4): 204-206, 211.
Analysis of 177 Cases of Adverse Events of CSF Flow Control Shunts Based on Spontaneous Response System
【Writers】ZHAO Ying1, SHI Chen1, HUANG Hui2, ZHAO Li2, ZHENG Siwei1, HUANG Pu1
1 Department of Pharmacy, Union Hospital, Tongji Medical College of Huazhong University of Science and Technology, Wuhan, 430022
2 Monitoring Center for Adverse Reaction of Drug and Medical Instrument of Hubei, Wuhan, 430022
ObjectiveMonitoring and Analyzing CSF flow control shunts adverse event reports by SRS provide a reference for the safe and reasonable use.MethodsRetrospective analysis of 177 CSF flow control shunts adverse event reports, to proceed data mining analysis and early warning.Results170 cases of adverse events in 177 cases may be related to the use of CSF flow control shunts. Ventricular dilatation and infection were the most common adverse event performances, according for 21.2% and 19.4% respectively. Adverse events might be relevant to the risk factors of product quality, surgical operation, patient pathological conditions.ConclusionMonitoring should be strengthened in order to reduce the CSF flow control shunts adverse events and maintain public safety.
spontaneous reporting system, CSF flow control shunts, hydrocephalus, medical device, adverse events
R651.1
A
10.3969/j.issn.1671-7104.2016.04.017
1671-7104(2016)04-0294-03
2016-01-25
湖北省药品(医疗器械)不良反应监测中心项目(2015B6Q9)
赵瑛,E-mail: 50430498@qq.com
黄璞,E-mail: 741245198@qq.com
