N-苄基酰胺类化合物的合成与工艺研究
2016-02-07刘跃金董娜娜于春影
刘跃金, 董娜娜, 于春影
(1.沈阳化工大学 制药与生物工程学院, 辽宁 沈阳 110142;2.江苏豪森药业股份有限公司, 江苏 连云港 224200)
N-苄基酰胺类化合物的合成与工艺研究
刘跃金1, 董娜娜1, 于春影2
(1.沈阳化工大学 制药与生物工程学院, 辽宁 沈阳 110142;2.江苏豪森药业股份有限公司, 江苏 连云港 224200)
研究了一些N-苄基酰胺类化合物的合成.以苄胺或3-甲氧基苄胺为原料,以对甲苯磺酸为催化剂,甲苯为溶剂,分别与乙酸、丙酸、巴豆酸、对氯苯甲酸和十六碳酸于110 ℃反应制得N-苄基乙酰胺、N-苄基丙酰胺、N-(3-甲氧基苄基)巴豆酰胺、N-(3-甲氧基苄基)对氯苯甲酰胺(m.p.89.1~90.3 ℃)和N-苄基十六碳酰胺(m.p.92.1~93.2 ℃),收率分别为16.7 %、14.3 %、15.8 %,19.8 %和30.2 %.经IR和1H-NMR确证结构正确.对N-苄基十六碳酰胺的合成研究表明:甲苯为较好的溶剂,对甲苯磺酸为较好的催化剂,对甲苯磺酸与十六碳酸的最佳质量比约1∶5,最佳反应时间为 14 h,最佳反应温度为回流温度.此反应条件可用于其他N-苄基酰胺类化合物合成的参考.
N-苄基酰胺类化合物; 辣椒素; 合成
辣椒素,(E)-N-(4-羟基-3-甲氧基苄基)-8-甲基-6-壬烯酰胺,属于N-苄基酰胺类化合物.目前其合成不少于七条路线[1],难点在(E)-8-甲基-6-壬烯酸的合成,最后一步酰胺的合成,都是以(E)-8-甲基-6-壬烯基酰氯与香草基胺反应生成辣椒素.而羧酸转变为酰氯不仅多一步反应,反应条件要求也较严格,因此本文对N-苄基酰胺类化合物的合成进行探讨.
1 合成路线
以苄胺或3-甲氧基苄胺为原料,以对甲苯磺酸为催化剂,甲苯为溶剂,分别与乙酸、丙酸、巴豆酸、对氯苯甲酸和十六碳酸反应制得N-苄基乙酰胺、N-苄基丙酰胺、N-(3-甲氧基苄基)巴豆酰胺,N-(3-甲氧基苄基)对氯苯甲酰胺和N-苄基十六碳酰胺.具体合成路线如下所示:

2 实验与结果
2.1 仪器与原料
熔点用毛细管测定,温度计未经校正;红外光谱用Bruker IFS-55红外分光光度计测定;核磁共振氢谱用Bruker ARX-300B核磁共振仪测定.
苄胺,分析纯,成都市科龙化工试剂厂;3-甲氧基苄胺,质量分数98 %,梯希爱(上海)化成工业发展有限公司;乙酸、丙酸、巴豆酸、十六碳酸、甲苯和对甲苯磺酸,分析纯,国药集团化学试剂有限公司;对氯苯甲酸,分析纯,上海紫一试剂厂.
2.2 N-苄基乙酰胺的合成
将1.0 g(0.009 3 mol)苄胺加入到40 mL甲苯中,再加5.6 g(0.093 mol)乙酸,搅拌均匀,加入对甲苯磺酸0.2 g,回流搅拌20 h,过滤,得深黄色液体0.71 g.干燥,柱硅胶层析,以石油醚-乙酸乙酯(体积比8∶1)为洗脱剂,得黄色液体0.23 g,收率16.7 %.IR,σ/cm-1:3 294(N—H),3 063(фC—H),3 032(фC—H),2 929(C—H),2 885(C—H),1 647(C==O),1 587(фC==C),1 557(фC==C),1 499(фC==C),741(γфC—H,单取代),696(γфC==C,单取代).
2.3 N-苄基丙酰胺的合成
将1.0 g(0.009 3 mol)苄胺滴加到7.0 g(0.094 mol)丙酸中,高温加热,至固体溶解,加入对甲苯磺酸0.1 g,回流搅拌15 h,过滤,得深黄色液体0.69 g,干燥,柱硅胶层析,以石油醚-乙酸乙酯(体积比8∶1)为洗脱剂,得黄色液体0.22 g,收率14.3 %.IR,σ/cm-1:3 430(N—H),3 099(фC—H),3 054(фC—H),2 921(C—H),2 849(C—H),1 682(C==O),1 591(фC==C),1 573(фC==C),1 491(фC==C),1 323(C—N和γN—H).
2.4 N-(3-甲氧基苄基)巴豆酰胺的合成
将0.31 g(0.003 6 mol)巴豆酸加入到40 mL甲苯中,再加入0.50 g(0.003 6 mol)3-甲氧基苄胺,加热搅拌至完全溶解,加入对甲苯磺酸0.1 g,回流搅拌15 h.过滤,滤液减压浓缩得深黄色液体0.32 g,干燥,柱硅胶层析,以石油醚-乙酸乙酯(体积比10∶1)为洗脱剂,得浅黄色液体0.12 g,收率15.8 %.IR,σ/cm-1:3 318(N—H),3 070(==C—H或фC—H),3 002(==C—H或фC—H),2 938(C—H),2 835(C—H),1 640(C==O),1 601(фC==C),1 585(фC==C),1 538(фC==C),1 487(фC==C),1 307(C—N和γN—H),756(γфC—H,1,3-二取代),691(γфC==C,1,3-二取代).1H-NMR(CDCl3),δ:7.39(1H,m,ene—H3),7.30(1H,m,ф—H5),7.03(1H,d,ф—H6),6.93(1H,d,ф—H4),6.89(1H,d,ф—H2),6.83(1H,d,ene—H2),6.47(1H,s,—CON—H),4.61(2H,d,ф—CH2—NHCO),3.79(3H,s,—OCH3),1.88(3H,d,3—CH3).
2.5 N-(3-甲氧基苄基)对氯苯甲酰胺的合成
将0.57 g(0.003 6 mol)对氯苯甲酸加入到60 mL甲苯中,再加3-甲氧基苄胺0.50 g(0.003 6 mol),加分水器,加热搅拌至完全溶解,加入对甲苯磺酸0.2 g,继续回流搅拌19 h.过滤,滤液减压浓缩析出结晶,得白色固体 0.76 g,干燥,柱硅胶层析,以石油醚-乙酸乙酯(体积比4∶1)为洗脱剂,得白色固体0.20 g,收率19.8 %,m.p.89.1~90.3 ℃.IR(KBr压片),σ/cm-1:3 430(N—H),3 099(фC—H),3 054(фC—H),2 921(C—H),2 849(C—H),1 682(C==O),1 591(фC==C),1 573(фC==C),1 491(фC==C),1 323(C—N和γN—H).
2.6 N-苄基十六碳酰胺的合成工艺
2.6.1 催化剂对反应的影响
以TLC检测终点,结果见表1、表2.
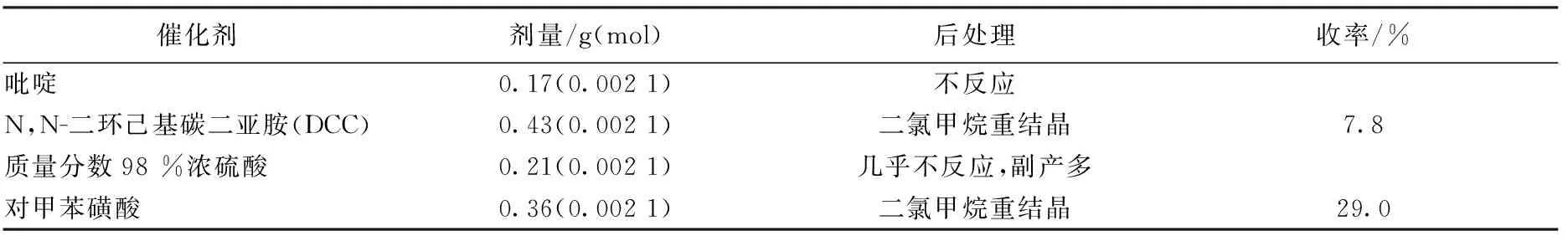
表1 不同催化剂对反应的影响
注:十六碳酸0.50 g(0.001 9 mol),苄胺0.20 g(0.001 9 mol),甲苯20 mL,回流搅拌15 h.

表2 不同剂量的对甲苯磺酸催化剂对反应的影响
注:十六碳酸0.50 g(0.001 9 mol),苄胺0.20 g(0.001 9 mol),甲苯20 mL,回流搅拌15 h.
2.6.2 反应溶剂对反应的影响
以TLC检测终点,结果见表3.
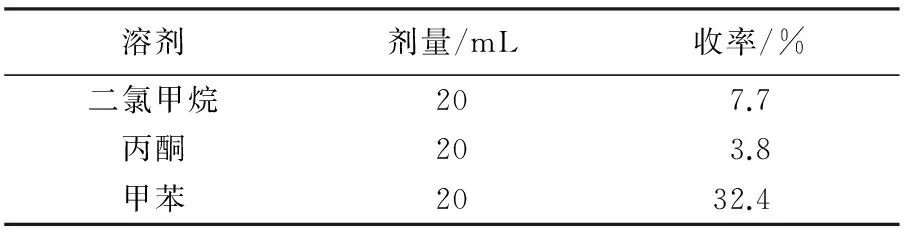
表3 反应溶剂对反应的影响
注:十六碳酸0.50 g(0.001 9 mol),苄胺0.20 g(0.001 9 mol),对甲苯磺酸0.1 g,回流搅拌15 h.
2.6.3 反应温度对反应的影响
以TLC检测终点,结果见表4.

表4 反应温度对反应的影响
注:十六碳酸0.50 g(0.001 9 mol),苄胺0.20 g(0.001 9 mol),甲苯20 mL,对甲苯磺酸0.1 g,搅拌15 h.
2.6.4 反应时间对反应的影响
以TLC检测终点,结果见表5.

表5 反应时间对反应的影响
注:十六碳酸0.50 g(0.001 9 mol),苄胺0.20 g(0.001 9 mol),甲苯20 mL,对甲苯磺酸0.1 g,回流.
2.6.5 实验结果
将0.50 g(0.001 9 mol)十六碳酸加入到20 mL甲苯中,再加入苄胺0.20 g(0.001 9 mol),加热搅拌至完全溶解,加入对甲苯磺酸0.1 g,继续回流搅拌14 h.过滤,滤液减压浓缩析出结晶,得浅黄色固体,以二氯甲烷重复结晶3次,得白色固体0.88 g,收率30.2 %,m.p.92.1~93.2 ℃.IR(KBr压片),σ/cm-1:3 298(N—H),3 085 (фC==H),3 033 (фC==H),2 954(—CH3),2 917(—CH2—),2 848(—CH2—),2 000~1 667(单取代泛频峰),1 632(—NC==O),1 553(фC==C),1 493(фC==C),1 478(фC==C),1 463(—CH2—),1 454(—CH3),1 374(—CH3),747(γфC—H单取代),727(—(CH2)n,n>4),696(γфC==C单取代).
3 讨论与结论
合成了N-苄基乙酰胺、N-苄基丙酰胺、N-(3-甲氧基苄基)巴豆酰胺、N-(3-甲氧基苄基)对氯苯甲酰胺和N-苄基十六碳酰胺,经IR和1H-NMR确证了结构正确.其中,N-(3-甲氧基苄基)巴豆酰胺为未见文献报道的化合物.对 N-苄基十六碳酰胺的合成研究表明:甲苯为较好的溶剂,对甲苯磺酸为较好的催化剂,对甲苯磺酸与十六碳酸的最佳质量比约1∶5,最佳反应时间为 14 h,最佳反应温度为回流温度.此反应条件可用于其他N-苄基酰胺类化合物的合成参考.羧酸与胺直接成酰胺操作简单但羧酸与胺易成盐,所以反应不易发生,收率不高.DCC作为催化剂在高温时副产多,且DCC的产物很难除净,价格也昂贵,在本实验中收率不高.
辣椒素经灌胃途径与对照组比较能明显延长小鼠游泳时间[2-4].辣椒酯类物质也具有相似的作用[5].辣椒素的另一个类似物N-苄基十六碳酰胺的小鼠负重游泳实验[6]显示,与对照组比较游泳时间有显著性延长.辣椒素类似物在抗疲劳方面具有进一步的研究价值.
[1] MCILVAIN S,CHEN W,RAMIYA P H,et al.Preparation and Purification of Synthetic Capsaicin:EP1615880[P].2006-01-18.
[2] KIM K M,KAWADA T,ISHIHARA K,et al.Increase in Swimming Endurance Capacity of Mice by Capsaicin-induced Adrenal Catecholamine Secretion[J].Biosci Biotechnol Biochem,1997,61(10):1718-1723.
[3] OH T W,OH T W,OHTA F.Dose-dependent Effect of Capsaicin on Endurance Capacity in Rats[J].Br J Nutr,2003,90(3):515-520.
[4] OH T W,OHTA F.Capsaicin Increases Endurance Capacity and Spares Tissue Glycogen through Lipolytic Function in Swimming Rats[J].J Nutr Sci Vitaminol(Tokyo),2003,49(2):107-111.
[5] KIM K M,KAWADA T,ISHIHARA K,et al.Swimming Capacity of Mice is Increased by Oral Administration of a Nonpungent Capsaicin Analog,Stearoyl Vanillylamide[J].J Nutr,1998,128(11):1978-1983.
[6] 王钰楠.N-苄基酰胺类化合物的合成及抗疲劳研究[D].沈阳:沈阳化工大学,2013.
Study on Synthetic Process and Syntheses of N-Benzyl Amides
LIU Yue-jin1, DONG Na-na1, YU Chun-ying2
(1.Shenyang University of Chemical Technology, Shenyang 110142, China;2.Jiangsu Province Haosen Pharmaceutical Co., Ttd, Lianyungang 224200, China)
To synthesize N-Benzyl amides,acetamide was synthesized from benzylamine and acetic acid,the yield was 16.7 %,N-benzyl propylamides from benzyl amine and propionic acid,the yield 14.3 %,N-(3-methoxy benzyl)-2-butenamide from 3-methoxy benzyl amine and 2-butenoic acid and its yield 15.8 %,N-(3-methoxy benzyl)-4-chlorobenzamide from 3-methoxybenzylamine and 4-chlorobenzoic acid,m.p.89.1~90.3 ℃,the yield 19.8 %,and N-benzyl hexadecanamide from 3-methoxybenzylamine and hexadecanoic acid,m.p.92.1~93.2 ℃,the yield 30.2 %,at 110 ℃ in toluene.The five compounds were corroborated structurally by IR and1H-NMR.Synthesis of N-benzyl hexadecanamide:toluene was better solvent,p-toluenesulfonic acid catalyst was better one,the ratio ofp-toluenesulfonic acid to N-benzyl hexadecanamide was 1∶5,the optimum reaction time was 14 h,and the optimum reaction temperature was the reflux temperature.The reaction conditions can be used for reference to synthesize other N-benzyl amides.
N-benzyl amides; capsaicin; synthesis
2014-11-03
刘跃金(1964-),男,吉林九台人,副教授,博士,主要从事生物化学与药物化学方面的研究.
2095-2198(2016)04-0322-04
10.3969/j.issn.2095-2198.2016.04.008
R914.5
A
