黄藤素柔性纳米脂质体水凝胶贴剂的制备及体外透皮给药研究
2016-02-07李伟泽韩文霞赵宁付丽娜周永强
李伟泽,韩文霞,赵宁,付丽娜,周永强
(1.西安医学院,西安 710021;2.烟台威特纳瑞医药科技有限公司,山东烟台 264000)
黄藤素柔性纳米脂质体水凝胶贴剂的制备及体外透皮给药研究
李伟泽1,2,韩文霞1,赵宁1,付丽娜1,周永强2
(1.西安医学院,西安 710021;2.烟台威特纳瑞医药科技有限公司,山东烟台 264000)
为奶牛乳房炎的治疗提供了一种新型高效的透皮给药制剂,并考察其体外透皮给药的行为特点。采用薄膜分散法制备黄藤素柔性纳米脂质体(PFL),高效液相色谱仪(HPLC)测定包封率,透射电镜(TEM)观察PFL的结构、激光粒度仪(LPSA)测定PFL的粒径和表面Zeta电位;然后将PFL制备成水凝胶贴剂(PFL-HP),并采用立式双室扩散池考察PFL-HP体外透皮给药的行为特点,并同药物水凝胶贴剂(P-HP)与加入5%氮酮的水凝胶贴剂(P-A-HP)进行对照。结果表明,PFL对黄藤素的包封率为(79±2.23)%,PFL为圆球形层状囊泡结构,粒径为(190±24)nm,Zeta电位为(-54±2.65)mV;PFL-HP膏体柔软、膏面平整光洁,黏附性良好可48 h黏附于奶牛乳房而不脱落;24 h时,PFL-HP的药物累积透过量是P-HP与P-A-HP的2.12倍(t-test,P<0.05)与1.13倍(t-test,P>0.05),同时,PFL-HP组中药物在皮肤组织的滞留量(即“储库效应”)也高于P-HP与P-A-HP(t-test,P< 0.05)。黄藤素柔性纳米脂质体水凝胶贴剂(PFL-HP)药物透皮吸收效率高、黏附性良好、使用方便,奶牛对其具有良好的依从性。PFL-HP可作为治疗奶牛乳房炎的一种新型高效透皮给药制剂。
黄藤素;柔性脂质体;水凝胶贴剂;透皮给药
奶牛乳房炎是一种严重危害奶牛养殖业的疾病,在我国的发病率为33%左右[1-2]。奶牛乳房炎多因环境卫生、挤奶不当特别是机械挤奶或饲养管理不合理等引起病原微生物感染而发病。黄藤素(palmatine,PN)是从防己科植物黄藤(FibraurearecisaPierre)中提取精制而得的一种季胺盐异喹啉类生物碱,具有较好的抗菌、抗病毒作用[3]与抗炎作用,还能显著增强体内白细胞的吞噬能力;其在自然界易代谢、不残留,因此,在兽药领域具有广阔的应用前景。临床上对于奶牛乳房炎的治疗主要有注射给药、乳房灌注、口服给药与乳房外敷给药等,其中,乳房外敷给药具有给药方便、药物可透皮吸收而直达病灶与克服奶牛对注射、灌注和口服给药的恐惧引起的应激反应等优点,因此,备受关注。但是,传统的外敷给药剂型如涂膜剂、气雾剂、软膏剂与洗剂等由于载药量小、给药后易损失、药物透皮吸收效率低等原因而受到一定的限制。柔性脂质体是一种高效透皮给药载体,可以通过多种机制促进药物特别是水溶性药物通过皮肤与黏膜吸收[4-5],但脂质体混悬液具有易流动而在皮肤上滞留时间短、易损失的弊端。水凝胶贴剂是由水溶性高分子材料等制备而成的具有三维网络结构的新型透皮给药载体,具有载药量大、膏体柔软舒适、黏性良好、无刺激无过敏等优点而成为研究热点;水凝胶基质不仅与脂质体具有良好的相容性,也能提高脂质体的稳定性[6]。本文首次将黄藤素制备成柔性纳米脂质体水凝胶贴剂,并研究了其体外透皮给药的行为特点,为进一步的应用奠定基础。
1 材料
1.1 试药 黄藤素(纯度≥98%,批号XC20140514)购自西安小草植物科技有限责任公司;黄藤素标准品(中国食品药品检定研究院,纯度≥98%,批号110732-201108);大豆磷脂(湖北远成药业有限公司);胆固醇(天津博迪化工股份有限公司);丙三醇、1,2-丙二醇(厦门星鲨制药有限公司);TritonX-100、硫酸鱼精蛋白(Sigma公司);甘氨酸铝、聚丙烯酸钠NP-700与NP-800(美国国际特品公司);PVP K-120(河南博爱新开元有限公司);EDTA-2Na(天津市科密欧化学试剂有限公司);酒石酸(安徽华源生物药业有限公司);高弹无纺布(上海一蓝无纺布制造有限公司);双硅纸(江苏宇宣工业有限公司);其他试剂均为分析纯,水为双蒸水。
1.2 仪器 Quintix224-1CN电子天平、SIGMA 1-14离心机(赛多利斯科学仪器公司);52-AA旋转蒸发仪(上海亚荣生化仪器厂);B11-1型恒温磁力搅拌器(上海司乐仪器有限公司);FJ-200高速分散匀质机(上海标本模型厂);JEM-2000EX透射电镜(日本电子株式会社,日本);ZEN-3600激光粒度仪(马尔文,英国);HIC-10ASP高效液相色谱仪(SPD-10A检测器,岛津,日本);ZJ-50型真空搅拌混合机、GST-II型涂布切割机(温州市皓丰机械有限公司);贴剂黏性检测装置(按照《中国药典》2015年版自制)。水平双室扩散池(扩散面积Ae=1.54 cm2,容积V=5.0 mL)。
1.3 动物 健康奶牛30头,山东省烟台市某养殖场;奶牛乳房部位皮肤(烟台市屠宰场)。
2 方法
2.1 含量测定方法 色谱柱为Hypersil BDS C18(4.6 mm×150 mm,5.0 μm),流动相为乙腈-0.4%磷酸(20:80,V/V),检测波长345 nm,流速1.0 mL/min,进样量20 μL。取黄藤素标准品,精密称定,用双蒸水配制成浓度为0.8、2.8、8.4、14.0、25.0 μg/mL的标准品溶液,精密移取各浓度溶液20 μL,注入HPLC中测定,并以峰面积A为纵坐标,以浓度C为横坐标,进行线性回归,得线性方程A=95.5116C-48.9829,r=0.9995,表明黄藤素浓度C在0.8~25.0 μg/mL范围内与峰面积A具有良好的线性关系。
2.2 黄藤素柔性纳米脂质体(PFL)的制备及其性质考察 取3.0 g卵磷脂与0.05 g胆固醇置于茄形瓶内,用10 mL无水乙醇振摇至溶解;于50 ℃、-0.05 MPa条件下旋转除掉乙醇,至物料在瓶壁上形成干燥的脂质膜。将20 g 1,2-丙二醇加入双蒸水中混合均匀,得水相,取出1/3量,将0.3 g的PN加入其中溶解并于50 ℃预热,然后缓慢加入茄形瓶中,氮气氛围下与脂质膜水合60 min,再转移至锥形瓶内,高速(20000 r/min)匀质5 min,再通过0.22 μm聚丙烯滤膜过滤2次,之后将剩余的2/3水相加入其中,振摇混匀,即得,4 ℃保存。
PFL包封率测定:取0.75 mL脂质体于2 mL离心管中,加入0.75 mL鱼精蛋白溶液(10 mg/mL),摇匀,静置3 min,离心(10000 r/min)15 min,弃掉上清液,用2 mL 10% TritonX-100 甲醇溶液消解沉淀物至澄清透明,取20 μL进样测定PN的含量。包封率按照如下公式计算:包封率(%)=(W1/W2)×100%,其中W1为被脂质体包封的药量,W2为实际加入的总药量。粒径与Zeta电位:取PFL稀释液样品适量,注入激光粒度仪测定PFL的粒径与Zeta电位。结构观察:将PFL稀释液样品适量滴于铜载网上,晾干后用磷钨酸(1.5%,W/W)进行负染色,晾干,置于透射电镜下进行结构观察。
2.3 黄藤素柔性纳米脂质体水凝胶贴剂(PFL-HP)的制备及其黏性考察 取NP-800与NP-700各1.5、0.45 g甘氨酸铝和0.05 g EDTA-2Na,加入至35 g丙三醇中,真空搅拌均匀,作为甘油相;另取0.45 g酒石酸,9.5 g PVP K-120,加入25 g纯化水中,搅拌至充分溶解,作为水相;再取70 g PFL与水相共同加入甘油相中,真空搅拌(80 r/min)8 min,得到膏体;再将膏体转移至涂布切割机上进行涂布切割,得到半成品贴剂并置于温度为28~30 ℃、湿度为50%~55%的条件下放置72 h,封装,于室温下再放置96 h,即得PFL-HP。将70 g PFL更换为70 g 0.3%PN水溶液,其余操作不变,即可制备得到黄藤素水凝胶贴剂(P-HP);再添加5%氮酮则得到含氮酮的水凝胶贴剂(P-A-HP)。
贴剂黏性的测定:参照《中国药典》2015年版的斜坡滚球法测定,实验前,除去供试品包装材料,使互不重叠在室温放置2 h以上;取供试品3片,置于倾斜板(倾斜角30°)中央,膏面向上,斜面上部10 cm及下部15 cm用0.025 mm厚的涤纶薄膜覆盖,中间留出5 cm膏面,将各标准钢球自斜面顶端自由滚下,以至少2片供试品黏性面能够粘住的最大球号钢球表示其黏性的大小,试验重复3次,本实验所用钢球球号及规格符合规定。同时,将奶牛30头分为3组,每组10头,然后将PFL-HP、P-HP与P-A-HP各10贴分别贴于各组奶牛乳房部位,观察记录贴剂自帖敷到完全脱落的时间即为奶牛在体帖敷时间,帖敷药物期间奶牛自由饮食走动。2.4 体外透皮给药 用剃须刀小心剔除奶牛乳房部位皮肤毛发并剥离皮下组织,用水冲洗干净后夹于立式扩散池中间,角质层面向供给池,真皮层面向接收池;立式扩散池固定在调温恒控磁力搅拌器上,并以恒定的速度搅拌接收液,保持恒温在(32±0.5)℃;在供给池中分别加入PFL-HP、P-HP与P-A-HP各4.5 g,在接收池中加入5 mL的双蒸水作为接收液。然后于0.5、1.0、2.0、6.0、12.0、24.0 h取接收液0.3 mL,并补加等量的双蒸水,共取6个样,重复3次。样品经0.22 μm滤膜过滤,取20 μL注入液相色谱仪测定PN的含量,并按下公式计算药物的累积透过量(△M):△M=∑CV/Ae,其中V为接收液的体积(mL),C为接收液中的药物浓度(μg/mL),Ae为有效扩散面积(cm2)。实验结束后,皮肤样品用生理盐水冲洗3 min,再将其剪成小块,加入等量的生理盐水,进行匀浆;匀浆液于5000 r/min离心10 min,移取上清液20 μL注入液相色谱仪测定PN的含量,PN在皮肤组织中的滞留量以单位面积皮肤组织中含有的药量表示(μg/cm2)。
3 结果与分析
3.1 黄藤素柔性纳米脂质体(PFL)及其性质 本文所制备的PFL由透射电镜(图1)观察为具有层状囊泡结构的圆球形或椭球形,PFL的层状囊泡结构可能是由于1,2-丙二醇增加了脂质体脂质双分子层磷脂膜的变形性所致,与以乙醇为柔软剂的醇质体具有类似的层状结构[7]。PFL的粒径为190±24 nm,表面Zeta电位为-54±2.65 mV;研究表明当微粒表面Zeta电位的绝对值大于30 mV时,脂质体微粒间由大量净电荷产生较强的静电斥力而利于微粒体系的稳定性提高与粒径分布均匀[8]。
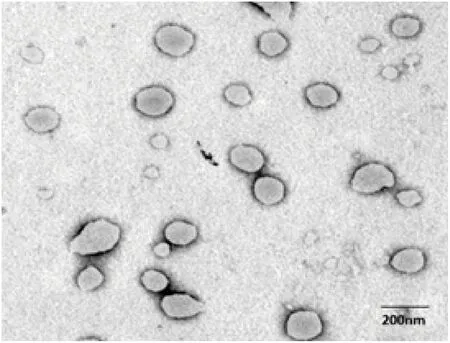
图1 黄藤素柔性纳米脂质体的透射电镜图
3.2 黄藤素柔性纳米脂质体水凝胶贴剂(PFL-HP)及其黏性 制备的黄藤素柔性纳米脂质体水凝胶贴剂(PFL-HP)外观为淡黄色层状膏体、膏面平整光洁、无冷流无渗析(图2)。贴剂的黏性与药物释放、治疗效果等密切相关,黏性的评价指标有初粘力、持黏力与剥离强度等,其中初粘力不仅能够反映材料表面与整体的性质,也能够反映贴剂的黏性特别是贴敷于皮肤上长时间的真实黏附性能,因此,初粘力常被用于评价水凝胶贴剂的黏附性[9-10],PFL-HP的初粘力与贴敷于奶牛的黏附性如下表1所示。

图2 黄藤素柔性纳米脂质体水凝胶贴剂图(A-膏体面层,B-无纺布背衬层)

贴剂类型初粘力(标准钢球号)奶牛在体帖敷时间/hPFL-HP28±250±2.0P-HP27±245±3.5P-A-HP24±240±3.0
3.3 水凝胶贴剂的体外透皮给药 体外透皮给药实验表明,随着时间的延长,三种载体PFL-HP、P-HP与P-A-HP的药物累积透过量均不断增加。如图3所示在透皮给药的前1.5 h内,P-A-HP的药物累积透过量大于PFL-HP和P-HP;但2.0 h后,PFL-HP的药物累积透过量最大,表明2.0 h后柔性纳米脂质体促进药物透皮吸收的作用大于传统的氮酮促渗剂。24 h时,PFL-HP的药物累积透过量分别是P-HP与P-A-HP的2.12倍(t-test,P<0.05)与1.13倍(t-test,P>0.05);同时,PFL-HP药物在皮肤中的滞留量也显著高于P-HP与P-A-HP(t-test,P<0.05),表明柔性纳米脂质体能够促使药物在皮肤组织中形成良好的“储库效应”而更利于奶牛乳房炎的局部靶向治疗,具体如图4所示。
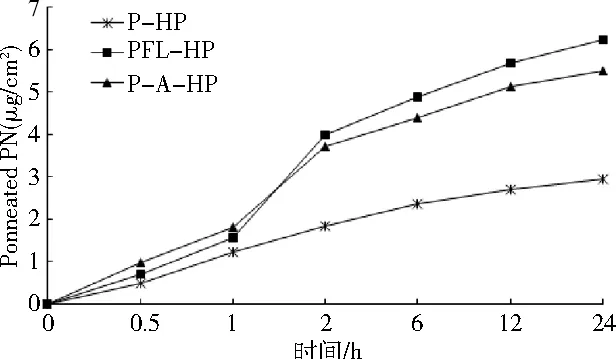
图3 不同载体中黄藤素通过皮肤的累积渗透量(n=3)
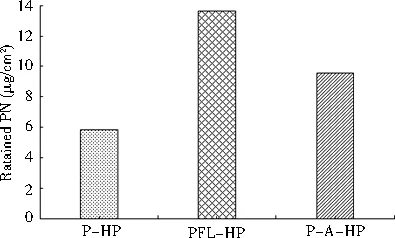
图4 不同载体透皮给药后黄藤素在皮肤中的滞留量(n=3)
4 讨论与小结
奶牛乳房炎已经成为我国奶牛养殖业的重大威胁,加之抗生素类药物滥用的潜在不良反应和危害逐渐被认识,因此,亟待开发新型高效的天然药物制剂用于奶牛乳房炎的治疗。本文首次制备了天然单体药物黄藤素的柔性纳米脂质体水凝胶贴剂(PFL-HP),并研究了PFL-HP的黏性与体外透皮给药行为。结果表明,PFL-HP具有良好的黏性,其初粘力达到28±2(标准钢球号)、奶牛在体贴敷时间为50±2.0 h;良好的黏性意味着药物制剂可与皮肤持久接触而不脱落,从而使药物持续缓慢释放而直达病灶;体外透皮给药实验表明,PFL-HP作为PN透皮给药的载体,不仅能够促进药物透皮吸收而提高其累积透过量,也能促进药物在皮肤组织中形成良好的“储库效应”而利于长效缓释,这可能是由于柔性脂质体具有较好柔软性和变形性的脂质双分子层膜,能够通过变形作用、与细胞发生融合或扰乱皮肤角质层的有序结构[11]等机理促进PN进入皮肤并在皮肤组织中形成“药物储库”。脂质体混悬液本身是一种热力学与动力学不稳定体系,易发生聚集、融合与药物泄露等,因此,成为临床应用的瓶颈之一;本文将药物柔性脂质体与水凝胶贴剂结合制成柔性纳米脂质体水凝胶贴剂,避免了单纯脂质体混悬液存在的稳定性低的问题、易于流动而损失给药剂量与在病灶部位滞留时间短的弊端;同时,柔性纳米脂质体水凝胶贴剂的膏体柔软,贴敷后奶牛无不适反应且不影响挤奶操作而具有良好的依从性。因此,本文为奶牛乳房炎的治疗提供了一种新型透皮制剂,填补了领域空白,具有广阔的应用前景。
[1] 荣霞,王自力,张翥,等.抑制奶牛乳腺炎致病菌的中药复方筛选及其抗炎效果研究[J].中国兽药杂志,2015,49(9) :25-31.
[2] 尹柏双,付连军,沙万里,等.我国奶牛乳房炎治疗技术研究进展[J].畜牧与兽医,2013,45(11) : 101-103.
[3] 杨小良,谢丽莎,龚志强.黄藤素的研究综述[J].中国医药指南,2009,7(17) : 42-44.
[4] Thirapit S,Nanthida W,Pucharee S,et al.Visualization of ultradeformable liposomes penetration pathways and their skin interaction by confocal laser scanning microscopy[J].Int J Pharm,2013,441 (1/2) : 151-161.
[5] Wei Z L,Yong Q Z,Ning Z,et al.Pharmacokinetic behavior and efficiency of acetylcholinesterase inhibition in rat brain after intranasal administration of galanthaminehydrobromide loaded flexible liposomes[J].Environ Toxicol Pharm,2012,34(2) : 272-279.
[6] PaveliC'Zˇ ,Basnet N ,Filipovic'-Grc ic'J,et al.Developmentand in vitro evaluation of a liposomal vaginaldelivery system for acyclovir[J].J Control Release,2005,106 (1) : 34-43.
[7] Zhang Y T,Shen L N,Wu Z H,et al.Comparison of ethosomes and liposomes for skin delivery of psoralen for psoriasis therapy[J].Int J Pharm,2014,471 (1 /2) : 449-452.
[8] Huijuan W,Meifeng L,Song D.Optimization of madecassoside liposomes using response surface methodology and evaluation of its stability[J].Int J Pharm,2005,473(1 /2) : 280-285.
[9] Ren,C.S.,Fang,L.,Ling,L.,et al.Design and in vivo evaluation of an indapamide transdermal patch[J].Int J Pharm,2009,370(1/2) : 129-135.
[10] Gutschke,E.,Bracht,S.,Nagel,S.,et al.Adhesion testing of transdermal matrix patches with a probe tack test-In vitro and in vivo evaluation[J].Eur J Pharm Biopharm,2010,75(3) :399-404.
[11] 韩文霞,李伟泽,汪兴军,等.盐酸青藤碱纳米柔性脂质体的制备及其性质研究[J].中草药,2011,42(4) : 671-675.
(编辑:侯向辉)
Studies on the Preparation and Transdermal Drug Delivery of Hydrogel Patches of Palmatine Loaded Flexible Nano-liposomes
LI Wei-ze1,2,HAN Wen-xia1, ZHAO Ning1, FU Li-na1, ZHOU Yong-qiang2
(1.Xi’anMedicalUniversity,Xi’an710021,China;2.YantaiWeitenaruiPharmaceuticalCompanyLimited,Yantai,Shandong264000,China)
In order to develop a new type of highly effective transdermal drug delivery preparation for the treatment of cow mastitis,and the transdermal drug delivery of the preparation was also investigated.The palmatine loaded flexible nano-liposomes (PFL)were prepared by thin-film homogenization method.The entrapment rate of palmatine was evaluated by HPLC, the pharmaceutical properties(such asstructure, size and zeta potential)of PFL were evaluated by the TEM and LPSA, respectively.Then the PFL added to hydrogel patches and PFL loadedhydrogel patches(PFL-HP)were obtained. The vertical dual chamber diffusion cells were used to investigate the characteristics of palmatine transdermal drug delivery from PFL-HP, and the P-HP and P-A-HP used as control group.Results showed that the prepared PFL had aclosed spherical shape and lamellar structure with a homogeneous size of 190±23nm, and exhibited a negative charge of -54±2.65mV. The PFL-HP with characteristics of better flexibleness, matrix surface smooth and clean,also possess higher adhesive force and adhere to the cow breasts and not fall off in 48 h.At 24 h, the accumulated permeation amount of palmatine from the PFL-HP was 2.12(t-test,P<0.05)and 1.13(t-test,P> 0.05)folds than that of P-HP and P-A-HP, respectively.And the quantityof palmatine remaining in theskin tissue at the end of the 24 h experiment was also significantly greaterfrom the PFL-HP than from P-HP and P-A-HP.The PFL-HP with characteristics of higher transdermal permeability of drug, better flexibleness and adhesive force. Cows also have good compliance with PFL-HP. So, the PFL-HP was shown to be a new and effective transdermal drug delivery preparation for the treatment of cowmastitis and has a broad application prospects.
palmatine;flexible liposomes; hydrogel patches;transdermal drug delivery
国家自然科学基金资助项目(81303231);烟台高新区高端人才引进'蓝海英才计划'资助项目(2015-17)
李伟泽,博士,副教授,从事药物新剂型、新技术与新制剂方面的研究。E-mail: weizeli@126.com
2015-12-14
A
1002-1280 (2016) 02-0046-05
S859.79
