超高效液相色谱-四级杆-静电场轨道肼高分辨质谱筛查测定饲料中19种磺胺类药物
2016-02-07严凤李丹妮吴剑平周哲张鑫潘娟张婧
严凤,李丹妮,吴剑平,周哲,张鑫,潘娟,张婧
(1.上海市兽药饲料检测所,上海 201103;2.赛默飞世尔科技(中国),上海 201206)
超高效液相色谱-四级杆-静电场轨道肼高分辨质谱筛查测定饲料中19种磺胺类药物
严凤1,李丹妮1,吴剑平1,周哲2,张鑫1,潘娟1,张婧1
(1.上海市兽药饲料检测所,上海 201103;2.赛默飞世尔科技(中国),上海 201206)
建立了超高效液相色谱-四级杆-静电场轨道阱高分辨质谱联用( UPLC-Q-Exactive Orbitrap) 快速筛查和确证定量饲料中19种磺胺类药物的分析方法。饲料样品经乙腈-0.1%甲酸溶液(80:20,V/V)超声提取,Agilent SB C18色谱柱(100 mm×3.0 mm,1.8 μm)分离,以0.1%(V/V)甲酸乙腈溶液和0.1%(V/V)甲酸水溶液为流动相进行梯度洗脱。静电场轨道阱全扫描得到磺胺类药物的一级精确质量数与理论精确相对分子质量对比,相对质量偏差在0.006×10-6~1.252×10-6之间,有效去除了基质干扰,实现对饲料中磺胺类药物的快速筛查;同时建立了19种磺胺类药物的二级质谱数据库,实现对19种磺胺类药物的定性筛查及同步定量。19种磺胺类药物在0.1~200 μg/L浓度范围内线性关系良好r>0.99,方法检测限为50 μg/kg,回收率在59.61%~106.45%之间。
磺胺类;饲料;超高效液相色谱;四级杆-静电场轨道阱高分辨质谱
磺胺类药物( Sulfonamides,SAs) 是人工合成的具有对氨基苯磺酰胺结构的一类抗菌药物的总称,广泛应用于畜禽养殖业[1]。饲料添加是该类药物在畜牧业中的主要用药方式,随着SAs的滥用,细菌耐药性问题日益突出,这不仅会影响畜禽的正常生长发育,而且还会造成畜产品中药物残留超标,危害人体健康,影响环境卫生和生态平衡。针对磺胺类药物的检测手段多样化,如采用免疫分析法[2]、HPLC法[3-4]以及液质联用方法[5-6]。这些方法在靶向目标定性、定量检测方面有极为广泛的应用,但是这种模式也存在无法获取样品中非靶目标结构信息的局限[7],为实现高通量筛查的多组分物质,基于高分辨质谱技术的全扫描的质谱分析方法逐渐进入研究者们的视野[8-9]。本实验利用高效液相色谱-四极杆-静电场轨道阱高分辨质谱快速检测饲料中添加的19种磺胺类药物,采用正离子全扫描模式进行测定,通过提取的二级质谱进行定性,提取一级质谱的精确相对分子质量进行定量。该方法用实际添加实验进行验证,在较低质量浓度添加水平条件下仍可以保证良好的检测结果。
1 材料与方法
1.1 仪器与试剂 Q-Exactive四极杆-静电场轨道阱高分辨质谱,配有H-ESI Ⅱ源(美国Thermo Fisher Scientific公司);Ultimate 3000液相色谱系统(美国Thermo Fisher Scientific公司);TraceFinder 数据处理系统(美国Thermo Fisher Scientific公司);AE240 电子天平( 瑞士Mettler 公司) ; Allegra X-22R 高速冷冻离心机( 德国Beckman 公司) ; 多管旋涡振荡器( 北京Targin 公司) ; Milli-Q 超纯水系统( 美国Millipore 公司)。
乙腈(色谱纯,美国Merck 公司) ; 甲酸( 色谱纯,美国Tedia 公司) ;实验用水为超纯水(Milli-Q 自制) 。
标准品:苯甲酰磺胺(纯度99.8%),磺胺醋酰(纯度99.5%),磺胺喹噁啉(纯度98.0%),磺胺氯哒嗪(纯度99.8%),磺胺嘧啶(纯度99.0%),磺胺间二甲氧嘧啶(纯度99.0%),磺胺邻二甲氧嘧啶(纯度98.0%),磺胺甲基嘧啶(纯度99.2%),磺胺对甲氧嘧啶(纯度98.0%),磺胺二甲嘧啶(纯度99.0%),磺胺甲噻二唑(纯度98.5%),磺胺甲基异恶唑(纯度99.0%),磺胺甲氧哒嗪(纯度99.2%),磺胺间甲氧嘧啶(纯度98.0%),磺胺二甲恶唑(纯度98.0%),磺胺苯吡唑(纯度99.0%),磺胺吡啶(纯度99.0%),磺胺噻唑(纯度99.5%),磺胺二甲异嘧啶(纯度98.0%),以上均购自德国Dr. Ehrenstorfer GmbH。
标准贮备液配制:分别精密称取19种磺胺类标准品10 mg,用甲醇溶解稀释并定容至10 mL,浓度各为1 mg/mL。
混合标准工作液配制:分别取各标准贮备液500 μL,于同一10 mL容量瓶中,并定容,混合标准中间液浓度为50 μg/mL。
混合标准工作曲线配制:取适量混合标准工作液用0.1%甲酸溶液稀释为浓度0.1、1、10、100、200 μg/L的系列混合标准工作曲线。
1.2 仪器条件
1.2.1 液相色谱条件 色谱柱: Agilent SB C18柱(3.0 mm×100 mm,1.8 μm), 流动相A 为0.1% 甲酸水溶液,B 为含0.1%甲酸的乙腈溶液; 梯度洗脱程序: 0~15 min,5%~95% B;15~17 min,95% B;17~17.5 min,95%~5% B;17.5~21 min,5% B;流速0.3 mL/min;柱温30 ℃; 进样量10 μL。
1.2.2 质谱条件 可加热的电喷雾离子源(HESI-Ⅱ);离子传输管温度325 ℃;毛细管电压3200 V(正离子模式);气化温度350 ℃;鞘气压(N2)40 arb;辅助气压(N2)10 arb;一级质谱驻留时间100 ms;二级质谱驻留时间50 ms;一级全扫描范围:m/z100~1200;分辨率(R):70000;扫描模式:Fullscan+ddms2(一级全扫描+自动触发二级质谱扫描),碰撞裂解气为高纯氮气,碰撞能量为20、40、60 eV。
1.2.3 样品前处理 称取饲料2.00 g,加入10 mL乙腈-0.1%甲酸溶液(80:20,V/V),混匀,超声提取10 min,8500 r/min离心5 min,取上清液0.1 mL与0.9 mL 0.1%甲酸溶液混匀,12000 r/min高速离心5 min,取上清液待测。
2 结果与分析
2.1 线性范围 本方法线性范围为0.1~200 μg/L,线性相关良好,相关系数r均大于0.99,线性结果见表1。

表1 磺胺类药物线性方程及相关系数表
2.2 回收率与精密度 采用空白饲料进行添加回收率试验,添加浓度为50、100、10000 μg/kg,每个浓度做6个平行,处理方法按1.2.3项进行,用相近浓度的空白基质添加标准单点对样品进行定量,结果见表2。19种磺胺类药物的平均回收率为59.61%~106.45%,相对标准偏差为0.40%~35.94%,实际测得精确分子量与理论精确分子量的差值均<2 mDa。

表2 回收率、精密度与质量偏差
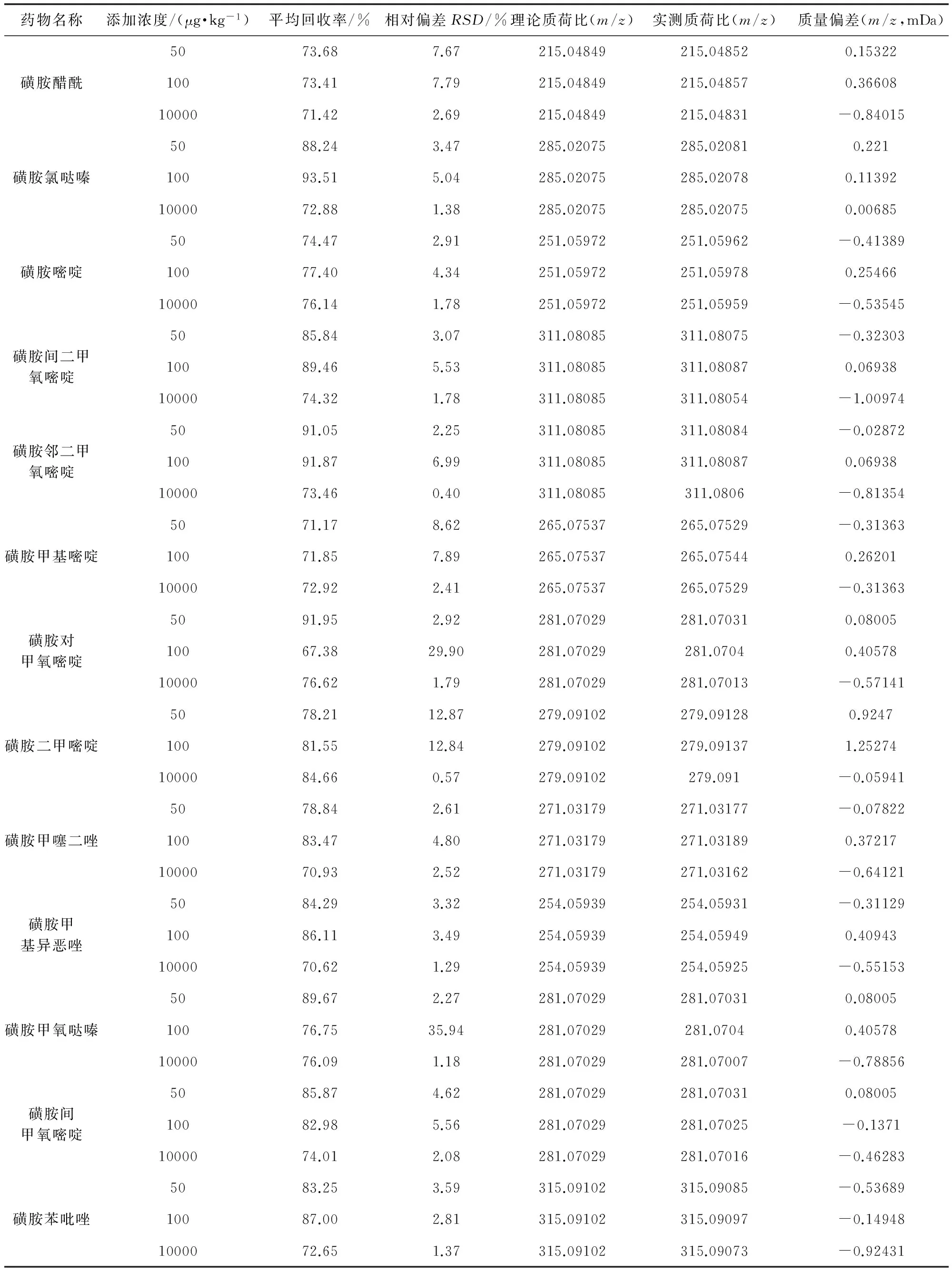
续表

续表
2.3 检测限与定量限 按照检测限信噪比S/N(Peak to Peak)>3,定量限信噪比S/N(Peak to Peak)>10的要求,本方法检测限为50 μg/kg,定量限为100 μg/kg(表3)。空白图谱、检测限图谱和定量限图谱见图1、图2和图3。

表3 检测限与定量限表
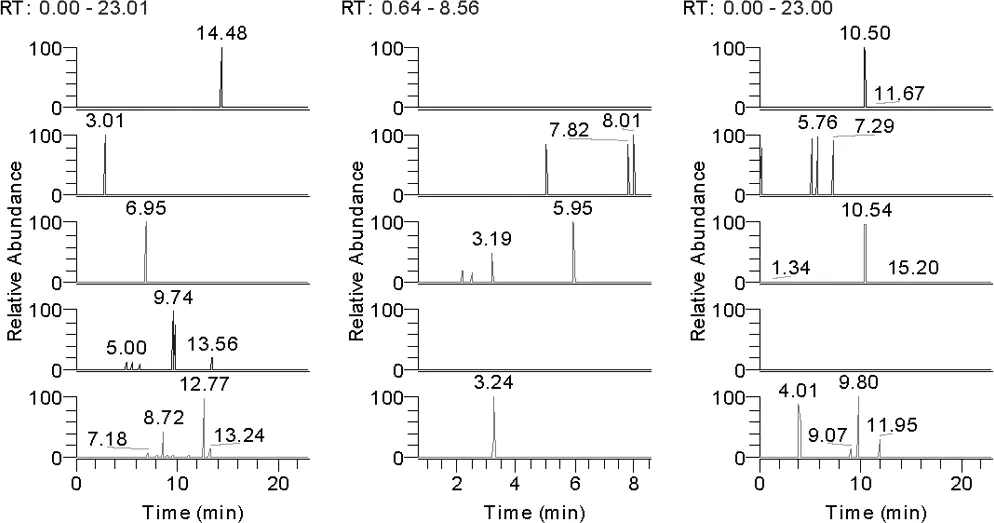
图1 空白饲料提取离子色谱图
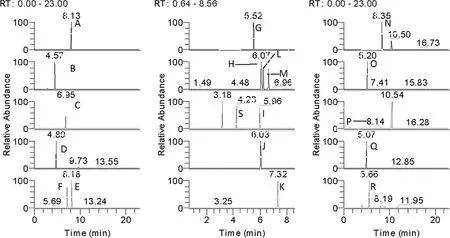
图2 空白饲料添加50 μg/kg检测限提取离子色谱图(A: 苯甲酰磺胺B: 磺胺醋酰 C: 磺胺氯哒嗪 D: 磺胺嘧啶E: 磺胺间二甲氧嘧啶F: 磺胺邻二甲氧嘧啶G: 磺胺甲基嘧啶H: 磺胺对甲氧嘧啶 I: 磺胺二甲嘧啶J: 磺胺甲噻二唑K: 磺胺甲基异恶唑L: 磺胺甲氧哒嗪M: 磺胺间甲氧嘧啶 N: 磺胺苯吡唑O: 磺胺吡啶P: 磺胺喹噁啉Q: 磺胺噻唑R: 磺胺二甲恶唑S: 磺胺二甲异嘧啶)
2.4 实际样品筛查 随机抽取11份饲料样品,用已优化的色谱-质谱条件和前处理方法进行筛查分析,采集一级质谱数据及二级碎片信息,进行谱库检索,根据保留时间、碎片离子和质量误差等信息确证并同时定量。结果表明,随机抽取的11份样品中检出1份样品含有磺胺间甲氧嘧啶,一级母离子精确质量偏差为0.028×10-6,含量为311.85 μg/kg,筛查结果见图4。
3 讨论与小结
3.1 色谱柱的选择 本实验比较了Thermo Hypersil GOLD C18(150 mm×2.1 mm,1.9 μm)与Agilent SB C18(100 mm × 2.1 mm,1. 8 μm)两款色谱柱。实验表明,虽然两款色谱柱对磺胺类药物的检测灵敏度及药物峰形均无明显差异,但在分离度方面Agilent SB C18柱的表现更优于Thermo Hypersil GOLD C18柱,尤其是分离同分异构体磺胺甲氧哒嗪和磺胺对甲氧嘧啶。Thermo Hypersil GOLD C18柱无法将这两个同分异构体分离,但Agilent SB C18柱就能很好的分离开。

图3 空白饲料添加100 μg/kg定量限提取离子色谱图(A-S代表物质与图2相同)

图4 饲料样品中检出磺胺间甲氧嘧啶的筛查结果图(A:母离子精确质量提取色谱图;B:母离子同位素精确质量质谱图;C:碎片离子精确质量质谱图)
3.2 提取溶剂比较 磺胺类药物都属于弱碱性药物,本方法选用酸性水溶液与有机溶剂不同的比例组合作为提取溶剂进行比较,6种提取溶剂分别为乙腈-0.1%甲酸溶液(80+20)、乙腈-0.2%甲酸溶液(95+5)、甲醇-0.1 mol/L盐酸溶液(50+50)、乙腈-0.1 mol/L盐酸溶液(50+50)、纯乙腈和纯甲醇。实验结果表明,大部分药物用乙腈-0.1%甲酸溶液(80+20)提取效果最好、乙腈-0.2%甲酸溶液(95+5)和纯甲醇的提取效果相对弱些,纯乙腈的提取效果最差回收率约30%,因此本方法选用乙腈-0.1%甲酸溶液(80+20)作为提取溶剂。
3.3 滤膜比较 考察了不同品牌、不同材质的滤膜对磺胺类药物的吸附影响。选用了进口的Millipore Millex-GN尼龙、PALL-GHP和国产的PTFE、尼龙、聚醚砜材质滤膜进行比较,实验表明国产的PTFE对大部分磺胺类药物影响较小,但对磺胺甲氧哒嗪影响较大,过滤后损失50%。其余滤膜对不同的药物均会有一定的影响,所以本实验最终未使用滤膜过滤。
目前,高分辨质谱在饲料中药物的筛查应用主要是以液相色谱-四极杆飞行时间质谱为主[10],而液相色谱-四级杆-静电场轨道肼质谱的应用则更多在蛋白质组学、代谢组学研究[11]和食品安全[12]等方面,在国内饲料领域的应用甚少。本方法用四级杆-静电场轨道肼质谱建立饲料中药物筛查方法,也是该技术在饲料领域应用的初探。
本文建立了饲料中19 种磺胺类药物的超高效液相色谱-四级杆-静电场轨道肼质谱筛查与确证方法。饲料所含成分复杂,因此采用高选择性、高准确性的分析手段是检测方法建立的关键。本法通过母离子精确分子质量、二级质谱碎片的精确分子量和液相色谱保留时间信息,达到对化学物质准确定性,可快速、准确地对饲料中磺胺类药物同时进行定性及定量检测。
[1] 吴永宁,邵兵,沈建忠.兽药残留检测与监控技术[M].北京:化学工业出版社,2007: 189.
[2] 赵书景.贺绍君.罗国琦,等.动物性食品中磺胺类药物残留检测方法的研究进展[J].中国畜牧兽医,2009,36(8):60-63.
[3] GB/T 19542-2007.饲料中磺胺类药物的测定—高效液相色谱法[S].
[4] 陈吉之.闫超.饲料中9种磺胺类药物的HPLC法快速分离与检测中国医药工业杂志[J].2015, 46(8):892-894.
[5] 陈文慧.高效液相色谱-串联质谱法测定饲料中九种磺胺类药物的残留量[J].分析试验室,2010,29(9):52-56.
[6] 罗辉泰.黄晓兰.吴惠勤,等.分散固相萃取/高效液相色谱-串联质谱法快速测定饲料中87种药物残留[J].分析测试学报,2015,34(9):979-985.
[7] 熊岑.李苑雯.郑彦婕,等.静电场轨道阱质谱分析技术在食品分析中的应用进展[J].食品科学,2015, 36(13):283-287.
[8] 姚凤花.冯永巍.高效液相色谱串联飞行时间质谱法快速检测饲料中多种β-受体激动剂[J].食与饲料工业,2013,1:62-64.
[9] 贡松松.顾欣.曹慧,等.超高效液相色谱-四极杆飞行时间质谱法快速筛查生鲜牛乳中的14 种磺胺类药物[J].分析测试学报,2014,33(12):1342-1348.
[10]吴宁鹏.班付国.彭丽,等.超高效液相色谱-串联四极杆飞行时间质谱法筛查饲料中11种镇静剂类药物[J].质谱学报,2012,33(2):94-98,117.
[11]李明.马家辰.李红梅,等.静电场轨道阱质谱的进展[J].质谱学报,2013,34(3):185-192.
[12]熊岑.李苑雯.郑彦婕,等.静电场轨道阱质谱分析技术在食品分析中的应用进展[J].食品科学,2015,36(13):283-287.
(编辑:侯向辉)
Screening and Confirmation of 19 Sulfonamides in Feed by Ultra High Performance Liquid Chromatography-quadrupole-exactive Orbitrap Mass Spectrometry
YAN Feng1, LI Dan-ni1,WU Jian-pin1,ZHOU Zhe2, ZHANG Xin1, PAN Juan1,ZHANG Jing1
(1.ShanghaiMunicipalSupervisoryInstituteVeterinaryDrugsandFeedstaff,Shanghai201103,China;2.ThermofisherScientific(China),Shanghai201206,China)
An ultra high performance liquid chromatography- quadrupole-exactive orbitrap mass spectrometry method( UPLC-Q-Exactive Orbitrap) was developed for rapid screening,confirmation and quantitative of 19 sulfonamides in feed. The samples were extracted with acetonitrile-0.1% aqueous formic acid solution (80∶20,V/V), and the extracts were then separated on an Agilent SB C18 (50 mm×3.0 mm, 1.8 μm) using a binary solvent system composed of 0.1% formic acid acetonitrile solution and 0.1% aqueous formic acid solution by gradient elution. The relative molecular masses of the target compounds were obtained in full scan mode with a relative deviation in the range of 0.006×10-6~1.252×10-6compared to the theoretical value, indicating effective elimination of the matrix interference. Tandem mass spectrometric database based on characteristic fragment ions for the 19 sulfonamides was built. This method allowed qualitative screening and quantitative analysis at the same time. Calibration curve was linear between 0.1 and 200 μg/L, with the correlation coefficientr>0.99.The limit of detection was 50 μg/kg. The recovery in feed was from 59.61% to 106.45%.
sulfonamides;feed;ultra high performance liquid chromatography (UPLC); quadrupole-exactive orbitrap
严凤,畜牧师,从事兽药残留分析工作。E-mail:yan508@163.com
2015-11-25
A
1002-1280 (2016) 02-0029-08
S859.83
