两种伊维菌素注射液在家兔体内的生物等效性研究
2016-02-07李朋朋张聪张晓会周德刚李召斌张晓东刘栓
李朋朋,张聪,张晓会,周德刚,李召斌,张晓东,刘栓
(1.国家兽用药品工程技术研究中心,洛阳 471003;2.普莱柯生物工程股份有限公司,洛阳 471003)
两种伊维菌素注射液在家兔体内的生物等效性研究
李朋朋1,张聪1,张晓会1,周德刚1,李召斌1,张晓东1,刘栓2
(1.国家兽用药品工程技术研究中心,洛阳 471003;2.普莱柯生物工程股份有限公司,洛阳 471003)
为评价两种伊维菌素注射液在家兔体内的生物等效性,采用双周期交叉给药方式,将16只健康家兔随机分成2 组,按5 mg/kg体重皮下单剂量注射两种伊维菌素注射液,使用HPLC法测定血浆中的伊维菌素,利用3P97药动软件计算主要药动学参数。结果显示,受试制剂和参比制剂的Tmax分别为(26.45±8.62) h,(22.33±11.72) h;Cmax分别为(182.73±59.27) ng/mL,(166.77±65.25) ng/mL;AUC0-t分别为(21122±9999) ng·h·L-1,(19475±7009) ng·h·L-1;AUC0-∞分别为(27390±12197) ng·h·L-1,(31559±13412) ng·h·L-1。伊维菌素注射液受试制剂与参比制剂的AUC0-t、AUC0-∞、Cmax、Tmax均无显著性差异(P>0.05),双单侧t检验结果显示两种制剂生物等效,可为兽医临床给药方案的制定以及合理用药提供参考。
伊维菌素注射液;生物等效性;家兔
伊维菌素是阿维菌素药物(AVM)的一种衍生物,是一种新型的广谱、高效、低毒抗生素类抗寄生虫药[1],对体内外寄生虫特别是线虫和节肢动物均有良好驱杀作用[2],兽医临床中广泛用于马、牛、羊、猪、犬、猫、兔等的寄生虫病治疗。20世纪80年代,伊维菌素注射液在法国上市,成为动物抗寄生虫药的首选。梅里亚公司生产的伊维菌素注射液,具有安全、高效、长效等特点,且已有文献报道其对牛、羊、猪等家畜的体内线虫和体外寄生虫驱除效果佳[3]。根据伊维菌素注射液特点,河南新正好生物工程有限公司研制了一种伊维菌素注射液。本试验以家兔为研究对象,以梅里亚公司生产的伊维菌素注射液作为参比制剂,通过HPLC法测定家兔血浆中的伊维菌素,评价了受试制剂与参比制剂的生物等效性,为兽医临床合理使用伊维菌素注射液提供参考。
1 材料与方法
1.1 材料
1.1.1 动物 清洁级健康家兔16 只,雌雄各半,体重(2.7±0.2)kg。试验前饲养1周,饲喂不含任何抗菌药物的配合日粮,自由饮水和采食。1.1.2 药品与试剂 伊维菌素对照品,批号:201405001,含量:92.7%,普莱柯生物工程股份有限公司;受试制剂:伊维菌素注射液(Ⅰ),规格为100 mL:1 g,批号:20150312,由河南新正好生物工程有限公司提供;参比制剂:伊维菌素注射液(Ⅱ),规格为100 mL:1 g,批号:AF210112,购自梅里亚动物保健有限公司。乙腈,批号:D1409018,西陇化工股份有限公司,色谱级;甲醇,批号:2014121101,成都市科龙化工试剂厂,色谱级;三乙胺,批号:20140217,天津市福晨化学试剂厂,分析级。
1.1.3 仪器 高效液相色谱仪,美国Waters公司;电子分析天平,型号:AB-265s,梅特勒-托利多集团公司;HLB固相萃取小柱,美国Waters公司,1cc/30 mg,批号:128A34266A。
1.2 试验方法
1.2.1 标准储备液配制 伊维菌素标准储备液:精密称取伊维菌素对照品150 mg,置25 mL容量瓶中,用甲醇稀释至刻度,制成6 mg/mL标准储备液,2~8 ℃保存。系列浓度标准工作液的配制:标准储备液用甲醇稀释而成,现配现用。
1.2.2 血样采集 16 只家兔随机分成2 组,每组8 只,进行编号,采用双周期交叉试验设计。一组先给予受试制剂,再给予参比制剂;另一组先给予参比制剂,再给予受试制剂,清洗期为50 d。通过皮下注射给药,给药剂量5 mg/kg体重。分别于给药后2、4、6、8、12、20、24、48、96、144、168 h自耳缘动脉采血,每次2.5~4 mL,置含10 mg(40 μL 25%枸橼酸钠溶液)枸橼酸钠的离心管中,混匀,3000 r/min离心10 min,分离血浆,-70 ℃冰箱保存,待测。
1.2.3 样品前处理 准确吸取血浆样品1 mL,置5 mL离心管中,加乙腈2 mL,涡旋1 min,8000 r/min离心10 min,取上清液于10 mL离心管中,加入3 mL水、7.5 μL三乙胺,旋涡1 min,备用。
取HLB固相萃取小柱,用1 mL乙腈活化,1 mL乙腈-水-三乙胺溶液(40∶60∶0.1)平衡,将备用液过柱,之后用1 mL乙腈-水-三乙胺溶液淋洗,抽干后用2 mL乙腈洗脱,收集洗脱液于5 mL离心管中,40 ℃氮气吹干,加90 μL甲醇溶解后检测。
1.2.4 色谱条件 色谱柱:kromasil 100-5C18柱(5 μm,4.6 mm×250 mm);流动相:甲醇∶乙腈∶水=35∶53∶12[4];流速:1.0 mL/min;柱温:30 ℃;检测波长:254 nm;进样量:30 μL。
1.3 方法学验证1.3.1 检测限和定量限 照“1.2.3”项处理血浆样品进样检测,当仪器信噪比(S/N)=3时,对应样品中的含药浓度即为检测限;当仪器信噪比(S/N)=10时,对应的样品中的含药浓度即为定量限。
1.3.2 回收率及精密度 取空白血浆1 mL,加入伊维菌素标准工作用,制备成低、中、高3个质量浓度(30、300、600 ng/mL)的血浆样品,每一浓度6个样品并测定,按“1.2.3”方法进行处理后进行测定,以测定值与加入值之比计算回收率,并计算批内精密度。连续3 d配制并测定伊维菌素浓度,考察批间精密度。
1.3.3 标准曲线及线性范围 分别吸取浓度为1、3、6、15、22.5、30、45、60 μg/mL的系列伊维菌素标准工作液10 μL,置1 mL空白血浆中,涡旋混匀,使血浆样品中伊维菌素浓度分别10、30、60、150、225、300、450、600 ng/mL。按“1.2.3”项下的血浆样品处理方法进行处理,每个浓度做5个重复。以最终药物浓度(x,ng/mL)为自变量,相应各浓度对应的平均峰面积(y)为变量,得出标准曲线的回归方程和相关系数。
1.3.4 数据处理 取两种制剂中各家兔的血浆样品进行检测,根据标准曲线计算出血浆中伊维菌素的浓度。采用药代动力学软件3P97对血药浓度-时间数据处理,计算药代动力学参数。
2 结 果
2.1 方法检测限及定量限 按照S/N=3为检测限,S/N=10为定量限测定,该方法伊维菌素在家兔血浆中的检测限为7 ng/mL,定量限为16 ng/mL。
2.2 提取回收率及精密度验证 血浆中伊维菌素空白添加浓度分别为30、300和600 ng/mL时,提取回收率在65.23%~85.88%之间,三个浓度精密性测定结果小于10%。
2.3 标准曲线及线性范围 该方法在10~600 ng/mL范围内的线性方程为:y=1349.3x-4301.9,r=0.9999,血药浓度与峰面积线性关系良好,可用于血浆药物浓度测定。
2.4 血药浓度数据与药代动力学参数 16只家兔以5 mg/kg体重皮下注射受试制剂和参比制剂,取受试家兔11个采样点的血浆样品,按“1.2.3”项下的血浆样品处理方法处理后进行测定,用标准曲线计算伊维菌素血液浓度,采用3P97软件处理血药浓度并进行计算,得到受试制剂和参比制剂的平均血药浓度-时间曲线(图1)和各药动参数(表1)。
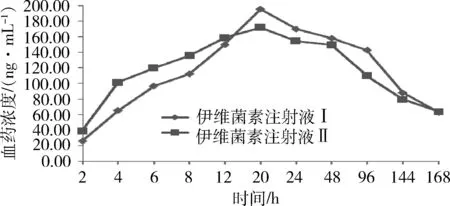
图1 两组伊维菌素注射液的药时曲线
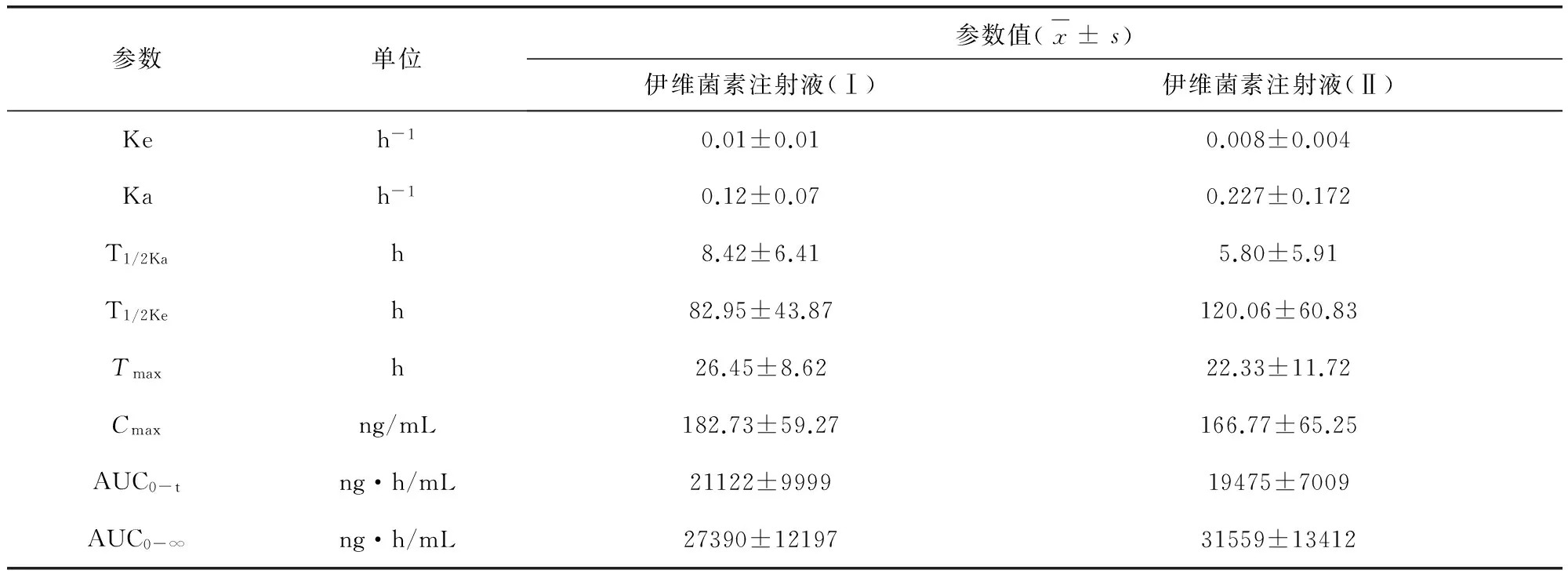
参数单位参数值(x±s)伊维菌素注射液(Ⅰ)伊维菌素注射液(Ⅱ)Keh-10.01±0.010.008±0.004Kah-10.12±0.070.227±0.172T1/2Kah8.42±6.415.80±5.91T1/2Keh82.95±43.87120.06±60.83Tmaxh26.45±8.6222.33±11.72Cmaxng/mL182.73±59.27166.77±65.25AUC0-tng·h/mL21122±999919475±7009AUC0-∞ng·h/mL27390±1219731559±13412
2.5 生物等效性评价 采用SPSS软件对受试制剂和参比制剂的药动学参数AUC0-t、AUC0-∞和Cmax进行对数转化后进行方差分析,然后进行双单侧t检验及置信区间法计算,结果表明:受试制剂与参比制剂的AUC0-t、AUC0-∞、Cmax均无显著性差异(P>0.05)。受试制剂AUC0-t、AUC0-∞的90%置信区间分别为4.13~4.43、4.24~4.54,参比制剂AUC0-t、AUC0-∞的80%~125%的范围分别为3.41~5.33,3.56~5.56,受试制剂AUC0-t、AUC0-∞的90%置信区间均在参比制剂的80%~125%范围内。受试制剂Cmax的90%置信区间为2.15~2.34,落在参比制剂Cmax的70%~143%范围内(即1.53~3.13)。试验结果说明受试制剂与参比制剂具有生物等效性。
3 讨 论
健康家兔皮下注射受试制剂后,达峰时间为26.45 h,峰浓度为182.73 ng/mL,消除半衰期为82.95 h,皮下注射参比制剂后,达峰时间为22.33 h,峰浓度为166.77 ng/mL,消除半衰期为120.06 h,与参比制剂相比,受试制剂的达峰时间晚,峰浓度高,消除较快。由AUC0-∞数值得知,在相同剂量下,受试制剂在受试个体内的暴露量较参比制剂较低,但AUC0-t结果表明,在0~168 h内,受试制剂在受试个体内的暴露量较参比制剂高,这可能与受试制剂达峰时间晚,消除较快有关。受试制剂与参比制剂的AUC0-t、AUC0-∞、Cmax等药动参数均无显著性差异,并结合生物等效性评价结果,可判定受试制剂与参比制剂具有生物等效性。
试验中家兔单剂量皮下注射伊维菌素后,药时数据采用3P97药动学软件进行分析,结果与文献报道[5-6]的一致。从数据可以看出,虽然两制剂的各药动学参数无显著性差异,但也不全相同,这可能是因为制剂工艺不同而导致,至于两制剂的具体临床效果仍需临床试验,尚需做进一步研究。
[1] Fink D W,Porras A G. Pharmacodynamics of ivermectin in animals and humans[M]// Ivermectin and Abamectin. New York: Springer, 1989.
[2] 王敏儒, 陈杖榴, 冯淇辉. 伊维菌素微球在家兔体内的药动学[J]. 畜牧兽医学报, 2000, 31(2): 171-178.
[3] 白生芳, 雷萌桐. 害获灭注射剂对猪体内外寄生虫的驱虫试验[J]. 青海畜牧兽医杂志, 2012, 42(4): 26-27.
[4] 中国兽药典委员会. 中华人民共和国兽药典(二〇一〇年版)[S].
[5] 张瑞丽, 崔亮亮, 郝智慧, 等. 5种伊维菌素注射液在家兔体内的比较药动学研究[J].中国畜牧兽医, 2011, 38(11): 188-190.
[6] Atsushi Miyajima, Yosuke Yamamoto, Takashi Hirota. Effect of high fat intake on the pharmacokinetic profile of ivermectin in rabbits[J]. Drug Metabolism and Pharmacokinetics, 2015, 30(3): 253-256.
(编辑:李文平)
Bioequivalence of Two Different Ivermectin Injections in Rabbits
LI Peng-peng1,ZHANG Cong1,ZHANG Xiao-hui1,ZHOU De-gang1,LI Zhao-bin1,ZHANG Xiao-dong1,LIU Shuan2
(1.NationalResearchCenterforVeterinaryMedicine,Luoyang471003,China; 2.PulikeBiologicalEngineering,INC,Luoyang471003,China)
To evaluate the pharmacokinetics and bioequivalence of two kinds of ivermectin injections in rabbits, in a randomized two-way self-crossover study, 16 healthy rabbits were randomly divided into two groups, and were given respectively a single dose of two kinds of ivermectin injection by subcutaneous injection (5 mg/kg). Plasma concentrations of ivermectin were measured by HPLC. The pharmacokinetic parameters were calculated by 3P97 pharmacokinetic software, and the bioequivalence were evaluated. The main pharmacokinetic parameters of the test and reference preparations were as follows:Tmaxwere (26.45±8.62) h,(22.33±11.72) h;Cmaxwere (182.73±59.27) ng/mL,(166.77±65.25) ng/mL;AUC0-twere (21122±9999) ng·h·L-1,(19475±7009) ng·h·L-1;AUC0-∞were (27390±12197) ng·h·L-1,(31559±13412) ng·h·L-1. The pharmacokinetic parameters (AUC0-t、AUC0-∞、Cmax、Tmax) showed no significant difference between test and reference preparations of ivermectin injections. The test and reference formulations were bioequivalent after two one-sidet-test. This study provided theoretical basis for making of veterinary clinical dosage regimen and clinical rational administration.
ivermectin injection; bioequivalence; rabbits
李朋朋,硕士,兽医师,从事兽药研究及开发工作。E-mail:13526496019@163.com
2015-11-04
A
1002-1280 (2016) 01-0043-04
S859.79
