EDTA对Zn胁迫下紫花苜蓿生长和Zn积累特性的影响
2016-02-06吴三桥代惠萍贾根良李新生裴金金陕西理工学院生物科学与工程学院陕西汉中7300陕西理工学院陕西省资源生物重点实验室陕西汉中7300兰州大学生命科学学院甘肃省环境生物监测与修复重点实验室甘肃兰州730000西北农林科技大学理学院陕西杨凌700
吴三桥,代惠萍,,3*,贾根良,李新生,裴金金(.陕西理工学院 生物科学与工程学院, 陕西 汉中 7300; .陕西理工学院 陕西省资源生物重点实验室,陕西 汉中 7300; 3.兰州大学 生命科学学院/甘肃省环境生物监测与修复重点实验室,甘肃 兰州 730000;.西北农林科技大学 理学院,陕西 杨凌 700)
EDTA对Zn胁迫下紫花苜蓿生长和Zn积累特性的影响
吴三桥1,代惠萍1,2,3*,贾根良4,李新生2,裴金金2
(1.陕西理工学院 生物科学与工程学院, 陕西 汉中 723001; 2.陕西理工学院 陕西省资源生物重点实验室,陕西 汉中 723001; 3.兰州大学 生命科学学院/甘肃省环境生物监测与修复重点实验室,甘肃 兰州 730000;4.西北农林科技大学 理学院,陕西 杨凌 712100)
以紫花苜蓿为材料,采用盆栽法,研究了EDTA对Zn胁迫下紫花苜蓿生长和Zn积累特性的影响, 为螯合剂诱导植物修复Zn污染土壤提供理论指导依据。结果表明,与CK(不施加Zn和EDTA)相比,单一Zn胁迫(250 μg/kg Zn)下紫花苜蓿的株高、叶片干质量、根系干质量、叶片相对生长量、叶绿素a含量、叶绿素b含量和叶绿素a/b增加,但与CK差异不显著;而Zn+EDTA复合处理(250 μg/kg Zn+10 μg/kg EDTA)的紫花苜蓿叶片干质量、叶片相对生长量、根系相对生长量、叶绿素a含量、叶绿素b含量、叶片Zn含量、耐性指数较单一Zn胁迫处理分别显著增加了24.9%、35.7倍、2.3倍、13.0%、11.8%、27.2%、18.6%。可见,EDTA 有助于提高Zn胁迫下紫花苜蓿的叶绿素含量,从而增加生物量、转运指数和耐性指数。因此,紫花苜蓿可作为重金属Zn污染土壤的修复植物,而EDTA则能有效地促进紫花苜蓿对Zn的吸收。
Zn胁迫; EDTA; 紫花苜蓿; 生物量; 积累特性
矿区开采和冶炼产生的废水、废气及固体废物所导致的重金属污染对生态系统的破坏极为严重[1-4]。由于金属采矿所产生的尾矿砂颗粒较小,植物养分含量低,保水、保肥性能较差,重金属含量较高,故对其进行植被恢复非常困难[5-7]。植物修复是治理土壤重金属污染常用技术,具有治理成本的低廉性、治理过程的原位性以及治理效果的永久性等优点[8-12]。施加螯合剂可以促进土壤固相中重金属的释放,提高重金属的生物有效性[13-14]。Liu 等[15]研究发现,添加乙二胺四乙酸(EDTA)使金盏菊土壤Cd的修复效率提高217%。Cui等[16]研究表明,施加螯合剂EDTA后植物中Pb的累积浓度增加了2.5倍。Sun等[17]研究认为,EDTA能提高根际土壤Pb的植物有效性,促进Pb从根系向地上部的运输,显著提高植物对Pb的富集能力。
紫花苜蓿(MedicagosativaL.)是豆科苜蓿属多年生植物,能同时积累 Cd、Zn、Cu等多种重金属元素,因此成为治理污染土壤的首选植物材料[7-8]。然而,关于EDTA对Zn胁迫下紫花苜蓿生长发育的影响研究尚未见报道。鉴于此,通过添加外源EDTA,初步探讨EDTA对Zn胁迫下紫花苜蓿叶、根Zn积累量和生长的影响,解析紫花苜蓿在Zn胁迫下的耐受机制,为螯合剂诱导植物修复Zn污染土壤提供理论指导依据。
1 材料和方法
1.1 供试材料及试验地概况
紫花苜蓿品种为大叶苜蓿,种子由西北农林科技大学动物科学学院提供,供试土壤为草炭土、蛭石、农田表层土壤以质量比3∶1∶1混合。土壤性质:pH值为6.5,全氮含量为3.71 g/kg、有机质含量为76.8 g/kg、有效钾含量为28.2 mg/kg、有效磷含量为18.8 mg/kg,土壤阳离子交换量为0.033 mmol/kg。盆栽试验在陕西省资源生物重点实验室生物修复实验室温室内进行。
1.2 试验设计
试验采用盆栽法,塑料盆直径25 cm、高16 cm,每盆土壤质量约 2 kg。2014年3月播种,选饱满、无病虫害苜蓿种子,用0.1%的HgCl2消毒10 min,将HgCl2冲洗干净后,每盘播种20粒,在自然光照条件下培养,苜蓿生长期间用自来水浇灌,苜蓿幼苗生长3个月后,选生长一致的幼苗进行以下处理。
在去离子水中分别加入ZnSO4·7H2O母液和EDTA配成不同质量浓度的处理液,施入土壤中,形成对照(CK,不施加Zn和EDTA)、250 μg/kg Zn、250 μg/kg Zn+10 μg/kg EDTA 3个处理。每处理重复6次,共18盆。培养期间,采用称质量法补充消耗的水分。
1.3 测定项目及方法
1.3.1 生物量 Zn胁迫后50 d时取样,每个处理取12株,测量每株苜蓿的株高,分叶片和根系采收,并用去离子水冲洗。根系在20 mmol/L 乙二胺四乙酸二钠(EDTA-Na2) 溶液中浸泡交换10 min,以去除根系表面粘附的金属离子。然后烘箱内100 ℃杀青15 min,80 ℃下烘至恒质量。之后用万分之一天平称量苜蓿叶片和根系的干质量。按照如下方法计算相对生长量:相对生长量=(胁迫后生物量-胁迫前生物量)/胁迫前生物量。
1.3.2 Zn含量 将1.3.1中测定过干质量的叶片和根系的样品,粉碎成粉末,65%HNO3消解,用原子吸收分光度计测定Zn含量[17]。
1.3.3 转运指数、耐性指数和积累量 根据Dai等[12]的方法计算转运指数。转运指数=地上部Zn含量/根部Zn含量;耐性指数=Zn胁迫处理植物干质量/对照植物干质量[12];Zn积累量=植物地上(或根系)Zn含量×植物地上(或根系)生物量。
1.3.4 叶绿素含量 Zn胁迫后50 d取样,每个处理取12株,将叶片混合,利用分析天平准确称取0.02 g剪碎的样品(设3次重复),置于10 mL具塞刻度试管(各管先分别加入约0.5 mL纯丙酮),再加入80%丙酮浸提叶绿素,样品完全褪色后,以80%丙酮作为空白调零,分别在645、663 nm波长下测定提取液的光密度,计算叶绿素a、叶绿素b含量和总叶绿素含量[18]。
1.4 数据分析
采用SPSS 12.0进行统计分析, 采用one-way ANOVA方差分析比较不同处理间各项指标的差异,通过LSD法进行差异显著性(P<0.05)分析。
2 结果与分析
2.1 EDTA对Zn胁迫下紫花苜蓿生长的影响
由表1可见,与CK相比,单一Zn胁迫处理紫花苜蓿株高、叶片干质量、根系干质量均增加,但差异不显著;而Zn+EDTA复合处理紫花苜蓿株高、叶片干质量、根系干质量均较CK显著增加。Zn+EDTA复合处理紫花苜蓿的株高、叶片干质量、根系干质量分别比单一Zn胁迫处理提高了13.3%、24.9%、10.8%。
表1 EDTA对Zn胁迫下紫花苜蓿生长的影响
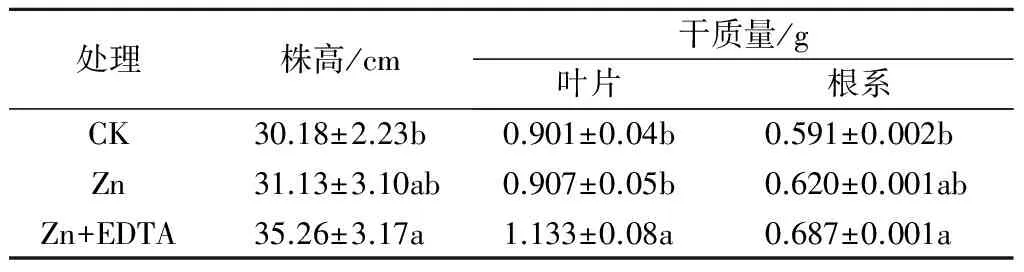
处理株高/cm干质量/g叶片根系CK30.18±2.23b0.901±0.04b0.591±0.002bZn31.13±3.10ab0.907±0.05b0.620±0.001abZn+EDTA35.26±3.17a1.133±0.08a0.687±0.001a
注:同列不同小写字母表示差异显著(P<0.05),下同。
2.2 EDTA对Zn胁迫下紫花苜蓿相对生长量的影响
由图1可知,与CK相比,单一Zn胁迫处理紫花苜蓿叶片和根系的相对生长量均稍有增加,Zn+EDTA复合处理紫花苜蓿叶片和根系相对生长量均有明显增加。Zn+EDTA复合处理紫花苜蓿的叶片、根系的相对生长量分别较单一Zn胁迫处理提高了35.7倍和2.3倍(P<0.05)。可见,EDTA可显著提高Zn胁迫下紫花苜蓿叶片和根系的相对生长量。
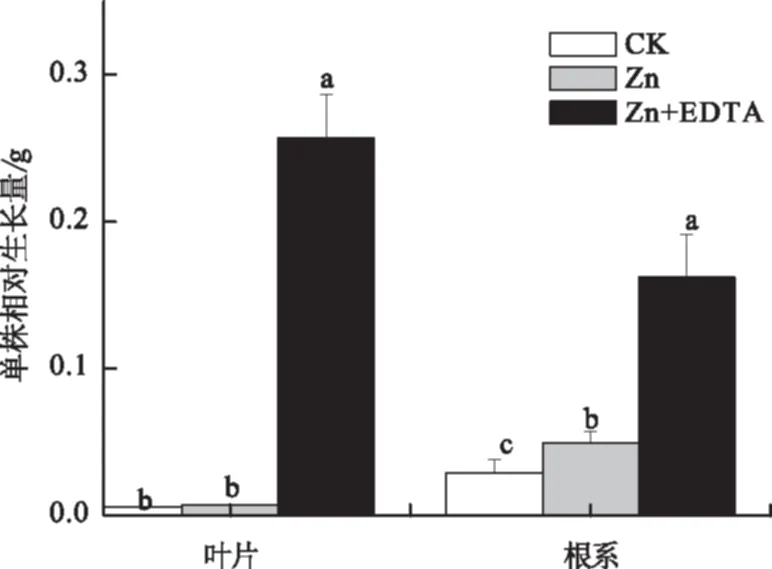
不同字母表示同一部位不同处理间差异达0.05显著水平图1 EDTA对Zn胁迫下紫花苜蓿相对生长量的影响
2.3 EDTA对Zn胁迫下紫花苜蓿叶绿素含量的影响
表2显示,与CK相比,单一Zn胁迫处理和Zn+EDTA复合处理下紫花苜蓿叶片叶绿素a、叶绿素b、总叶绿素含量和叶绿素a/b值均增加,且Zn+EDTA复合处理紫花苜蓿叶片叶绿素a、叶绿素b、总叶绿素含量和叶绿素a/b分别比单一Zn胁迫处理提高了13.0%、11.8%、12.6%和3.6%。可见,EDTA可以提高Zn胁迫紫花苜蓿叶片叶绿素含量。
表2 EDTA对Zn胁迫下紫花苜蓿叶绿素含量的影响
2.4 EDTA对Zn胁迫下紫花苜蓿积累特性的影响
表3表明,与CK相比,单一Zn胁迫处理和Zn+EDTA复合处理紫花苜蓿Zn含量、转运指数、耐性指数和 Zn积累量均提高,而且Zn+EDTA复合处理紫花苜蓿叶片Zn含量、根系Zn含量、转运指数、耐性指数、叶片积累量、根系积累量别比单一Zn胁迫处理高了27.2%、15.5%、9.9%、18.6%、2.0%、4.2%。可见,EDTA提高了紫花苜蓿的富Zn能力。
表3 EDTA对Zn胁迫下紫花苜蓿体内积累和分布的影响

处理Zn含量/(mg/kg)叶片根系转运指数耐性指数Zn积累量/(μg/株)叶片根系CK2.0±0.3c3.9±0.02c0.51±0.01b2.2±0.31b6.6±0.4bZn32.4±2.2b40.1±0.35a0.81±0.01a1.02±0.01b35.7±3.11a64.7±6.7aZn+EDTA41.2±2.9a46.3±0.42a0.89±0.02a1.21±0.02a36.4±3.26a67.4±7.8a
3 结论与讨论
逆境条件下,植株相对生长量的大小反映其抗逆性的强弱,相对生长量愈大,抗逆能力愈强[18]。本试验中,Zn+EDTA复合处理下紫花苜蓿相对生长量分别高于单一Zn胁迫处理相对生长量。由此可见, EDTA对Zn胁迫下紫花苜蓿的生长具有一定的促进作用。
EDTA能增加土壤中重金属的生物有效性,促进植物对重金属的吸收,降低重金属对土壤和植物的毒性[19-20]。添加EDTA能够使Cu、Cd、Pb和Zn在灯心草和龙须草体内的积累量显著增加[15]。本研究证实,与单一Zn胁迫比较,添加EDTA提高了紫花苜蓿的株高、叶片干质量、根系干质量及其对Zn的吸收、积累量和转运指数,与王红新等[8]和邱莉萍等[14]的研究结果相似。这可能是由于向土壤中施加螯合剂EDTA,活化了土壤中的重金属,提高重金属的生物有效性,促进植物对重金属的吸收。
叶片叶绿素含量作为植物的重要功能性状指标可以较好地反映其对非生物胁迫的生理响应[18]。王学锋等[21]研究表明,添加EDTA促进了茼蒿的生长,使茼蒿中的叶绿素含量增加。本试验也验证了这一点。Zn+EDTA复合处理苜蓿的叶绿素a、叶绿素b含量较单一Zn胁迫处理显著增加。说明添加EDTA对紫花苜蓿未产生毒害且使土壤中Zn受EDTA络合,更易被苜蓿吸收,而Zn对叶绿素合成有重要的影响。
EDTA通过提高Zn胁迫下叶绿素的含量增强光合作用,进而促进Zn胁迫下紫花苜蓿的生物量积累。同时,EDTA促进了紫花苜蓿根系和叶片对Zn的吸收、转运及积累。因此,EDTA 对Zn 污染土壤中的重金属元素有较好的络合作用,对紫花苜蓿修复Zn污染土壤有较好的促进作用。
[1] Jeyakumar P,Loganathan P,Anderson C W,etal.Comparative tolerance ofPinusradiataand microbial activity to copper and zinc in a soil treated with metal-amended biosolids[J].Environmental Science and Pollution Research International,2014,21(5):3254-3263.
[2] Nunes B,Capela R C,Sérgio T,etal.Effects of chronic exposure to lead,copper,zinc,and cadmium on biomarkers of the European eel,Anguillaanguilla[J].Environmental Science and Pollution Research International,2014,21(8):5689-5700.
[3] Dai H P,Shan C J,Zhao H,etal.The difference in antioxidant capacity of four alfalfa species in response to Zn[J].Ecotoxicology and Environmental Safety,2015,111,312-317.
[4] 董悦,刘晓群,李翠兰,等.土壤重金属污染研究进展[J].现代农业科技,2009(4):143-145.
[5] Peralta-Videa J R,Gardea-Torresdey J L,Gomez E,etal.Effect of mixed cadmium,copper,nickel and zinc at different pHs upon alfalfa growth and heavy metal uptake[J].Environmental Pollution,2002,119(3):291-301.
[6] Lahive E,O'callaghan M J,Jansen M A.Uptake and partitioning of zinc in Lemnaceae[J].Ecotoxicology,2011,20(8):1992-2002.
[7] 代惠萍,赵桦,贾根良,等.Zn和EDTA对紫花苜蓿叶片光合特性的响应[J].华北农学报,2016,31(2):132-137.
[8] 王红新,胡锋,许信旺,等.EDTA对铅锌尾矿改良土壤上玉米生长及铅锌累积特征的影响[J].生态学报,2011,31(23):7125-7132.
[9] 汪楠楠,胡珊,吴丹,等.柠檬酸和EDTA对铜污染土壤环境中吊兰生长的影响[J].生态学报,2013,33(2):631-639.
[10] 杨良柱,武丽.植物修复在重金属污染土壤中的应用概述[J].山西农业科学,2008,36(12):132-134.
[11] 罗琼,何录秋,杨文淼.油葵修复重金属污染农田研究进展[J].现代农业科技,2016(5):225-226,232.
[12] Dai H P,Shan C J,Jia G L,etal.Responses to cadmium tolerance,accumulation and translocation inPopulus×canescens[J].Water Air and Soil Pollution,2013,224:1504.
[13] 杨明琰,陈华,梁语燕,等.EDTA强化黑麦草对铅污染土壤的诱导修复效应[J].环境科学与技术,2014,37(9):19-22.
[14] 邱莉萍,张兴昌.Cu、Zn、Cd和EDTA对土壤酶活性影响的研究[J].农业环境科学学报,2006,25(1):30-33.
[15] Liu J,Zhou Q X,Wang S.Evaluation of chemical enhancement on phytoremediation effect of Cd-contaminated soils withCalendulaofficinalisL.[J].International Journal of Phytoremediation,2010,12(5):503-515.
[16] Cui S,Zhou Q X,Wei S H,etal.Effects of exogenous chelators on phytoavailability and toxicity of Pb inZninniaelegansJacq[J].J Hazard Mate,2007,146(1/2):341-346.
[17] Sun J,Tie B Q,Qin P F,etal.The potential of juncus effuses and eulaliopsis binata for phytoremediation of lead/zinc mine tailings contaminated soil under the adjustment of EDTA[J].Research of Environmental Sciences,2006,19(4):105-110.
[18] 代惠萍,赵桦,曹婷,等.Zn2+胁迫对4种紫花苜蓿光合色素的影响[J].西北农业学报,2014,23(3):128-132.
[19] 孙健,铁柏清,秦普丰,等.EDTA调控下灯心草和龙须草对铅锌尾矿污染土壤的修复潜力[J].环境科学研究,2006,19(4):105-110.
[20] Li X N,Yang Y L,Jia L Y,etal.Zinc-induced oxidative damage,antioxidant enzyme response and proline metabolism in roots and leaves of wheat plants[J].Ecotoxico-logy and Environmental Safety,2013,89(1):150-157.
[21] 王学锋,罗晓东,皮运清.EDTA对Pb、Cd及Pb-Cd处理下茼蒿中叶绿素的影响[J].环境科学与技术,2011,34(1):52-55.
Effects of ETDA on Growth and Zn Accumulation ofMedicagosativaL.under Zn Stress
WU Sanqiao1,DAI Huiping1,2,3*,JIA Genliang4,LI Xinsheng2,PEI Jinjin2
(1.College of Biological Science & Engineering,Shaanxi University of Technology,Hanzhong 723001,China; 2.Shaanxi Province Key Laboratory of Bio-resources/Shaanxi University of Technology,Hanzhong 723001,China; 3.School of Life Sciences,Lanzhou University/Gansu Province Key Laboratory of Biomonitoring and Bioremediation for Environmental Pollution,Lanzhou 730000,China; 4.College of Science, Northwest A&F University,Yangling 712100,China)
The effects of EDTA on Zn accumulation and growth ofMedicagesativaL. under Zn stress were studied by pot experiment,so as to provide theoretical basis for the chelator induced remediation of Zn contaminated soils by alfalfa.The results showed that there were no significant differences in dry weight of leaves and roots,relative growth yield of leaves,chlorophyll a content,chlorophyll b content and chlorophyll a/b between Zn stress treatment and control without Zn and EDTA.Compared with Zn stress treatment,dry weight of leaves,relative growth yield of leaves and root,contents of chlorophyll a,chlorophyll b,Zn contents of leaves,tolerance factor of the treatment with Zn and EDTA were increased by 24.9%,35.7 times,2.3 times,13.0%,11.8%,27.2%,18.6%.Above all,EDTA could alleviate the injuries induced by Zn stress by increasing the contents of chorophyll a,and chorophyll b,biomass translocation factor and tolerance factor of alfalfa.So,alfalfa can be the remediation plant for Zn contaminated soils,and EDTA can promote the absorbtion of Zn for alfalfa.
Zn stress; EDTA;MedicagesativaL.; biomass; accumulation character
2016-01-06
陕西省教育厅重点实验室项目(15JS019);陕西省自然科学基金项目(2015JM3086);甘肃省环境生物监测与修复重点实验室开放基金项目(GBBL2015006);国家大学生创新项目(201510720570);陕西省科技厅项目(SZS-15-05)
吴三桥(1962-),男,湖北郧县人,教授,本科,主要从事植物生理生化研究。E-mail:wsq800318@126.com
*通讯作者:代惠萍(1972-),女,陕西武功人,副教授,博士,主要从事植物逆境生理学研究。E-mail:daihp72@aliyun.com
S963.22+3.3;X53
A
1004-3268(2016)08-0049-04
