同步荧光法同时测定溶解态的菲与2-乙基菲
2016-01-27刘洋之杨承虎朱亚先
刘洋之,杨承虎,朱亚先,张 勇,3*
(1.近海海洋环境科学国家重点实验室,厦门大学 环境与生态学院,福建 厦门 361102;2.厦门大学
化学化工学院 化学系,福建 厦门 361005;3.漳州职业技术学院,福建 漳州 363000)
同步荧光法同时测定溶解态的菲与2-乙基菲
刘洋之1,杨承虎1,朱亚先2,张勇1,3*
(1.近海海洋环境科学国家重点实验室,厦门大学环境与生态学院,福建厦门361102;2.厦门大学
化学化工学院化学系,福建厦门361005;3.漳州职业技术学院,福建漳州363000)
摘要:将同步荧光法结合人工神经网络(ANN)和支持向量回归(SVR)用于混合体系中荧光光谱重叠的菲(Phe)和2-乙基菲(2-EP)两组分的同时测定。通过三维同步荧光法结合平行因子(PARAFAC)分析寻得Phe和2-EP的特征波长差Δλ为118 nm。在220~280 nm范围内,以31个波长处荧光强度值作为模型的输入变量用于建立ANN和SVR模型。结果显示,ANN模型分析Phe和2-EP预测样本的回收率分别为92.5%~104.9%和96.1%~104.3%,预测均方根误差(RMSEP)分别为2.08和2.95;SVR模型分析预测样本的回收率分别为98.2%~101.3%和94.9%~104.2%,RMSEP分别为0.74和2.42。实际水样的加标回收实验显示,基体简单的矿泉水中两种模型均取得满意结果;而基体复杂的湖水中样品预测值较实际值低,且SVR模型比ANN的预测性能更加稳健,泛化能力更强。将同步荧光法结合SVR模型应用于Phe和2-EP单独及混合状态下与腐植酸(HA)相互作用的研究,结果显示混合体系中Phe和2-EP与HA的结合系数均小于各自单组分体系,表明Phe和2-EP之间存在竞争吸附。
关键词:同步荧光法;菲;2-乙基菲;人工神经网络(ANN);支持向量回归(SVR)
目前有关多环芳烃(Polycyclic aromatic hydrocarbons,PAHs)环境行为和毒理学的研究大多针对母环PAHs(Parent PAHs)开展[1],但已有研究结果表明,忽略烷基PAHs(Alkyl PAHs)的存在对PAHs进行环境风险评价将会显著低估其值[2]。实际环境中Parent PAHs与Alky PAHs共同存在且会进一步代谢转化,为科学有效地评价水环境中PAHs的毒性效应,有必要建立同时测定Parent PAHs与Alky PAHs的分析方法。
多年来,Parent PAHs的分析方法不断改进[3-5],但仅有少数有关Alkyl PAHs的检测报道[6],所用气相色谱-质谱(GC-MS)法成本高、耗时长、前处理过程复杂,且萃取法破坏了目标化合物在水环境中的原始赋存状态。相对于常规荧光法,同步荧光法因具有选择性好等优点而被用于环境样品中多组分PAHs的分析检测[7]。另一方面,化学计量学方法在多组分PAHs分析中的应用也日益受到重视。屈薇薇等[8]使用荧光法结合人工神经网络(Artificial neural network,ANN)对蒽和芘进行同时测定,取得满意结果。Larrechi等[9]利用平行因子(Parallel factor analysis,PARAFAC)分析法研究了4种Parent PAHs的光降解行为。
本文以菲(Phe)和2-乙基菲(2-EP)分别代表Parent PAHs和Alkyl PAHs,利用同步荧光法结合ANN和支持向量回归(Support vector regression,SVR),尝试建立了同时测定Phe和2-EP的分析方法,并用于实际水样的测定及其与腐植酸(Humic acid,HA)相互作用的研究。以期为Parent PAHs与Alkyl PAHs的环境行为及生物有效性评价提供方法基础。
1实验部分
1.1仪器与试剂
Cary Eclipse荧光分光光度计(Varian,USA),1.0 cm石英比色皿,Cary-50紫外可见分光光度计(Varian,USA),KQ3200型超声波清洗器(150 W,昆山市超声仪器有限公司)。
Phe(纯度> 98%,Aldrich,USA),2-EP(纯度>99%,Aldrich,USA),HA(Technical grade Aldrich,USA),乙醇(分析纯,上海振兴化工一厂),实验用水为Milli-Q水,实际水样来自厦门大学翔安校区内湖水及商品矿泉水。
1.2实验方法
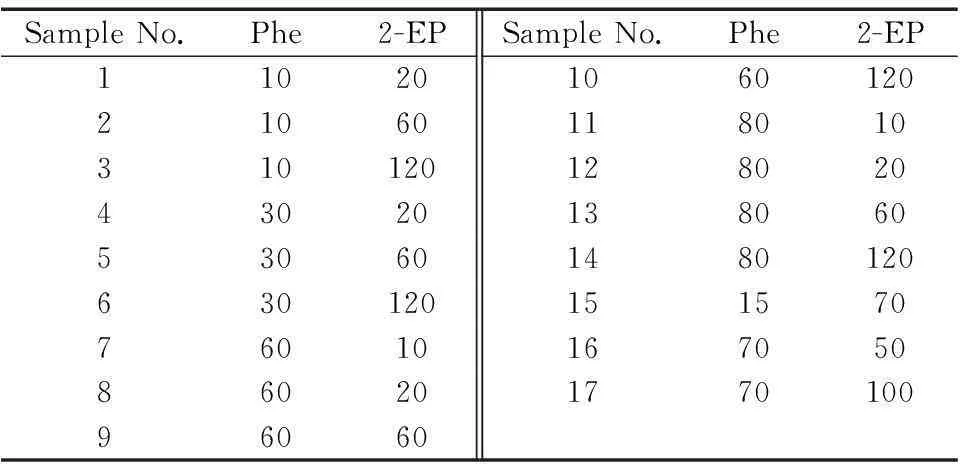
表1 训练样本及预测样本的浓度设置
准确称0.10 g Phe和2-EP分别配制成1.0 g·L-1乙醇储备液,采用逐级稀释法分别配成400 μg·L-1的Phe和2-EP工作液,避光储存于4 ℃冰箱中。配制14个不同浓度比的两组分混合溶液作为训练样本(Sample No.:1~14)[6],另取3个人工合成样品为预测样本(Sample No.:15~17)。具体浓度配比如表1所示。
三维荧光光谱扫描:激发波长200~350 nm,发射波长330~450 nm,步距均为2 nm;三维同步荧光光谱扫描:激发波长220~280 nm,步距均为2 nm;同步荧光光谱扫描:Δλ=118 nm,激发波长范围为220~280 nm。激发狭缝为10 nm,发射狭缝为5 nm。实验数据在Matlab中进行PARAFAC及ANN分析,在Libsvm软件包中进行SVR分析。
2结果与讨论
2.1同步荧光波长差Δλ的选择
由图1可知,单组分Phe和2-EP的三维荧光和三维同步荧光光谱严重重叠,因此传统荧光法无法实现Phe和2-EP混合组分的同时检测。同步荧光法具有简化谱图、提高选择性等优点[10],且与三维荧光法相比能缩短分析时间。利用PARAFAC解析三维同步荧光光谱,可获取Phe和2-EP的一个特征差异Δλ。对17个样本的三维同步荧光数据采用一组分PARAFAC分析,得到激发波长和Δλ载荷(如图2),从图中可观察到Δλ为118 nm时,Δλ载荷最高,说明118 nm可作为Phe和2-EP混合组分的特征Δλ。
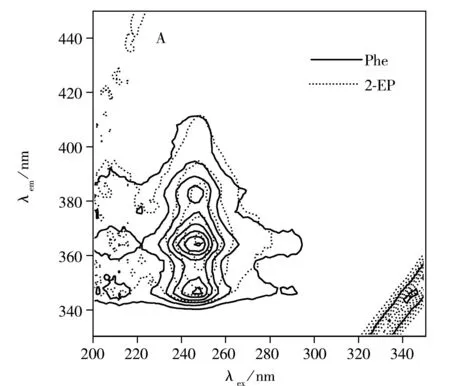
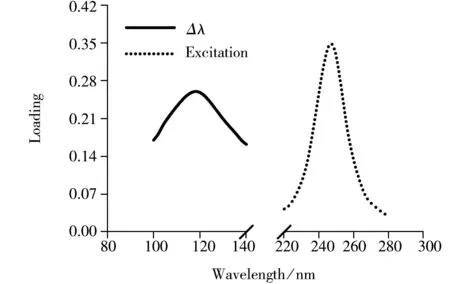
图2 激发波长和Δλ载荷Fig.2 Excitation wavelength and Δλ loading
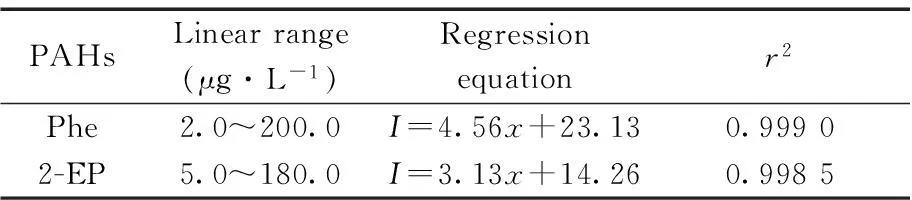
表2 同步荧光光谱法的分析特性(Δλ=118 nm)
2.2工作曲线、精密度与检出限
分别配制一系列不同浓度的单组分Phe和2-EP溶液,Δλ为118 nm,以激发波长248 nm处的荧光强度值(I)对其浓度(x,μg/L)作图,结果见表2。
分别配制9份50 μg·L-1的Phe和2-EP单组分溶液,测定其荧光值,计算得到Phe和2-EP的相对标准偏差(n=9)分别为1.0%和0.94%。同时测定10份Milli-Q水的荧光值,以其3倍标准的偏差除以工作曲线的斜率,计算得到Phe和2-EP检出限分别为0.21 μg·L-1和0.30 μg·L-1。
2.3 ANN建模分析
本实验使用包含一个隐含层的三层反向传播网络。以220~280 nm范围内所测波长点对应的荧光强度值作为输入变量,将对应样品浓度作为输出变量。因此,输入层和输出层的节点数分别为31和2。隐含层节点数需不断调整以适应不同问题和数据集的复杂性[11]。参考Kolmogorov定理,根据经验公式初步确定隐含层节点数范围[12]。设置最大训练次数为5 000,误差目标值为10-4,以均方误差(Mean square error,MSE)性能分析函数评估ANN性能。不断改变网络参数,当隐含层节点数为7,隐含层和输出层传递函数分别为tansig和purelin函数,训练函数为trainlm函数时,模型误差最小,预测性能最佳。为保证网络稳定并提高收敛速度,模型运行前对数据进行归一化处理,随后再反归一化获取实际值。
表3中Phe和2-EP的预测值均为10次随机训练结果的平均值。Phe和2-EP训练样本的预测回收率分别为94.6%~104.7%和91.4%~105.9%,校正均方根误差(Root mean square error of calibration,RMSEC)分别为1.23和1.40,相关系数(r2)分别为0.998 0和0.999 1。Phe和2-EP预测样本的预测回收率分别为92.5%~104.9%和96.1%~104.3%,预测均方根误差(Root mean square error of prediction,RMSEP)分别为2.08和2.95,相关系数(r2)分别为0.997 4和0.982 2。
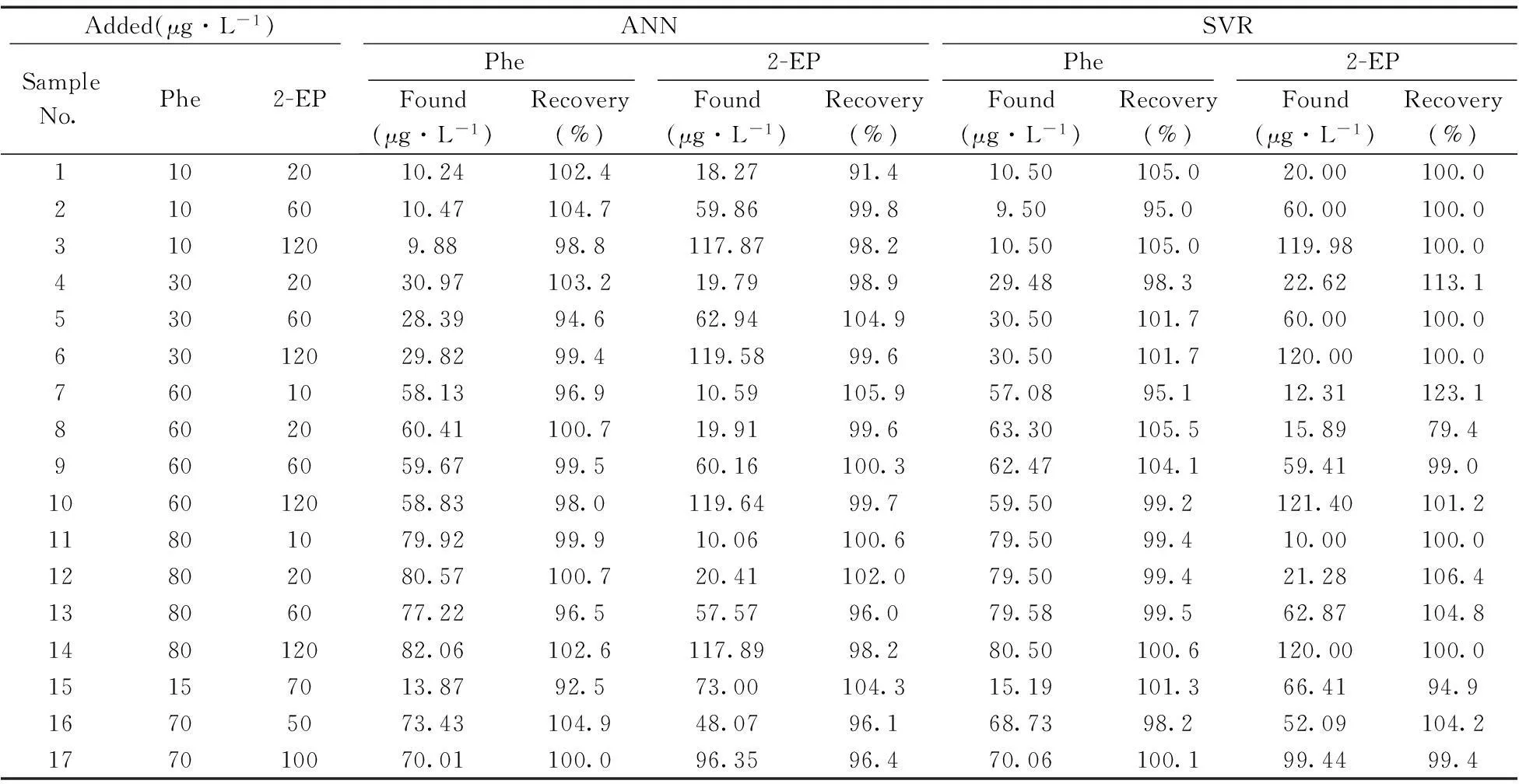
表3 训练样本及预测样本的回收率结果
2.4SVR建模分析
采用Libsvm(Library for support vector machine)[13]进行回归分析,其特点是简单、易使用,并能快速有效地进行支持向量机(Support vector machine,SVM)模式识别和回归,所采用的算法是序列最小优化算法[14]。本文采用Vapnik提出的ε-SVR模型[15]。SVR有不同的核函数类型,如径向基核函数RBF、多项式核函数、二层神经网络核函数及线性核函数,其中RBF核函数能减少训练过程的复杂性,使用最为广泛[16]。通过对不同核函数建模分析,显示RBF核函数的效果最好,所以本文选取RBF核函数进行ε-SVR分析。
首先将数据缩放到[0,1]之间,并对数据进行归一化处理。惩罚因子C、核宽度参数γ及ε是建立ε-SVR模型的3个最重要参数。该参数在很大程度上决定了算法的学习和泛化能力,所以需寻找合适的参数值以提高SVR预测精度。本文采用网格搜索法结合留一交叉验证法寻找最佳参数值,采用交叉验证过程可有效避免过拟合问题[13]。对于Phe,寻得C,γ及ε的最优参数值分别为1 024,0.031 3和0.5,2-EP的对应值分别为1 024,0.125和1。
选用RBF核函数为最优参数值,采用两个SVR模型分别对Phe和2-EP建模分析。如表3所示,Phe和2-EP训练样本的预测回收率分别为95.0%~105.5%和79.4%~123.1%,RMSEC分别为1.42和1.72,相关系数(r2)分别为0.997 2和0.998 5。Phe和2-EP预测样本的预测回收率分别为98.2%~101.3%和94.9%~104.2%,RMSEP分别为0.74和2.42,相关系数(r2)分别为0.999 5和0.988 1。
2.5实际水样中Phe与2-EP的测定
为验证两种模型方法的准确性,取矿泉水和湖水(过0.22 μm滤膜)两种不同基体的实际水样,分别向水样中加入Phe 和2-EP。采用上述条件对基体样品和加标样品进行同步荧光扫描,并采用ANN和SVR进行建模分析。湖水含有一定量的溶解性有机质(Dissolved organic matter,DOM),部分DOM有吸收和荧光,建模前需扣除基体荧光信号,并进行内滤校正[17]。表4为实际水样的预测结果,矿泉水对荧光信号测定无干扰,所以两种模型的预测值与真实值一致。湖水样中预测值比加标值低(除ANN模型下2-EP样品外),可能与DOM对Phe和2-EP的结合有关,且基体复杂样品中SVR模型比ANN模型的预测性能更加稳健。由表3结果同样可以看出,尽管ANN模型的RMSEC比SVR模型小,但RMSEP较SVR模型大,表明SVR模型的泛化能力比ANN强。因为,ANN以传统统计学为基础,需有大量数据进行网络训练,而SVR以统计学习理论为基础,能较好解决小样本、非线性和局部极小点等问题。由表4可知,荧光法结合化学计量法的回收率结果与固相萃取(SPE)联合气相色谱(GC)法的结果基本一致,但荧光法较SPE-GC法的操作简单,无需额外有机溶剂,且不改变PAHs原始赋存状态,可实现快速原位检测。
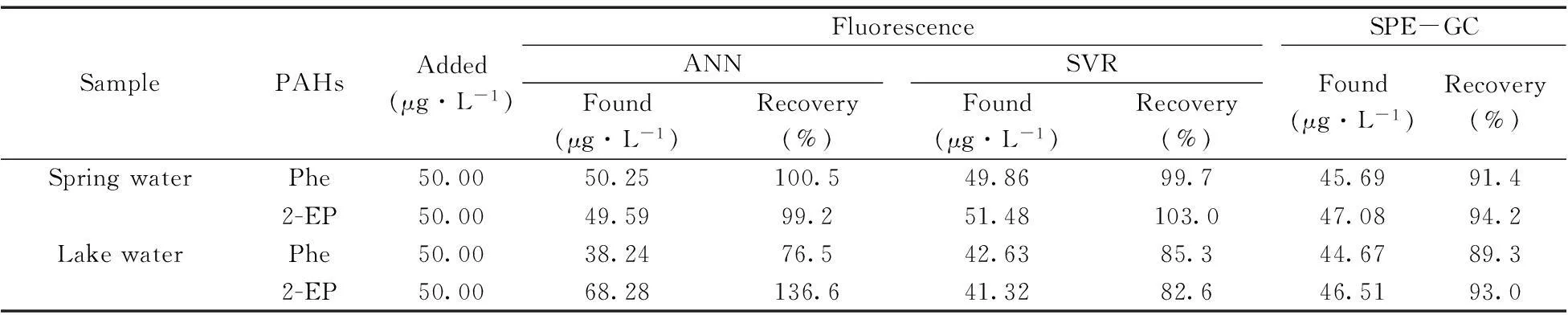
表4 实际水样的回收率结果
2.6Phe及2-EP与腐植酸(HA)结合能力的测定
荧光猝灭法因快速、灵敏及非破坏性等优点被广泛用于PAHs与HA结合能力的研究[18]。通常将有机碳归一化结合常数(KOC)作为衡量PAHs与HA结合能力强弱的重要指标。利用文献所述KOC计算方法[19],分别将50 μg·L-1Phe和2-EP加至HA溶液(2 mg·L-1DOC)中,利用同步荧光法结合SVR模型研究Phe和2-EP单独及共存状态下与HA的结合能力。如表5所示,同步荧光法结合SVR模型与传统荧光猝灭法所得lgKOC无显著差异,且2-EP与HA的结合能力比Phe大,这与2-EP的辛醇水分配系数lgKOW大于Phe的lgKOW有关。混合体系中Phe和2-EP的结合能力均小于单组体系,表明Phe和2-EP之间存在竞争吸附。
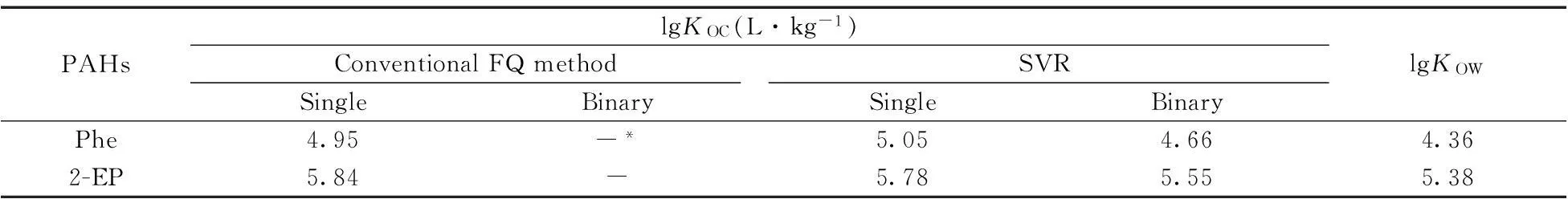
表5 Phe和2-EP单组分及两组分与腐殖酸的结合常数
*no data
3结论
利用同步荧光法结合ANN和SVR模型可实现混合溶液中光谱严重重叠的Phe和2-EP两组分的同时测定。对于基体复杂水样,SVR模型比ANN模型的预测性能更加稳健。相比于SPE-GC法,所建方法操作简便,为原位快速同时测定水溶液中Phe和2-EP的浓度提供了一种新思路。利用同步荧光法结合SVR模型可测定Phe和2-EP单独及共存时与HA的结合常数。该方法有望用于原位研究微生物对溶解态Parent PAHs及Alkyl PAHs两组分共存时降解过程及其生物毒性(如青鳉鱼)评价,为进一步认识PAHs的生态风险提供了一种新方法。
参考文献:
[1]Mastral A M,Callen M S.Environ.Sci.Technol.,2000,34(15):3051-3057.
[2]Barron M G,Holder E.Hum.Ecol.RiskAssess.,2003,9(6):1533-1545.
[3]Chen J N,Cai Z Q,Zhu Y X,Zhang Y.Chin.J.Anal.Chem.(陈佳宁,蔡宗群,朱亚先,张勇.分析化学),2008,36(3):301-305.
[4]Gao R,Rao Z,Guo X C,Huang Y,Li X J.J.Instrum.Anal.(高冉,饶竹,郭晓辰,黄毅,李晓洁.分析测试学报),2014,33(5):539-544.
[5]Zheng X Y,He L J,Zhang K G,Jiang X M,Xiang G Q,Liu J P.J.Instrum.Anal.(郑小焱,何丽君,张凯歌,江秀明,向国强,刘建平.分析测试学报),2014,33(5):566-571.
[6]Wenzel K D,Vrana B,Hubert A,Schuurmann G.Anal.Chem.,2004,76(18):5503-5509.
[7]Cai Z Q,Lu Z B,Zhu Y X,Hong L Y,Zhang Y.Chin.J.Anal.Lab.(蔡宗群,鹿贞彬,朱亚先,洪丽玉,张勇.分析试验室),2006,25(4):61-64.
[8]Qu W W,Shang L P,Li X X,Liu J.Spectrosc.SpecrtalAnal.(屈薇薇,尚丽平,李晓霞,刘晶.光谱学与光谱分析),2010,30(10):2780-2783.
[9]Bosco M V,Larrechi M S.Talanta,2007,71(4):1703-1709.
[10]Sun Y H,An H Y,Jia X L,Wang J.Spectrosc.SpecrtalAnal.(孙艳辉,安海洋,贾小丽,王娟.光谱学与光谱分析),2012,32(10):2726-2729.
[11]Yusaf T F,Buttsworth D R,Saleh K H,Yorsif B F.Appl.Energ.,2010,87(5):1661-1669.
[12]Wang F,Liu Y,Wang X F,Zhang C,Cao Q,Zhang F,Deng S,Chen Y W,Wang L G.Environ.Chem.(王凡,刘宇,王相凤,张辰,曹晴,张凡,邓双,陈育武,王立刚.环境化学),2014,33(1):93-99.
[13]Hsu C W,Chang C C,Lin C J.A Practical Guide to Support Vector Classification,2010[2015-05-10].http://www.csie.ntu.edu.tw/~cjlin/.
[14]Wang C Y,Shi X F,Li W D,Ren W W,Zhang J L.J.Instrum.Anal.(王春艳,史晓凤,李文东,任伟伟,张金亮.分析测试学报),2014,33(3):289-294.
[15]Vapink V N.StatisticalLearningTheory.New York:Wiley Interscience,1998:272-291.
[16]Filgueiras P R,Alves J C L,Poppi R J.Talanta,2014,119:582-589.
[17]Zhang Y,Zhong L,Du J,Chen J Y,Dong X Q,Li C M.Spectrosc.SpecrtalAnal.(张颖,钟莉,杜静,陈金玉,董晓倩,李春美.光谱学与光谱分析),2014,4(1):116-121.
[18]Gauthier T D,Shane E C,Guerin W F,Selltz W R,Grant C L.Environ.Sci.Technol.,1986,20(11):1162-1166.
[19]Hur J,Lee B M,Shin K H.Chemosphere,2014,111:450-457.

欢迎订阅欢迎投稿欢迎刊登广告
《分析测试学报》
国内刊号: CN 44-1318/TH国际标准刊号: ISSN 1004-4957
国际刊名化代码 CODEN: FCEXES邮发代号: 46-104
国外代号: BM 6013广告经营许可证:440000100186
《分析测试学报》是由中国广州分析测试中心、中国分析测试协会共同主办的全国性学术刊物,中文核心期刊。刊登质谱学、光谱学、色谱学、波谱学、电化学、电子显微学等方面的分析测试新理论、新方法、新技术的研究成果,介绍新仪器装置及在生物、医药、化学化工、商检、食品检验等方面实用性强的实验技术。适合科研院所、高等院校、检测机构、医药、卫生以及厂矿企业分析测试工作和管理人员阅读。
经过多年的发展,本刊已成为国内知名的化学类核心期刊。2015年,本刊的影响因子为1.227,在全国化学类刊物排名中位列第4名,被引频次每年递增约30%,稿源丰富,基金论文比超过70%。近几年,本刊刊发的论文被CA(美国化学文摘)收录率达94%,2006年引文频次在CA千种表中国部分中列第38名,并被国际上其它知名的数据库如日本科技文献速报、俄罗斯文摘、英国分析文摘(AA)、《质谱公报》等收录。入选2012年度“中国国际影响力优秀学术期刊”;进入由全国8000种期刊遴选出的500种科技期刊组成的“中国科技期刊精品数据库”;本刊是中国学术期刊综合评价数据库(CAJCED)统计刊源;中国科技论文统计源期刊(中国科技核心期刊);《中国科学引文数据库》来源期刊;中国期刊全文数据库(CJFD)收录期刊;《中国核心期刊(遴选)数据库》收录期刊;《中国学术期刊(光盘版)》全文收录期刊;《中国期刊网》全文收录期刊;《中国学术期刊文摘(中、英文版)》源期刊。
本刊为月刊, 国内外公开发行。大16开,单价:18.00元/册,全年216元。请在全国各地邮局订阅。 未在邮局订到者可直接向本编辑部补订。 补订办法: 请从邮局汇款至广州市先烈中路100号《分析测试学报》编辑部,邮编: 510070,写明订户单位、详细地址、收刊人姓名、邮编及补订份数(全年或某期), 电话:(020)87684776或37656606,http://www.fxcsxb.com(可在线投稿),E-mail:fxcsxb@china.com。

Simultaneous Determination of Dissolved Phenanthrene and 2-Ethylphenanthrene in Aqueous Solution by Synchronous FluorescenceLIU Yang-zhi1,YANG Cheng-hu1,ZHU Ya-xian2,ZHANG Yong1,3*
(1.State Key Laboratory of Marine Environmental Science of China(Xiamen University),College of Environment and Ecology,
Xiamen361102,China;2.Department of Chemistry,College of Chemistry and Chemical Engineering,Xiamen
University,Xiamen361005,China;3.Zhangzhou Institute of Technology,Zhangzhou363000,China)
Abstract:A method was developed for the simultaneous determination of phenanthrene(Phe)and 2-ethylphenanthrene(2-EP) in water by synchronous fluorescence spectroscopy combined with artificial neural network(ANN) and support vector regression(SVR).The characteristic wavelength offset(Δλ)is 118 nm by adopting three dimensional synchronous fluorescence spectroscopy with parallel factor analysis(PARAFAC).In range of 220-280 nm,the fluorescence intensities at 31 wavelengths were regarded as input variables for ANN and SVR models analysis.The results showed that the recoveries of Phe and 2-EP prediction samples were in the ranges of 92.5%-104.9%and 96.1%-104.3%,respectively,obtained by ANN model,while the recoveries of Phe and 2-EP were 98.2%-101.3%and 94.9%-104.2%,respectively by utilizing SVR model.The prediction root mean square errors(RMSEP)of Phe and 2-EP were 2.08 and 2.95 with ANN model,meanwhile they were 0.74 and 2.42 with SVR model,respectively.Recovery experiments by standard addition in actual water samples demonstrated that a satisfactory result was obtained with the two models for mineral water(simple matrix).However,predictive values were lower than the actual values for lake water(complex matrix),in which the performance of SVR model was more steady,and had stronger generalization ability than ANN model.Moreover,the synchronous fluorescence spectroscopy coupled with SVR was used to simultaneously calculate the binding coefficients of Phe and 2-EP with humic acid(HA)in a mixture solution.The result showed that the bonding capabilities of Phe and 2-EP in the mixed systems are both less than those in single component system,which indicated that there is a competing absorption existing between Phe and 2-EP.
Key words:synchronous fluorescence spectroscopy;phenanthrene(Phe);2-ethylphenanthrene(2-EP);artificial neural network(ANN);support vector regression(SVR)
中图分类号:O657.3;O625.15
文献标识码:A
文章编号:1004-4957(2015)12-1366-06
doi:10.3969/j.issn.1004-4957.2015.12.006
通讯作者:*张勇,博士,教授,研究方向:环境化学,Tel:18959288685,E-mail:yzhang@xmu.edu.cn
基金项目:国家自然科学基金(21177102,21075102);国家海洋局海洋溢油鉴别与损害评估技术重点实验室开放基金(201405)
收稿日期:2015-05-10;修回日期:2015-05-25
