ICP-OES与ICP-MS测定人体汗液的5种微量重金属元素
2016-01-21汤盛翔吴次南
汤盛翔,孟 达,吴次南
(1.贵州大学 生命科学学院,贵州 贵阳 550025;2.贵州大学 理学院,
贵州 贵阳 550025;3. 遵义师范学院,贵州 遵义 563002)
ICP-OES与ICP-MS测定人体汗液的5种微量重金属元素
汤盛翔1,孟达2,吴次南3*
(1.贵州大学 生命科学学院,贵州贵阳550025;2.贵州大学 理学院,
贵州贵阳550025;3. 遵义师范学院,贵州遵义563002)
摘要:采用不同的样品消化方法和电感耦合等离子体发射光谱法(ICP-OES)与质谱法(ICP-MS),尝试建立适合的测定汗液中铬(Cr)、铜(Cu)、锌(Zn)、镉(Cd)和铅(Pb)五种微量重金属元素的方法。结果显示,湿法消解-ICP-MS法检测汗液中这五种微量金属元素的相对偏差(RSD)为0.3%~9.4%,ICP-MS的加标回收率为92.8%~118.6%。相较其他方法,该法能快速精确地同时检测出汗液中多种微量重金属元素。
排汗是人体正常生理功能,排汗不仅通过水蒸气散发身体中的热量,从而防止体温过高[1],同时汗液是排出体内有害物质的重要途径,是检测体内有毒元素积累的重要检测物[2, 3]。当前对汗液的研究多集中在其对人体水分与渗透压等生理代谢方面的作用[4, 5]。此外,还有研究倾向于排汗对体内钠、钾等元素平衡的影响[6]。但是,由于汗液收集与检测方面的困难[7],汗液在生物病理和排出体内有害元素等方面的研究与应用较少。
对汗液成分的检测依据检测内容的不同,采用的方法也各有差别。对有机物如尿素、尿酸和部分元素的检测分析可采用比色法等,对活性物质如肌酐的检测分析可采用酶法等[4],对钠离子(Na+)、钾离子(K+)、氯离子(Cl-)、钙离子(Ca2+)、磷离子(P5+)等电解质的检测分析可使用紫外分光光谱法等[5, 6]。而对汗液中重金属元素检测研究方法鲜见于文献报道。检测其他体液(如血液或尿液)中微量重金属元素时,常采用方法有原子吸收光谱法[主要包括火焰原子吸收光谱(FAAS)和石墨炉原子吸收光谱(GFAAS)][8~11]、电感耦合等离子体发射光谱法(ICP-OES)[11~15]或质谱法(ICP-MS)[10, 11, 16~18]、气相色谱-质谱联用技术(GC-MS)[11, 15]等。本文将通过检测汗液中铬(Cr)、铜(Cu)、锌(Zn)、镉(Cd)和铅(Pb)五种重金属,对比ICP-OES与ICP-MS两种常用的多元素同时检测方法。
此外,生物基质样品进行元素分析都需要进行样品预处理,直接稀释[10, 19]、湿法消解[10, 12, 13, 20]和微波消解[9, 13, 14, 16, 18]是目前液态生物基质样品预处理主要采用的三种方法。本文也将探究这三种样品处理方法对消除人体汗液中干扰的能力,以期建立一个高效、准确、可靠的检测汗液中微量重金属的方法。
1材料与方法
1.1仪器与试剂
1.1.1实验仪器电感耦合等离子体光谱仪(美国Thermo Icap 6300MFC);电感耦合等离子体质谱联用仪(美国Thermo X Series 2);微波消解仪(美国CEM MARS6 PyNN130279);超纯水仪(美国Thermo Barnstead GenPure xCAD);电热板(中国 莱伯泰科DB-1A)。聚乙烯采样瓶、试管、烧杯、玻璃容量瓶若干,均用30%(V/V) HNO3浸泡48 h以上,使用前用超纯水反复冲洗6次,自然晾干。
1.1.2实验试剂浓硝酸(优级纯 成都金山化学试剂有限公司 批号20131106);高氯酸(分析纯 成都金山化学试剂有限公司 批号20140608);铅标准溶液、镉标准溶液、铬标准溶液、铜标准溶液和锌标准溶液(国家有色金属及电子材料分析测试中心,批号分别是GSB 04-1742-2004, GSB 04-1721-2004, GSB 04-1723-2004, GSB 04-1725-2004, GSB 04-1761-2004)。
1.2对象选择与样品采集
实验对象招募贵州大学本科二年级成年健康男性志愿者参与。通过调查确认他们没有抽烟酗酒等不良嗜好、无单独补充或服用特殊维生素或矿物质习惯,饮食结构相似;参试人员均在贵州大学北校区生活学习,属同一地理环境;在明确告知实验内容前提下,参试者自愿参与该项实验。
参试人员在室内恒温情况下,赤裸上身进行羽毛球运动2小时,使用经事先处理过的聚乙烯采样瓶刮取汗液20mL以上。静置30 min后用9 mm滤纸过滤后取10 mL放入试管中,4℃冰箱保存。
1.3样品处理
1.3.1直接稀释法取1 mL汗液,使用5% HNO3于50mL容量瓶定容[10]。
1.3.2HNO3-HClO4湿法消解于100 mL烧杯中加入5 mL汗液、3 mL HNO3和1 mL HClO4,放置电热板上温度由低至高进行消解,至烧杯中有浓烈白烟冒出,液体残余量≤0.5 mL停止加热,待冷却至室温后再加入0.75 mL HNO3,超纯水于50 mL容量瓶中定容[12]。
1.3.3微波消解于消解罐内加入1.25 mL汗液和4.5 mL 65% HNO3[10],按表1设置消解参数进行消解,完成后待消解罐冷却至常温,用超纯水于50 mL容量瓶中将消解样品定容。
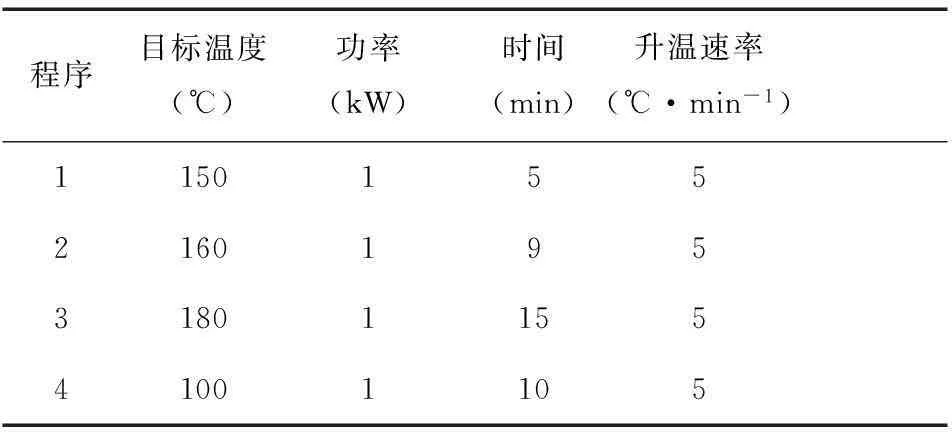
表1 微波消解仪各程序参数
以超纯水作为空白溶液,按照以上方法进行处理,作为实验空白对照。
1.4混标制备
使用5% HNO3配制混合标准溶液, 混合标准溶液包括Pb、Cr、Cd、Cu、Zn等5种重金属元素,其浓度梯度分别为0.00, 1.00, 10.00, 100.00 μg·L-1。
2实验结果
2.1精密度
按照试验方法对每种样品分别使用ICP-OES和ICP-MS进行9次平行检测,同时进行空白试验,各处理方法的精密度见表2(排出误差较大的无效数据)。

表2 精密度实验结果(n=9)
精密度与样品浓度、谱线强度相关。有研究表明样品浓度越低,谱线强度越弱,RSD值越大,其精密度越差,且精密度还受到仪器性能和分析条件的限制[21]。根据Lomakin-Scherbe公式[21],结合表2可知,ICP-OES与三种消解方法中铅(Pb)的精密度差,表明该法检出铅(Pb)元素浓度偏低;直接稀释法中镉(Cd)、铜(Cu)和锌(Zn)元素的RSD值小于10%,表明直接稀释法处理的样品中这三种元素能被检出的浓度较高;湿法消解和微波消解检测铬(Cr)和锌(Zn)元素的RSD值小于10%,而镉(Cd)和铜(Cu)元素的RSD值偏高,表明这两种方法处理样品中铬(Cr)和锌(Zn)元素能被检出的浓度较高,而镉(Cd)和铜(Cu) 元素能被检出的浓度偏低;ICP-MS中唯有湿法消解各被测元素检测的RSD值均小于10%,直接稀释法检测铬(Cr)元素和微波消解检测镉(Cd)元素的RSD值小于10%,但比湿法消解大,表明ICP-MS中湿法消解处理样品中各元素能被检出的浓度较高。
2.2加标回收实验
取一份汗液样品微波消化液作为基液,分别添加1.00, 10.00, 100.00 μg·L-1混合标准溶液,使用ICP-OES和ICP-MS分别进行加标回收实验,结果见表3。
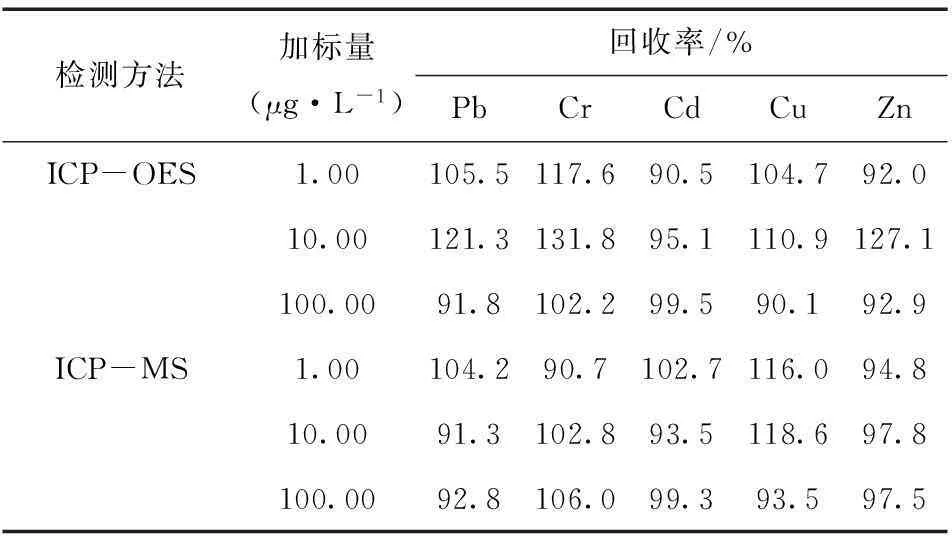
表3 各检测方法的加标回收率
由表3可知,ICP-OES和ICP-MS呈现不同元素其加标回收效果的不同。铅(Pb)、铬(Cr)元素回收实验中,ICP-OES的回收效果好于ICP-MS;而镉(Cd)、铜(Cu)和锌(Zn)元素回收实验显示,ICP-OES的回收效果与ICP-MS无较大差别。
2.3汗液中5种重金属的含量
根据样品处理方法的精密度(表2),接受RSD值为10%以下的测试结果,ICP-OES中铅(Pb)元素精密度较差被排出,故不在结果中显示;铬(Cr)元素选取微波消解测试结果;镉(Cd)、铜(Cu)、锌(Zn)元素选取直接稀释法测试结果。ICP-MS选择RSD值相对较小湿法消解结果显示,并进行差异分析得出结果见表4。

表4 汗液中5种重金属的含量测试结果
从表4可知,ICP-OES检测结果均显著高于ICP-MS,但ICP-OES检测结果的误差也均高于ICP-MS。
3讨论
关于汗液中重金属元素的检测较少见于文献报道,其检测方法也没有相关的标准。参考当前检测其他生物样品(如血液或尿液)微量元素检测方法的研究,其中FAAS和GFAAS在检测生物样品中微量元素时,前处理过程复杂,要加入不同的基体改进剂[8, 9],且分析元素种类较少,故检测生物基质中微量重金属元素时较少采用该方法[10, 11]。GC-MS中的气相色谱能高效分离混合物中的各组分,质谱能鉴定分离出的未知化合物,该法能高效快速进行定性与定量分析,应用广泛。但GC-MS检测时间长、机器运行成本高,对样品处前处理要求复杂[11, 15]。本文所采用的ICP-OES则具有较宽的动态线性范围、良好的准确度和精密度、基体干扰小等优点,能同时测定生物样品的多种微量元素[11],常应用于食品和生物样品的微量元素检测[12~15]。而ICP-MS的受干扰程度、精密度、检测速度、检出限和动态线性范围均优于ICP-OES和其他无机分析技术,不仅可以进行多元素同时测定,还能提供精确的同位素信息[10, 11, 16~18]。三种样品预处理方法也具有各自的特点。直接稀释法即用稀酸或稀碱稀释生物基质,此法不宜完全消除基质干扰,仅适用于基质中有机杂质较少的液体,故在检测水质方面有广泛的应用[10, 19];湿法消解是在加热条件下用浓碱或浓酸破坏生物基质中还原物或有机物以降低基体干扰,此法适用于生物基质样品的前处理,如血液、血清、尿液等[10, 12, 13, 20];微波消解是传统湿法消解的技术革新,既保留湿法消解的优点,同时在密闭环境下避免挥发性元素的损失,在生物基质样品的元素检测中应用较多[9, 13, 14, 16, 18]。近年来有研究提出新的消解方式,如酶消解[22]、紫外光[10, 23]和超声波降解[15],但技术尚不成熟,应用较少。
研究结果表明不同的样品处理方法和检测方法能检出的汗液中微量元素浓度是不同的。ICP-OES检测的数量级可以达到ppm-ppb级,ICP-MS检测的数量级可以达到ppb-ppt级[11],测量汗液样品时需要根据被测元素含量预估进行选择;样品处理方法的选择则需要根据被测元素的含量和特点来确定,对此还需要进行进一步深入的研究。依据本文的实验探索,湿法消解-ICP-MS法精确度达到0.3%~9.4%,相较其他方法其测量值的误差最小,说明该法能方便快捷地同时检测汗液中多种微量重金属元素,具备灵敏度高、精确度好等优点。
参考文献:
[1]左伊·黛安娜·德雷罗斯,田颖,李禾嘉. 止汗研究[J]. 日用化学品科学, 2003, 26(1): 39-41.
[2]Genuis S J, Birkholz D, Rodushkin I,etal. Monitoring and Elimination of Bioaccumulated Toxic Elements[J]. Archives of Environmental Contamination & Toxicology, 2011, 61(2):344-357.
[3]Genuis S J, Beesoon S, Birkholz D,etal. Human excretion of bisphenol A: blood, urine, and sweat (BUS) study.[J]. Journal of Environmental & Public Health, 2012,2012:185 731-185 731.
[4]崔晓,宣敏,陈葵,等. 湿热环境下高强度有氧训练诱发大量排汗对部分物质代谢的影响[J]. 中华实验外科杂志,2015,32(5):1 133-1 136.
[5]吴潇男,林建棣,曲平,等. 湿热环境下运动对汗液中尿素、乳酸和电解质的影响[J]. 武警医学, 2012,23(1):8-10.
[6]顾星,谭秦湘.自汗患者汗液中的钠、氯、钙、钾无机离子测定[J]. 中国中医基础医学杂志, 2005,11(5):371-372.
[7]Rock M J, Makholm L, Eickhoff J. A new method of sweat testing: the CF Quantum (R) sweat test[J]. Journal of Cystic Fibrosis Official Journal of the European Cystic Fibrosis Society, 2014,13.
[8]雷红琴,史岷山,杨菊清,等. 火焰原子吸收光谱法测定羊血中铁、铜和锌3种微量元素[J]. 光谱实验室, 2013, 30(6):2 969-2 972.
[9]刘祖强,钟伟燕,徐小作,等. 微波消化石墨炉原子吸收分光光度法测定血中铅镉[J]. 中国热带医学, 2005, 5(4):808-809.
[10]张素静. 血液和尿液中34种元素检测方法及其应用研究[D]. 苏州:苏州大学, 2013.
[11]蔡丽君. 重金属含量的分子光谱检测方法研究[D]. 南昌:华东交通大学, 2013.
[12]侯坤, 季宏兵, 李海蓉,等. ICP-OES法测定内蒙古饮茶型氟中毒病区人发、人尿中多种生命元素[J]. 光谱学与光谱分析, 2009, 29(4):1 100-1 103.
[13]石元值, 冯启华, 马立峰,等. ICP-OES法同时测定茶叶中La、Ce、Pr、Sm、Nd五种稀土元素[J]. 食品科学, 2008,(29):310-313.
[14]Szymczycha-Madeja A, Welna M, & Pohl P. Fast method of elements determination in slim coffees by ICP OES.[J]. Food Chemistry, 2014, 146(1):220-225.
[15]Santos D C M B, Carvalho L S B, Lima D C,etal. Determination of micronutrient minerals in coconut milk by ICP OES after ultrasound-assisted extraction procedure[J]. Journal of Food Composition & Analysis, 2014, 34(1):75-80.
[16]张秀武, 李永华, 杨林生,等. 温控湿法消解ICP-MS测定全血中铅镉硒砷汞5种微量元素[J]. 光谱学与光谱分析, 2010,30(7):1 972-1 974.
[17]王小燕, 李玉锋, 李柏, 等. 稀释法快速测定人体血液和尿液中多种重金属元素[J]. 分析试验室, 2010, 29(6):41-45.
[18]Taner Bora, Cagdas Aksoy, Zeki Tunay, & Frat Aydn. Determination of trace elements in illicit spice samples by using ICP-MS[J]. Microchemical Journal, 2015,123(6):179-184.
[19]吕杰. ICP-AES法同时测定饮用水中Pb,As等11种金属元素[J]. 光谱学与光谱分析, 2003, 23:779-784.
[20]许军, 温宏利, 魏复盛,等. ICP-MS/ICP-AES法分析成年男性血清中18种元素含量参照值[J]. 广东微量元素科学, 2006, 13:17-23.
[21]辛仁轩. 等离子体发射光谱分析(第三版) [M]. 北京: 化学工业出版社, 2011:123-124,156-157.
[22]许瑛华, 马文军, 邓峰,等. 酶消化-ICP/MS法测定广东省部分地区居民血中稀土元素含量[J]. 华南预防医学, 2006,32(4):1-5.
[23]Begerow J, Turfeld M, Dunemann L. New horizons in human biomonitoring of environmentally and occupationally relevant metals—sector-field ICP-MS versus electrothermal AAS[J]. J.anal.at.spectrom, 2000,15(4):347-352.


关键词:汗液;ICP-OES;ICP-MS;重金属
Determination of five heavy trace metal elements in human sweat by ICP-OES and ICP-MS
TANGSheng-xiang1,MENGDa2,WUCi-nan3*(1.CollegeofLifeScience,GuizhouUniversity,Guiyang550025,China; 2.CollegeofScience,GuizhouUniversity,Guiyang550025,China; 3.ZunyiNormalCollege,Zunyi563002,China)
Abstract:In this study, different digestion methods were used to prepare samples for determination of five heavy trace metal elements (Cr, Cu, Zn, Cd and Pb) in human sweat by inductively coupled plasma optical emission spectrometry (ICP-OES) and inductively coupled plasma mass spectrometry (ICP-MS). We found that the HNO3-HClO4wet digestion method combining with ICP-MS is more accurate to determine these five heavy trace metal elements because their relative standard deviations (RSDs) were 0.3%~9.4% and the recovery rates of ICP-MS were 92.8%~118.6%. It is concluded that, comparing with other combinations, HNO3-HClO4wet digestion-ICP-MS is the fast and accurate method for determining the heavy metal elements in human sweat.
Key words:Sweat; ICP-OES; ICP-MS; Heavy metal element
文章编号:1008-0457(2015)05-0038-04国际
DOI编码:10.15958/j.cnki.sdnyswxb.2015.05.007
中图分类号:Q984
文献标识码:A
通讯作者:*E-mail:cnwu@gzu.edu.cn。
基金项目:贵州大学研究生创新 (研农2015017)。
收稿日期:2015-09-05;修回日期:2015-10-15
