注射用头孢拉定在25 ℃时的稳定性研究
2016-01-19佘定平陈钦榜唐辉英
佘定平,何 英 ,陈钦榜,唐辉英
(1.深圳市第二人民医院药学部,深圳 518035;2.深圳市儿童医院,深圳 518035)
注射用头孢拉定在25 ℃时的稳定性研究
佘定平1,何英1,陈钦榜1,唐辉英2
(1.深圳市第二人民医院药学部,深圳518035;2.深圳市儿童医院,深圳518035)
摘要:目的考察注射用头孢拉定在25 ℃时的稳定性,为其贮存条件的选择提供依据。方法选择3个厂家3个批号的注射用头孢拉定样品在25 ℃下贮存3个月,依据《中国药典》2010年版二部注射用头孢拉定项下规定,考察其性状、溶液澄清度和颜色、水分、pH值、有关物质和含量的变化情况。结果注射用头孢拉定在25 ℃下贮存3个月,性状、水分、pH值、有关物质和含量均符合《中国药典》2010年版的规定;其中,一个厂家一个批次的样品溶液颜色在放置2个月后,颜色超过规定的黄绿色8号标准比色液。结论不同厂家生产的注射用头孢拉定其稳定性不同,大部分厂家的药品可在25 ℃下贮存3个月。
关键词:头孢拉定;温度;稳定性
日常生活中,抗生素在临床上失效导致治疗失败的案例屡见不鲜,造成抗生素失效的因素很多,除生产过程中的因素外,贮存、运输、配制过程中的影响也
不容忽视,如温度、湿度和配制后放置的时间等对抗生素的稳定性都可能带来影响[1]。在很多说明书中未明确地规定贮存的时间,如《中国药典》2010年版二部中头孢拉定要求遮光、密闭、在阴凉干燥处保存。阴凉处系指不超过20 ℃,但在炎热夏季将阴凉库的温度控制在20 ℃以下比较困难[2]。根据医院内药库的设备,基本能够满足药品的贮存要求,但由于湿热天气的影响,以及按绿色环保要求空调温度为最佳温度25 ℃,在药品运输到医院中,再由医院发放给患者,如果没有相应的冷藏、阴凉条件,中间流通的温度难以保证在20 ℃以下,这样会给药品质量带来严重的危害和隐患,这也是目前GSP监控的缺陷环节[3]。相对国外(或合资)制药企业相同成分的贮藏温度不同,国外(或合资)制药企业产品的贮藏温度普遍比国内的高5~10 ℃,使得药物更容易按照药品要求保管[4]。英国药典中规定阴凉处的温度为8~15 ℃,室温是15~25 ℃。美国药典同样规定阴凉处的温度为8~15 ℃,还说明了是8~15 ℃之间任一温度;对于室温有详细的规定,定义为工作区的温度,即可控的房间温度,是指将环境温度控制在20~25 ℃计算得到的平均动态温度不超过25 ℃;允许在15~30 ℃之间变动,15~30 ℃是药房、医院和病房的温度,只要平均动态温度保持在允许的范围内,温度偶尔达到40 ℃,但持续时间不超过24 h是允许的,物品的标签可能要求将其在可控房间温度在25 ℃或上述的平均动态温度下贮存,除非个论或标签上另有规定,要求在可控房间温度贮藏的物质,可直接在凉处贮藏和调配。张李锁认为需要阴凉贮藏的药品在营业厅待售期间,营业厅温度是否应该保持在<20 ℃?能够符合则好,但是由于药品营业厅是一个人流量大的场所,夏季控制在<20 ℃时不利于人的健康,更影响营业环境的舒适度,还加大能耗。因此,建议药品营业厅的温度可以放宽到25 ℃[5]。根据《中国药典》2010年版规定,关于药品的贮藏温度标准:阴凉处系指不超过20 ℃,凉暗处系指避光并不超过20 ℃,冷处系指2~10 ℃,常温系指10~30 ℃,但大多数药品的说明书上,却出现了各种各样的贮藏条件[6],苏婧建议《中国药典》应将常温贮藏、凉处贮藏、冷处贮藏、冷冻贮藏用具体的温度范围加以限制[7]。因此本文以头孢拉定为例,将药物放置在25 ℃下存放,放置时间分别为0,1,2和3个月,探讨25 ℃下药物的稳定性。
1仪器与试药
1.1仪器高效液相色谱仪(型号Waters 2690/2487,编号115020603800,美国Waters公司)(自动进样器,柱温箱,2487紫外检测器,Millenium数据处理系统);HANNA213型pH计;XS105Du型电子天平;水分测定仪;TH-150D-ZH恒温箱。
1.2试药对照品:头孢拉定(中国药品生物制品检定所,批号30427-200306,含量91.8%),精氨酸(中国药品生物制品检定所,批号110872-200506,含量100%);样品:注射用头孢拉定(规格:0.5 g,批号:RB3130303,1305205,20130109);乙腈为色谱纯,醋酸、醋酸钠、枸橼酸、磷酸氢二钠等均为分析纯。
2方法与结果
2.1稳定性实验将注射用头孢拉定置于恒温箱中,温度为25 ℃,分别于0,1,2和3月取样,考察其性状、溶液澄清度和颜色、水分、pH值、有关物质和含量。
2.2含量
2.2.1色谱条件十八烷基硅烷键合硅胶柱(色谱柱编号:2009-034);流动相:含0.027 mol·L-1辛烷磺酸钠的0.027 mol·L-1磷酸氢二钠溶液(用磷酸调节pH值至8.0)-甲醇(75∶25);检测波长:206 nm;流速:0.8 mL·min-1;进样量:10 μL;柱温:40 ℃。
2.2.2溶液配制系统适用性实验溶液:取头孢拉定对照品30 mg,头孢氨苄对照品5 mg与精氨酸对照品15 mg,精密称定,置于100 mL量瓶中,加水溶解并稀释至刻度,摇匀。
对照品储备液制备:精密称取头孢拉定对照品30 mg,置于100 mL量瓶中,加水溶解后,稀释至刻度,摇匀,得0.30 mg·mL-1的头孢拉定对照品储备液。精密称取精氨酸对照品15 mg,置于100 mL量瓶中,加水溶解后,稀释至刻度,摇匀,得0.15 mg·mL-1精氨酸储备液。
供试品溶液制备:取头孢拉定10瓶,分别加水溶解并定量稀释制成1 mL含头孢拉定0.3 mg的溶液。
2.2.3含量测定方法精密量取头孢拉定供试品溶液10 μL注入色谱仪,记录色谱图;另取头孢拉定与精氨酸混合对照品溶液、头孢拉定对照品溶液,同法测得,按外标法以峰面积计算供试品中C16H19N3O4S和C6H14N4O2的含量。
2.2.4含量测定结果结果见表1。
表1注射用头孢拉定含量测定结果
Tab.1 The contents of Cefradine for Injection (25 ℃)

批号时间/月无水、无精氨酸物含量/%精氨酸含量/%RB3130404097.534.621100.136.51298.435.73398.935.681305205096.736.48198.638.01298.138.03398.037.9520130109097.633.16198.734.02297.033.76396.732.91
《中国药典》2010年版规定,按无水、无精氨酸物计算,含头孢拉定不得少于90.0%,在25 ℃下放置0~3个月后,3批不同厂家的注射用头孢拉定含量符合药典规定的标准。
2.3有关物质
2.3.1色谱条件色谱柱:十八烷基硅烷键合硅胶柱(色谱柱编号:2009-022);流动相:水-甲醇-38.6 g·L-1醋酸钠溶液-40 mL·L-1醋酸溶液(1 564∶400∶30∶6);检测波长:254 nm;柱温:40 ℃。
2.3.2溶液配制系统适用性实验溶液:取杂质对照品7-氨基乙酰氧基头孢烷酸(7-ADCA)20 mg,精密称定,置于200 mL量瓶中,先加73 mL·L-1的盐酸溶液4 mL,超声使溶解,再用对照溶液稀释至刻度,摇匀。精密量取10 mL,置于100 mL量瓶中,加对照品溶液稀释至刻度,摇匀。
供试品溶液:取本品的内容物,混匀,精密称取80 mg,置于50 mL量瓶中,加流动相溶解并稀释至刻度,摇匀。
对照溶液制备:加精密量取供试品溶液1 mL。置于200 mL量瓶中,加流动相稀释至刻度,摇匀。
2.3.3测定方法取头孢拉定装量差异项下的内容物,混匀,精密称取适量,加流动相溶解并稀释成1 mL中含头孢拉定1 mg的溶液,作为供试品溶液。按照含量项下的色谱条件,检测波长为254 nm,精密量取供试品溶液与对照溶液各10 μL,分别注入液相色谱仪,记录色谱图。
2.3.4有关物质测定结果见表2。
表2注射用头孢拉定有关物质测定结果
Tab.2 The content of the related substances in Cefradine for Injection (25 ℃)

批号时间/月7-ADCA/%单个杂质/%各杂质的和/%RB313040400.0011.01.010.0201.11.120.0021.01.030.0021.01.0130520500.0021.21.210.0021.31.320.0101.21.230.0101.21.22013010900.0021.31.310.0101.41.420.0101.41.430.0101.31.3
根据《中国药典》2010年版规定,头孢拉定有关物质含量为7-ADCA≤1.0%、单个杂质≤2.0%、各杂质的和≤3.0%。在25 ℃下放置0~3个月后,3批不同厂家的注射用头孢拉定有关物质检查中,单个杂质以及各杂质和的测定结果均符合规定。
2.4性状和颜色取头孢拉定5瓶,分别按标示量加水制成1 mL中含头孢拉定0.1 g的溶液,若显色,与黄色或黄绿色8号标准比色液(《中国药典》2010年版附录Ⅸ A第一法)比较,均不得更深。性状检查则用肉眼观察。结果见表3。
表3注射用头孢拉定性状、颜色观察结果
Tab.3 The traits and color of Cefradine for Injection (25 ℃)
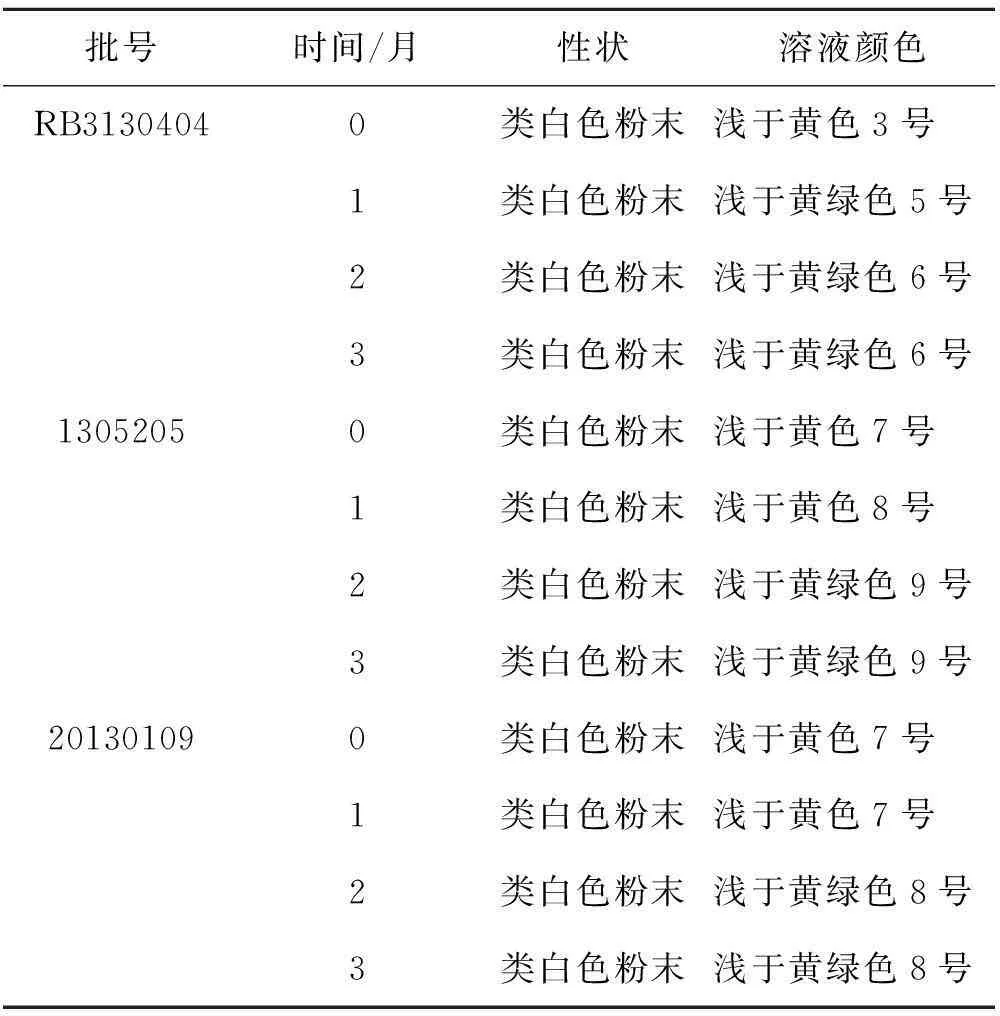
批号时间/月性状溶液颜色RB31304040类白色粉末浅于黄色3号1类白色粉末浅于黄绿色5号2类白色粉末浅于黄绿色6号3类白色粉末浅于黄绿色6号13052050类白色粉末浅于黄色7号1类白色粉末浅于黄色8号2类白色粉末浅于黄绿色9号3类白色粉末浅于黄绿色9号201301090类白色粉末浅于黄色7号1类白色粉末浅于黄色7号2类白色粉末浅于黄绿色8号3类白色粉末浅于黄绿色8号
《中国药典》2010年版规定,头孢拉定为白色或类白色粉末,溶液颜色不得深于黄色或黄绿色8号标准比色液。在25 ℃下放置0~3个月后,3批不同厂家的注射用头孢拉定性状符合规定,但批号为1305205的样品,放置2个月后,颜色浅于黄色9号标准比色液,不符合规定。
2.5碱度取头孢拉定适量,加水制成1 mL中含头孢拉定0.1 g的溶液,依法用pH计测定(附录Ⅵ H),《中国药典》2010年版规定,头孢拉定酸碱度在8.0~9.6之间。在25 ℃下放置0~3个月后,3批不同厂家的注射用头孢拉定碱度符合规定,结果见表4。
2.6水分取头孢拉定适量(含精氨酸),用水分测定仪按照《中国药典》2010年版规定测定,《中国药典》2010年版规定,头孢拉定水分不得超过5.0%。在25 ℃下放置0~3个月后,3批不同厂家的注射用头孢拉定水分符合规定,结果见表4。
表4注射用头孢拉定碱度和水分测定结果
Tab.4 The pH and water content of Cefradine for Injection (25 ℃)
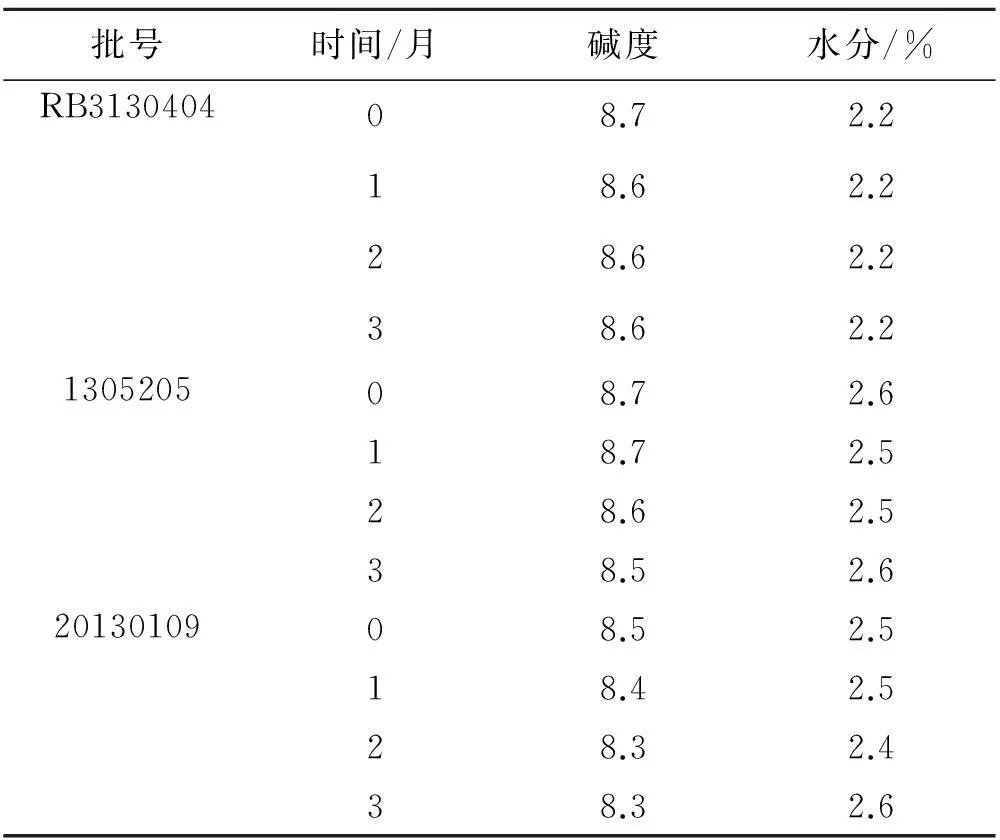
批号时间/月碱度水分/%RB313040408.72.218.62.228.62.238.62.2130520508.72.618.72.528.62.538.52.62013010908.52.518.42.528.32.438.32.6
3讨论
Yamana等[8]指出,根据化学动力学研究,头孢拉定在水溶液中的降解遵循一级动力学,其降解途径为C-7侧链氨基的分子内氢核攻击β-内酰胺环降解、分子内一般酸和特殊碱催化β-内酰胺环断裂;由于C-3无乙肽氧基,对强酸也较稳定;pH值在较低(3~5)时也为水催化β-内酰胺环降解;pH值为8.0时降解速率比C-7侧链无α-氨基的头孢类约高出10~20倍。干燥的头孢拉定在(水分≤0.1%)25 ℃下贮存可保持原效价达2年。据实验,注射用头孢拉定在25 ℃下贮存3个月,药物的含量、有关物质、酸碱度、水分、性状均符合《中国药典》2010年版的规定,一个样品溶液颜色在放置2个月后,颜色变深,应更加注意药品的贮存。
建议《中国药典》应将常温贮藏、凉处贮藏、冷处贮藏、冷冻贮藏用具体的温度范围加以限制。将药物的贮存温度进行细化,能在25 ℃下贮存的药物不应定为20 ℃下,这样能方便药房管理并节约能源。
参考文献:
[1]陈凯.注射用头孢他啶在3种输液中的稳定性[J].西北药学杂志,2005,20(3): 121-122.
[2]袁国顺. 药品储存管理之我见[J].首都医药,2007,6(11): 48-49.
[3]徐明军,王维,纪炜. GSP管理实践及认证检查中几个问题的思考与对策[J].西北药学杂志,2011,26(3): 217-220.
[4]曾明艺,黄春,李建.对药品贮藏温度的调查分析[J].海峡药学,2009,21(2): 157-158.
[5]张李锁.对《中华人共和国药典》2005年版药品贮藏温度规定存在问题的探讨[J].医药导报,2006,25(1): 83-84.
[6]候晓宁. 对规范药品贮藏温度标示的若干思考[J].中国药房,2008,19(10): 788-789.
[7]苏婧,郑仁礼,陈敏.药品说明书中贮藏温度标识调查分析[J].中外健康文摘,2012, 9(5): 388-389.
[8]Yamana T,Tsuji A.Comparative stability of cephalosporins in aqueous solution: Kinetics and mechanisms of degradation[J]. J Pharm Sci,1976,65(11): 1563-1574.

Study on the stability of Cefradine for Injection at 25 ℃
SHE Dingping1,HE Ying1,CHEN Qinbang1,TANG Huiying2(1.The Second People′s Hospital of Shenzhen,Shenzhen 518035,China;2.Shenzhen Children′s Hospital,Shenzhen 518035,China)
Abstract:Objective To provide the basis for selecting storage conditions,the stability of Cefradine for Injection at 25 ℃ was studied. Methods Three batches of Cefradine for Injection samples from three manufacturers were stored at 25 ℃ for 3 months,and the physicochemical properties,solution clarity and color,moisture,pH,the related substances and the content of cefradine were determined according to Chinese Pharmacopoeia(2010 edition). Results The physicochemical properties,moisture,pH,the related substances and the content of cefradine met the requirements of Chinese Pharmacopoeia(2010 edition) under 25 ℃ storage for 3 months,but the color for a batch of samples placed for 2 months later was yellow and more than the prescribed standards for the 8th standard colorimetric solution. Conclusion The stability of Cefradine for Injection of the different manufacturers was different,and some of them could be stored for three months at 25 ℃.
Key words:cefradine;temperature;stability
收稿日期:(2015-05-05)
基金项目:深圳市科技创新委科技研发项目(编号:JCYJ20130401113107214)
中图分类号:R94
文献标志码:
文章编号:1004-2407(2016)01-0079-04
doi:10.3969/j.issn.1004-2407.2016.01.024
