不同固体制剂中白杨素的溶出度评价
2016-01-19郑少华张沛沛
李 欣,郑少华,张沛沛,苏 进*
(1.西安交通大学医学部第一附属医院,西安 710061;2.西安交通大学医学部,西安 710061)
不同固体制剂中白杨素的溶出度评价
李欣1,郑少华1,张沛沛2,苏进1*
(1.西安交通大学医学部第一附属医院,西安710061;2.西安交通大学医学部,西安710061)
摘要:目的考察白杨素不同固体制剂的体外溶出度,并建立白杨素制剂的溶出度HPLC测定方法。方法分别以体积分数40%和50%乙醇溶液,5和10 g·L-1十二烷基硫酸钠(SLS)溶液为溶出介质,对制备的3种白杨素固体制剂进行体外溶出度考察,并建立白杨素溶出度HPLC测定方法。结果10 g·L-1十二烷基硫酸钠溶液更适合作为本研究中制备的3种白杨素固体制剂的溶出介质,白杨素微粉化胶囊剂的溶出度最高。此外,初步探讨了白杨素固体制剂体外溶出标准。结论不同制剂的白杨素溶出度差异较大,微粉化工艺能显著提高白杨素的溶出度。
关键词:白杨素;固体制剂;溶出度
合适的剂型是药物发挥其药理作用的必要形式[1-2]。剂型能够改变药物的作用性质,吸收速率,生物利用度。除此之外,运用剂型的改变能够使药物具有靶向作用,如脂质体、微粒、微球、微囊、纳米囊等具有被动靶向脾、肝、肾等网状内皮系统的作用[3-4]。同一药物的不同制剂类型往往具有不同的疗效,如起效的强度和持续时间,甚至产生不良反应等[1-4]。因此,药物发挥疗效往往受到剂型因素的影响。
目前存在大量的中药提取物具有良好的药理、生理活性[5],但是,其中大多数药物面临着溶解性差[3],生物利用度低的现状[6]。白杨素(chrysin),又名白杨黄素,化学名为5,7-二氢基黄酮,结构式如图1所示。存在于紫葳科植物木蝴蝶的种子、茎皮,松科植物山白松的心木,芒松的心木等。白杨素具有抗氧化、抗肿瘤、抗癌、抗病毒、抗高血压、抗糖尿病[7]、抗菌、抗过敏等药理生理活性[8]。尤其抗肿瘤疗效表现显著,因其毒性较低,近几年来,国内外学者对白杨素的药效,作用机制进行了广泛研究[9-13]。本文则将白杨素分别制备成3种口服固体剂型,并对3种剂型进行了体外溶出度评价,并建立了高效液相色谱法测定白杨素制剂的溶出度,以期开发出生物利用度更高,更具有临床应用价值的白杨素制剂。
1试药与仪器
1.1仪器高效液相色谱仪(岛津,LC-20AT);ZRS-智能药物溶出仪(天津大学无线电厂);WL-1型微粒球磨机(天津市电工专用设备厂)。
1.2试药白杨素原料药(陕西嘉禾植物化工有限责任公司);白杨素对照品(北京世纪奥科生物技术有限公司);微晶纤维素、交联羧甲基纤维素纳(安徽山河药用辅料股份有限公司,药用级);硬脂酸镁(安徽山河药用辅料股份有限公司,药用级);无水乳糖(镇江市康富生物工程有限公司,药用级);无水乙醇(沈阳化学试剂厂,分析纯);十二烷基硫酸钠(天津市博迪化工有限公司,分析纯);磷酸(天津化学试剂厂,分析纯);甲醇(天津市天力化学试剂有限公司,色谱纯)。

图1白杨素结构
Fig.1 Structure of chrysin
2方法与结果
2.1白杨素3种固体制剂的制备白杨素处方如表1所示。
表1白杨素制剂处方
Tab.1 Prescription of chrysin preparations

成分用量(片质量/胶囊填充量:200mg)/mg/%作用白杨素70.035.0主药微晶纤维素80.040.0黏合剂交联羧甲基纤维素纳2.01.0崩解剂硬脂酸镁1.00.5润滑剂无水乳糖47.023.5填充剂
根据表1处方的组成,分别制备白杨素片剂,白杨素颗粒化胶囊剂,白杨素微粉化胶囊剂。
2.1.1白杨素片剂的制备将白杨素原料药和各辅料粉碎,过100目筛,按处方比例称取白杨素原料药与各辅料。将硬脂酸镁与交联羧甲基纤维素纳混合均匀,加入无水乳糖,使其充分混合,然后再加入微晶纤维素及白杨素原料药,继续混合均匀,采用粉末直接压片法制得片剂,片质量为200 mg。
2.1.2白杨素颗粒化胶囊剂的制备取2.1.1项所述的粉碎过筛后的原料药及各辅料进行混合,混合均匀后加入适量体积分数70%的乙醇制备软材、制粒、干燥,充分干燥后进行整粒,将颗粒剂装入胶囊,每粒含有200 mg颗粒,即为白杨素颗粒化胶囊剂。
2.1.3白杨素微粉化胶囊剂的制备按处方比例准确称取白杨素原料药,置于微粒球磨机中研磨2 h 后过120目筛,与处方中其余各成分混合均匀后装胶囊,使每粒含有200 mg粉末,即得白杨素微粉化胶囊剂。
2.2HPLC法测定白杨素方法学的建立
2.2.1色谱条件色谱柱:Phenomenex-C18(250 mm×4.6 mm,5 μm);流动相为甲醇-4 mL·L-1的磷酸水溶液(65∶35);波长:256 nm;柱温:30 ℃;流速:1.0 mL·min-1;进样量:20 μL。理论板数按白杨素计算不得少于3 000。
2.2.2对照品溶液制备精密称取干燥至恒质量的白杨素对照品适量,加甲醇使溶解,制成1 mL含白杨素0.040 mg的溶液。
2.2.3供试品溶液制备取10片白杨素片剂,研磨,取适量的粉末,加甲醇溶解,将溶液经0.45 μm的滤膜过滤,弃去初滤液,将续滤液稀释成1 mL含白杨素0.040 mg的溶液。
2.2.4空白溶液制备按处方量精密称取各辅料,混合均匀,加甲醇溶解,将溶液经0.45 μm的滤膜过滤,弃去初滤液,使其与供试品溶液质量浓度一致,即为空白溶液。
2.2.5专属性考察取上述对照品溶液、供试品溶液、空白溶液在2.2.1项中的色谱条件下进行检测,结果如图2所示,在该色谱条件下,能够使白杨素与制剂中的各辅料实现良好分离,且辅料对白杨素的测定无干扰。
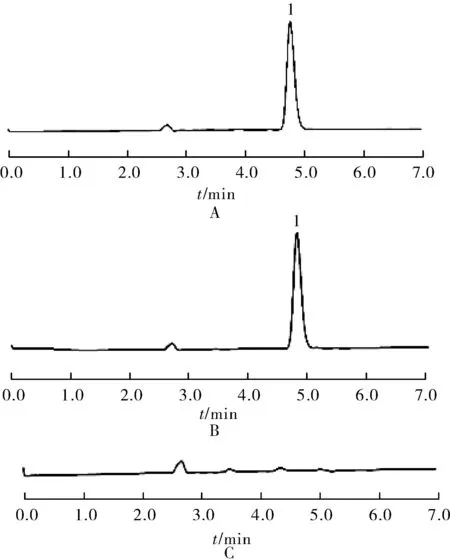
图2HPLC图
A.对照品;B.供试品;C.空白溶液;1.白杨素
Fig.2 HPLC chromatograms
A.reference substance; B.sample; C.blank; 1.chrysin
2.2.6线性关系考察精密吸取白杨素对照品溶液1,2,4,6和8 mL,分别置于10 mL量瓶中,用甲醇稀释至刻度,摇匀,各取20 μL注入液相色谱仪,按2.2.1项下的色谱条件进行测定,记录峰面积,以峰面积对质量浓度线性回归,在0.004~0.040 mg·mL-1范围内呈良好的线性关系,回归方程:Y=1 459 341X-1 528,r=0.999 0。
2.2.7精密度考察取2.2.3项下同一供试品溶液在2.2.1项的色谱条件下进行HPLC检测,进样量为20 μL,连续进样6次,测定白杨素的峰面积值,其RSD(%)为0.75%。表明精密度良好。
2.2.8回收率实验称取白杨素原料药5.6 ,7.0 和8.4 g分别约为处方量的80,100和120倍。分别置于①、②、③号研钵中,再分别加入空白辅料(无水乳糖、交联羧甲基纤维素纳、微晶纤维素、硬脂酸镁)13.0 g(约为处方量的100倍)混合均匀。分别从3个研钵中取样品粉末,每个含量各取3份,称量它们各自的质量。将这些粉末分别置于9个100 mL的容量瓶中,用适量的甲醇溶解,摇匀,用0.45 μm的滤膜过滤,弃去初滤液,得续滤液,即回收率80%(3份),100%(3份)和120%(3份)的供试品溶液。在2.2.1项的色谱条件下分别精密量取对照品溶液及各样品溶液20 μL,注入色谱仪,记录色谱图,按外标法以峰面积计算。结果回收率分别为80%(3份):101.28%,99.48%和98.83%;100%(3份):100.09%,100.62%和101.02%;120%(3份):99.95%,100.50%和100.68%,回收率良好。
2.3溶出度考察
2.3.1溶出介质中的稳定性考察分别以体积分数40%和50%的乙醇溶液、5 g·L-1、10 g·L-1的十二烷基硫酸钠溶液(SLS)为溶剂,分别配制成质量浓度为70 mg·L-1的白杨素溶液,经37 ℃恒温2 h ,冷却至室温,测定恒温前后含量,其恒温前后的含量变化的相对标准差小于2.0%,分别为0.63%,0.84%,0. 92%和0.77%,表明白杨素在这4种溶出介质中经37 ℃恒温2 h相对稳定,且SLS不会干扰白杨素的含量测定。
2.3.2溶出度测定方法取白杨素的3种固体制剂,照溶出度测定法(2010年版《中国药典》二部附录XC)第二法。溶出介质为900 mL,转速为100 r·min-1,依法操作,分别在5,10,20,30,45,60,90和120 min时取溶液2 mL,滤过,弃去初滤液,精密量取1 mL续滤液置于5 mL量瓶中,分别用2.3.1项下的溶出介质稀释至刻度,混合均匀,即为溶出度实验的供试品溶液。供试品溶液照2.2.1项下的色谱条件进行检测,进样量为20 μL,按标准曲线计算含量并换算溶出度。
白杨素的3种固体制剂(A:普通片剂;B:颗粒化胶囊;C:微粉化胶囊)在4种溶出介质中的溶出曲线见图3至图6。

图3白杨素固体制剂在体积分数40%乙醇溶出介质中的溶出曲线
Fig.3 Dissolution profiles of chrysin in 40% ethanol medium

图4杨素固体制剂在体积分数50%乙醇溶出介质中的溶出曲线
Fig.4 Dissolution profiles of chrysin in 50% ethanol medium
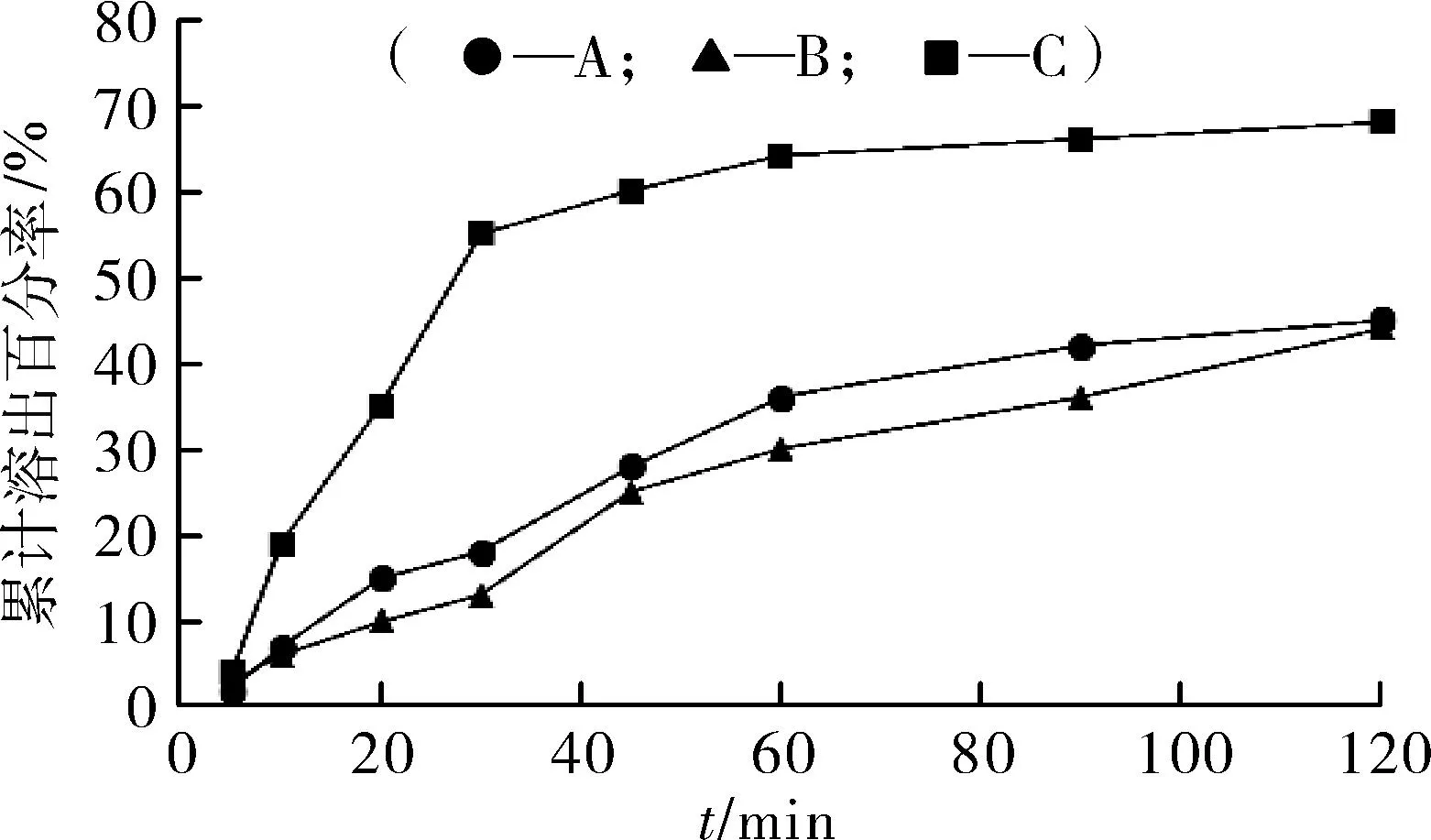
图5白杨素固体制剂在5 g·L-1SLS溶出介质中的溶出曲线
Fig.5 Dissolution profiles of chrysin in 5 g·L-1SLS
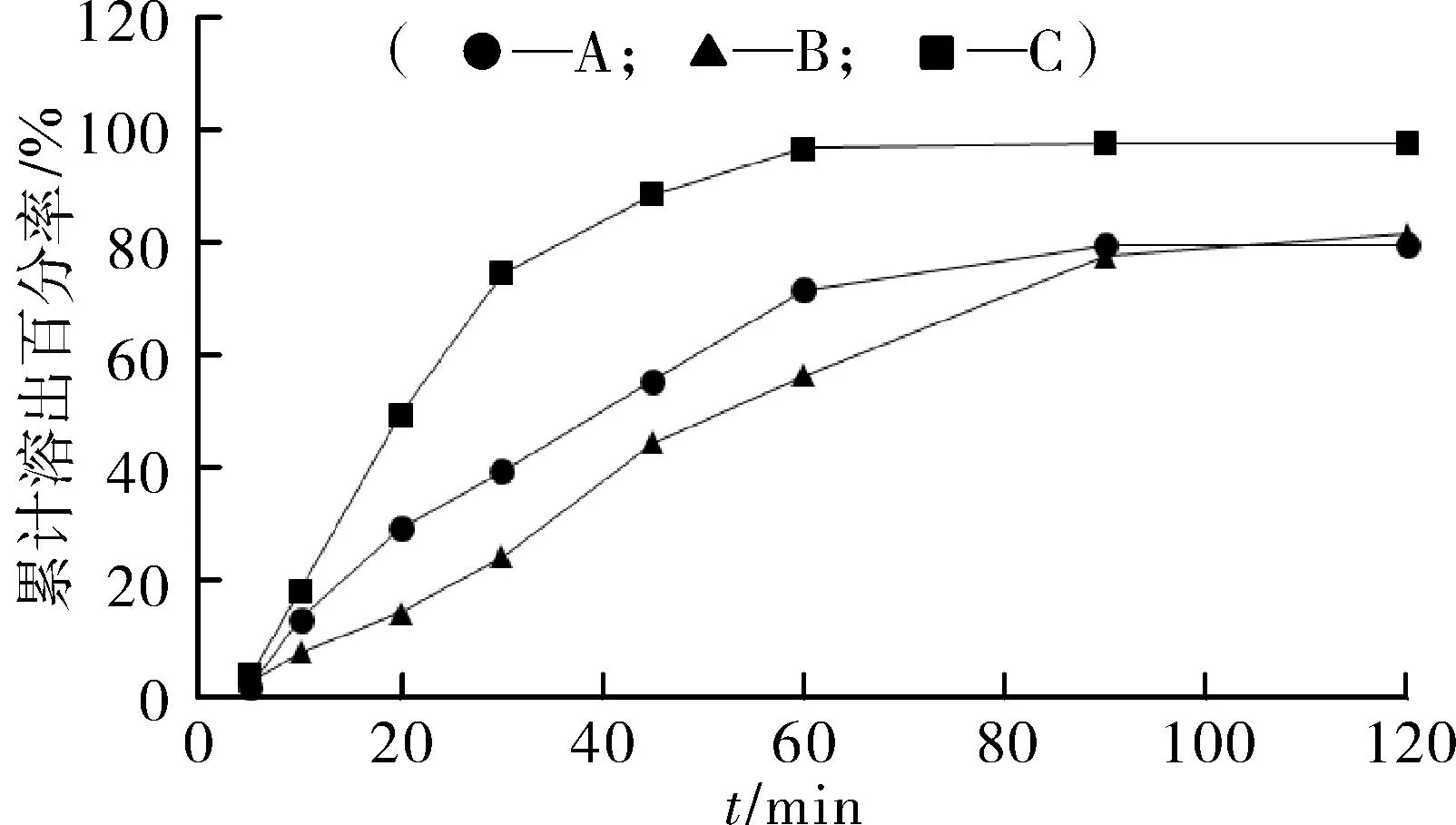
图6白杨素固体制剂在10 g·L-1SLS溶出介质中的溶出曲线
Fig.6 Dissolution profiles of chrysin in 10 g·L-1SLS
3讨论
由图3可知,各制剂在40%乙醇中1 h的累积溶出率均小于70%。由图4可知,在50%乙醇中A溶出速率较快,1 h累积溶出率接近90%。45 min内,A在40%乙醇和50%乙醇中溶出速度较胶囊剂快,由于胶囊壳明胶在乙醇中脱水硬化,溶解减慢,囊壳溶解后则溶出速率显著加快,类似突释。因此,乙醇溶液作为溶出介质不合适。另外选用5 g·L-1SLS溶液作为溶出介质累1 h累积溶出率仍小于70%,在10 g·L-1SLS中,微粉化胶囊溶出速率明显快于其他制剂,不同制剂之间产生显著差异,微粉化制剂达到2010版《中国药典》对溶出度标准的一般要求(70%),所以白杨素胶囊的溶出度标准可暂定为:温度37 ℃,转速100 r·min-1,溶出介质为900 mL10 g·L-1的SLS溶液,在此条件下,每粒的溶出量应符合规定。
室温时,白杨素在SLS溶液中经37 ℃恒温2 h,溶液澄清,谱峰面积相对稳定,SLS溶液可作为溶出介质,不干扰溶出度实验中主药的含量测定。对比图6中溶出曲线可知,微粉化后的白杨素胶囊剂溶出度比其他两个制剂明显提高。新的微粉化工艺操作简便且效率高,更适合工业生产。
参考文献:
[1]肖锦仁,吴红娟,郭昱,等. 不同剂型银翘散抗菌、抗病毒作用的研究[J].湖南中医学院学报,2003, 23(1): 15-18.
[2]施洁明,何仲贵,孙淑英. 非诺贝特体外溶出度考察及其微粉化制剂的研究[J]. 沈阳药科大学学报,2003,20(5): 317-320, 324.
[3]靳世英. 难溶性中药有效成分(黄芩苷)纳米混悬剂固体化及其体内外评价研究[D]. 成都:成都中医药大学,2013.
[4]王伟,董国力,孟玲宇. 药物剂型与临床药效分析[J]. 中国现代药物应用, 2009,3(17): 111.
[5]李涛,盛喜霞,刘继平. 中药有效组分抗炎机制及临床应用研究进展[J]. 西北药学杂志,2013,28(3): 330-332.
[6]谷艳. 冠心Ⅱ号不同配伍方及不同剂型对丹参素、阿魏酸药代动力学的影响[D]. 郑州:郑州大学,2010.
[7]丁华兰. NO供体型白杨素衍生物的合成及抗糖尿病并发症作用研究[D]. 湘潭:湘潭大学,2009.
[8]张祥芳. 黄酮磺酰胺衍生物的合成与生物活性评价[D]. 大连:大连理工大学,2013.
[9]李培培. 基于1,3-偶极环加成对白杨素磷酸酯类化合物的设计及合成研究[D]. 郑州:郑州大学,2014.
[10]史娟. 白杨素-6-磺酸根与金属离子自组装作用及晶体结构研究[D]. 西安:陕西师范大学,2006.
[11]李文锋. 白杨素含磷衍生物的合成及与溶菌酶弱相互作用研究[D]. 郑州:郑州大学,2007.
[12]王馨. 蜂胶黄酮对小鼠N2a细胞缺氧缺糖所致损伤的保护作用及机理研究[D]. 北京:中国农业科学院,2014.
[13]杜晓燕,张琰,韩艳,等. HPLC法测定中药木蝴蝶中黄芩苷和白杨素[J]. 西北药学杂志,2013,28(6): 578-579.
·药剂·
Evaluation of chrysin dissolution from different solid preparations
LI Xin1,ZHENG Shaohua1,ZHANG Peipei2,SU Jin1*(1.The First Affiliated Hospital, Health Science Canter,Xi′an Jiaotong University, Xi′an 710061, China; 2.Health Science Center,Xi′an Jiaotong University, Xi′an 710061, China)
Abstract:ObjectiveTo investigate different chrysin solid preparation dissolution in vitro and to establish an HPLC method for the determination of dissolution. MethodThe dissolution of three chrysin solid preparations were evaluated in 40% and 50% ethanol,5 g·L-1sodium dodecyl sulfate solution, and 10 g·L-1sodium dodecyl sulfate solution, respectively.The HPLC method for determination of the chrysin dissolution was carried out on a C18column using methanol-phosphoric acid-water (65∶35) as a mobile phase. The detection wavelength was at 256 nm, the flow rate was 1.0 mL·min-1, and the temperature of column was 30 ℃. Results10 g·L-1sodium dodecyl sulfate solution as a dissolution medium is suitable for evaluating the three chrysin solid preparations in this study. In addition, the dissolution quality standards of chrysin solid preparation were discussed. ConclusionThe dissolution of three chrysin solid preparations showed significant difference and the dissolution of micronized chrysin solid preparations was significantly improved.
Key words:chrysin; solid preparation; dissolution
收稿日期:(2015-03-01)
通信作者:*苏进,男,主治医师
作者简介:李欣,女,主治医师
基金项目:陕西省自然科学 (编号:2012JQ4025)
中图分类号:R944
文献标志码:A
文章编号:1004-2407(2016)01-0076-04
doi:10.3969/j.issn.1004-2407.2016.01.023
