新型氧钒(IV)席夫碱配合物[VO(dtbsal-met)(phen)和VO(naph-met)(phen)]的合成及其抗肿瘤活性*
2016-01-17曹亚萍易岑兰刘洪梅李海霞左建丽袁泽利遵义医学院药学院贵州遵义563003
曹亚萍,易岑兰,刘洪梅,李海霞,左建丽,袁泽利(遵义医学院药学院,贵州遵义 563003)
新型氧钒(IV)席夫碱配合物[VO(dtbsal-met)(phen)和VO(naph-met)(phen)]的合成及其抗肿瘤活性*
曹亚萍,易岑兰,刘洪梅,李海霞,左建丽,袁泽利
(遵义医学院药学院,贵州遵义563003)
摘要:以L-蛋氨酸(met),1,10-邻菲啰啉(phen)和3,5-二叔丁基水杨醛(dbsal)[或2-羟基-1-萘醛(naph)]为原料,经胺醛缩合反应合成了两个新型的氧钒(IV)席夫碱配合物[VO(dtbsal-met)(phen)(1)和VO(naph-met)(phen)(2)],其结构经IR,HR-ESI-MS,摩尔电导和X-射线单晶衍射表征。1(CCDC:1 429 158)和2(CCDC:1 429 159)分别属单斜晶系和三斜晶系。用MTT法研究了1和2对人肺腺癌细胞(A549)和人源肝癌细胞(HepG2)的体外抗肿瘤活性。结果表明:1和2对A549和HepG2均表现出一定的抑制活性。
关键词:蛋氨酸; 1,10-邻菲啰啉;席夫碱;氧钒(IV)配合物;合成;晶体结构;抗肿瘤活性
(2014GZ 71255);贵州省大学生创新项目(201510661007);遵义医学院大学生创新项目{[2014]5809}
通信联系人:袁泽利,博士,教授,硕士生导师,Tel.0851-8608577,E-mail:zlyuan2002@126.com
氨基酸席夫碱含手性碳原子,其与过渡金属形成的配合物表现出良好的抗菌、抗肿瘤、抗结核等生物活性[1]。对新型氨基酸席夫碱化合物的设计合成、结构及药理活性筛选已成为医药学的重要研究方向之一[2]。
自顺铂被发现具有抗肿瘤活性并成功应用于临床以来,小分子金属配合物作为抗癌药研究成为经久不衰的热门研究课题。虽在后续研究中相继开发了卡铂、奥利沙铂等铂类新抗肿瘤药物,但其在临床使用过程中具有的肾毒性、骨髓毒性、耳毒性、外周神经毒性、催吐性以及长期使用产生的耐药性等问题仍未得到圆满解决[3]。此外,价格昂贵的铂类药物也为患者带来经济负担。这促使研究者们目光转向开发具有高效、经济的非铂类金属抗癌药物探寻。
钒作为人体必需的一种微量元素,具有比较复杂的生物学功能。研究表明:钒配合物具有降糖、消炎、抗菌等潜在的治疗效用[4-5]。与无机钒盐相比,有机钒配合物不仅可提高钒化合物的生物利用度,而且可增强或改进药物分子的活性,同时可能降低钒的毒性[6]。当用VO2+作为钒配合物时,其毒性会显著降低[7]。研究还证实,钒化合物产生的活性氧物种能使部分细胞表现出静止的作用,进而表现出显著的抗肿瘤活性[8]。此外,钒氧无机盐原料易得、价格低廉,对其进行药物开发研究,有望开发出价廉的前药[9-10]
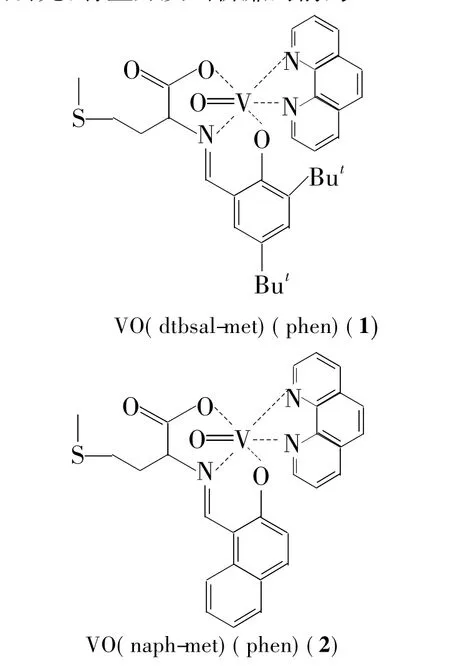
Chart 1
本课题组对席夫碱及其金属配合物开展了一些研究工作[11-13]。在此基础上,本文以L-蛋氨酸(met),1,10-邻菲啰啉(phen)和3,5-二叔丁基水杨醛(dtbsal)[或2-羟基-1-萘醛(naph)]为原料,经胺醛缩合反应合成了两个新型的氧钒(IV)席夫碱配合物[VO(dtbasl-met)(phen)(1,Chart 1)和VO(naph-met)(phen)(2,Chart 1)],其结构经IR,HR-ESI-MS,摩尔电导和X-射线单晶衍射表征。并用MTT法初步研究了1和2对人肺腺癌细胞(A549)和人源肝癌细胞(HepG2)的体外抗肿瘤活性。
1 实验部分
1.1仪器与试剂
Varian 1000 FT-IR型红外光谱仪(KBr压片); Micromass LCT Premier XE型高分辨质谱仪; Bruker APEX2 Smart CCD型X-射线单晶衍射仪; DDS-307精密型电导率仪。
A549和HepG2,遵义医学院医学研究中心;其余所用试剂均为分析纯。
1.2 1和2的合成
在反应瓶中加入met 149 mg(1 mmol),氢氧化钠40 mg(1 mmol)和50%甲醇10 mL,加热搅拌使其完全溶解;加入dtbsal 234 mg(1 mmol)的甲醇(10 mL)溶液,回流(80℃)反应1 h。缓慢滴加硫酸氧钒163 mg(1 mmol)的水(5 mL)溶液,滴毕,回流反应至反应液变土红色为止(约1 h)。缓慢滴加phen 198 mg(1 mmol)的无水甲醇(10 mL)溶液,滴毕,回流反应1 h。冷却至室温,抽滤,滤饼依次用水、甲醇和乙醚(3×15 mL)洗涤,真空干燥,用混合溶剂[V(二氯甲烷)∶V(甲醇)=1∶1]重结晶得褐色块状晶体1 468 mg。
用naph替代dtbsal,用类似的方法合成红色针状晶体2 438 mg。
1:产率76.7%; IR ν:3 552,3 475,3 414,3 232,3 145,2 957,2 871,1 658,1 636,1 616,1 560,1 534,1 423,1 339,1 170,955,852,729,618,545,471 cm-1; HR-ESI-MS m/z:Calcd for C28H23N3O4SVNa{[M +Na]+}633.184 2,found 633.181 8;Λm[V(MeOH)∶V(DMF)=1∶1,c 1.0×105mol·L-1,下同):5.38 Ω–1· mol–1·cm2。
2:产率79.9%; IR ν:3 461,3 440,2 923,2 854,1 651,1 639,1 617,1 553,1 534,1 496,1 425,1 400,1 332,1 232,1 175,1 138,1 090,958,852,726,609,429 cm-1; HR-ESI-MS m/z:Calcd for C32H37N3O4SVNa{[M + Na]+} 571.074 7,found 571.071 7;Λm:8.41 Ω–1·mol–1·cm2。
1.3 晶体结构测定
分别将1和2用混合溶剂[V(甲醇)∶V(二氯甲烷)=1∶1]溶解,置室温下缓慢挥发1 w得适宜测试的单晶1和2。将其置衍射仪上,采用经石墨单色化的Mo Kα射线(λ=0.071 073 nm),以φ-ω扫描方式收集单晶衍射数据。强度数据进行了经验吸收校正、LP校正。晶体结构由直接法解得。对全部非氢原子坐标及其各向异性热参数进行了全矩阵最小二乘法修正。所有计算均用SHELX-97程序完成。
1.4 抗肿瘤活性测定
取对数生长期的肿瘤细胞,用细胞悬浮液[含10%胎牛血清、双抗(青霉素100 ug·mL-1,链霉素100 μg·mL-1)]的DMEM培养基(A549)和RPMI1640培养基(HepG2),调整细胞浓度为5×104个/mL,加于96孔板中,100 μL/孔。于5%CO2,37℃条件下培养24 h;用培养基稀释由DMSO配制的样品母液,再分别加入样品孔中,使样品组最终浓度分别为(5,10,20,40,60,80,100,120)μg·L-1,其它各设置孔补加100 μL培养基,孵育24 h。小心洗去孔内液体,每孔加入MTT溶液(5 mg·mL-1)10 μL及90 μL培养基,于37℃孵育24 h。小心吸去孔内液体,每孔加DMSO 100 μL/孔,于室温振摇5 min。用酶联免疫检测490 nm处的OD值,计算抑制率{1-(OD样品-OD空白)/(OD细胞对照-OD空白)]× 100%};用统计软件SPSS 17.0计算其IC50值。
2 结果与讨论
2.1 物理性能
1和2在DMSO和DMF中均表现出良好的溶解性,在无水甲醇、乙醇中微溶,在二氯甲烷和三氯甲烷等有机溶剂中均表现出良好的溶解性。
1和2的Λm值均很小,说明其在研究的溶液中以非离子的形式存在,即配合物在溶液中不会自发分解14~16]。
2.2 结构表征
在1和2的IR谱图(略)中,1 651 cm-1~1 658 cm-1处吸收峰为席夫碱(C=N)特征振动吸收峰[17-18],表明席夫碱结构的生成;在1 616 cm-1~1 617 cm-1处的吸收峰归属νas(CO-同时,在1 391 cm-1~1 418 cm-1处出现νs(CO2-)吸收峰[22],对称和不对称的羧基振动吸收峰的出现,表明了羧基中仅有单个氧原子与金属离子配位[21];在1 170 cm-1~1 175 cm-1附近出现了酚环的νPh-O特征振动吸收峰[22],进一步说明了酚环存在于目标配合物结构中。另外,在955 cm-1~958cm-1处还观察到νV=O特征振动吸收峰[23-25],说明目标配合物中有过渡金属氧钒的存在。
1和2的高分辨质谱数据与计算值吻合较好,表明其结构与预期结构(Chart 1)的分子组成相吻合。
2.3 晶体结构
1和2的晶体学数据见表1(结构数据存放于英国剑桥数据中心,CCDC号分别1 429 158和1 429 159),晶体结构图见图1,主要键长和键角数据见表2。
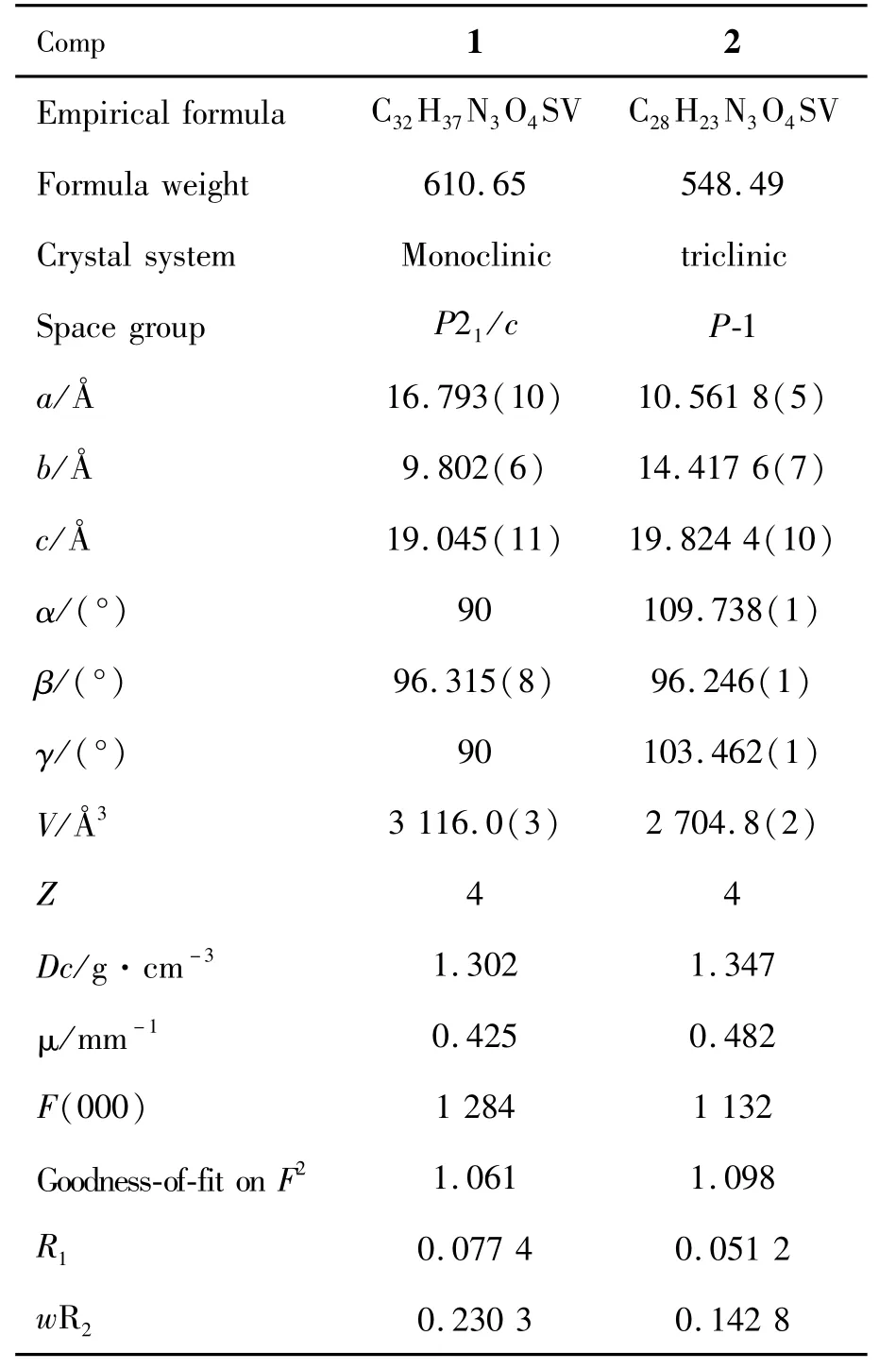
表1 1和2的晶体学参数*Table 1 Crystal data and refinement details of 1 and 2
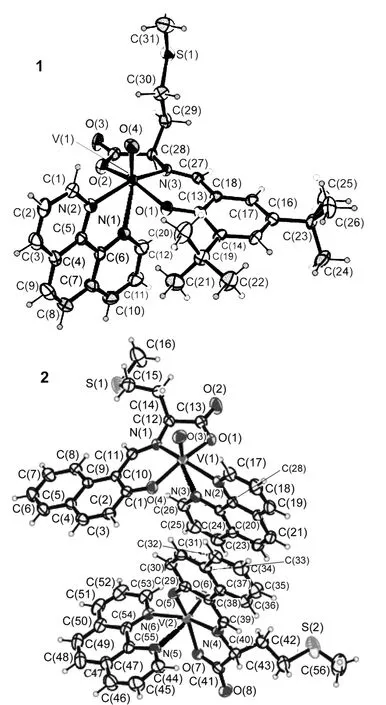
图1 配合物的晶体结构图(椭球几率30%)Figure 1 Crystal structures of complexes
从图1可以看出,1和2的分子结构中均由VO2+,席夫碱配体和phen配体共同组成。1的晶体结构由一个配合物分子组成,而2的晶体结构由两个配合物分子组成。在1和2的分子结构中,配位的中心金属离子钒(IV)以六配位分别与席夫碱配体中的N,O和phen中的两个N以及氧钒中的O进行配位。
从图1还可以看出,1和2分子中的钒(IV)[V(1)]处于变形的八面体配位环境之中,通过席夫碱配体上三齿的酚羟基O,席夫碱亚氨基N,氨基酸羧基O和phen上的N处于该变形八面体的赤道平面上,而phen配体上的N(2)和钒氧中的O(4)或O(3)则在该八面体的轴向位置之上。在2的分子结构中,phen和另一分子的萘环形成两两相互平行的空间结构。
此外,在1的分子结构中,以V(1)为中心,分别形成了V(1)-O(2)-C(29)-C(28)-N(3)的五元环(i)和V(1)-N(2)-C(5)-C(6)-N(1)的五元环(ii)以及V(1)-O(1)-C (27)-C(18)-C(13)-N(3)六元环(iii)。i的扭转角为8.59(18)°,ii和iii的扭转分别为2.22 (16)°和6.89(18)°,说明形成的i的共面性不是很好,但是它们的形成却能增加1的稳定性。i与iii形成的二面角为79.024(172)°, ii与iii形成
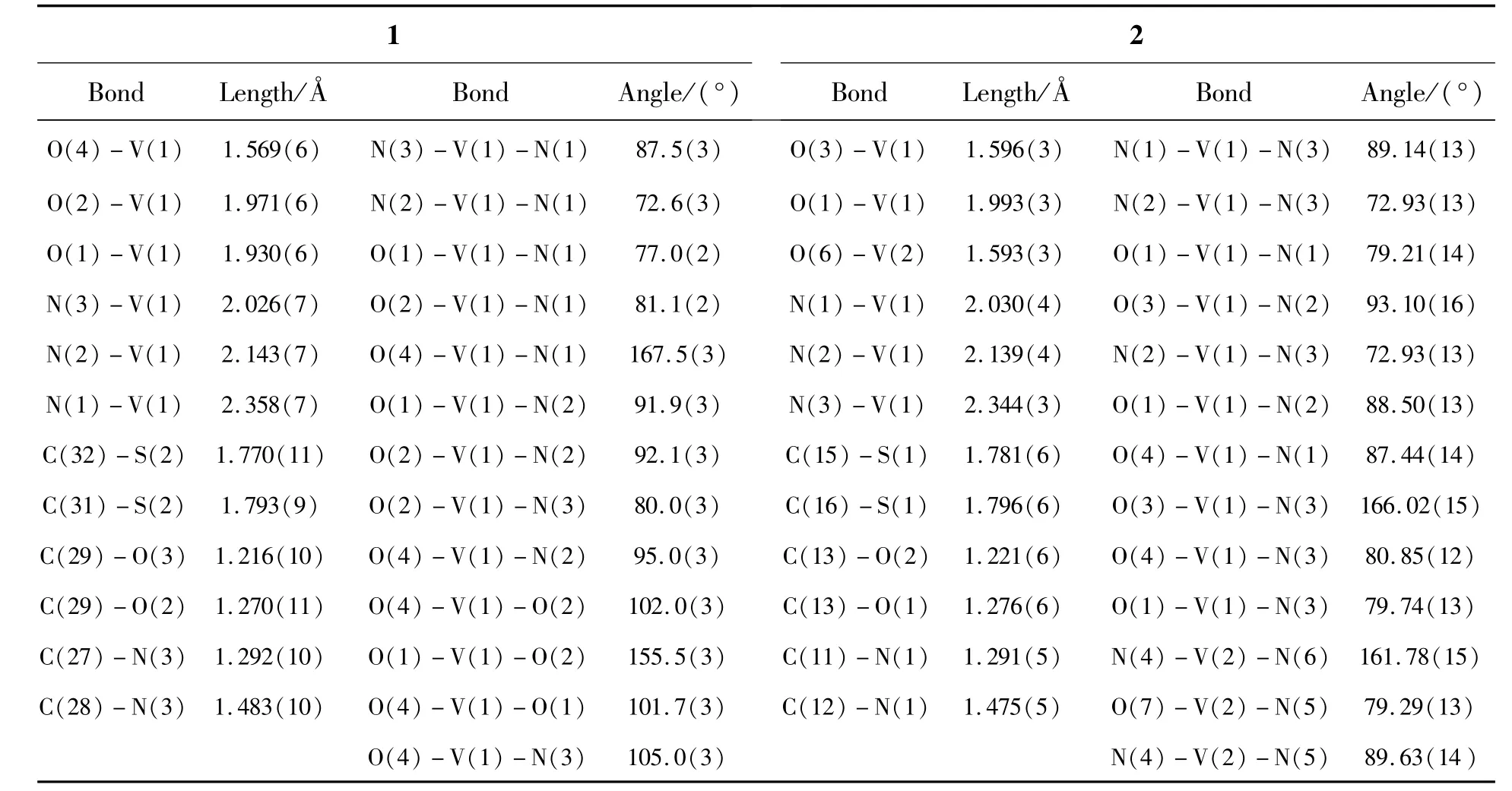
表2 1和2的选择性键长和键角Table 2 Selected bond lengths and bond angles of 1 and 2
的二面角为17.223(168)°;i与ii形成的二面角为83.821(154)°。类似地,而2的分子结构中,也存在着分别以V(1)和V(2)为中心,分别形成有V(1)-O(1)-C(13)-C(12)-N(1)的五元环(i′),V(1)-N(2)-C(28)-C(27)-N(1)的五元环(ii′),V(2)-O(7)-C(41)-C(40)-N(4)的五元环(iii′)和V(2)-N(5)-C(48)-C(49)-N(6)的五元环(iv′),它们的扭转角分别为:16.64(19)°,6.40(17)°,13.49(9)°和1.79(20)°。
其余两个六元环为V(1)-O(4)-C(1)-C (10)-C(13)-N(1)(v′)和V(2)-O(5)-C(29)-C(38)-C(39)-N(4)(vi′),其扭转角分别为:2.61(20)°和5.78(21)°。在2中的i′和ii′,i′和v′以及ii′和v′间的二面角分别为:81.603 (90)°,18.032(81)°和82.759(77)°;而iii′和iv′,iii′和vi′以及iv′和vi′间的二面角分别为:80.075(93)°,17.826(94)°和82.326(84)°。
由表2可知,1和2的钒氧键[V(1)-O(4),V(1)-O(3)和V(2)-O(6)]的键长分别为1.569(6)?,1.596(3)?和1.593(3)?,为典型的钒氧双键(V=O)[26-27],与类似配合物的钒氧键键长几乎相等,其余键长与类似结构相比均在合理范围内[28-30]。
2.4 抗肿瘤活性
1和2对A549的IC50分别为41.995 μM和58.007 μM;1和2对HepG2的IC50分别为38.982 μM和28.621 μM。由此可见,1和2对A549和HepG2具有一定的抑制活性(对照品顺铂对A549和HepG2的IC50分别为2.99 μM和1.66 μM)。
3 结论
设计并合成了两个新型的氨基酸钒氧配合物(1和2),其结构特点为:钒(IV)原子处于变形的八面体配位环境之中,通过席夫碱配体上三齿的酚羟基O,席夫碱亚氨基N,氨基酸羧基O和phen配体上的N形成目标配合物。
体外抗肿瘤活性结果表明:1和2对A549和HepG2均表现出一定的体外肿瘤生长抑制活性。1 和2的合成,为寻低毒、高效的新非铂系小分子金属配合物进行抗肿瘤前体药物筛选提供实验基础。
参考文献
[1] 郭琼,李连之,董建方,等.氧钒配合物[VO(o-Van-Asn)(Phen)]·1.5CH3OH的合成、晶体结构及与DNA和BSA的相互作用[J].化学学报,2012,70:1617-1624.
[2] Dong J F,Jing B,Li L Z.Synthesis and crystal struc-ture of an oxovanadium(IV)complex containing L-phenylalanine Schiff base and 1,10-phenanthroline[J].Advanc Mater Research,2014,(1033):588-591.
[3] 刘杰,计亮年,梅文杰.金属钌配合物的抗肿瘤活性及其作用机理[J].化学进展,2004,16(6):969-974.
[4] 边琳,李连之,王霞,等.混配氧钒配合物[VO (Naph-Phe)(Phen)]的合成、晶体结构及与DNA作用研究[J].无机化学学报,2011,27(4):649-654.
[5] 仇晓阳,刘起峰,张平,等.二齿肼基硫代甲酸苄酯席夫碱锌配合物的合成、晶体结构和抗肿瘤活性[J].无机化学学报,2012,28(2):362-366.
[6] 冯静楠.钒-药物分子模拟物的合成、表征及性质研究[D].北京:首都师范大学,2008.
[7] Ku W J,Suzuki T,Sugiura Y,et al.Effective DNA cleavage by bleomycin-vanadium(IV)complex plus hydrogen-peroxide[J].Biochem Biophys Res Com-mun,1985,129(2):368-374.
[8] Bishayee A,Waghray A,PatelM A,et al.Synthesis and characterization of some oxovanadium complexes [J].Cancer Letters,2010,294(19):1-12.
[9] Ebrahimipour S Y,Sheikhshoaie I,Kautz A C,et al.Mono-and dioxido-vanadium(V)complexes of a tri-dentate ONO Schiff base ligand:Synthesis,spectral characterization,X-ray crystal structure,and anticancer activity[J].Polyhedron,2015,93:99-105.
[10] Habala L,Bartel C,Giester G,et al.Complexes of N-hydroxyethyl-N-benzimidazolyl methyl-ethylenedia-minediacetic acid with group 12 metals and vanadium-synthesis,structure and bioactivity of the vanadium complex[J].J Inorg Biochem,2015,147:147-152.
[11] 袁泽利,杨名惠,吴庆,等.壳聚糖嫁接大环席夫碱的合成[J].合成化学,2012,20(3):375-377.
[12] 袁泽利,吴庆,杨兴变,等.新型水溶性大环席夫碱锰(Ⅱ)配合物的合成及其模拟超氧化物歧化酶的活性研究[J].合成化学,2011,19(4):446-449.
[13] 袁泽利,吴庆,杨兴变,等.新型含均三唑席夫碱型大环化合物的合成及其抗菌活性[J].有机化学,2011,31(10):1698-1702.
[14] Roy M,Saha S,Ashis K P,et al.Ternary iron(III)complex showing photo-cleavage of DNA in the photo-dynamic therapy window[J].Inorg Chem,2007,46:4368-4370.
[15] Saha S,Majumdar R,Rajan R D,et al.Enhanced photodynamic effect of cobalt(III)dipyridophenazine complex on thyrotropin receptor expressing HEK293 cells[J].Metallomics,2010,2:754-765.
[16] Balaji B,Somyajit K,Banik B,et al.Photoactivated DNA cleavage and anti-cancer activity of oxovanadi-um(IV)complexes of curcumin[J].Inorg Chim Ac-ta,2013,400:142-150.
[17] Pijus K S,Ashis K P,Munirathinam N,et al.DNA cleavage by new oxovanadium(IV)complexes of N-salicylidener-amino acids and phenanthroline bases in the photo-dynamic therapy window[J].Inorg Chem,2007,46:1112-1116.
[18] 赵小菁,张丽影,金黎明,等.氨基酸席夫碱的合成及性质研究[J].有机化学,2011,31(9):1561-1521.
[19] Ashis K P,Tuhin B,Suryanarayanarao R,et al.DNA cleavage in red light promoted by copper(II)complexes of α-amino acids and photoactive phenan-throline bases[J].Dalton Trans,2008:6966-6976.
[20] Yue H J,Zhang D,Shi Z,et al.Synthesis and char-acterization of two oxovanadium(IV)Schiff base complexes derived from amino acids and pyridoxal [J].Solid State Sci,2006,8:1368-1372.
[21] 谢海泉,党元林,卓立宏.过渡金属氨基酸席夫碱配合物的合成[J].合成化学,2007,15(3):362-364.
[22] 林秋月,冯旭文,胡瑞定,等.水杨醛缩赖氨酸Schiff碱金属配合物的合成和表征[J].化学研究与应用,2004,16(4):547-548.
[23] Tridib K G,Balabhadrapatruni V S K C,Mithun R,et al.Ferrocene conjugated L-tryptophan copper(II)complexes of phenanthroline bases showing DNA pho- to-cleavage activity and cytotoxicity[J].Inorg Chem,2011,50:8452-8464.
[24] Prasad P,K Sasmal P,Majumdar R,et al.Photocy-totoxicity and near-IR light DNA cleavage activity of oxovanadium(IV)Schiff base complexes having phenanthroline bases[J].Inorg Chim Acta,2010,363:2743-2751.
[25] Banik B,Somyajit K,Koley D,et al.Cellular uptake and remarkable photocyto-toxicity of pyrenylter pyri-dine oxovanadium(IV)complexes of dipyridophena-zine bases[J].Inorg Chim Acta,2012,393:284-293.
[26] 高山,刘世雄.烷氧基键合的VO3+腙配合物的合成和晶体结构及氧化还原性质研究[J].高等学校化学学报,2000,21(5):671-674.
[27] Pijus K S,Sounik S,Ritdnkar M,et al.Photocyto-toxic oxovanadium(IV)complexes showing light-in-duced DNA and protein cleavage activity[J].Inorg Chem,2010,49:849-859.
[28] Pijus K S,Sounik S,Ritankar M,et al.Oxovanadi-um(IV)complexes of phenanthroline bases:The dipyridophenazine complex as a near-IR photocytotox-ic agent[J].Dalton Trans,2010,39:2147-2158.
[29] Pijus K S,Ritankar M,Rajan R D,et al.Photocyto-toxicity and DNA cleavage activity of L-arg and L-lys Schiff base oxovanadium(IV)complexes having phenanthroline bases[J].Dalton Trans,2010,39:7104-7113.
[30] Banerjee S,Prasad P,Hussain A,et al.Remarkable photocytotoxicity of cur-cumin in HeLa cells in visible light and arresting its degradation on oxovanadium (IV)complex formation[J].Chem Commun,2012,48:
Synthesis and Anticancer Activities of Novel Oxovanadium(IV)Complexes[VO(dtbsal-met)(phen)and VO(naph-met)(phen)]
CAO Ya-ping,YI Cen-lan,LIU Hong-mei,LI Hai-xia,ZUO Jian-li,YUAN Ze-li
(School of Pharmacy,Zunyi Medical University,Zunyi 563003,China)
Abstract:Two novel oxovanadium(IV)complexes,VO(dtbsal-met)(phen)(1)and VO(naphmet)(phen)(2),were synthesized by aldimine condensation reaction reaction,using L-methionine(meth),1,10-phenanthroline(phen),3,5-di-tert-butyl salicylaldehyde(dtbsali)[or 2-hydroxy-1-naphthaldehyde(hnaph)]as materials.The structures were characterized by IR,HR-ESI-MS,molar conductance and single-crystal X-ray.1(CCDC:1 429 158)and 2(CCDC:1 429 159)belongs to monoclinic crystal system and triclinic system,respectively.The in vitro anticancer activities of 1 and 2 against A-549 and HeGp2were tested by MTT method.The results showed that 1 and 2 exhibited certain antitumor activities.
Keywords:methionine; 1,10-phenanthroline; Schiff base; oxovanadium(IV)complex; synthesis; crystal structure; anticancer activity
作者简介:曹亚萍(1994-),女,汉族,湖北武汉人,本科生,主要从事配合物的设计合成与活性研究。E-mail:1138892808@ qq.com
基金项目:国家自然科学基金资助项目(81360471);贵州省国际合作项目{[2012]7036} ;贵州省科技创新人才团队项目
收稿日期:2015-10-08
DOI:10.15952/j.cnki.cjsc.1005-1511.2015.12.1124 *
文献标识码:A
中图分类号:O614.51; O641.4
