新型SPECT/MRI双模态显像剂SPION-DMSA-RGD-99Tcm的合成与生物评价
2016-01-11王晓,崔海平,史旭东等
新型SPECT/MRI双模态显像剂SPION-DMSA-RGD-99Tcm的合成与生物评价
王晓1,2,崔海平1,2,史旭东1,2,梁积新1,孙钰林2,申一鸣1,2,沈浪涛1,2,*
(1.中国原子能科学研究院 国家同位素工程技术研究中心,北京102413;
2.原子高科股份有限公司,北京102413)
摘要:为制备纳米材料SPION-DMSA-RGD及其标记物SPION-DMSA-RGD-99Tcm,探讨该标记物作为SPECT/MRI双模态显像剂的可能性,在水溶性纳米颗粒SPION-DMSA上连接c(RGDfC),得到了SPION-DMSA-RGD,并进行了结构表征。用99Tcm对SPION-DMSA-RGD进行标记,并对该标记物进行了正常鼠和荷U87MG人脑神经胶质瘤裸鼠的生物分布研究,及荷U87MG人脑神经胶质瘤裸鼠的MRI和SPECT显像研究。研究结果表明,SPION-DMSA-RGD具有超顺磁性,99Tcm标记率约为98%。正常鼠和荷U87MG人脑神经胶质瘤裸鼠的生物分布结果表明,SPION-DMSA-RGD-99Tcm在血液中清除较快,在肝脏中摄取较高,在肿瘤中有摄取。荷U87MG人脑神经胶质瘤裸鼠的MRI和SPECT显像结果表明,SPION-DMSA-RGD和SPION-DMSA-RGD-99Tcm的肿瘤主动靶向作用明显。以上结果提示,对于荷U87MG人脑神经胶质瘤裸鼠,SPION-DMSA-RGD-99Tcm是一种SPECT/MRI双模态显像剂。
关键词:超顺磁氧化铁纳米颗粒;二巯基丁二酸;c(RGDfC);99Tcm;SPECT/MRI双模态显像剂
中图分类号:O615.4 文献标志码:A
收稿日期:2014-06-23;修回日期:2014-09-23
作者简介:王晓(1986—),女,山西运城人,博士研究生,放射性同位素技术专业
doi:10.7538/yzk.2015.49.11.1932
*通信作者:沈浪涛,E-mail: shenlt@yahoo.com
Synthesis and Biological Evaluation
of SPECT/MRI Dual-modal Imaging Agent SPION-DMSA-RGD-99Tcm
WANG Xiao1,2, CUI Hai-ping1,2, SHI Xu-dong1,2, LIANG Ji-xin1,
SUN Yu-lin2, SHEN Yi-ming1,2, SHEN Lang-tao1,2,*
(1.NationalIsotopeCenterofEngineeringandTechnology,ChinaInstituteofAtomicEnergy,
Beijing102413,China; 2.AtomHi-TechCo.,Ltd.,Beijing102413,China)
Abstract:In order to investigate the possibility of SPION-DMSA-RGD-99Tcm as a SPECT/MRI dual-modal imaging agent, SPION-DMSA-RGD and its radiolabeled SPION-DMSA-RGD-99Tcm were prepared. SPION-DMSA-RGD was prepared based on SPION-DMSA and c(RGDfC). SPION-DMSA-RGD was characterized by means of various methods. SPION-DMSA-RGD-99Tcm was given by labeling with 99Tcm. The biodistribution studies of SPION-DMSA-RGD-99Tcm in normal mice and the nude mice bearing U87MG human glioma were performed. The MRI and SPECT imaging of SPION-DMSA-RGD and SPION-DMSA-RGD-99Tcm in the nude mice bearing U87MG human glioma were carried out, respectively. The results show that SPION-DMSA-RGD exhibits super-magnetic properties. The labeling yield of SPION-DMSA-RGD with 99Tcm is about 98%. SPION-DMSA-RGD-99Tcm displays fast clearance from the blood and high accumulation in the liver. The tumor uptake of SPION-DMSA-RGD-99Tcm is higher than that of SPION-DMSA-99Tcm. The MRI and SPECT images show that the tumor active targeting of SPION-DMSA-RGD and SPION-DMSA-RGD-99Tcm are obvious. Therefore, SPION-DMSA-RGD-99Tcm can be acting as a SPECT/MRI dual-modal imaging agent for nude mice bearing U87MG human glioma.
Key words:super-magnetic iron oxide nanoparticle; DMSA; c(RGDfC);99Tcm; SPECT/MRI dual-modal imaging agent
提高药物的肿瘤靶向性一直是药物学家的努力方向[1]。人们已对多种肿瘤生物标志物进行了研究,其中整合素αVβ3特别引人注目[2-4]。在各种类型的人类肿瘤中,整合素αVβ3在约25%的肿瘤细胞中过度表达,包括胶质母细胞瘤、黑色素瘤、前列腺癌、乳腺癌、卵巢癌等[5-7]。整合素αVβ3在调节肿瘤生长、转移和血管生成中均发挥着重要作用。RGD序列多肽(即精氨酸-甘氨酸-天门冬氨酸三肽)能与整合素αVβ3特异性地结合[8],且环状RGD较线性RGD具有更高的肿瘤亲和力和特异性摄取(环状RGD的IC50为19.6 nmol/L)[9-11]。
与小分子药物相比,磁性纳米粒子可显著延长药物在循环系统中的滞留时间,通过被动靶向等作用在肿瘤中浓集。磁性纳米粒子已被用作药物载体、磁共振成像(MRI)造影剂等[12]。以磁性氧化铁纳米粒子为核心、合适材料的表面包覆层和肿瘤特异性靶向分子构成的多模态影像剂的研究是当前医学影像剂的研究前沿。单光子发射计算机断层成像(SPECT)和磁共振成像(MRI)在临床医学中应用广泛,而融合了SPECT和MRI各自优点的双模态影像技术 SPECT/MRI有望进一步提高对肿瘤和其他疾病检测的灵敏度[13],具有广阔的发展前景。SPECT/MRI双模态影像剂的研发将促进SPECT/MRI双模态影像技术的发展[14]。
最近的研究[15]表明,99Tcm标记的水溶性氧化铁纳米粒子SPION-DMSA在肿瘤部位没有较高的浓集,不是U87MG肿瘤理想的SPECT/MRI双模态显像剂。为改善SPION-DMSA在肿瘤中的靶向作用,本研究将主动靶向分子cyclo-(RGDfC)(c(RGDfC))多肽与SPION-DMSA偶联获得SPION-DMSA-RGD,并经放射性核素标记得到SPION-DMSA-RGD-99Tcm,评价该标记物在正常小鼠和荷U87MG人脑神经胶质瘤裸鼠体内的生物分布,最终分别进行荷瘤裸鼠的SPECT和MRI显像,以探讨SPION-DMSA-RGD-99Tcm作为荷U87MG人脑神经胶质瘤裸鼠SPECT/MRI双模态显像剂的可能性。
1实验材料
1.1仪器及试剂
FD-80型真空冷冻干燥机,北京博医康实验仪器有限公司;高纯水器,美国Millipore公司;IRAffinity-1傅里叶变换红外光谱仪,日本Shimadazu公司;JEM2100F透射电镜,日本电子株式会社;Nano ZS动态光散射纳米粒度分析仪(DLS),英国Malvern公司;BKT-4500Z振动样品磁强计,美国Quantum Design公司;1470自动伽玛计数器,芬兰Perkin Elmer公司;CRC-15 R放射性活度计,美国Capintec公司;AR-2000薄层扫描仪,德国Eckert Ziegler公司;NanoScan SPECT/CT,匈牙利MEDISO公司;7.0T小动物磁共振成像仪,美国Varian公司。
c(RGDfC),纯度95%,北京中科亚光生物科技有限公司;N-(氨基乙基)-马来酰亚胺三氟乙酸盐(NH2-CH2CH2-MAL·CF3COOH),纯度98%,百灵威公司;1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐(EDCI),纯度98%,TCI公司;Na99TcmO4淋洗液,原子高科股份有限公司;SPION-DMSA,自制[15]。其他化学试剂均为分析纯,国药集团化学试剂有限公司。
1.2实验动物
昆明小白鼠:雌性,重约18~20 g,一级,由中国医学科学院肿瘤研究所提供。荷U87MG人脑神经胶质瘤裸鼠,SPF级,由中国医学科学院肿瘤研究所提供。取4~5周龄Balb/c雌性裸鼠,右前肢腋下接种5×106个U87MG人脑神经胶质瘤细胞,在无菌环境下饲养,待肿瘤平均直径达到8~10 mm时用于实验。
2实验方法
2.1SPION-DMSA-RGD的合成与表征
图1为SPION-DMSA[15]、c(RGDfC)的结构示意图。

图1 SPION-DMSA(a)和c(RGDfC)(b)的结构示意图 Fig.1 Structures of SPION-DMSA (a) and c(RGDfC) (b)
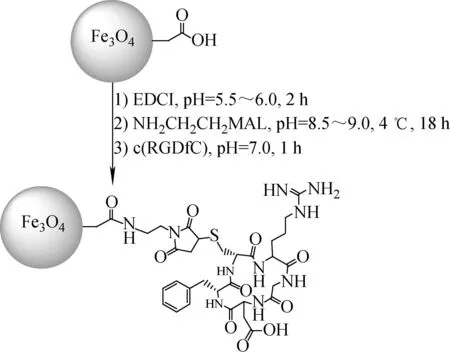
图2 SPION-DMSA-RGD合成示意图 Fig.2 Synthetic route of SPION-DMSA-RGD
SPION-DMSA-RGD是在SPION-DMSA的基础上引入RGD多肽分子。图2为SPION-DMSA-RGD的合成示意图。移取1 mL SPION-DMSA,加入20 μmol EDCI,用0.1 mol/L HCl和NaOH将其pH值调至5.5~6.0,常温下反应2 h,之后加入18 μmol NH2CH2CH2MAL·CF3COOH,再用0.1 mol/L HCl和NaOH将其pH值调至8.5~9.0,4 ℃下反应18 h。将反应液pH值调至7.0左右,再加入15 μmol c(RGDfC),常温下反应1 h。反应产物用3 500 Da的透析袋在蒸馏水中透析48 h,然后过0.22 μm膜,过膜后得到的液体于真空冷冻干燥机中冻干,即得SPION-DMSA-RGD粉末。
傅里叶变换红外光谱(FT-IR)的测定:取适量冻干后的SPION-DMSA-RGD粉末与KBr混合、研磨后压片,在IRAffinity-1傅里叶变换红外光谱仪的样品舱中进行测定。
纳米粒子在溶液中的粒径测定:采用动态光散射(DLS)法,将1%(w/V)的SPION-DMSA-RGD水溶液倒入石英比色皿中,在Nano ZS纳米粒度分析仪的样品室中用633 nm的He/Ne激光进行扫描测定。
样品的磁性分析:将固体样品装入约7 mm的棉签管中,两端封口后于BKT-4500Z振动样品磁强计的样品舱中进行测试。
2.299Tcm的标记与质控分析
称取2.4 mg SnCl2·2H2O,加入1 mL 0.1 mol/L的HCl,溶解后取0.05 mL加入小青霉素瓶中,加入1 mL含10 mg NaHCO3的Na99TcmO4洗脱液(活度为1.85×107~7.4×108Bq,pH=8~9),放置10 min后再加入1 mL SPION-DMSA-RGD (含Fe约0.57 mg/mL)水溶液,于室温下反应20 min,整个反应过程中均通氮气保护。
采用快速薄层色谱(ITLC)法测定SPION-DMSA-RGD-99Tcm的标记率,以Whatman 1色层纸为支持体,丙酮为展开剂,展开距离为10 cm,用Bioscan放射性扫描仪测定其放射性分布。
2.3生物分布与显像
取健康雌性昆明小白鼠16只,随机分成4组,每组4只,每只小鼠均经尾静脉注射0.1 mL(约0.74 MBq)标记物,于注射后0.5、1、2、4 h分别摘除眼球取血,继而断颈处死,取心、肝、脾、肺、肾、胃、肠、肉、骨、脑等脏器称重,并用γ计数器测量放射性计数,经衰变校正后,计算百分注射剂量率(%ID/g)。
取荷U87MG人脑神经胶质瘤裸鼠9只,随机分成3组,每组3只,经尾静脉注射0.1 mL(约0.74 MBq)标记物,于注射后0.5、2、4 h分别摘眼球取血,继而断颈处死,取心、肝、脾、肺、肾、胃、肠、肉、骨、脑、瘤等称重,并用γ计数器测定放射性计数,经衰变校正后,计算百分注射剂量率(%ID/g)及肿瘤与正常组织的摄取率之比(T/NT)。
取荷U87MG人脑神经胶质瘤裸鼠4只,随机分成2组,每组2只,一组经尾静脉注射0.1 mL(约37.0 MBq)标记物,于给药后0.5 h和4 h进行SPECT显像,显像条件为:矩阵尺度256×256,中心能窗140.5 keV。另一组经尾静脉注射0.1 mL SPION-DMSA-RGD,于注射后0.5 h和4 h进行MRI显像,显像条件为:视窗,100 mm×100 mm,矩阵尺度,256×256,层厚,1.5 mm,重复时间3 000 ms,回波时间120 ms。
3结果与讨论
3.1SPION-DMSA-RGD的合成与表征
纳米粒子SPION-DMSA(图1)合成方法参见文献[15],其表面游离的羧基可与氨基发生反应从而引入氨基-乙基-马来酰亚胺,c(RGDfC)中的—SH再与马来酰亚胺基团发生加成反应从而实现多肽与纳米粒子的偶联。

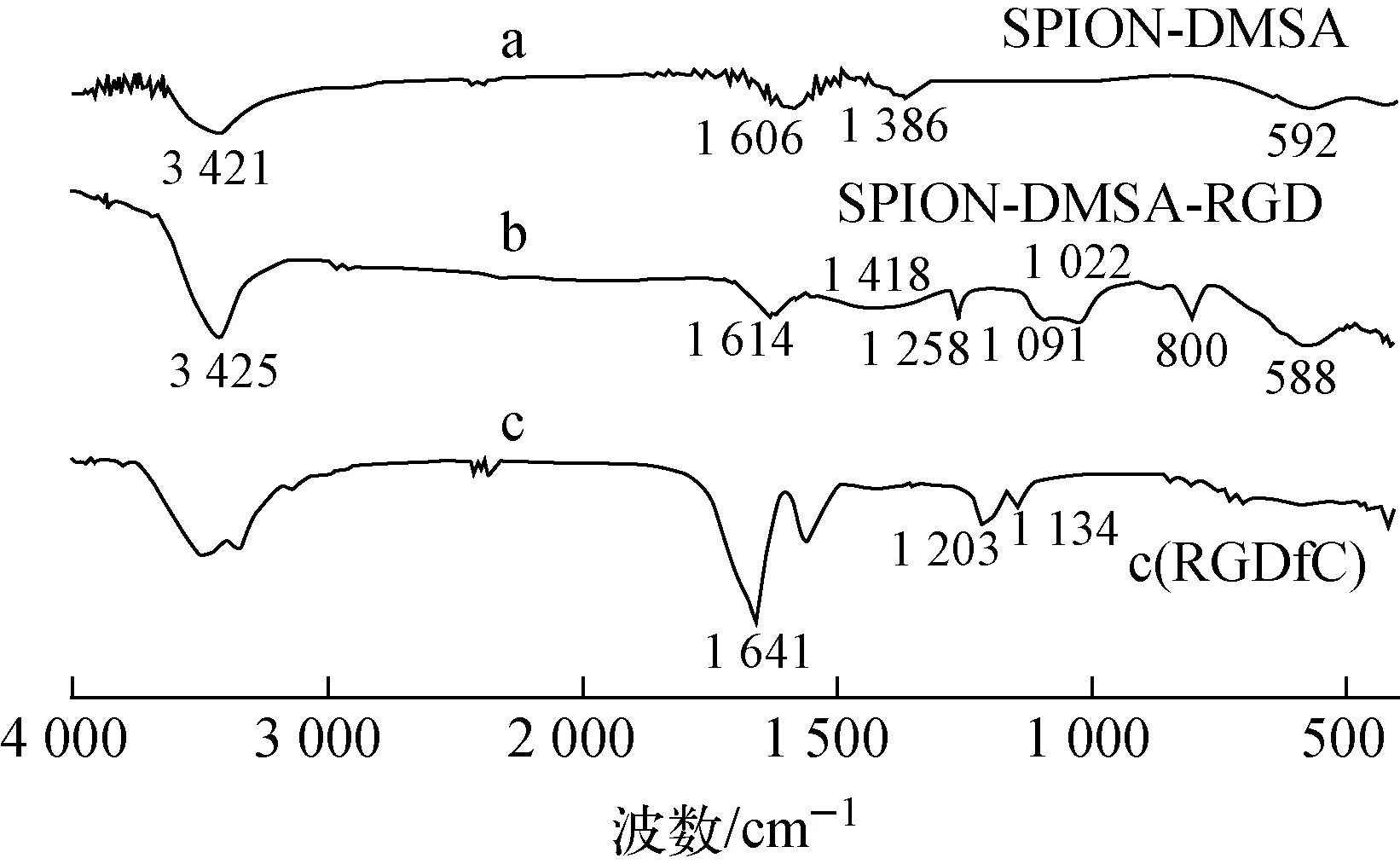
图3 SPION-DMSA、SPION-DMSA-RGD 和c(RGDfC)的红外光谱 Fig.3 FT-IR spectra of SPION-DMSA, SPION-DMSA-RGD and c(RGDfC)

图4 SPION-DMSA和SPION-DMSA-RGD的 水合动力学直径分布 Fig.4 Hydrodynamic diameter distribution of SPION-DMSA and SPION-DMSA-RGD
SPION-DMSA和SPION-DMSA-RGD的DLS分析结果如图4所示。强度权重的DLS显示均为单峰,即两种纳米粒子的粒径分别集中在约80 nm和106 nm处。连接了RGD的SPION-DMSA-RGD的粒径较SPION-DMSA的粒径略有增大。
SPION-DMSA和SPION-DMSA-RGD的磁性分析结果如图5所示。图5的磁滞回线表明,随着外加磁场强度的增大,纳米粒子的磁化强度增大,当外加磁场强度增大到一定值(10 000 Oe)时,磁化强度增速趋缓,逐渐达到磁饱和。SPION-DMSA和SPION-DMSA-RGD的比饱和磁化强度分别为26.0和19.4 emu/g。由于RGD的偶联使SPION-DMSA-RGD的比饱和磁化强度较SPION-DMSA有所减小,但剩磁和矫顽力几乎可忽略不计,因此,所制得的SPION-DMSA-RGD仍具有良好的超顺磁性。该结果表明,SPION-DMSA-RGD可作为下一步构筑SPECT/MRI双模态影像剂的良好平台。

图5 SPION-DMSA和 SPION-DMSA-RGD的磁滞回线 Fig.5 Hysteresis loops of SPION-DMSA and SPION-DMSA-RGD
3.299Tcm的标记率

3.3生物分布与显像
SPION-DMSA-RGD-99Tcm注入小鼠体内后,主要在肝脏聚集,其次在脾和肾,且给药0.5 h后,标记物在肝、脾和肾的摄取都逐渐减少。本研究组最近的研究[15]结果表明,SPION-DMSA-99Tcm在正常小鼠体内的生物分布主要集中在肝、脾和肾,且随给药时间的延长,摄取量相应减少。该结果与Fatahian等[17]报道的Fe3O4@DMSA-99Tcm结果一致。本研究揭示,SPION-DMSA-RGD-99Tcm在正常小鼠体内的生物分布与未偶联靶向分子c(RGDfC)的纳米粒子生物分布[15]基本相同,也主要在肝、脾和肾中聚集。SPION-DMSA-RGD-99Tcm在肝和脾的高摄取主要与星状巨噬细胞的吞噬作用有关。
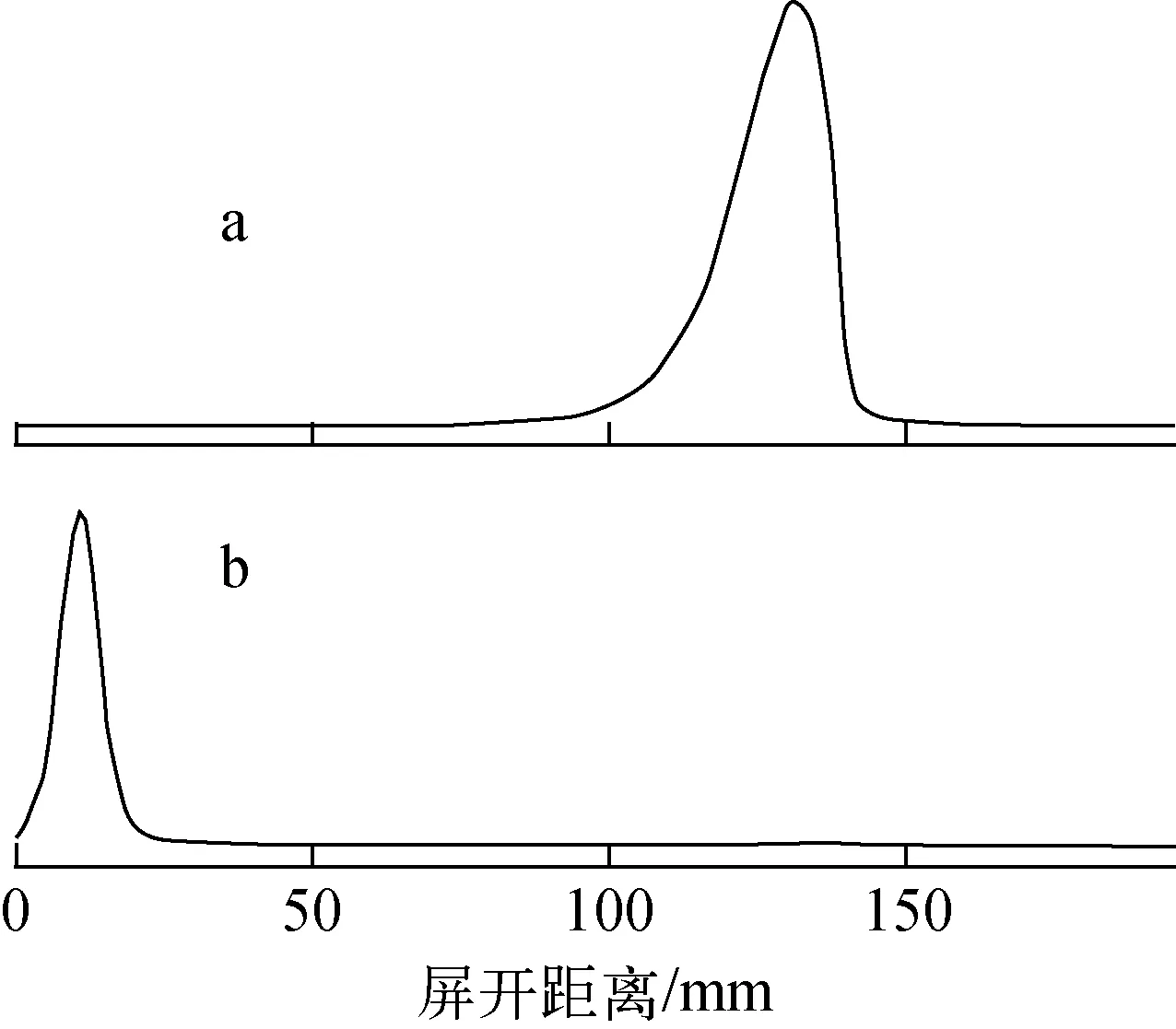
图6 99Tc mO - 4(a)和 SPION-DMSA-RGD- 99Tc m(b)的ITLC谱 Fig.6 ITLC chromatograph of 99Tc mO - 4(a) and SPION-DMSA-RGD- 99Tc m(b)
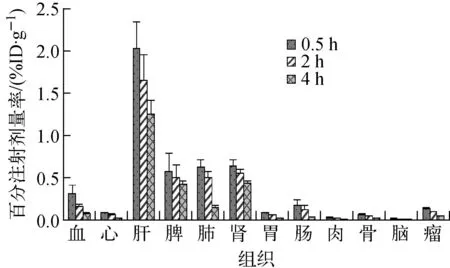
图7 SPION-DMSA-RGD- 99Tc m 在荷U87MG人脑神经胶质瘤裸鼠体内的生物分布 Fig.7 Biodistribution of SPION-DMSA-RGD- 99Tc m in nude mice bearing U87MG human glioma
SPION-DMSA-RGD-99Tcm在荷U87MG人脑神经胶质瘤裸鼠体内的生物分布结果如图7所示。由图7可知,给药0.5 h后,SPION-DMSA-RGD-99Tcm在荷瘤鼠体内主要聚集于肝脏((2.03±0.31) %ID/g),其次为肾((0.65±0.06) %ID/g)和肺((0.63±0.09) %ID/g);给药2 h后,主要聚集器官为肝((1.66±0.30) %ID/g)、肾((0.56±0.05) %ID/g)和脾((0.50±0.16) %ID/g));给药4 h后,主要聚集器官仍为肝((1.25±0.16) %ID/g)、肾((0.44±0.03) %ID/g)和脾((0.43±0.04) %ID/g)。SPION-DMSA-RGD-99Tcm在肿瘤中的摄取较肌肉中的高,在肝、肾中有较长的滞留时间,而脑部放射性摄取很低。SPION-DMSA-RGD-99Tcm在血液中清除较快,在肝脏中摄取率较高,表明其在体内主要经肝脏代谢。
SPION-DMSA-RGD-99Tcm在肿瘤中的摄取与未连接c(RGDfC)的SPION-DMSA-99Tcm[15]相比,有明显提高,给药0.5 h分别为(0.15±0.008) %ID/g和(0.04±0.006) %ID/g,给药2 h分别为(0.10±0.009) %ID/g和(0.03±0.001) %ID/g,给药4 h分别为(0.05±0.001) %ID/g和(0.03±0.002) %ID/g。这表明连接上c(RGDfC)后,纳米粒子对肿瘤具有明显的靶向作用。
在3个时间点中,肿瘤与脑的T/NT在给药2 h后达到最高,为8.38,而肿瘤与肌肉的T/NT此时最低,为3.78;给药4 h后,肿瘤与肌肉的T/NT升高为4.45,而肿瘤与脑的T/NT降低至7.48,但仍大于7,这表明由于纳米的特性,SPION-DMSA-RGD-99Tcm在肿瘤组织中具有较长的滞留时间,靶与非靶组织的反差较大,有望在较宽的时间范围内作为肿瘤靶向显像剂。
荷U87MG人脑神经胶质瘤裸鼠静脉注射SPION-DMSA-RGD-99Tcm后,0.5 h和4 h的显像结果如图8所示,图中箭头所指部位为肿瘤。从图8中SPECT图像可见,静脉注射0.5 h后,肿瘤部位已有明显摄取,4 h后肿瘤部位摄取范围有所增加。这说明在SPECT模态下,SPION-DMSA-RGD-99Tcm可用作U87MG肿瘤的SPECT显像剂。
超顺磁性氧化铁纳米粒子在MRI成像中为T2显像剂。从图8可见,与未注射SPION-DMSA-RGD的荷瘤裸鼠相比,注射SPION-DMSA-RGD 0.5 h后,肿瘤部位变暗,4 h后肿瘤部位变暗更明显,表明肿瘤部位有摄取。这说明在MRI模态下,SPION-DMSA-RGD可作为U87MG肿瘤的T2MRI显像剂。
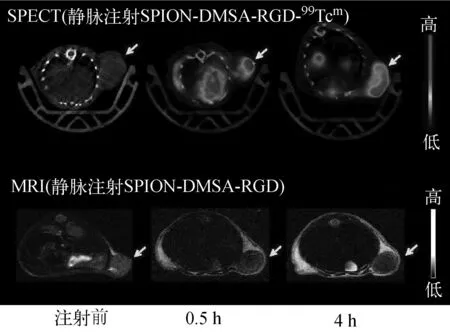
图8 静脉注射SPION-DMSA-RGD- 99Tc m 和SPION-DMSA-RGD前后荷U87MG 人脑神经胶质瘤裸鼠的SPECT和MRI图像 Fig.8 SPECT and MRI images of SPION-DMSA-RGD- 99Tc m and SPION-DMSA-RGD in nude mice bearing U87MG human glioma before and after intravenous injection
对照未连接c(RGDfC)的SPION-DMSA情形[15],注射SPION-DMSA-RGD-99Tcm后,无论在SPECT模态还是在MRI模态下,均表现出了明显的靶向作用,即显像剂在U87MG肿瘤部位均有较高的聚集。这种肿瘤靶向作用可能与RGD多肽的主动靶向有关,因为在U87MG肿瘤细胞中有过度表达能与RGD多肽特异结合的整合素αVβ3[18]。
综合图8中SPECT和MRI的显像研究结果,显而易见,SPION-DMSA-RGD-99Tcm在肿瘤中有明显的浓集,可作为一种新型的U87MG肿瘤SPECT/MRI双模态显像剂进行进一步研究。
4结论
1) 成功制备了SPION-DMSA-RGD及其标记物SPION-DMSA-RGD-99Tcm。
2) SPION-DMSA-RGD-99Tcm在血液中清除较快,在肝脏中摄取率较高,表明其主要经肝脏代谢。
3) SPION-DMSA-RGD-99Tcm与SPION-DMSA-99Tcm相比,对U87MG人脑神经胶质瘤有明显的主动靶向作用。
4) SPECT和MRI图像显示,SPION-DMSA-RGD-99Tcm是具有U87MG肿瘤靶向作用的新型SPECT/MRI双模态显像剂。SPION-DMSA-RGD-99Tcm作为一种新型的SPECT/MRI双模态显像剂,其自身性能的持续改善及对其他肿瘤的适用性还有待进一步研究。
参考文献:
[1]LAMMERS T, KIESSLING F, HENNINK W E, et al. Drug targeting to tumors: Principles, pitfalls and (pre-) clinical progress[J]. Journal of Controlled Release, 2012, 161(2): 175-187.
[2]DESGROSELLIER J S, CHERESH D A. Integrins in cancer: Biological implications and therapeutic opportunities[J]. Nature Reviews Cancer, 2010, 10(1): 9-22.
[3]BEERA J, SCHWAIGER M. Imaging of integrin alphavbeta3 expression[J]. Cancer Metastasis Reviews, 2008, 27(4): 631-644.
[4]SCHOTTELIUS M, LAUFER B, KESSLER H, et al. Ligands for mapping alphavbeta3-integrin expression in vivo[J]. Accounts for Chemical Research, 2009, 42(7): 969-980.
[5]CAI W, CHEN X. Anti-angiogenic cancer therapy based on integrin αvβ3 antagonism[J]. Anti-cancer Agents in Medicinal Chemistry, 2006, 6(5): 407-428.
[6]MIZEJEWSKI G J. Role of integrins in cancer: Survey of expression patterns[J]. Proceeding of the Society for Experimental Biology and Medicine, 1999, 222(2): 124-138.
[7]JIN H, VARNER J. Integrins: Roles in cancer development and as treatment targets[J]. British Journal of Cancer, 2004, 90(3): 561-565.
[8]DOBRUCKI L W, de MUINCK E D, LINDNER J R, et al. Approaches to multimodality imaging of angiogenesis[J]. Journal of Nuclear Medicine, 2010, 51(5): 66S-79S.
[9]GURRATH M, MULLER G, KESSLER H, et al. Conformation/activity studies of rationally designed potent anti-adhesive RGD peptides[J]. European Journal of Biochemistry, 1992, 210(3): 911-921.
[10]DECHANTSREITER M A, PLANKER E, MATHA B, et al. N-methylated cyclic RGD peptides as highly active and selective αvβ3 integrin antagonists[J]. Journal of Medicinal Chemistry, 1999, 42(16): 3 033-3 040.
[11]DIJKFRAAF I, KRUIJTZER J A W, LIU S, et al. Improved targeting of the αvβ3 integrin by multimerisation of RGD peptides[J]. European Journal of Nuclear Medicine and Molecular Imaging, 2007, 34(2): 267-273.
[12]VEISEH O, GUNN J W, ZHANG M Q. Design and fabrication of magnetic nanoparticles for targeted drug delivery and imaging[J]. Advanced Drug Delivery Reviews, 2010, 62(3): 284-304.
[13]HAMAMURA M J, HA S, ROECK W W, et al. Development of an MR-compatible SPECT system (MRSPECT) for simultaneous data acquisition[J]. Physics in Medicine and Biology, 2010, 55(6): 1 563-1 575.
[14]MISRI R, MEIER D, YUNG A C, et al. Development and evaluation of a dual-modality (MRI/SPECT) molecular imaging bioprobe[J]. Nanomedicine: Nanotechnology, Biology and Medicine, 2012, 8(6): 1 007-1 016.
[15]王晓,崔海平,史旭东,等. SPECT/MRI双模态显像剂SPION-DMSA-99Tcm的制备及其性质研究[J]. 原子能科学技术,2015,49(9):1 557-1 564.
WANG Xiao, CUI Haiping, SHI Xudong, et al. Preparation and evaluation of SPION-DMSA-99Tcmas SPECT/MRI dual-modal imaging agent[J]. Atomic Energy Science and Technology, 2015, 49(9): 1 557-1 564(in Chinese).
[16]SILVERSTEIN R M, WEBSTER F X, KIEMLE D J. Spectrometric identification of organic compounds[M]. 6th Edition. US: John Wiley & Sons, 2005.
[17]FATAHIAN S, SHAHBAZI-GAHROUEI D, POULADIAN M, et al. Biodistribution and toxicity assessment of radiolabeled and DMSA coated ferrite nanoparticles in mice[J]. Journal of Radioanalytical and Nuclear Chemistry, 2012, 293(3): 915-921.
[18]LEE H Y, LI Z, CHEN K, et al. PET/MRI dual-modality tumor imaging using arginine-glycine-aspartic(RGD)-conjugated radiolabeled iron oxide nanoparticles[J]. Journal of Nuclear Medicine, 2008, 49(8): 1 371-1 379.
