锂系热电池电化学体系性能比较
2015-12-31赵小玲陈克靖
张 艳,刘 波,赵小玲,郑 奕,陈克靖
(1.中国人民解放军海军驻上海地区航天系统军事代表室,上海 201109;2.上海空间电源研究所,上海 200245)
0 引言
早期热电池采取的钙-铬酸钙体系在20世纪80年代已逐步被锂系热电池所取代[1-3]。与其他类型的化学电源相同的是,热电池中也包括正极、负极及填充在两者间的电解质,不同的是,热电池中还含由点火头、引燃纸和加热片构成的加热体系,可为自身提供热量。热电池的电解质由低温共熔盐组成,常温下为不导电的固体,在激活前一直处于高阻状态不能输出电能,自放电极低,因此具有非常长的贮存寿命(约20年);使用时通过撞击或电流引燃点火头,并通过引燃纸迅速点燃加热片,电池内部温度瞬间升高,使熔盐熔融并形成离子导体,电池开始放电。为防止电解质在热电池工作时的溢流,必须使用流动抑制剂,如氧化镁、二氧化硅固定电解质。热电池的自身加热体系决定了热电池具有极短的激活时间(<1.5s),另外热电池工作时,呈熔融状态的无机盐电解质具高离子电导能力,内阻仅为毫欧级,故热电池可输出大电流。基于上述优势,热电池被广泛作为武器系统工作电源[4-5]。分析锂系热电池技术发展趋势,早先基本采用LiCl-KCl双元共熔盐作为电解质,近来则越来越多地使用多元共熔盐(如LiF-LiCl-LiBr,LiCl-LiBr-KBr)[6-7]。为进一步提高热电池性能,对电池正极和负极活性材料进行了大量研究。美Sandia实验室在研制需高功率输出的热电池时,优先选用了CoS2而不是技术成熟的FeS2[8]。文献[9]发现CoS2的内阻明显小于FeS2,表明前者的大电流放电能力优于后者。虽然LiB合金早在20世纪70年代即已被发现并曾用于研制热电池,但据报道,目前国外的热电池技术还是以LiSi合金负极材料为主,而国内对LiB合金的制备及其应用取得了显著进展[8、10-12]。本文对目前锂系热电池技术中广泛使用的电解质、正极材料,以及负极材料各自的电化学性能系统地进行了比较。
1 实验部分
1.1 实验材料
LiSi,LiB合金用文献[11-13]的方法制备。从硫铁矿中提纯获得FeS2[14]。CoS2用固相合成法制备。自制3种熔盐电解质,分别为三元全锂电解质(LiF-LiCl-LiBr)、二元常规电解质(LiCl-KCl)和三元低温电解质(LiCl-LiBr-KBr)。流动抑制剂采用MgO,添加量为50%;加热药为Fe粉和KClO4的混合物,质量比为84∶16。
1.2 主要仪器和设备
100t油压机,自制单体放电设备,H&H ZS1812型直流电子负载器,DEWETRON DEWE-3020型多通道数据采集仪。
1.3 实验方法
所有实验均在温度(20±5)℃,相对湿度<2%的干燥房里进行。单体放电实验所用单体电池由正极、隔离和负极3层片构成。单体测试采用恒温放电。构成电池组的单体电池为4层片结构,分别为加热片、正极片、隔离片和负极片,加热粉用量按最佳值进行热设计。电池组采用28个单体组合形式,其中每类单体各14只串联,电堆按对称方式组装,以减少放电环境不同引起的误差。电池测试采用恒流方式放电,在测试过程中加脉冲考察电池内阻变化。
2 结果与讨论
2.1 共熔盐电解质选择
热电池采用的低温共熔盐电解质须满足以下要求:
a)常温下为不导电的固态,激活后处于液态,此时应具有较高的离子电导率和较低的电子电导率;
b)熔点不宜太低,否则不利于热电池长时间贮存,但也不能过高,应明显低于电极材料的热分解温度;
c)自身性能稳定,分解电压高,蒸汽压低;
d)与正负极材料的相容性好,不与正负极材料发生反应,并且对正负极材料以及放电产物的溶解度小。
另外,在热电池的工作温度下,熔融盐电解质的黏性很小,为防止熔融盐电解质流动,需加入流动抑制剂,因此合适的电解质须要有相应的流动抑制剂与之相配:电解质对流动抑制剂的润湿能力良好,但不能溶解流动抑制剂。常用热电池电解质的3种低温共熔盐主要性能参数见表1[6]。
以LiSi为负极,FeS2为正极,分别用含LiFLiCl-LiBr,LilCl-LiBr-KBr,LiCl-KCl的隔离粉制备单体电池,在不同温度和电流密度下进行放电性能测试,设放电终止电压为1.5V,放电结果如图1所示。在450℃和200mA/cm2放电条件下,LiFLiCl-LiBr,LiCl-KCl,LiCl-LiBr-KBr的工作时间分别为252,200,182s;在500℃和200mA/cm2放电条件下,三者的工作时间分别为327,266,201s;在500℃和400mA/cm2放电条件下,三者的工作时间分别为171,119,87s。以上结果表明:当热电池工作温度高于LiF-LiCl-LiBr的熔点(436℃)时,电池以大电流密度(400mA/cm2)或相对较小电流密度(200mA/cm2)在温度(500℃)或相对较低温度(450℃)下放电,LiF-LiCl-LiBr的放电性能最优,这主要是因为LiF-LiCl-LiBr具相对较高的锂离子传导能力。因此,在设计需要大功率工作热电池时,LiF-LiCl-LiBr有明显优势。

表1 热电池用低温共熔盐电解质性能Tab.1 Performance of molten-salt electrolytes for thermal batteries

图1 电解质对热电池电性能影响Fig.1 Effect of electrolytes on performances of thermal batteries
2.2 热电池正极材料选择
锂系热电池的正极材料,主要有FeS2、CoS2和过渡金属卤化物(MClx)。过渡金属卤化物虽然具容量大、电极电位高和热稳定性好等特点,但在卤盐熔盐中的溶解度较大导致电池自放电现象非常严重,限制了它在热电池中的应用。更具实用价值的FeS2,CoS2的与热电池应用相关的理化性质见表2。FeS2主要从天然矿石中提取,性能稳定,价格便宜,但电阻率较大(0.036Ω·cm),热分解温度550℃;CoS2仅能通过人工合成方式制备,相较FeS2,其电子导电能力有较大改进,电阻率仅0.002Ω·cm,且热分解温度提高约100℃。根据表2的电极反应,FeS2的理论比容量为1 206C/g,略高于CoS2的1 045C/g。
以LiSi为负极,使用 LiF-LiCl-LiBr,分别用FeS2,CoS2为正极制备单体电池,在500℃和200mA/cm2条件下放电,放电曲线如图2所示。放电初期,LiSi|FeS2的放电电压1.82V,高于 LiSi|CoS2的放电电压约0.1V,与表2中CoS2,FeS2的电极电位趋势一致。随着放电的进行,LiSi|FeS2体系的放电电压持续快速下降,而LiSi|CoS2体系则相对保持平稳,在放电约270s时LiSi|CoS2体系的放电电压超过了LiSi|FeS2体系。以1.5V作为放电终点,LiSi|FeS2体系可放电325s,LiSi|CoS2体系放电时间达360s。以上结果表明:虽然FeS2的理论计算容量高于CoS2,但实际可利用容量却不及CoS2,FeS2的有效利用率(约48%)低于CoS2(约60%)。
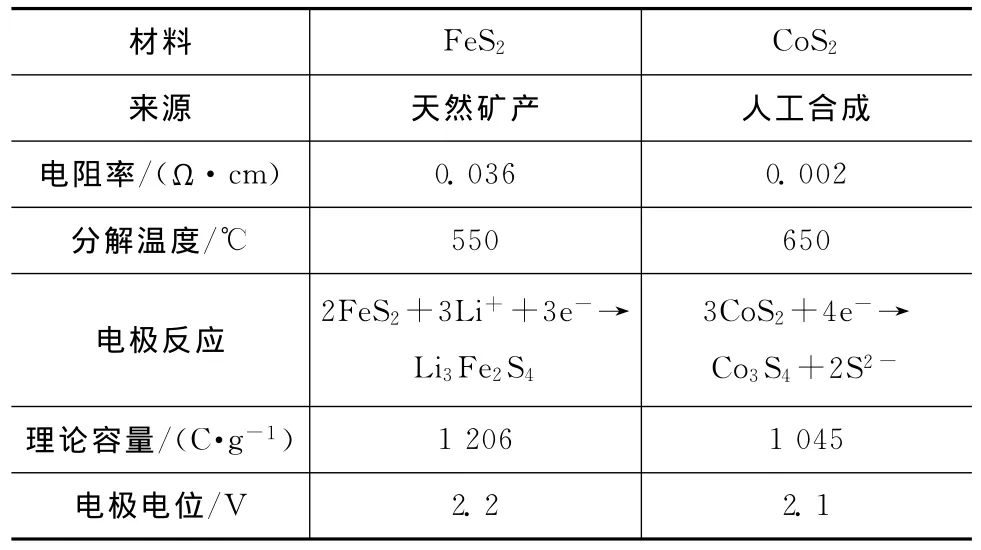
表2 FeS2,CoS2性能Tab.2 Performance of FeS2and CoS2
分析两个单体电池的内阻变化趋势,结果如图3所示。由图可知:在相同的放电深度,LiSi|CoS2内阻明显小于LiSi|FeS2,这可归因于CoS2的电导性能优于FeS2。
上述结果表明:CoS2作为热电池正极材料,相对FeS2的优势有:虽然理论电容量不及FeS2,但热分解温度高,容量损耗少,因此利用率高,实际放电容量高于FeS2;放电初期,LiSi|CoS2体系的电压下降相对LiSi|FeS2较平稳,利于提高电池放电电压精度;由CoS2正极产生的电池内阻较小,在大电流放电时造成的压降降低,利于容量的快速输出。综合而言,CoS2较FeS2更适于用于高比功率热电池。

图2 不同正极材料热电池放电曲线Fig.2 Discharge curves of thermal batteries with different cathodes

图3 不同正极材料热电池内阻变化趋势Fig.3 Trend of internal resistance for thermal batteries with different cathodes
值得注意的是,与FeS2作为正极材料需经特殊处理相同,人工合成的CoS2也需经改性处理后方能作为热电池正极材料使用。将改性前后的CoS2与LiB合金构成单体电池,并以14个单体电池串联的形式制备单元热电池,激活瞬间的电压变化趋势如图4所示。由图可知:未经处理的CoS2,空载电压接近32V;改性后的CoS2,该电压降至约30V,接近于LiB|CoS2体系的理论电动势。CoS2经改性处理后放电初期的峰压得到有效抑制,提高了热电池的放电电压精度,由此可见CoS2改性处理的重要性。
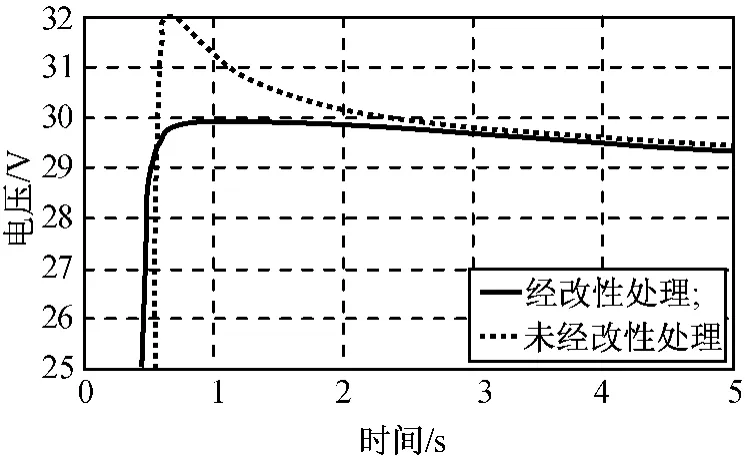
图4 CoS2用作热电池正极的放电曲线Fig.4 Discharge curves for CoS2
2.3 热电池负极材料选择
国内外研究和使用过的锂系热电池负极材料主要有LiAl,LiSi,LiB合金。在LiAl合金中,当Li质量分数超过23%时,便会出现液相,因此该材料在热电池中使用受限。目前锂系热电池中最常见的负极材料为LiSi合金,其Li质量分数约44%,在热电池应用中的电极反应为

据此推算出其理论比容量约0.49A·h/g,电极电位较Li+/Li电位高约0.15V。为进一步提高合金中Li含量以获得大容量负极材料,LiB合金获得青睐。对LiB合金的研究自20世纪70年代就已经开始,但由于性能不稳定,直到1995年才有在热电池中的应用报道。通过对LiB合金的表征测试发现:LiB合金是由海绵状的多孔Li7B6骨架和嵌在孔隙中的金属锂组成;LiB合金在电极反应时实际上是骨架中的游离Li参加反应,故它显示出纯锂的电极特性。由于致密Li7B6骨架的存在,LiB合金负极在放电时不仅能保持原有的形状与尺寸,而且也不会溢出金属Li而造成短路,但也正因为此,LiB合金中的金属Li在放电时,极化较大,放电倍率特性较差,并导致LiB体系热电池激活时间延长。适当提高LiB合金中Li含量,则合金中主要成分将由Li7B6骨架变为金属Li,Li7B6骨架的限制作用将有所减弱,从而可改善LiB合金的放电性能,但同时Li7B6骨架抑制高温下金属Li流动的能力也将明显减弱,有可能造成金属Li的流动,导致电池短路而引起安全问题。另一个方法是对LiB合金进行改性处理,适当打破LiB合金中致密的Li7B6骨架结构,提高材料的微观比表面积,从而减少LiB合金放电时的极化。
在负极材料略有差别,其他参数,如电解质、正极材料、测试温度、放电电流密度均一致的条件下,LiB合金未经改性和两种不同方法改性后用作热电池负极材料的放电性能如图5所示。由图可知:未经改性的LiB合金构成的热电池峰值电压1.9V,但电压下降很快;经复合负极法改性的LiB合金解决了电压快速下降的趋势,但以初始电压下降为代价;经脱锂助剂法改性的LiB不仅解决了电压快速下降的趋势,同时还保持了初始的高电压。

图5 LiB合金放电曲线Fig.5 Discharge curves for LiB alloy
以处理过的CoS2作为正极材料,对LiF-LiCl-LiBr,分析了以LiB,LiSi作为热电池负极材料的电性能,结果如图6所示。由图可知:
a)LiB|CoS2和LiSi|CoS2体系的开路电压分别为2.03,1.83V,表明 LiB的电极电位略低于LiSi,更接近纯锂的电极电位,与文献中结果一致。
b)加相同恒流负载后,两者电压分别下降为1.93,1.73V,均下降0.10V,两者在内阻上并无明显差异;这也反映出在热电池中负极材料电导率表现出纯金属特性,远高于正极材料和电解质,因此热电池的内阻主要取决于正极材料和电解质。
c)相对LiSi|CoS2体系放电电压持续下降,LiB|CoS2体系的放电电压在较长一段时间给出一个相对平稳的平台,表明后者在热电池实际应用时可有较好的电压精度。
d)LiSi|CoS2体系恒流放电300s后,放电电压迅速下降,电池内阻迅速增加,主要是由于电极材料电容量消耗完导致;LiB|CoS2体系的放电电压至放电500s后才开始下降。计算发现,LiB|CoS2体系中LiB的利用率大于90%,高于LiSi|CoS2体系中LiSi的利用率(约82%)。

图6 不同负极材料热电池放电曲线Fig.6 Discharge curves of thermal batteries with different anodes
基于以上分析比较可认为:LiB合金具含锂量高、理论电容量大、实际利用率高、电极电位低、放电电压精度高和热稳定性好等优势,利于提高功率型热电池的比能量。
3 结论
本文用实验对锂系热电池电化学体系的性能进行了研究。结果发现:当工作温度超过450℃时,因有较高的锂离子传导能力,LiF-LiCl-LiBr的电性能优于LiCl-KCl,LiCl-LiBr-KBr;经改性处理后,CoS2放电电压精度和实际可利用电容量远优于FeS2;经适当改性处理的LiB合金多种性能优于LiSi合金。本文研究结果表明,需要高功率热电池时,可优先考虑采用LiB|LiF-LiCl-LiBr|CoS2电化学体系。
[1] 陆瑞生,刘效疆.热电池[M].北京:国防工业出版社,2005:80-280.
[2] LINDEN D,T.REDDY B.Handbook of batteries(3rded.)[M].汪继强(译).北京:化学工业出版社,2007:362-378.
[3] 李国欣.新型化学电源技术概论[M].上海:上海科学技术出版社,2007:219-259.
[4] 张春晓,穆仕博.热电池在空空导弹上的应用及发展趋势[J].电源技术,2010,134(6):614-615.
[5] 赵广波,徐 莹,汴纪庆,等.热电池技术进展及在引信中的应用[J].探测与控制学报,2008,30(6):64-68.
[6] MASSET P,GUIDOTTI R A.Thermal activated(thermal)battery technology partⅡ.molten salt electrolytes[J].Journal of Power Sources,2007,164:397-414.
[7] 种 晋,董 静,张霣霞,等.两种常用电解质体系的LiB/FeS2热电池性能的差异及其影响机理的研究[J].中国电子科学研究院学报,2007,2(4):365-370.
[8] GUIDOTTI R A,REINHARDT F W.Evaluation of the Li(Si)/FeS2and Li(Si)/CoS2couples for a highvoltage,high-power thermal battery[R].Sandia Report,2000-1408.
[9] 孙淑洋,刘延东,曹军记,等.二硫化钴作高功率热电池正极材料的研究[J].电源技术,2003,27(1):28-30.
[10] RAYMOND A S,FREDERICK E W.Battery with boron-lithium alloy anode[P].US:4162352,1979.
[11] 段 伟,刘志坚,章四琪,等.锂硼合金的反应合成及相关现象研究[J].粉末冶金材料科学与工程,1998,3(3):168-171.
[12] 种 晋,马越军,郝津臣,等.Li(B)合金负极在热电池中的应用研究[J].电源技术,2007,31(3):220-224.
[13] 黎彦希.锂硅合金粉工业生产试验[J].特种铸造及有色合金,2004(1):66.
[14] 廖 青.高纯二硫化铁的研制与应用[J].江苏冶金,1998(6):15-17.
