三种有机膦酸阻垢剂对碳酸钙晶面吸附作用的分子动力学研究
2015-12-28
(青海黄河上游水电开发有限责任公司新能源分公司,青海西宁810008)
多晶硅生产装置的连续稳定运行,需要对循环冷却水系统进行日常维护。碳酸钙垢是循环冷却水系统中最常见的水垢之一,碳酸钙垢附着在换热器管壁会影响装置的换热效果,造成多晶硅各工艺段物料达不到要求的温度,影响产品品质。结垢严重还会造成换热器堵塞、管内压力增大、物料泄漏,引发安全事故。碳酸钙晶型存在的形式主要有3种:方解石(calcite)、文石(aragonite)和球霰石(vaterite)[1-2]。常温常压下,方解石是碳酸钙颗粒在热力学上最稳定的结晶相[3],而文石和球霰石是亚稳晶型,很容易转变为方解石[4]。因此,如何抑制方解石晶体生长已成为多晶硅生产的研究热点。
有机膦酸阻垢剂具有良好的化学稳定性、协同效应和一定的阈值效应,对Ca2+、Ba2+和Mg2+等多种金属离子具有较强的螯合作用,能够很好地抑制碳酸钙垢的生长,而且不需调节循环水系统的pH 值,因此被广泛应用于循环冷却水系统中[5-9]。Bromley等[10]研究表明,有机膦酸阻垢剂至少要含有2个以上的膦酸基团才能达到良好的阻垢效果。
作者在此选择氨基三亚甲基膦酸(NTMP)、乙二胺四亚甲基膦酸(EDTMP)和二乙烯三胺五亚甲基膦酸(DTPMP)[11]3 种有机膦酸阻垢剂,基于Material Studio 3.0软件,采用分子动力学模拟方法研究其与碳酸钙晶面之间的吸附作用,探讨其阻垢能力的强弱和吸附作用的本质,为阐述阻垢机理提供理论依据。
1 模拟
由于多晶硅生产的实际循环冷却水系统的pH 值大约在8~10之间,水温约为70 ℃左右,在此条件下有机膦酸基团会发生脱氢,形成质子化PO2-3基团。NTMP、EDTMP 和DTPMP 去质子化分子结构如图1所示。
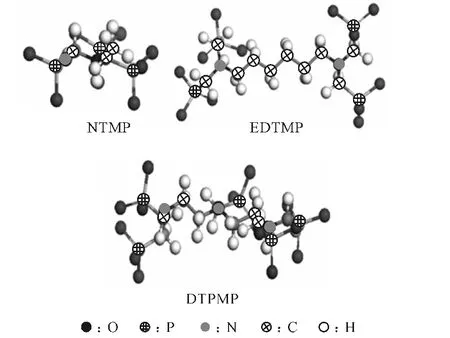
图1 3种有机膦酸阻垢剂的去质子化分子结构Fig.1 The deprotonated molecular structures of three organic phosphonate scale inhibitors
由图1可以看出:NTMP是1个N 原子上连接3个亚甲基膦酸基团(-CH2-PO2-3);EDTMP 是2个N 原子上分别连接2个-CH2-PO2-3基团;DTPMP是在3个N 原子上连接5个-CH2-PO2-3基团,含膦酸基团数最多。
方解石属于R-3C 空间群,六方晶系,晶胞参数为:a=b=4.99 Å、c=17.06 Å、α=β=90.0°、γ=120.0°。方解石晶体形态学上最稳定的生长面是(104)面和(110)面[12-13],因此选择其作为本研究的目标晶面。借助Cleave Surface工具进行切割分面来得到要考察的方解石习性面。考虑到计算成本,先对(104)面和(110)面设置3×3×3超晶胞,建立方解石晶面层;再采用Smart Minimizer方法对方解石晶面层进行能量最小化,优化步数为10 000,收敛水平为精细,目的是消除超晶胞结构中不合理的能量和构象;然后采用Smart Minimizer方法对目标分子的初始结构进行几何优化,步数为10 000,收敛水平为精细,得到势能面上最稳定的阻垢剂分子结构;将优化的有机膦酸阻垢剂分子沿Z轴方向放置在晶面层上方,真空层厚度设置为50Å,并应用周期性边界条件建立有机膦酸阻垢剂分子-方解石晶面吸附模型;最后,设置水的介电常数(ε=78)来近似模拟水溶液环境。
COMPASS力场[14]能够准确模拟凝聚态的结构和性质,而且能将混合体系分类计算,因此,选择COMPASS力场作为模拟力场。在分子动力学模拟之前,首先对吸附模型的初始结构执行能量最小化。对于分子动力学模拟,将晶面层固定,而有机膦酸阻垢剂分子可以自由运动。采用NVT 系统,选择Andersen方法控温,温度设定为350K 来模拟循环水环境温度。模拟时间根据平衡依据及前人的研究先进行200 ps动力学模拟平衡;再执行200ps进行数据采集,每100fs输出一个结果;统计最后50ps的输出结果进行数据分析。采用Atom Based和Ewald方法分别计算范德华力和静电作用力,应用long-range校正。
有机膦酸阻垢剂分子与方解石晶面之间的吸附能(ΔEads)按式(1)计算[15]:

式中:Esys为动力学模拟后有机膦酸阻垢剂分子与方解石晶面吸附体系的总能量;Esur为方解石晶面层的能量;Einhib为模拟计算后有机膦酸阻垢剂分子的单点能。
2 结果与讨论
2.1 体系平衡
一个体系是否达到动力学平衡,可以根据模拟过程中的温度和能量平衡曲线来判断。一般认为,如果温度和能量曲线的上下波动在5%~10%范围内,那么可以认为体系达到了动力学平衡。图2是有机膦酸阻垢剂EDTMP与方解石(104)面吸附体系的温度和能量平衡曲线。

图2 EDTMP与方解石(104)面吸附体系的温度(a)和能量(b)平衡曲线Fig.2 Temperature(a)and energy(b)equilibrium curves of EDTMP-calcite(104)face adsorption system
由图2可看出:温度在(350±10)K 范围内上下波动,表明体系已处于温度平衡;能量平衡曲线光滑平整,表明体系实现了能量平衡。因此,阻垢剂EDTMP与方解石(104)面的吸附体系达到了分子动力学平衡,后续计算结果是可靠的。另2种有机膦酸阻垢剂与方解石晶面吸附体系也可以得到以上结论。
2.2 吸附作用
以EDTMP 为例建立有机膦酸阻垢剂分子-方解石晶面的吸附模型,如图3所示。
由图3可看出,有机膦酸阻垢剂EDTMP 在吸附前的初始位置与晶面保持了一定的距离,以获得足够的空间使其自身弯曲形变;吸附平衡时,靠近方解石晶面,表明二者之间存在着强的吸附作用。另2种有机膦酸阻垢剂NTMP、DTPMP 在吸附平衡时,也不同程度地靠近方解石晶面(图略)。
表1列出了3种有机膦酸阻垢剂与方解石晶面之间的吸附能。

图3 有机膦酸阻垢剂分子-方解石晶面的吸附模型Fig.3 Adsorption model of organic phosphonate scale inhibitor-calcite crystal surface

表1 3种有机膦酸阻垢剂与方解石晶面之间的吸附能/(kcal·mol-1)Tab .1 Adsorption energies between three organic phosphonate scale inhibitors and calcite crystal surfaces/(kcal·mol-1)
由表1可知:(1)吸附能均为负值,表明阻垢剂分子对方解石晶面的吸附是一个放热过程。DTPMP分子与(110)面的吸附能最大(-160.12kcal·mol-1),而NTMP分子与(104)面的吸附能最小(-82.90kcal·mol-1)。(2)3种有机膦酸阻垢剂对碳酸钙晶面吸附作用顺序为DTPMP>EDTMP>NTMP。(3)3种有机膦酸阻垢剂对(110)面的吸附作用均强于其对(104)面的吸附作用。
表2是有机膦酸阻垢剂与方解石晶面之间吸附能的组成。

表2 有机膦酸阻垢剂与方解石晶面之间吸附能的组成/(kcal·mol-1)Tab.2 Composition of adsorption energies between organic phosphonate scale inhibitors and calcite crystal surfaces/(kcal·mol-1)
由表2可以看出,吸附能主要由范德华作用能和静电作用能组成,其中静电作用能远大于范德华作用能,对吸附作用的贡献占主导位置。Chen等[16]认为基团的O 原子会与晶面的Ca2+形成离子键,其键长接近Ca-O 离子键键长。表明有机膦酸阻垢剂分子与碳酸钙晶面之间能发生很强的静电作用,从而解释了静电作用能的贡献要远远强于范德华作用能。Gill等[17]提出阻垢剂与成垢晶面之间的吸附作用主要是静电作用力,与本研究的结果一致。
吸附能越大,阻垢剂与成垢晶面之间的吸附作用就越强。有机膦酸阻垢剂分子可以通过与晶面之间的吸附作用占据碳酸钙晶面的活性生长点,从而破坏成垢晶面的正常生长,导致晶格发生转换,进而抑制碳酸钙垢的形成,最终达到阻垢效果。
因此,根据有机膦酸阻垢剂对方解石晶面的吸附作用,可以得出3种有机膦酸阻垢剂的阻垢作用顺序为:DTPMP>EDTMP>NTMP,这可能与3 种有机膦酸阻垢剂分子中所含基团个数及N 原子之间碳链长度不同有关[10]。此外,有机膦酸阻垢剂分子对碳酸钙(110)面的吸附作用强于(104)面,即与(110)面的结合比(104)面更牢固,可以推测有机膦酸阻垢剂分子会优先吸附在碳酸钙(110)面上。
3 结论
通过对3种典型有机膦酸阻垢剂(NTMP、EDTMP、DTPMP)与碳酸钙晶面吸附作用的分子动力学研究,发现NTMP、EDTMP 和DTPMP 分子能够牢牢吸附在方解石晶面上,而吸附能均为负值,表明吸附过程为放热过程,有机膦酸分子能够自发吸附在晶面上;有机膦酸阻垢剂分子对碳酸钙(110)面的吸附作用强于(104)面,即有机膦酸阻垢剂分子会优先吸附在(110)面上;吸附能主要由静电作用能和范德华作用能组成,其中静电作用能远大于范德华作用能,占主导作用;3种有机膦酸阻垢剂对方解石晶面吸附作用的顺序为DTPMP>EDTMP>NTMP,对碳酸钙垢的阻垢作用顺序为DTPMP>EDTMP>NTMP,吸附作用越大,对碳酸钙垢抑制作用就越强。
[1]GREENLEE L F,TESTA F,LAWLER D F,et al.The effect of antiscalant addition on calcium carbonate precipitation for a simplified synthetic brackish water reverse osmosis concentrate[J].Water Research,2010,44(9):2957-2969.
[2]YANG Y,KIM H,STARIKOVSKIY A,et al.Application of pulsed spark discharge for calcium carbonate precipitation in hard water[J].Water Research,2010,44(12):3659-3668.
[3]MILLO C,ADER M,DUPRAZ S,et al.Carbon isotope fractiona-tion during calcium carbonate precipitation induced by urease-catalysed hydrolysis of urea[J].Chemical Geology,2012,330-331:39-50.
[4]LUPU C,ARVIDSON R S,LUTTGE A,et al.Phosphonate mediated surface reaction and reorganization:Implications for the mechanism controlling cement hydration inhibition[J].Chem Commun,2005,(18):2354-2356.
[5]LESUEUR C,PFEFFER M,FUERHACKER M.Photodegradation of phosphonates in water[J].Chemosphere,2005,59(5):685-691.
[6]JONASSON R G,RISSPLER K,WIWCHAR B,et al.Effect of phosphonate inhibitors on calcite nucleation kinetics as a function of temperature using light scattering in an autoclave[J].Chem Geology,1996,132(1-4):215-225.
[7]LI T T,SHI F F,LI F C,et al.Effects of dry grinding on the structure and granularity of calcite and its polymorphic transformation into aragonite[J].Powder Technology,2014,254:338-343.
[8]REDDY M M.Calcite growth-rate inhibition by fulvic acid and magnesium ion—Possible influence on biogenic calcite formation[J].Journal of Crystal Growth,2012,352(1):151-154.
[9]ASAEDA T,SENAVIRATHNA M D H J,KANEKO K,et al.Effect of calcium and magnesium on the growth and calcite encrustation ofCharafibrosa[J].Aquatic Botany,2014,113:100-106.
[10]BROMLEY L A,COTTIER D,DAVEY R J,et al.Interactions at the organic/inorganic interface:Molecular design of crystalli-zation inhibitors for barite[J].Langmuir,1993,9(12):3594-3599.
[11]TOMSON M B,KAN A T,ODDO J E.Acid/base and metal complex solution chemistry of the polyphosphonate DTPMP versus temperature and ionic strength[J].Langmuir,1994,10(5):1442-1449.
[12]DUFFY D M,HARDING J H.Modeling the interfaces between calcite crystals and Langmuir monolayers[J].J Mater Chem,2002,12:3419-3425.
[13]VILLEGAS-JIMENE Z A,MUCCI A,WHITEHEAD M A.Theoretical insights into the hydrated(10.4)calcite surface:Structure,energetic and bonding relationships[J].Langmuir,2009,25(12):6813-6824.
[14]SUN H.COMPASS:An ab initio force-field optimized for condensed-phase applications—Overview with details on alkane and benzene compounds[J].The Journal of Physical Chemistry B,1998,102(38):7338-7364.
[15]COOPER T G,de LEEUW N H.A computer modeling study of the competitive adsorption of water and organic surfactants at surfaces of the mineral scheelite[J].Langmuir,2004,20(10):3984-3994.
[16]CHEN C Y,LEI W,XIA M Z,et al.Molecular modeling of several phosphonates onto the stepped calcite(011)surface[J].Desalination,2013,309:208-212.
[17]GILL J S,VARSANIK R G.Computer modeling of the specific matching between scale inhibitors and crystal structure of scale forming minerals[J].J Cryst Growth,1986,76(1):57-62.
