川芎嗪在大鼠肠吸收机理及当归提取液对其吸收的影响
2015-12-27翟晓晓张朋俊申滢娜王书杰张玉静李晓天
翟晓晓, 徐 雯, 张朋俊, 申滢娜, 王书杰, 张玉静, 张 颖, 李晓天
(郑州大学 药学院 河南 郑州 450001)
川芎嗪在大鼠肠吸收机理及当归提取液对其吸收的影响
翟晓晓, 徐 雯, 张朋俊, 申滢娜, 王书杰, 张玉静, 张 颖, 李晓天
(郑州大学 药学院 河南 郑州 450001)
研究川芎嗪在大鼠肠吸收动力学,考察不同质量浓度川芎嗪及不同体积比的当归提取液混合物对其吸收速率及相关参数的影响.运用大鼠在体单向肠灌流法测定,重量法校正系统误差,HPLC测定吸收前后药物质量浓度的变化,考察其吸收动力学及当归提取液对其吸收的影响. 结果表明,不同质量浓度(10,20,40 mg/L)川芎嗪的大鼠肠吸收速率常数分别为(0.006 39±0.052 3),(0.006 51±0.019 1),(0.006 03±0.073 7) min-1,无显著性差异;川芎嗪标准溶液与当归提取液按体积比为1∶2,1∶1,2∶1混匀时,川芎嗪的吸收速率常数分别为(0.012 32±0.106 4),(0.010 24±0.086 1),(0.006 195±0.079 9) min-1,结果显示,川芎嗪的吸收速率常数与当归提取液占混合液的体积分数呈现正相关.川芎嗪在大鼠肠道为被动吸收过程,当归提取液对其有一定的促吸收作用,且随着当归提取液量的增加而增大.
当归; 川芎嗪; 单向肠灌流; 吸收
0 引言
川芎为伞形科植物川芎的干燥根茎,其主要活性成分为川芎嗪(tetramethylpyrazine,TMP);当归为伞形科植物当归的干燥根,其主要活性成分为阿魏酸.川芎、当归为临床常用之药对,多用于补血、活血[1].现代医学研究表明,其对血小板聚集、凝血功能、原发性痛经、血虚等有一定的影响[2-4].但对于其配伍的研究大多限于药效学方面,对于其药物动力学,如吸收的影响,至今尚未见报道.作者采用大鼠在体单向肠灌流法研究不同质量浓度川芎嗪在体肠吸收特点及不同组分比例的当归提取液对其吸收参数的影响,以探讨川芎主要活性成分川芎嗪与当归在配伍过程中对其吸收的影响,为更合理用药,以及使其两者之间的配伍能更好地实现中药现代化提供一定的依据[5-6].同时,川芎嗪的半衰期较短,为开发其新剂型以及与当归合用时其剂量的变化提供一定的依据.
1 材料
1.1 仪器
Waters e2695型高效液相色谱仪(美国Waters公司);KQ3200DE型数控超声清洗器(昆山市超声仪器有限公司);METTER TOLEDO XS-105型分析天平(瑞士梅特勒-托利多集团);XK96-A 型快速匀浆机(姜堰市新康医疗器械有限公司);BT100-2J蠕动泵(保定兰格恒流泵有限公司).
1.2 试剂
川芎嗪对照品(中国药品生物制品检定所,供含量测定,批号20080112);当归(购于郑州市九州通医药股份有限公司,经郑州大学药学院中药系潘成学副教授鉴定为伞形科植物当归的干燥根);甲醇(色谱纯,河北四友卓越科技有限公司);三乙胺(分析纯,天津市风船化学试剂科技有限公司);无水乙醇(天津市富宇精细化工有限公司);超纯水由Mille-Q超纯水机制备;戊巴比妥(北京市博奥拓达科技有限公司).
1.3 实验动物
健康SD大鼠,♂,体重180~220 g,由河南省实验动物中心提供,实验动物卫生许可证:SCXK(豫)2010-0002 .
2 方法与结果
2.1 试液的配制
2.1.1 当归提取液的配制 取当归药材35 g,粉碎后置于圆底烧瓶中,加10倍量体积分数60%的乙醇进行提取,上接球形冷凝管,超声功率100%,75 ℃超声2 h.用纱布过滤后取提取液,旋转蒸发回收乙醇使其成流浸膏,用Krebs-Ringer(K-R)溶液超声溶解,定容于100 mL容量瓶中,使其质量浓度为0.35 g/mL,备用[7].
2.1.2 K-R溶液的配制 每1 L该溶液含NaCl 7.8 g,KCl 0.35 g,NaHCO31.37 g,NaH2PO4·2H2O 0.32 g,MgCl20.02 g,CaCl20.37 g,葡萄糖1.4 g(临用前添加),用1 mol/L磷酸调pH值至6.8.加入顺序为NaCl,KCl,CaCl2,NaH2PO4·2H2O,葡萄糖,MgCl2,NaHCO3.由于K-R溶液在空气中放置极易产生浑浊,对测定结果有较大的影响,因此,现用现配[8].
2.1.3 肠循环液的配制 分别精密称取适量川芎嗪标准品,用K-R溶液定容于50 mL容量瓶中,使其质量浓度为10,20,40 mg/L,此为川芎嗪标准品肠循环液.分别取20 mg/L川芎嗪标准溶液及0.35 g/mL当归提取液适量,使其体积比分别为1∶1,1∶2,2∶1,涡旋1 min,此为川芎嗪-当归提取液混合肠循环液.
2.2 肠循环液中药物质量浓度的测定
2.2.1 色谱条件 Waters e2695型高效液相色谱仪,Prodigy 5u 100A C18柱(250 mm×4.60 mm,美国菲罗门公司),同时配备一个C18预柱(KJO- 4282,美国菲罗门公司),流动相为甲醇-水(含0.1%三乙胺,体积比62∶38),流速为0.8 mL/min,运行时间为10 min,进样量为50 μL,柱温为25 ℃,检测波长为296 nm.
2.2.2 标准曲线的绘制 精密称取川芎嗪标准品5 mg,置于50 mL容量瓶中,用K-R溶液溶解并稀释至刻度,混匀,配制成100 mg/L的川芎嗪储备液.精密量取川芎嗪储备液适量,用K-R溶液稀释成含川芎嗪0.5,1,2,5,10,20,50 mg/L的系列溶液,按“2.2.1”项下色谱条件进样,以峰面积为纵坐标,以川芎嗪质量浓度为横坐标进行线性回归,回归方程为:y=229 09x+3 437.1,r=0.999 9.结果表明,在0.5~50 mg/L范围内,其线性相关性良好.
2.2.3 专属性实验 分别取空白肠循环液(K-R溶液进行大鼠小肠循环灌流2 h即得)、当归提取液、川芎嗪标准品溶液,川芎嗪-当归提取液混合肠循环液,按“2.2.1”项下色谱条件进行进样,其色谱图结果见图1~4.由图可知,川芎嗪的出峰时间在6.279 min附近,空白肠循环液及当归提取液在此色谱条件下对其测定不产生干扰.

图1 空白肠循环液高效液相色谱图Fig.1 The HPLC spectrum of blank intestinal liquid
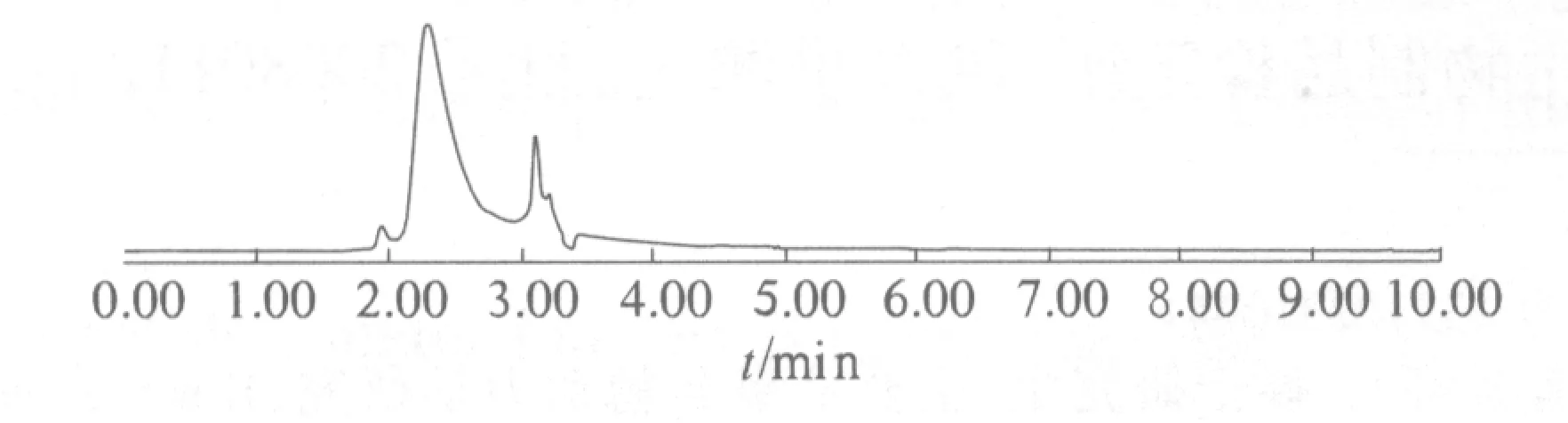
图2 当归提取液高效液相色谱图Fig.2 The HPLC spectrum of Angelica sinensis extraction
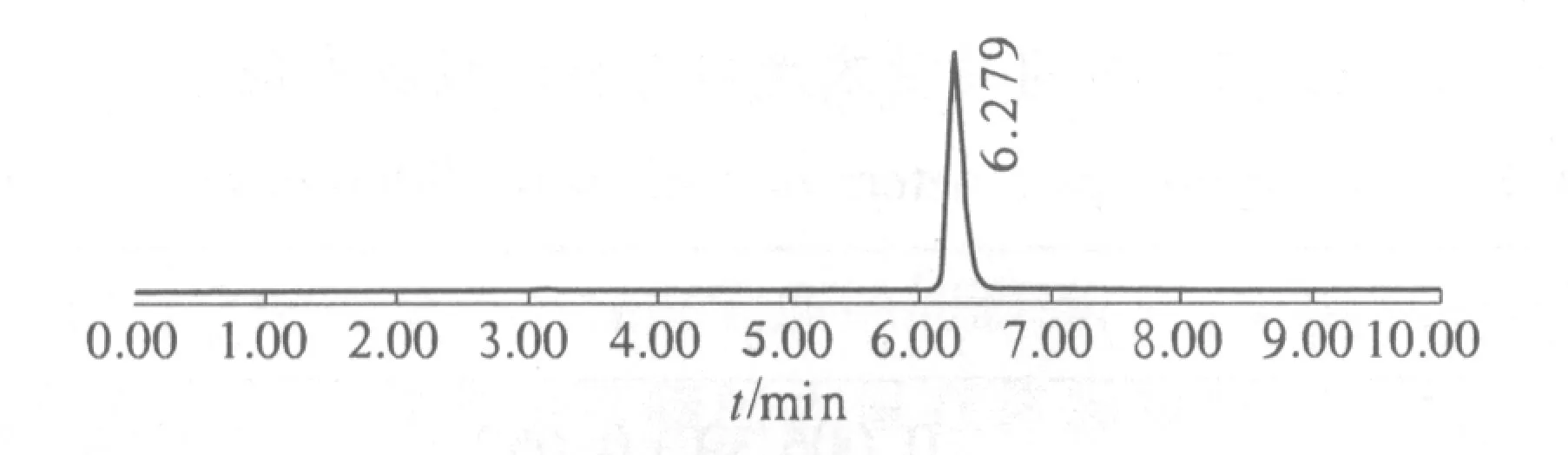
图3 川芎嗪标准品溶液高效液相色谱图Fig.3 The HPLC spectrum of TMP standard
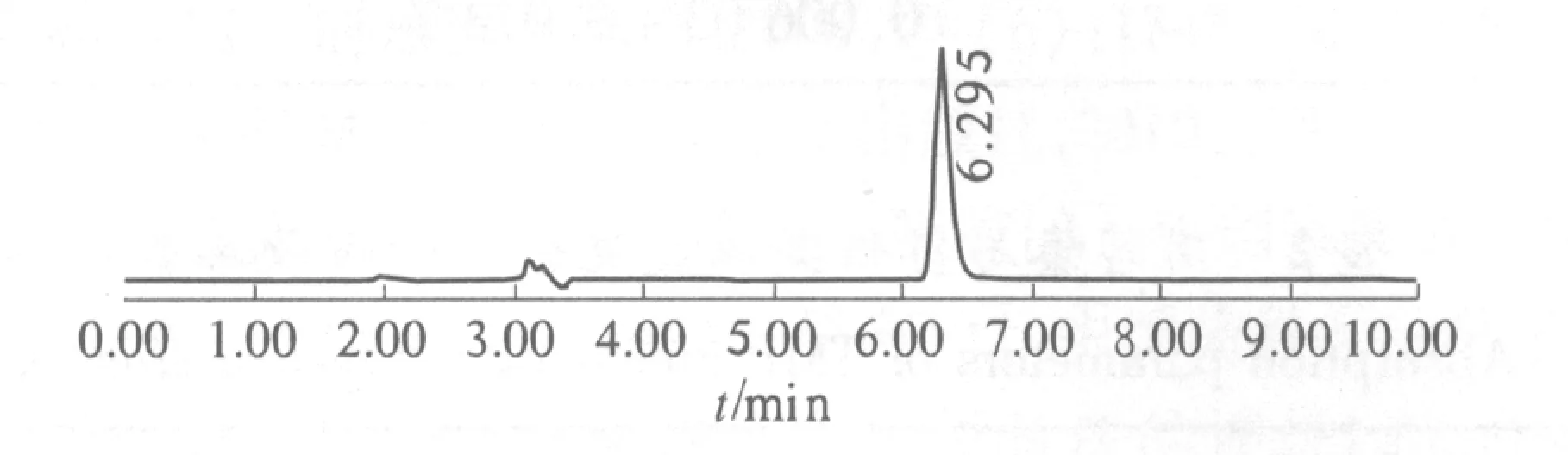
图4 川芎嗪-当归提取液混合肠循环液高效液相色谱图Fig.4 The HPLC spectrum of TMP mixed with Angelica sinensis extraction
2.2.4 精密度实验 取低、中、高3个质量浓度分别为0.5,5,40 mg/L的川芎嗪对照品溶液,于0,2,6 h进样(n=5),计算日内精密度.分别于1周的不同3天再次配制标准溶液,并稀释至上述3个低、中、高质量浓度,按“2.2.1”项下色谱条件进样(n=15),计算日间精密度.其日内精密度RSD<2.30%,日间精密度RSD<4.38%,表明该方法的精密度良好.
2.2.5 准确度实验 精密吸取川芎嗪对照品储备液,用K-R溶液稀释至0.5,5,40 mg/L低、中、高3个系列质量浓度,各5份,过0.22 μm微孔滤膜,按照“2.2.1”项下色谱条件进样,测定峰面积,代入标准曲线计算质量浓度,与原始质量浓度相比,计算方法的回收率.低、中、高3个质量浓度的平均方法回收率分别为98.63%,99.82%,98.75%,RSD分别为1.67%,0.78%,1.18%,表明该方法的回收率良好.
2.2.6 稳定性实验 用K-R溶液配制0.5,5,40 mg/L的川芎嗪溶液(n=5),置于37 ℃水浴中,并于0,2,4,6,8 h测定溶液中川芎嗪含量,根据减少量来测定其稳定性.结果显示,川芎嗪置于37 ℃水浴中8 h,质量浓度未发生明显变化,表明川芎嗪在该实验条件下稳定性良好.
2.3 大鼠在体单向肠灌流实验
2.3.1 实验方法[8-9]为消除实验过程中管路对药物的物理吸附作用而对实验结果造成的误差,在实验开始前,将循环液在管路中反复冲洗,并隔一段时间分别取进口与出口循环液进行检测,直至进、出口循环液的浓度相同为止.
取禁食12 h的大鼠(可自由饮水),腹腔注射3%戊巴比妥(0.2 mL/100 g),待其痛觉不敏感时固定于37 ℃小电热板上保持体温,沿腹中线打开腹腔约2 cm,找到十二指肠上端处剪口插管,在回肠下端剪口,将生理盐水经十二指肠上部管路缓缓注入肠道,洗去肠管内容物,充分洗涤后送入空气使洗涤液尽量流尽.在回肠下端剪口处进行插管,构成通路,并用浸有37 ℃生理盐水的脱脂棉覆盖伤口暴露处,进行保湿.将保持在37 ℃的肠循环液以0.5 mL/min的速度快速灌流5 min,后将流速调至0.2 mL/min,开始计时,每20 min迅速更换1次供试液小瓶和收集液小瓶,直至120 min,实验后量取供试液与收集液的体积,并剪下被考察肠段,测量其长度(l)及横截面半径(r).所搜集的样品过0.22 μm滤膜后按“2.2.1”项下色谱条件进样,测定川芎嗪质量浓度.
2.3.2 数据处理 采用重量法对灌流液的流入与流出的体积进行校正.按(1)式计算其药物的吸收速率Ka和药物表观吸收系数Papp.

(1)
式中:Qin和Qout分别为肠道进、出口灌流液的体积(mL);Cin和Cout分别为肠道进、出口灌流液的质量浓度(mg/L);l和r分别为被灌流肠段的长度(cm)和横截面半径(cm);Q为灌流速度(0.25 mL/min);V为灌流肠段的容积;Ka和Papp为最后5个时间段(20 ~ 120 min)样品的平均值.
2.3.3 实验结果 不同质量浓度川芎嗪药物以及不同体积比的当归提取液混合物在体单向肠灌流实验结果见表1和表2.

表1 不同质量浓度川芎嗪的吸收参数Tab.1 Absorption parameters of TMP with different concentrations

表2 川芎嗪与当归提取液混合物的吸收参数Tab.2 Absorption parameters of TMP mixed with Angelica sinensis extraction
3 讨论
1) 小肠不仅吸收药物,也吸收和分泌水分,导致灌流液体积的变化.目前校正方法有酚红法、14C法及重量法.14C有一定的放射性,而酚红法有一定的肠吸收,并干扰某些药物的肠道转运和分析测定[10-11],其带来的误差有可能造成极大的影响.与传统的酚红法相比,采用重量法对灌流液体积进行校正,更能直接且真实地反映肠道吸收水分的实际情况,从而提高了Ka和Papp值的准确度.此外,采用重量法只需检测药物浓度,大大降低了检测的工作量,更适用于考察难溶性及难吸收药物的吸收机制[12].同时,检测中不存在标示物的紫外吸收干扰,采用紫外分光光度法即可测定药物的浓度,其不仅缩短了检测时间,更降低了检测费用.
2) 小肠为口服药物吸收的主要部位,测定方法有在体肠回流法、肠襻法、分离肠黏膜法、外翻肠囊法和Caco-2细胞模型法等[13].由于第一种方法能避免胃内容物排出及消化管固有运动的生理影响[6],故应用较多,其有循环法以及单向法两种.循环法以长时间(4~6 h)、高流速(2~5 mL/min)回流供试液,对肠黏膜损伤较大,使药物吸收增多,造成结果偏差较大.文献[14]报道,健康志愿者体内肠灌流的速度大多采用2.3 mL/min,而老鼠的肠道直径约为人体肠道的1/10,因而应选择灌流速度在0.2 mL/min附近较为适宜.作者采用0.2 mL/min的单向法肠段进行灌流,与口服给药后药物接触的肠道环境较接近[15],减小了实验的误差.
3) 在实验过程中,为消除肠壁对药物物理吸附的影响,取空白大鼠十二指肠至回肠全段置于已知浓度的肠循环液中,于37 ℃水浴中孵育2 h后进样分析.结果显示,孵育液中药物浓度变化的RSD为1.12%,认为肠壁对药物基本无物理吸附作用.
4) 阿魏酸为当归中主要有效成分,其为热不稳定性物质,长期加热会使其分解[15-17],经实验分析后采用超声辅助萃取的方法(75 ℃,超声功率100%,提取60 min).
5) 由表1可知,不同质量浓度的川芎嗪在体肠吸收系数并没有显著性差异,说明其吸收过程主要是被动扩散过程;比较表1与表2发现,在加入当归提取液之后,川芎嗪的吸收系数有显著性增加,说明当归提取液对其具有一定的促吸收作用,且随着当归提取液所占比例的增加而增大.
6)当归中主要有效成分阿魏酸可以延长川芎嗪在大鼠体内的作用时间,并没有增加吸收的量[18],故对于本实验结果,当归提取液中是何种物质造成的促吸收影响有待于进一步的研究.
[1] 周长征.当归川芎药对研究概况[J].山东中医杂志,2011,30 (8):587-589.
[2] 王欢,唐于平,郭建明,等.当归-川芎药对不同配比组方对家兔血小板聚集和凝血功能的影响[J].中国实验方剂学杂志,2010,16 (2):73-77.
[3] 李伟霞,唐于平,郭建明,等.当归-川芎药对及其组成药味对3种血虚模型补血作用的比较研究[J].中国中药杂志,2011,36 (13):1808-1814.
[4] 王欢,唐于平,郭建明,等.当归-川芎配伍对小鼠原发性痛经的影响[J].中国中药杂志,2010, 35 (7):892-895.
[5] 吴迪,张岩,姚慧敏,等.单向灌流法研究磷酸川芎嗪的大鼠在体肠吸收[J].沈阳药科大学学报,2008,25 (9):695-698.
[6] 沈凯,王景田.药物肠吸收实验研究方法进展[J].中国新药杂志,2003,12 (12):988-991.
[7] 晏亦林,周莉玲.川芎嗪的研究概况[J].时珍国医国药,2008,19 (6):1343-1345.
[8] 魏伟,吴希美,李元建.药理实验方法学[M].北京:人民卫生出版社,2010:524-525.
[9] 苏红,黄川生,陈文,等.单向灌流法研究紫草素的大鼠在体肠吸收[J].中国实验方剂学杂志,2011,17 (4):190-192.
[10] 胡一桥,郑梁元,钱陈钦,等.离子型药物酚红的小肠吸收研究[J].中国药科大学学报,1996,27 (6):355-359.
[11] 聂淑芳,潘卫三,杨星钢,等.对大鼠在体肠单向灌流技术中重量法的评价[J].中国新药杂志,2005,14 (10):1176-1179.
[12] 黄嗣航,龙晓英,袁飞,等.酚红法和改良重量法分别研究葛根素的大鼠在体肠吸收机制[J].广东药学院学报,2012,28 (6):603-607.
[13] 蒋学华,贾运涛,袁媛,等.Caco-2细胞模型在口服药物吸收过程研究中的应用[J].中国药学杂志,2002,37 (5):325-327.
[14] Stewart B H,Chan O H,Lu R H,et al.Comparison of intestinal permeabilities determined in multiple in vitro and in situ models: relationship to absorption in humans[J].Pharm Res,1995,12 (5):693-699.
[15] Lu Guanghua, Chan K,Leung K,et al.Assay of free ferulic acid and total ferulic acid for quality assessment ofAngelicasinensis[J].J Chromatogr A,2005, 1068(2): 209-219.
[16] 金汝城,李贵文,马素丽,等.当归中阿魏酸提取工艺的优化研究[J].中成药,2008,30 (4):516-519.
[17] 刘芝兰,王娟,沈平孃,等.当归中阿魏酸的提取和纯化研究[J].高等化学工程学报,2007, 21 (6):1008-1012.
[18] 冯彬彬,张建海,张继芬,等.不同配伍对川芎嗪体内药代动力学的影响[J].中国中药杂志,2012,37(9):1311-1314.
(责任编辑:孔 薇)
The Absorption Mechanism of Tetramethylpyrazine in Rat and the Impact ofAngelicasinensisExtraction
ZHAI Xiao-xiao, XU Wen, ZHANG Peng-jun,SHEN Ying-na, WANG Shu-jie, ZHANG Yu-jing, ZHANG Ying, LI Xiao-tian
(CollegeofPharmaceutical,ZhengzhouUniversity,Zhengzhou450001,China)
The absorption kinetics of tetramethylpyrazine(TMP) in small intestine of rats and the concentration influence of TMP andAngelicasinensisextraction on it were investigated. The effect of TMP’s absorption in small intestine of rats was studied by using the in situ rats single-pass intestinal perfusion model and HPLC. And the impact ofAngelicasinensisextraction on the absorption of TMP was obtained. The results showed that the absorptive rate constants(k) of TMP at the concentration of 10,20,40 mg/L were (0.006 39±0.052 3),(0.006 51±0.019 1),(0.006 03±0.073 7) min-1, while adding different quantity ofAngelicasinensisextraction to the TMP, thekof TMP were (0.012 32±0.106 4),(0.010 24±0.086 1),(0.006 195±0.079 9) min-1. The absorption mechanism of TMP was passive diffussion.Angelicasinensisextraction could promote the absorption of TMP in small intestine of rats, the concentration ofAngelicasinensisextraction had some effect on the absorption of TMP.
Angelicasinensis; tetramethylpyrazine; single-pass intestinal perfusion; adsorption
2015-01-16
河南省科技攻关项目,编号132102310241.
翟晓晓(1990-),女,河南漯河人,硕士研究生,主要从事药物动力学研究,E-mail:zhaixx1990@126.com ;通讯作者:李晓天(1965-),男,河南禹州人,教授,博士,主要从事药物动力学研究,E-mail:lixt@zzu.edu.cn.
翟晓晓,徐雯,张朋俊,等.川芎嗪在大鼠肠吸收机理及当归提取液对其吸收的影响[J].郑州大学学报:理学版,2015,47(3):87-91.
R285
A
1671-6841(2015)03-0087-05
10.3969/j.issn.1671-6841.2015.03.017
