葡萄糖酸亚锡热分解动力学
2015-12-27曹亚蒙周彩荣刘中平
曹亚蒙, 周彩荣, 刘中平
(郑州大学 化工与能源学院 河南 郑州 450001)
葡萄糖酸亚锡热分解动力学
曹亚蒙, 周彩荣, 刘中平
(郑州大学 化工与能源学院 河南 郑州 450001)
以葡萄糖酸内酯和氧化亚锡为原料,制备葡萄糖酸亚锡并研究其热行为.用红外光谱和元素分析法对产物进行了表征,推测出该化合物的分子式是SnC6H10O7.用热重分析法(DTA-TGA)研究了葡萄糖酸亚锡在N2气氛中的热分解行为及动力学规律.用Flynn-Wall-Ozawa、Kissinger和stava-esta’k法对非等温动力学数据进行了分析.结果表明,热分解过程分为2个阶段,第1阶段热分解温度范围为373~603 K,积分表达式为g(α)=[-ln(1-α)]3;第2阶段热分解温度范围为603~733 K,积分表达式为g(α)=[-ln(1-α)]1/3,同时,得到分解过程的焓变、熵变和Gibbs自由能的变化量,为葡萄糖酸亚锡的工程设计、工业生产奠定基础.
葡萄糖酸亚锡; 热力学过程; 非等温动力学; 活化能
0 引言
葡萄糖酸盐在电镀和医药方面[1]具有较大的应用价值,在金属或合金镀液中加入葡萄糖酸盐[2-4]可以改善电镀效果,使电镀层表面光滑、平整、致密均匀.锡镀层因其防腐蚀性、无毒性和良好的焊接性而受到重视,葡萄糖酸能够与锡离子形成各类配合物离子,参与电极上的电化学行为,改善镀层性能[5-6].普通镀锡液对陶瓷/玻璃组合物有腐蚀作用,并影响陶瓷/金属界面结合力,而以葡萄糖酸亚锡为锡源的镀液可以避免该类问题的出现.目前关于葡萄糖酸亚锡的文献报道较少,本文尝试用D-葡萄糖酸-δ-内酯和氧化亚锡制备葡萄糖酸亚锡,用红外光谱、元素分析法对该物质的结构进行确定,并对其热分解行为和非等温热分解过程的动力学机理进行探讨,为葡萄糖酸亚锡的工业化生产和应用奠定基础.
1 热分解动力学机理
本文采用Kissinger法、Flynn-Wall-Ozawa法和stava-esta’k法对葡萄糖酸亚锡的热分解行为进行非等温动力学分析,其方程如下:

(1)


(2)
式中,f(α)为动力学函数模型,α为转化率,是一个无量纲的量,定义为α=(M0-M)/(M0-Mf),对于非等温过程,这里M0是热分解开始时样品质量,Mf是反应结束达到稳定状态时样品的质量,M是t时刻样品的质量[11].由于不同βi下各热谱峰顶温度Tpi对应的αi值近似相等,因此可以用lnβ~1/T呈线性关系来确定E0.
stava-,
(3)
式中g(α)取自文献[13]给出的30种形式.对于固定的βi,将对应的Tij和αij的数值代入方程(3)就得到一个包含ki的方程组:

(4)
由于βi固定,ln(AsEs/Rβi) 就是一个常数,所以方程组(4)是一个线性方程组,从而可利用线性最小二乘法求解,得到ES和AS.

用非等温法求得E和A之后,其热分解过程的热力学参数焓变ΔH≠、熵变ΔS≠和Gibbs自由能的变化量ΔG≠就可以依据方程式(5)~(7)计算获得[15-16].

(5)
ΔH≠=E-RT,
(6)
ΔG≠=ΔH≠-TΔS≠,
(7)
式中:ν为爱因斯坦振动频率;T为热力学温度;h为Planck常量,其值为6.625×10-34J·s;k为Boltzmann常量,其值为1.380 7×10-23J/K.
2 结果与讨论
2.1 实验试剂和仪器
氧化亚锡(分析纯);D-葡萄糖酸-δ-内酯(分析纯);葡萄糖酸亚锡(99%);DTG-60热重分析仪(岛津); FI-IR2000型红外光谱仪(上海实验仪器厂);FLASH EA 1112型元素分析仪(Thermo公司).
2.2 样品制备及表征
称取适量氧化亚锡和D-葡萄糖酸-δ-内酯,于少量水中混合均匀,在氮气氛围下升温至指定温度开始反应,完成之后分离反应液,将得到的无色透明溶液进行真空旋蒸,加入无水乙醇,结晶得葡萄糖酸亚锡粗品.然后用溶剂洗涤,得到纯度大于99%的产品.用红外光谱仪分析结果如图1所示.

对合成的葡萄糖酸亚锡进行元素分析:C:23.59%,H:3.40%,O:36.02%,Sn:37.53%.由此推测,锡离子与葡萄糖酸根离子的化学计量比为1∶1,该化合物中各元素所占理论百分比为C:23.01%,H:3.22%,O:35.80%,Sn:37.94%.故该化合物的分子式是SnC6H10O7,其结构式如图2所示.
2.3 热分解反应机理
葡萄糖酸亚锡热分解曲线如图3所示.TG曲线显示,升温速率对失重率有一定的影响,随着升温速率的增加,葡萄糖酸亚锡的失重率增大,TG曲线右移.由图3可以看出,其热分解过程分2步进行(图4).第1步,分解温度区间为373~603 K,失重率38.18%,相当于失去4个C、8个H和4个O(理论值为38.38%,相当于2个醋酸分子),推测形成了中间产物SnC2O3H2.第2步,分解温度区间为603~733 K,失重率16.97%,相当于失去2个C、2个O和2个H(理论值为18.55%,相当于1个H2和2个CO),推测生成了氧化亚锡.

图1 D-葡萄糖酸-δ-内酯(a)和葡萄糖酸 亚锡(b)的红外光谱图Fig.1 Infrared absorption spectroscopy of both D-gluconic acid-δ-lactone(a) and stannous gluconate(b)

图2 葡萄糖酸亚锡的 分子结构式Fig.2 Molecular structural formula of stannous gluconate

图3 不同升温速率下葡萄糖酸亚锡的DTA-TGA曲线Fig.3 DTA-TGA curves of stannous gluconate at different heating rates
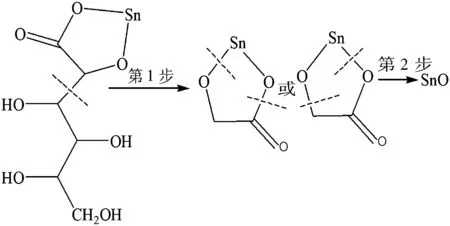
图4 葡萄糖酸亚锡的热分解过程Fig.4 Thermal decomposition process of stannous gluconate
为验证这一结论,采用红外-热分析进行证实.取适量样品,以5 K/min的速度升温至800 K,得到浅灰色固体粉末,对该残余样品进行红外扫描,如图5(b)所示;取市售氧化亚锡作为标准品,扫描红外谱图,结果如图5中曲线(a).两条线主要吸收峰的位置一致,应为同一种化合物,推测葡萄糖酸亚锡在氮气气氛下被加热至800 K时,生成氧化亚锡.同时,将终温600 K的试样残留物进行红外光谱测试,如图6所示,表明葡萄糖酸亚锡在热分解过程中发生了官能团瓦解,O—H弯曲面振动和分子内部羟基的O—H伸缩振动明显减少,推断形成中间产物SnC2O3H2.

图5 氧化亚锡(a)和残余样品(b)的红外光谱图Fig.5 Infrared absorption spectroscopy of both stannic oxide(a) and residual sample(b)

图6 中间产物的红外光谱图Fig.6 Infrared absorption spectroscopy of intermediates
2.4 热分解反应动力学和热分解过程的ΔH≠、ΔS≠和ΔG≠
根据TGA-DTA曲线,对各阶段热分解反应进行非等温动力学处理,得到动力学基础数据(见表1).将30种动力学机理函数分别带入方程(1)~(4)中,结果见表2.

表1 TG测定的动力学基础数据Tab.1 The basic data of the kinetic of TG measurement

表2 葡萄糖酸亚锡分解动力学参数Tab.2 Decomposition kinetic parameters for the first stage of stannous gluconate
将计算得到的E和A分别代入式(5)~(7)中,第1步,在峰温(取平均温度578.825 K)处计算热分解过程的ΔH≠、ΔS≠和ΔG≠分别为173.239 kJ/mol,21.179 J/(mol/K)和160.981 kJ/mol;第2步,在峰温(取平均温度684.95 K)处计算热分解过程的ΔH≠、ΔS≠和ΔG≠分别为122.921 kJ/mol,21.846 J/(mol·K)和113.839 kJ/mol.
3 结论
用葡萄糖酸内酯和氧化亚锡制备的葡萄糖酸亚锡的分子式为SnC6H10O7,结构式为五元环状.用热重分析法研究葡萄糖酸亚锡在氮气中的热分解行为.热分解过程分为两个阶段,第1阶段的机理函数为Avrami-Erofeev方程(n=3),表观活化能E=178.052 4 kJ/mol,指前因子A=3.530 0×1014/s;第2阶段的机理函数为Avrami-Erofeev方程(n=1/3),表观活化能E=128.624 4 kJ/mol,指前因子为A=3.408 9×1013/s.
[1] Schmitz K, Peter V,Meinert S, et al. Simultaneous utilization of glucose and gluconate in Penicillium chrysogenum during overflow metabolism[J]. Biotechnology and Bioengineering, 2013, 110(12): 3235-3243.
[2] Rudnik E, Wojnicki M, Woch G. Effect of gluconate addition on the electrodeposition of nickel from acidic baths[J].Surface and Coatings Technology, 2012, 207(21): 375-388.
[3] Abd El Meguid E A, Abd El Rehim S S, Moustafa E M.Electroplating of iron from alkaline gluconate baths[J]. Thin Solid Films, 2003, 443(1/2): 53-59.
[4] Vasantha V S, Muralidharan V S. Electrochemical behaviour of zinc gluconate complexes[J]. Journal of Chemical Sciences, 1994, 106(4): 825-836.
[5] Gómez E, Guaus E, Torrent J, et al. Tin-cobalt electrodeposition from sulfate-gluconate baths[J]. Journal of Applied Electrochemistry, 2001, 31(3): 349-354.
[6] Guaus E, Torrent-Burgués J. Tin-zinc electrodeposition from sulphate-gluconate baths[J]. Journal of Electroanalytical Chemistry, 2003, 549(3): 25-36.
[7] Rotaru A, Kropidlowska A, Anca M. Non-isothermal study of three liquid crystals in dynamic air atmosphere[J]. Journal of Thermal Analysis and Calorimetry, 2008, 92(1): 233-238.
[8] Kissinger H E. Reaction kinetic in differential thermal analysis[J]. Analytical Chemistry, 1957, 29(11): 1702-1706.
[9] Chen Feixiong, Zhou Cairong, Li Guopeng. Study on thermal tecomposition and the non-isothermal decomposition kinetics of glyphosate[J]. Journal of Thermal Analysis and Calorimetry, 2012, 109(3):1457-1462.
[10]Ozawa T. Kinetic Analysis of derivative curves in thermal analysis[J]. Journal of Thermal Analysis, 1970, 2(3): 301-310.
[11]周彩荣,任军亮,徐敏强,等.废弃糖醛的热分析研究[J].郑州大学学报:工学版,2011,32(4):81-85.
[13]胡荣祖, 史启祯. 热分析动力学[M]. 北京: 科学出版社, 2008.
[14]Huang Mingxing, Lv Shuchen, Zhou Cairong. Thermal decomposition kinetics of glycine in nitrogen atmosphere[J]. Thermochimica Acta, 2013,552(3): 60-64.
[15]周彩荣, 石晓华, 王海峰, 等. DL-2-萘普生热分解过程和非等温热分解动力学研究[J]. 高校化学工程学报, 2011, 25(3) :442-446.
[16]刘中平, 吕淑琛, 周彩荣. 肌醇热分解动力学[J]. 高校化学工程学报, 2013,27(3): 542-546.
(责任编辑:王浩毅)
Thermal Decomposition Kinetics of Stannous Gluconate
CAO Ya-meng, ZHOU Cai-rong, LIU Zhong-ping
(SchoolofChemicalEngineeringandEnergy,ZhengzhouUniversity,Zhengzhou450001,China)
Stannous gluconate was synthesized with D-Gluconic acid-δ-lactone and stannous oxide. It was characterized by FTIR techniques to speculate the formula (SnC6H10O7). The thermal decomposition and non-isothermal decomposition kinetic of stannous gluconate was investigated by the Differential Thermal Analysis and Thermogravimetric Analysis in nitrogen atmosphere. The mechanism function and kinetic parameters were obtained by the Flynn-Wall-Ozawa, Kissinger andstava-esta’k methods. The results showed that the thermal decomposition was divided into two stages, the thermal decomposition temperature range of first stage was 373~603 K, another was 603~733 K, the thermal decomposition methanism functions of them are Avrami-Erofeev equation, and the reaction orders (n) are 3 and 1/3, respectively. Moreover, the enthalpy change, entropy change and the change of Gibbs free energy were obtained, which can contribute to industrial production and application of stannous gluconate.
stannous gluconate; thermodynamic process; non-isothermal kinetic; activation energy
2015-06-25
河南省教育厅科技重点攻关项目,编号13A530712.
曹亚蒙(1989-),女,河南周口人,硕士研究生,主要从事精细有机合成研究,E-mail:hgdcym@163.com;通讯作者:周彩荣(1958-),女,江苏沐阳人,教授,博士,主要从事有机合成及分离研究, E-mail:zhoucairong@zzu.edu.cn.
曹亚蒙,周彩荣,刘中平.葡萄糖酸亚锡热分解动力学[J].郑州大学学报:理学版,2015,47(3):77-81.
O642
A
1671-6841(2015)03-0077-05
10.3969/j.issn.1671-6841.2015.03.015
