水胺硫磷半抗原分子的设计及其免疫效果*
2015-12-25刘波袁利鹏林丹琼熊波高秀杰
刘波,袁利鹏,林丹琼,熊波,高秀杰
1(广东农工商职业技术学院热作系,广东 广州,510507)2(广东产品质量监督检验研究院,广东顺德,528300)
3(中山大学 达安基因股份有限公司,广东广州,510665)
水胺硫磷(isocarbophos,ICP),手性有机磷农药(organophosphorus pesticides,OPs)的一种,由于具有杀虫效率高,碱性条件下易分解等优点,一度成为农业生产中的主要杀虫剂之一。但ICP的滥用,不仅会造成农药在环境中的残留,还可通过食物链的富集作用使动物和人中毒,进而对人体的代谢平衡产生影响,尤其是对儿童神经系统的正常发育产生更为严重的影响[1-2]。2010年海南发生的“毒豇豆”事件,其元凶就是ICP。
目前,水胺硫磷的检测方法主要有高效液相色谱法(HPLC)[3]、气相色谱法(GC)[4-5]、液相色谱-电喷雾串联质谱法(LC-ESI-MS/MS)[6-7]等。这些方法虽然具有很好的准确度和灵敏度,但需要昂贵的检测设备,且样品的前处理操作较繁琐,单个样品的检测耗时长,不能快速提供检测结果。因此建立一种新的快速、灵敏、检测成本低的检测ICP方法,尤其是痕量ICP的检测方法,是目前分析化学需要研究的重要课题。近年来,免疫分析技术已经越来越广泛地应用于农兽药残留分析和掺伪食品鉴定领域,以其简单、廉价、快捷、灵敏度高、适用于大批量样品检测等优点而成为一种重要的分析方法。目前国内外尚未见ICP的免疫化学检验方法及产品的报道,本研究设计合成了ICP半抗原,并制备了抗ICP多克隆抗体。
1 材料与方法
1.1 实验材料与仪器
1.1.1 主要试剂
弗氏完全佐剂、弗氏不完全佐剂、牛血清白蛋白(BSA)、卵清蛋白(OVA)、3,3',5,5'-四甲基联苯胺(TMB),美国Sigma公司;水胺硫磷及其相关标准品,德国Dr.Ehrenstorfer GmbH;羊抗兔IgG-HRP,购于博士德公司;三氯硫磷,西亚试剂公司;二环已基碳二亚胺(DCC)、N-羟基琥珀酰亚胺(NHS)、N,N-二甲基甲酰胺(DMF)和其他化学试剂,阿拉丁试剂公司;包被缓冲液(0.05 mol/L pH 9.6的碳酸盐缓冲液)、封闭液(含1% 明胶的0.05 mol/L pH 9.6的碳酸盐缓冲液)、洗涤液 PBST(含0.05%Tween-20的0.01 mol/L,pH 7.4的PBS)、底物缓冲液(pH 5.0的磷酸-柠檬酸缓冲液)、底物TMB(2 mg/L DMSO)、终止液(2 mol/L H2SO4),均为实验室配制。
1.1.2 实验动物
新西兰大白兔2只,雌性,体重3 kg以上,购自广东省实验动物中心。
1.1.3 主要仪器
HP1100液质联用仪,美国,Agilent;多功能酶标仪,美国,Perkin Elimer;Wellwash MK2洗板机,美国Thermo;UV-2450紫外-可见分光光度计,日本岛津分析仪器公司。
1.2 实验方法
1.2.1 半抗原的合成及结构鉴定
合成方法如图1所示。称取10.4 g水杨酸放入圆底烧瓶,然后依次加入4.5 L浓H2SO4和20 mL无水异丙醇,油浴加热至100℃冷凝回流12 h后冷却至室温加水稀释,用乙酸乙酯萃取3次,每次用乙酸乙酯20 mL,合并有机层用饱和NaHCO3洗涤2遍,最后再用饱和食盐水洗1遍,有机层用无水Na2SO4除水干燥后用旋转蒸发器蒸干有机溶剂得到浅黄色水杨酸异丙酯。

图1 水胺硫磷半抗原H-ICP的合成路线Fig.1 The synthesis scheme of H-ICP hapten
用量筒量取15 mL三氯硫磷于圆底烧瓶中,在-5~0℃强烈搅拌下缓慢加入30 mL无水甲醇反应2 h,产物用冰水振摇2~3次除去甲醇和产生的HCl,有机层用无水Na2SO4除水干燥后得到无色透明液体O-甲基硫代磷酰二氯,低温保存备用。
称取水杨酸异丙酯2 g加入10 mL二氯甲烷和60 mg四丁基溴化铵冷却至0℃左右,搅拌下逐滴加入4 g O-甲基硫代磷酰二氯,加热升至室温,再滴加20%的NaOH溶液,反应过程用pH试纸监控使溶液pH值保持在11左右,反应4 h后分离出二氯甲烷相蒸干,过柱纯化得到产物O-甲基-O-2-水杨酸异丙酯硫代磷酰一氯。
称取O-甲基-O-2-水杨酸异丙酯硫代磷酰一氯500 mg,加入5 mL二氧六环,置于0℃下搅拌,搅拌下逐滴加入2 mL溶有170 mg NaOH和210 mg 6-氨基己酸,随后加热升温至室温;反应4 h后点板监控,待反应完全后用稀盐酸将溶液的pH值调至酸性,用三氯甲烷萃取蒸干得到浅黄色油状物,过柱纯化得到终产物H-ICP。
由图2可见,在APCI-MS正离子谱图中存在m/z为403.9的质谱峰,该产物相对分子质量与目标产物的相对分子质量403.1一致,结合反应路线,可以推断合成产物即为所需的目标半抗原,说明该合成路线可以用于水胺硫磷半抗原的合成。同时可见,403.9的分子离子峰是最强峰,表明新产物为反应体系中的主要物质,说明反应产物具备相对较高的纯度。

图2 水胺硫磷半抗原H-ICP的质谱图Fig.2 The mass spectrum of H-ICP hapten
1.2.2 人工抗原制备与鉴定
采用活泼酯法制备免疫原H-ICP-BSA、包被原H-ICP-OVA,抗原鉴定采用文献[8]的方法进行。在波长200~400 nm区间,对各人工抗原的紫外吸收光谱进行测定,鉴定半抗原与载体蛋白(BSA或OVA)是否偶联成功[9]。
人工抗原的紫外扫描结果表明,与相应载体蛋白BSA或OVA比较,偶联产物的最大紫外吸收峰在波长215~225 nm或270~280 nm范围发生了明显变化,其中由半抗原与蛋白质偶联所得到的人工抗原在225~250 nm内出现了强吸收峰,与相应蛋白的吸收峰比较,发生了红移,可能是由于这些半抗原具有共轭结构,在250 nm左右有强吸收峰或吸收带所引起的。

图3 H-ICP人工抗原紫外扫描谱图Fig.3 UV spectrum of H-ICP artificial antigens and hapten
1.2.3 多克隆抗体的制备
选取2只新西兰雌性大白兔用免疫原H-ICPBSA进行免疫,免疫剂量为500 μg/只。首次免疫,取抗原与弗氏完全佐剂乳化,采用背部多点免疫健康大白兔。间隔3周,取抗原与弗氏不完全佐剂乳化,加强免疫。以后免疫每隔2周进行免疫。取耳缘静脉血,采用ELISA方法测定抗血清效价。待效价稳定后,再加强免疫一次。最后一次免疫后10 d心脏采血,室温静置1 h,再置4℃冰箱12 h,4 000 r/min离心10 min,收集血清,-20℃保存。
2 结果与分析
2.1 半抗原的设计合成
根据分析,手臂位点和ICP特征结构将成为ICP半抗原设计的关键点,这也是研究ICP农药免疫速测技术的关键点。考虑到ICP主要有2部分特征结构组成,即甲氧基硫代磷酸酯部分和苯环部分,其中从硫代磷酸酯部分衍生出的手臂不但可以最大化的保留其特征结构,而且在与载体蛋白偶联后使苯环部分也充分的暴露出来可以增强免疫原性(见图1)。
2.2 抗体灵敏度的测定
采用间接竞争ELISA工作程序测定抗血清对ICP的竞争曲线,参照刘凤权等人[10]的方法,并采用Originlab 7.5的四参数拟合模块对间接竞争ELISA反应曲线进行 S拟合,计算曲线IC50值,以H-ICPOVA为包被原,建立间接ELISA标准曲线(见图4)。该方法的IC50为5.3 ng/mL,检定量线性范围(IC20~IC80)为1.77~10.06 ng/mL。

图4 水胺硫磷的间接ELISA标准曲线Fig.4 The icELISA standard curve of ICP
2.3 抗体的特异性研究
采用间接竞争ELISA程序在同等条件下依次建立水胺硫磷及其类似物的标准品ELISA曲线,求出各自抑制率为50%时的标准品浓度,用IC50表示,然后再换算成摩尔浓度后用公式计算出每种结构类似物与抗体的交叉反应率,则:交叉反应率/%=(水胺硫磷IC50/类似物IC50)×100
由表1可以看出所制备的抗体特异性非常好,获得的抗血清和其他结构类似物均无交叉反应,可用于果蔬中水胺硫磷的快速检测。
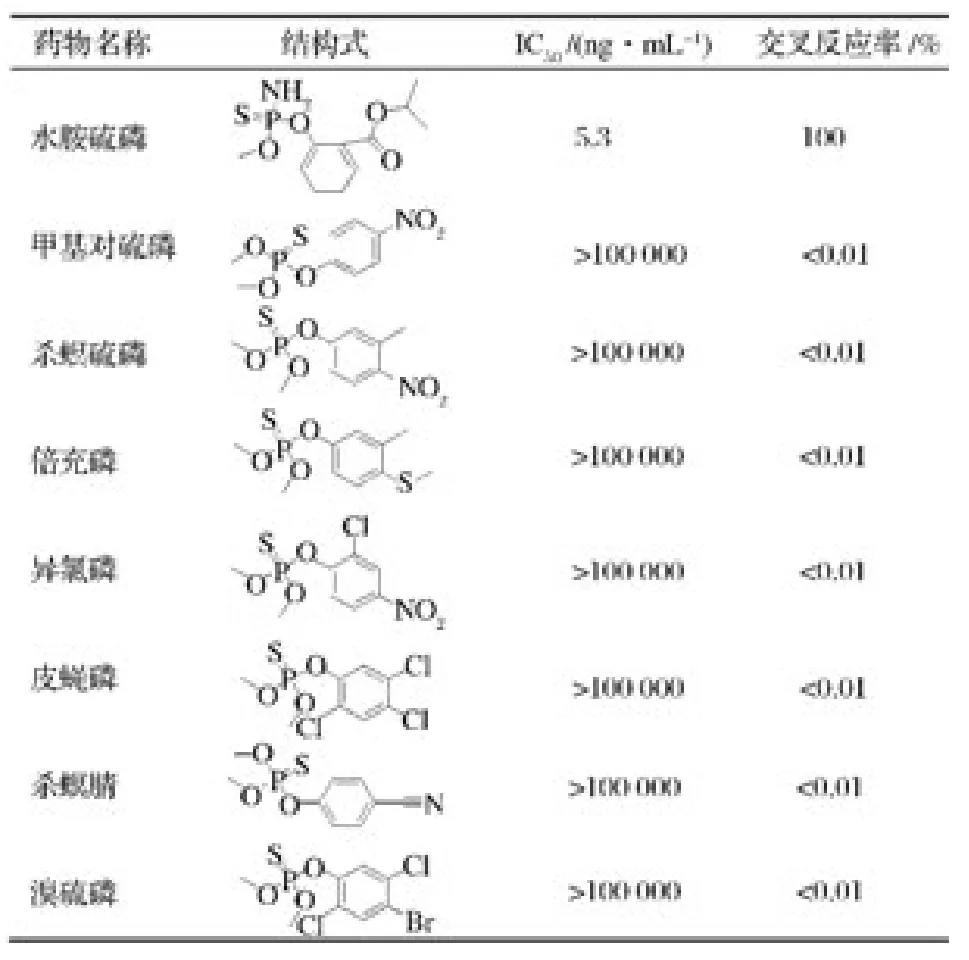
表1 水胺硫磷与结构类似物的交叉反应率结果(n=3)Table 1 Cross reactivity of ponoclonal antibody with analogous compound of ICP(n=3)
3 讨论
本实验通过设计合成水胺硫磷半抗原、制备人工抗原合成、动物免疫,首次获得针水胺硫磷的多克隆抗体,且该抗体对结构类似物均无明显的交叉反应,说明半抗原的结构设计合理,并为其单克隆抗体的研制、酶免分析方法的建立以及环境、食品中农药残留的快速检测提供了具有一定价值的研究基础和技术。
[1] Pehkonen S O,ZHANG Q.Critical Revi Environm[J].Science and Technology,2002,32(1):17
[2] 颜晓娜,许金生,王丽丽,等.水胺硫磷分子印迹传感器的制备与应用[J].分析试验室,2012,32(2):41-46
[3] 叶江雷,弓振斌,林芳,等.茶叶中水胺硫磷、亚胺硫磷、甲基对硫磷和伏杀硫磷农药残留的高效液相色谱法测定[J].厦门大学学报,2007,46(3):441-444.
[4] 楼国柱,徐倩,白晓荣,等.不同提取剂对茶叶中多种农药残留检测影响的研究[J].食品科学,2004,25(12):165-168.
[5] 杨小钢,邝培翠.气相色谱法测定蔬菜和小麦中乙基异柳磷和水胺硫磷两种农药残留量[J].湖北医科大学学报,1995,16(1):3-5
[6] Roger J,Hassan S,Emmanuel S,et al.Application of liquid chromatography with mass spectrometry combined with photodiode array detection and tandem mass spectrometry for monitoring pesticides in surface waters[J].Journal of Chromatography A,2000,879(1):51-71.
[7] Otero R R,Grande B C,Gandara J S.Multiresidue method for fourteen fungicides in white grapes by liquid-liquid and solid phase extraction followed by liquid chromatography-diode array detection[J].Journalof Chromatography A,2003,992(1/2):121-131.
[8] Cho Y A,Kim Y J,Hammock B D,et al.Development of a microtiter plate ELISA and a dipstick ELISA for the determination of the organophosphorus insecticide fenthion[J].Journal of Agricultural and Food Chemistry,2003,51(27):7 854-7 860.
[9] Singh K V,Kaur J,Varshney G C,et al.Synthesis and characterization of hapten-protein conjugates for antibody production against small molecules[J].Bioconjugate Chemistry,2004,15(1):168-173.
[10] 刘凤权,许志刚,王金生.定量测定甲胺磷残留的间接竞争ELISA的建立和初步应用[J].农业生物技术学报,1998,6(2):140-146.
