黄芪多糖组分-A1对豚鼠自身免疫性脑脊髓炎的抑制作用
2015-12-25郭喜霞,贾梅,齐恒田等
黄芪多糖组分-A1对豚鼠自身免疫性脑脊髓炎的抑制作用
郭喜霞贾梅1齐恒田2尹雅玲3潘国聘4赵繁荣4李鹏4
(新乡医学院第一附属医院,河南新乡453003)
摘要〔〕目的探讨黄芪多糖组分-A1(APS-A1)是对自身免疫性脑脊髓炎的抑制作用。方法用2.5、5、10 mg/kg 的APS-A1对自身免疫性脑脊髓炎豚鼠模型灌胃28 d。检测神经功能评分,血清含量,血浆白细胞介素(IL)-1、IL-2、IL-6、IL-10的含量及血浆神经肽Y(NPY)、阿片受体β-内啡肽(β-EP)的含量,并对神经元进行形态学观察。结果APS-A1剂量依赖性地抑制自身免疫性脑脊髓炎豚鼠神经功能评分下降、生化指标、神经递质及形态学等各项指标的变化(P<0.05)。结论APS-A1具有抑制自身免疫性脑脊髓炎的作用。
关键词〔〕黄芪多糖;自身免疫;脑脊髓炎
中图分类号〔〕R733.7〔
基金项目:河南省科技厅科技攻关项目(132102310247)
通讯作者:李鹏(1980-),男,副教授,硕士,主要从事天然药物活性成分研究。
1濮阳市卫生学校2新乡医学院第三附属医院
3新乡医学院基础医学院4新乡医学院药学院
第一作者:郭喜霞(1982-),女,住院医师,硕士,主要从事儿科学研究。
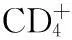
1材料与方法
1.1实验动物英国种短毛豚鼠,雄性,清洁级,4周龄,体质量(200±20)g(河南省实验动物中心提供,许可证号为SYXK-豫-005-0012)。动物房温度控制范围为18℃~22℃,环境洁净度为500 000~8 000级,相对湿度控制范围为40%~50%,换气次数控制范围为20次/h,气流速度控制范围为0.15~0.2 m/s,多级定向控制空气压差控制范围为10~15%,自动定时器控制光照周期(7:30~19:00为光照期,19:00~07:30为黑暗期),常规豚鼠饲料(河南省实验动物中心提供,许可证号为SYXK-豫-005-0012)及二次净化水饲养。
1.2药品APS-A1(实验室自备分离、纯化);醋酸泼尼松(武汉述元科技发展有限公司)。
1.3仪器及试剂Synergy H4全功能酶标仪(美国伯腾仪器有限公司); FACScan 型流式细胞仪(美国 Becton-Dickinson公司);IL-1、IL-2、IL-6、IL-10 ELISA 试剂盒(美国R-D公司);神经肽Y(NPY) 放射免疫试剂盒(天津杰瑞公司);阿片受体β-内啡肽(β-EP)放射免疫试剂盒(武汉博士德生物工程有限公司);转化生长因子(TGF)-β、基质金属蛋白酶(MMP)-2、一氧化氮合酶(NOS)、CD3免疫组化试剂盒(长沙力康生物有限公司)。
1.4方法
1.4.1EAE豚鼠模型制备豚鼠氯胺酮麻醉(5 ml/kg,腹腔注射),在无菌操作下,打开腹腔、胸腔,剪断两侧肋骨,用钝头针从心尖略偏左进针至主动脉,生理盐水灌注600 ml,4%多聚甲醛灌注固定。头部沿枕骨大孔处剪断,剥取脑和脊髓,去掉脊膜与马尾,称重,按照1∶3的质量比加入生理盐水并制备成25%的豚鼠全脊髓匀浆。豚鼠全脊髓匀浆和完全弗氏佐剂以2∶1 比例充分乳化制备成稳定的豚鼠全脊髓匀浆抗原乳剂待用。豚鼠氯胺酮麻醉(5 ml/kg,腹腔注射),将豚鼠全脊髓匀浆抗原乳(1 ml/kg)皮下注入豚鼠两个后足垫皮内,同时左后肢足背皮下注射百日咳原浆液(2 ml/kg),诱导 EAE 模型。免疫后每笼6只常规饲养。
1.4.2分组及处理豚鼠随机分5组,6只/组。①正常对照组:后足垫皮内注射等量生理盐水(1 ml/kg);②EAE模型组:按照本实验操作规定,注射豚鼠全脊髓匀浆抗原乳剂(1 ml/kg);③ 醋酸泼尼松组:注射豚鼠全脊髓匀浆抗原乳剂(1 ml/kg)后当日灌胃醋酸泼尼松(2 ml·kg-1·d-1);④ APS-A1低浓度组:注射豚鼠全脊髓匀浆抗原乳剂(1 ml/kg)后当日灌胃APS-A1(2.5 ml·kg-1·d-1);⑤ APS-A1中浓度组:注射豚鼠全脊髓匀浆抗原乳剂(1 ml/kg)后当日灌胃APS-A1(5 ml·kg-1·d-1);⑥ APS-A1高浓度组:注射豚鼠全脊髓匀浆抗原乳剂(1 ml/kg)后当日灌胃APS-A1(10 ml·kg-1·d-1)。第28天乙醚麻醉,指标检测。
1.4.3EAE神经功能评分从建模当天起观察每日发病情况,测体重1次/d,记录发病潜伏期、症状持续时间、发病率及病死率,并进行神经功能评分。EAE神经功能评分:0分:无明显异常;1分:尾部张力障碍;2分:后肢中度无力或麻痹;3分:后肢瘫痪,尿便失禁;4分:部分或完全前肢瘫痪;5分:濒死或死亡。每天进行3次神经功能评分,取均值作为每只豚鼠每天的神经功能评分。
1.4.5酶联免疫吸附法(ELISA)检测IL-1、IL-2、IL-6、IL-10按照ELISA试剂盒操作,450 nm单波长下,酶标仪读取标准管及测试管OD值。
1.4.6放射免疫法检测血浆NPY、β-EP的含量按照放射免疫试剂盒说明书要求操作,4℃冰箱过夜24 h,加入分离剂并充分混匀,室温放置20 min,4℃恒温3 000 r/min 离心20 min,弃去上清液。在γ计数仪上检测血清NPY、β-EP的含量。
1.4.7免疫组化检测脑组织TGF-β、MMP-2、NOS、CD3的含量按照免疫组化试剂盒说明书要求操作。200倍光镜下,每张切片随机选取5个视野,每个视野计数50个细胞,计数胞质呈棕黄色的阳性细胞。
1.4.8光镜下观察神经元形态豚鼠免疫后第28天乙醚麻醉,取出豚鼠脑,多聚甲醛固定,石蜡包埋,切片(3~4 μm),HE染色,光学显微镜下观察。
1.4.9电镜下观察神经元形态豚鼠免疫后第28天乙醚麻醉,取出豚鼠脑3~4块,每块1 mm大小,制作电镜切片,透射电镜下观察。
1.5统计学方法采用SPSS13.0统计软件进行单因素方差分析及SNK-q多重比较分析。
2结果
2.1EAE豚鼠神经功能评分EAE组豚鼠神经功能评分最高为2.5分,豚鼠相继出现进食减少、蜷缩少动、精神萎靡、皮毛干枯、大小便失禁、四肢无力及进行性全身瘫痪,部分豚鼠死亡;醋酸泼尼松组神经功能评分最高为0.45分,与同日EAE模型组比较有明显差异(P<0.05); APS-A1高浓度组神经功能评分最高为0.50分,与同日EAE模型组比较有明显差异(P<0.05)。见图1。
2.3血浆IL-1、IL-2、IL-6、IL-10的含量EAE模型组外周血IL-1、IL-2、IL-6、IL-10含量明显升高;与EAE模型组比较,醋酸泼尼松与APS-A1高浓度组的IL-1、IL-2、IL-6、IL-10均有明显差异(P<0.05)。见表2。
2.4血浆神经递质NPY、β-EP的含量EAE模型组外周血神经递质NPY、β-EP的含量明显升高;醋酸泼尼松组与APS-A1高浓度组明显抑制EAE豚鼠NPY、β-EP升高,与EAE模型组比较有明显差异(P<0.05)。见表2。
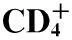
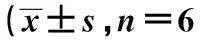
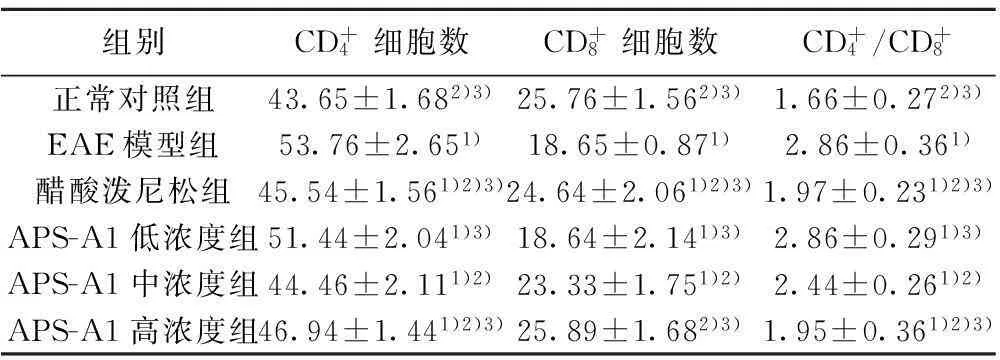
组别CD+4细胞数CD+8细胞数CD+4/CD+8正常对照组43.65±1.682)3)25.76±1.562)3)1.66±0.272)3)EAE模型组53.76±2.651)18.65±0.871)2.86±0.361)醋酸泼尼松组45.54±1.561)2)3)24.64±2.061)2)3)1.97±0.231)2)3)APS-A1低浓度组51.44±2.041)3)18.64±2.141)3)2.86±0.291)3)APS-A1中浓度组44.46±2.111)2)23.33±1.751)2)2.44±0.261)2)APS-A1高浓度组46.94±1.441)2)3)25.89±1.682)3)1.95±0.361)2)3)
与正常对照组比较:1)P<0.05;与EAE模型组比较:2)P<0.05;与APS-A1中浓度组比较:3)P<0.05,下表同
2.5脑组织TGF-β、MMP-2、NOS、CD3 含量EAE模型组豚鼠脑组织TGF-β降低、MMP-2升高、NOS升高、CD3升高;醋酸泼尼松组与PAS-A1高浓度组明显抑制豚鼠脑组织TGF-β降低、MMP-2升高、NOS升高、CD3升高,与EAE模型组比较有明显差异(P<0.05)。见表3。
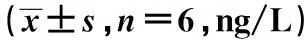
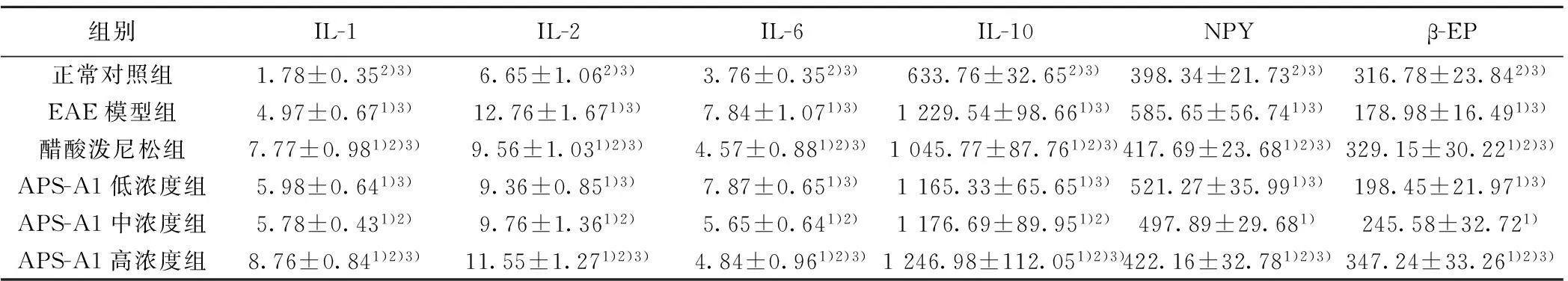
组别IL-1IL-2IL-6IL-10NPYβ-EP正常对照组1.78±0.352)3)6.65±1.062)3)3.76±0.352)3)633.76±32.652)3)398.34±21.732)3)316.78±23.842)3)EAE模型组4.97±0.671)3)12.76±1.671)3)7.84±1.071)3)1229.54±98.661)3)585.65±56.741)3)178.98±16.491)3)醋酸泼尼松组7.77±0.981)2)3)9.56±1.031)2)3)4.57±0.881)2)3)1045.77±87.761)2)3)417.69±23.681)2)3)329.15±30.221)2)3)APS-A1低浓度组5.98±0.641)3)9.36±0.851)3)7.87±0.651)3)1165.33±65.651)3)521.27±35.991)3)198.45±21.971)3)APS-A1中浓度组5.78±0.431)2)9.76±1.361)2)5.65±0.641)2)1176.69±89.951)2)497.89±29.681)245.58±32.721)APS-A1高浓度组8.76±0.841)2)3)11.55±1.271)2)3)4.84±0.961)2)3)1246.98±112.051)2)3)422.16±32.781)2)3)347.24±33.261)2)3)
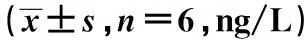

组别TGF-βMMP-2NOSCD3正常对照组20.65±3.332)3)6.76±1.472)3)13.65±1.232)3)12.60±1.292)3)EAE模型组12.67±0.691)3)32.73±2.731)3)36.63±4.051)3)36.56±5.451)3)醋酸泼尼松组17.87±0.831)2)3)7.17±1.471)2)3)16.55±2.551)2)3)12.37±1.751)2)3)APS-A1低浓度组14.65±0.641)3)25.77±4.721)3)32.83±4.661)3)32.35±3.981)3)APS-A1中浓度组15.58±0.491)15.54±3.901)22.40±3.651)25.64±2.671)APS-A1高浓度组17.56±0.641)2)3)10.53±1.971)2)3)16.96±1.961)2)3)14.96±1.761)2)3)
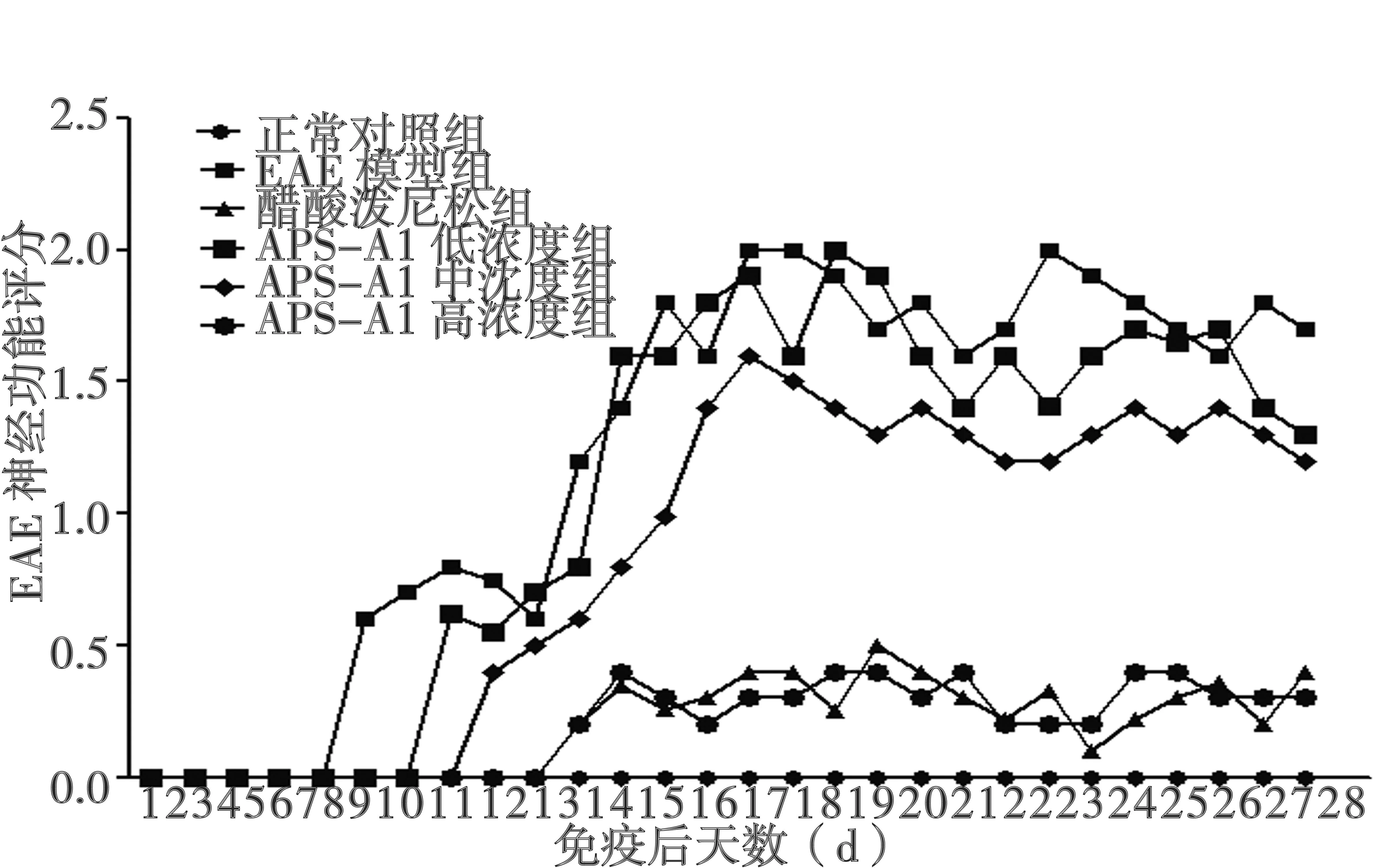
图1 各实验组EAE神经功能评分
2.6光镜下神经元形态EAE豚鼠大脑皮层神经元肿胀,并有炎细胞浸润,部分神经元胞体变小或呈三角形,基质疏松伴明显微空泡形成;醋酸泼尼松组和高浓度的APS-A1组明显抑制神经元凋亡现象。见图2。
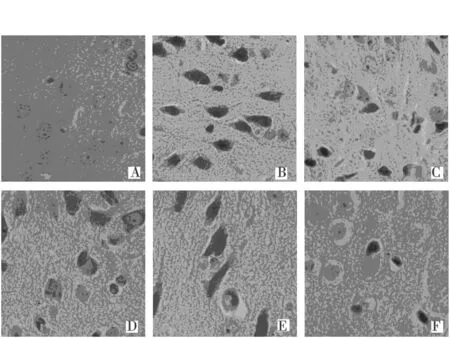
A.正常对照组;B.EAE模型组;C.醋酸泼尼松组;D.APS-A1低浓度组;E.APS-A1中浓度组;F.APS-A1高浓度组 图2 豚鼠大脑神经元光镜图像(HE,400×)
2.7电镜下神经元形态EAE豚鼠大脑皮层神经元皱缩、膜结构不清;胞核固缩,染色质聚集成团、异染色质增多,高尔基体增多,线粒体肿胀,嵴融合并出现空泡变性。醋酸泼尼松和高浓度的APS-A1组明显抑制神经元凋亡现象。见图3。
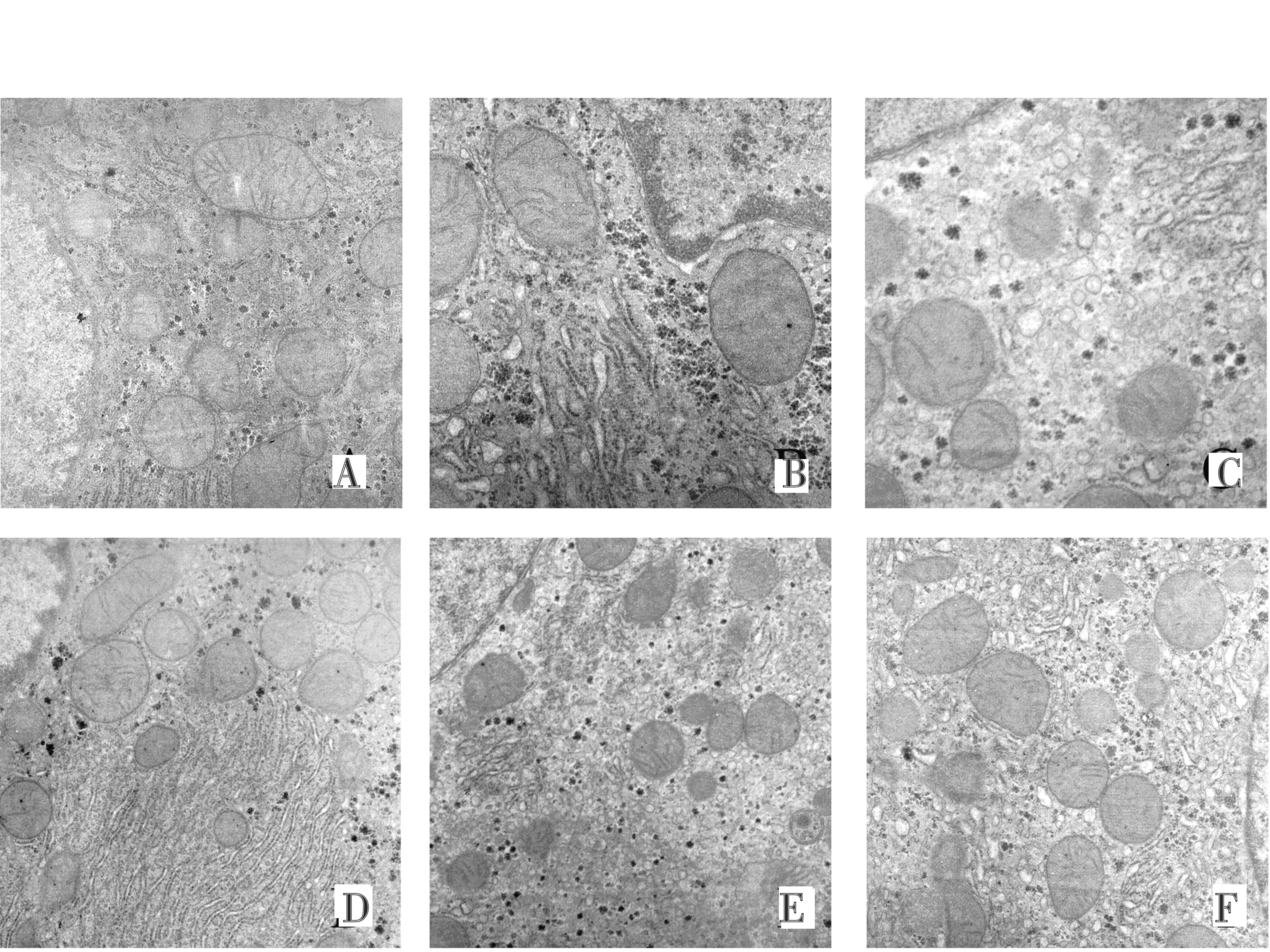
A.正常对照组;B.EAE模型组;C.醋酸泼尼松组;D.APS-A1低浓度组;E.APS-A1中浓度组;F.APS-A1高浓度组 图3 豚鼠大脑神经元电镜图像(8 000×)
3讨论
EAE在儿童中的发病几率较高,目前,糖皮质激素是治疗EAE的常用药物,具有抑制免疫应答、抗炎、抗毒、抗休克作用〔5〕。本研究结果显示,APS-A1(10 g·kg-1·d-1)能够推迟EAE发病时间,抑制EAE豚鼠神经功能下降,与醋酸泼尼松(2 g·kg-1·d-1)效果接近。
TGF-β对细胞的生长、分化和免疫功能都有重要的调节作用。活化的人MMP-2直接攻击血管基底膜,引起炎细胞浸润。NOS参与调节NO生成,NO是先天性免疫应答的调节性效应分子,作为一种信息传递物质维持正常的生理功能。CD3仅存在于T细胞表面,参与T细胞的信号转导。本结果显示,APS-A1(10 g·kg-1·d-1)抑制EAE豚鼠TGF-β、MMP-2、NOS、CD3的变化。APS-A1的作用与醋酸泼尼松类似,治疗EAE前景较好,其具体的作用机制有待进一步研究。
4参考文献
1Kwon HJ,Park YD.Determination of astragalin and astragaloside content in Radix Astragali using high-performance liquid chromatography coupled with pulsed amperometric detection〔J〕.J Chromatogr A,2011;12(16):1201-9.
2Kim MS,Kim SH.Inhibitory effect of astragalin on expression of lipopolysaccharide -induced inflammatory mediators through NF-κB in macrophages〔J〕.Arch Pharm Res,2011;34(12):2101-7.
3Kim GE,Kang HK,Seo ES,etal.Glucosylation of the flavonoid,astragalin by Leuconostoc mesenteroides B-512FMCM dextransucrase acceptor reactions and characterization of the products〔J〕.Enzyme Microb Technol,2012;50(1):50-6.
5Barnes D,Hughes RA,Morris RW,etal.Randomised trial of oral and intravenous methylprednisolone in acute relapses of multiple sclerosis〔J〕. Lancet,1997;349 (9056):902-6.
6Maimone D,Reder AT.Soluble CD8 levels in the CSF and serum of patient 25 with multiple sclerosis〔J〕.Neurology,1999;41(6):851-4.
7Panerai AE,Sacerdote P.Beta-endorphin in the immune system:a role at last〔J〕? Immunol Today,1997;18(7):317-9.
〔2012-12-20修回〕
(编辑安冉冉/曹梦园)
