高龄患者全胚冷冻后行解冻胚胎移植妊娠结局分析
2015-12-24李玉梅桂宝恒刘冬娥
李玉梅,桂宝恒,刘冬娥
(中南大学湘雅医院生殖医学中心,长沙 410008)
随着社会的进步,生育年龄逐渐延迟,高龄妊娠越来越多,同时随着我国二胎生育政策的开放,要求生育二胎的高龄患者也逐渐增多。众所周知,年龄是独立影响女性生育力的重要因素[1-2],女性在37~38岁时卵巢的储备卵泡数目明显下降,妇女的生育能力急剧下降。辅助生殖助孕成功率随着年龄增长而降低,卵母细胞获取率和胚胎可利用率降低,而胚胎碎片率增加,移植成功率降低,同时活产率降低而流产率增加。尽管辅助生殖技术为不孕患者带来了很多益处,但高龄患者成功并安全获得足月妊娠分娩的几率仍相对较低。如何提高高龄患者的妊娠率也是临床医师希望解决的一个重要临床问题。
随着冷冻技术的不断提高,冻融胚胎移植(FET)已经成为辅助生殖技术的一个重要组成部分。有文献表明,冻融胚胎移植后其临床妊娠率和活产率可达到甚至高于新鲜周期胚胎移植,同时,低体重儿及早产儿的出生比率低于鲜胚移植周期[3-7]。目前,全胚冷冻主要用于为防止卵巢过度刺激综合征(OHSS)或因其他各种原因不能行鲜胚周期移植的患者[8-12]。实施全胚冷冻是否能够改善高龄患者的临床妊娠结局,降低围产期母儿并发症,目前文献报道不多。本研究拟通过对2011年1月至2013年12月在我院生殖医学中心全胚胎冷冻后首次行FET 的147个周期高龄患者临床结局的回顾性分析,探讨全胚冷冻在高龄患者中的应用价值。
资料与方法
一、研究对象
收集2011年1月至2013年12月期间在本中心因各种原因行全胚冷冻且年龄≥38 岁的147个周期的患者临床资料,进行回顾性分析。
全胚冷冻原因包括:59 个周期(40.14%)行克罗米芬微刺激方案促排卵,内膜发育不良取消移植;28个周期(19.05%)因存在卵巢过度刺激倾向取消移植;24个周期(16.33%)因移植日发现宫腔积液取消移植;13 个周期(8.84%)黄体期取卵,内膜与胚胎发育不同步取消移植;10个周期(6.80%)取卵日发现孕激素升高取消移植;13个周期(8.84%)因感冒、肾结石绞痛、家人去世等个人原因取消移植。全胚冷冻患者取卵后休息2~3个月再行冻胚移植,休息期间无特殊治疗。
同时选取同期内年龄≥38岁的910个周期行新鲜胚胎移植的患者作为对照组。
二、控制性超促排卵和体外受精胚胎培养
根据患者的具体情况采用标准短效长方案或改良短方案或微刺激方案促排卵,当3个或以上卵泡平均直径≥18~20 mm 时肌注人绒毛膜促性腺激素(HCG,丽珠医药)5 000~10 000U 促卵母细胞进一步成熟,34~36h 后经阴道超声引导下取卵,按我中心的操作规则常规行IVF/ICSI及胚胎培养观察。如因各种原因不能行鲜胚移植,则将取卵后第3天(D3)可移植卵裂期胚胎行玻璃化冷冻。如无特殊情况,患者行第3天卵裂期胚胎移植,剩余可移植卵裂期胚胎亦行玻璃化冷冻。
三、卵裂期胚胎评级
根据我中心的胚胎评级标准,综合胚胎卵裂速度、卵裂球均匀程度及碎片比例,卵裂期胚胎分为4级。Ⅰ级胚胎:受精后第3天卵裂球7~10细胞,卵裂球大小均一,碎片<5%;Ⅱ级胚胎:受精后第3天卵裂球7~10细胞,卵裂球大小较均一,5%≤碎片≤20%;Ⅲ级胚胎:第3天卵裂球5~10细胞,碎片比例21~49%;Ⅳ级胚胎:碎片比例≥50%。Ⅰ~Ⅱ级胚胎为优质胚胎,Ⅰ~Ⅲ级胚胎为可移植胚胎。
四、FET 周期子宫内膜的准备
1.自然周期:月经周期规律患者于月经第10天开始定期B 超监测卵泡发育,排卵后第3天行胚胎移植,同时口服黄体酮胶丸(浙江爱生药业)200mg/d进行黄体支持。
2.激素替代周期:对于月经周期不规律或有排卵障碍的患者,于月经第3天开始口服戊酸雌二醇(拜耳医药,德国)6 mg/d,月经第10 天开始定期B超监测子宫内膜发育情况,同时根据内膜发育情况调整戊酸雌二醇剂量;当子宫内膜厚度≥8 mm时,加用微粒化黄体酮阴道栓剂(安琪坦,华杏制药,瑞士)600mg/d阴道给药行内膜转化,3d后行卵裂期胚胎解冻移植。
五、冻融胚胎解冻移植
胚胎解冻后有50%以上卵裂球存活的胚胎为存活胚胎。常规移植2枚存活胚胎。移植胚胎全部为D3卵裂期胚胎。同时,为降低多胎妊娠率的发生,我中心规定所有患者移植胚胎数均≤2 枚。移植2周后常规进行血HCG 的测定,阳性者3 周后行阴道超声检查,宫腔内见孕囊为临床妊娠。
六、统计学方法
使用SPSS 13.0统计软件,计量资料组间比较采用t检验,计数资料采用卡方检验,多因素变量与临床结局采用Logistic回归分析;P<0.05为差异有统计学意义。
结 果
一、两组患者一般资料的比较
研究组(FET 组)平均年龄大于对照组(鲜胚移植组),Gn用量及用药天数低于对照组,平均可移植胚胎数及优质胚胎数高于对照组,移植日子宫内膜厚度薄于对照组,差异均有统计学意义(P <0.05);两组间不孕年限、体重指数、基础FSH 浓度、平均获MII卵数、平均移植胚胎数均无统计学差异(P>0.05)(表1)。
二、两组患者临床结局比较
比较两组间的临床妊娠结局,临床妊娠率、种植率、流产率、活产率、多胎率等均无统计学差异(P>0.05);研究组妊娠周数及新生儿(双胎)出生体重均高于对照组,但无统计学差异(P>0.05);而研究组单胎出生体重显著高于对照组(P<0.05),单胎和双胎的早产发生率及妊娠期并发症发生率则显著低于对照组(P<0.05)(表2、表3)。
三、多因素对单胎体重影响的Logistic回归分析
因研究组与对照组在年龄、优胚获得率及内膜厚度等方面存在统计学差异,而妊娠结局中研究组单胎体重明显高于对照组,因此采用Logistic回归分析比较多因素对单胎体重的影响。结果表明,各因素单独对结局的影响均无统计学差异(P>0.05)(表4)。
表1 两组患者一般资料比较(±s)
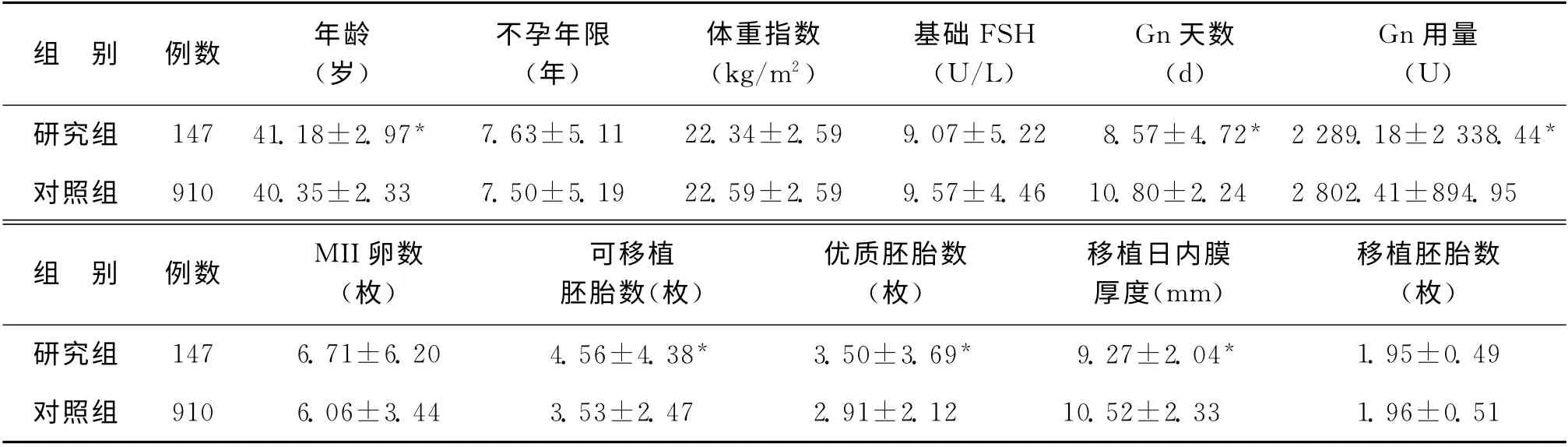
表1 两组患者一般资料比较(±s)
注:与对照组比较,*P<0.05
组 别 例数 年龄(岁)不孕年限(年)体重指数(kg/m2)基础FSH(U/L)Gn天数(d)Gn用量(U)研究组 147 41.18±2.97* 7.63±5.11 22.34±2.59 9.07±5.22 8.57±4.72* 2 289.18±2 338.44*对照组 910 40.35±2.33 7.50±5.19 22.59±2.59 9.57±4.46 10.80±2.24 2 802.41±894.95组 别 例数 MII卵数(枚)移植胚胎数(枚)研究组 147 6.71±6.20 4.56±4.38* 3.50±3.69* 9.27±2.04*可移植胚胎数(枚)优质胚胎数(枚)移植日内膜厚度(mm)1.95±0.49对照组 910 6.06±3.44 3.53±2.47 2.91±2.12 10.52±2.3 3 1.96±0.51
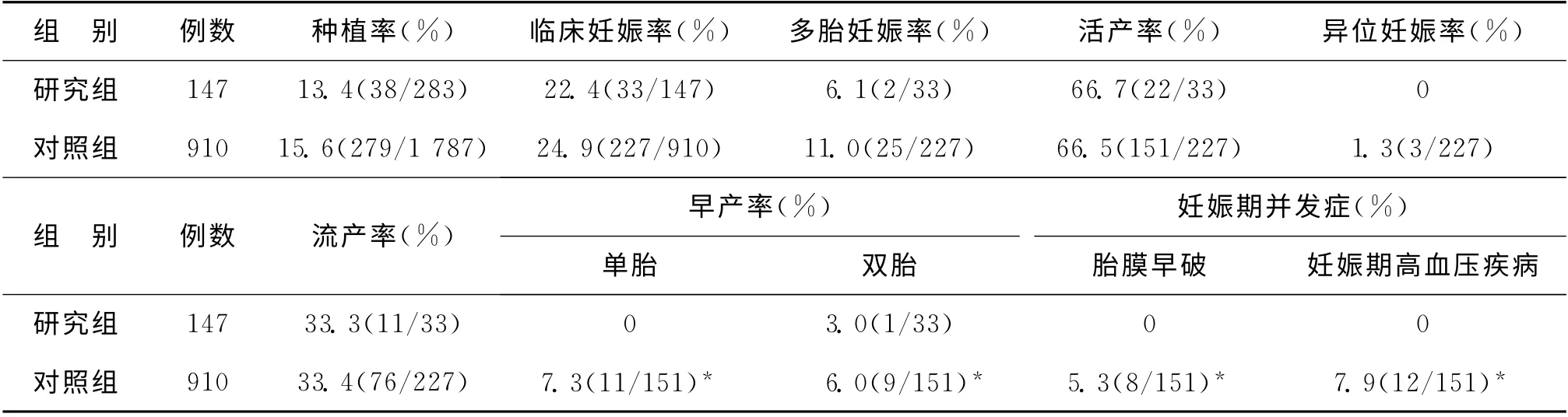
表2 两组患者临床妊娠结局比较
表3 两组患者孕周数及新生儿体重比较(±s)

表3 两组患者孕周数及新生儿体重比较(±s)
注:与对照组比较,*P<0.05;与单胎比较,#P<0.05
孕 周新生儿出生体重(g)组 别 例数单胎 多胎 单胎 多胎研究组 147 39.7±1.6 36.5±0.6# 3 521±377* 2 650±265#对照组 910 38.6±1.8 35.9±0.6# 3 166±624 2 522±588#
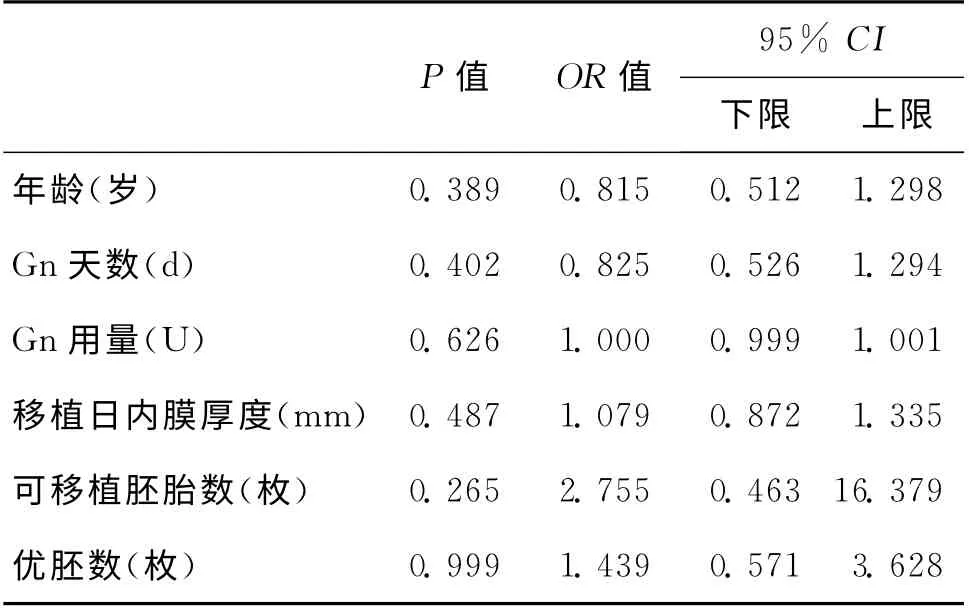
表4 多因素对单胎体重影响的Logistic回归分析
讨 论
本文回顾性分析了147个周期全胚冷冻后行冻融胚胎移植的高龄患者的临床结局,研究结果表明:冻胚移植周期的临床妊娠率和活产率与鲜胚移植周期相似;与鲜胚移植周期相比虽然无统计学差异,但是冻胚移植周期的单胎和多胎的孕龄有所增加;同时,冻胚移植周期的单胎出生体重明显高于鲜胚移植周期;早产发生率和妊娠期并发症发生率均明显低于鲜胚移植组。
有文献[4-5,13-16]表明年轻卵巢储备功能正常的患者实施辅助生殖助孕后全胚冷冻,行冻融胚胎移植可获得优于鲜胚移植的临床妊娠率和围产期结局。与文献报道相似,本研究中全胚冷冻的高龄患者,实施冻胚移植后,临床妊娠率与鲜胚移植组相似,但单胎出生体重明显高于鲜胚移植组;通过Logistic回归分析,两组中年龄、内膜厚度、所获优胚数等各项因素的差异对单胎出生体重的影响均无统计学意义。同时研究组的早产率和妊娠期并发症明显低于鲜胚移植组,获得了更好的围产期结局。目前导致这种结局的具体机制还不清楚,分析可能的原因是:(1)目前,评价胚胎发育潜力的标准仍以胚胎的形态学表现为主,鲜胚移植时主要是挑选形态学好的胚胎进行移植,但形态学好的胚胎不一定代表了胚胎的真实发育潜能,而经过胚胎冷冻和解冻过程,可能发育潜力差的胚胎被淘汰,筛选出了更优质的胚胎进行移植,从而能够获得更好的妊娠结局;(2)鲜胚移植周期超生理浓度的甾体激素水平可能影响胎盘形成和胎盘功能,进而影响临床结局;(3)本研究中全胚冷冻组平均获得的可移植胚胎数和优质胚胎数均高于鲜胚移植组,而平均获优质胚胎数较多者,移植胚胎时可选择高质量胚胎的几率更高,同样可能影响到妊娠结局。
查阅随访资料,本研究中妊娠期并发症主要为妊娠期高血压疾病及发生在妊娠37周前的胎膜早破,对于妊娠37周之后发生的胎膜早破,没有随访,因此无法纳入统计。高龄是妊娠高血压疾病的高危因素之一,而该疾病和胎膜早破是影响妊娠围产期结局的主要原因之一,本研究中全胚冷冻组妊娠高血压疾病及胎膜早破发生率均明显低于鲜胚移植组,从而获得了更好的围产期结局。因此,根据本文研究结果,可考虑通过全胚冷冻来改善高龄患者的围产期结局,值得大样本的前瞻性研究来证实。
众所周知,在辅助生殖助孕中,获得成功妊娠的影响因素包括优质胚胎与内膜的成功对话从而植入内膜继续发育。与优质胚胎相比,内膜容受性在多大程度上影响优质胚胎的植入,目前没有肯定答案。Shapiro等[5]研究表明:与冻胚移植组比较,与内膜容受性相关的多个基因的表达在促排卵周期组患者内膜中发生下调,而冻胚移植则消除了高剂量Gn及高甾体激素浓度对内膜的影响,因此认为冻胚移植优于鲜胚移植。本研究中全胚冷冻组与鲜胚移植组相比,种植率、临床妊娠率、多胎率、流产率均无显著性差异,与文献结果有所不同。分析可能的原因:本研究为回顾性分析,存在选择性偏倚,同时样本量较小,因此需要大样本的前瞻性研究来进一步证实。同时,需要优化胚胎评价系统,从而更客观科学地判断胚胎的发育潜力,也有利于判断胚胎与内膜对成功建立妊娠的影响。
本研究中冻胚移植组患者平均年龄显著高于鲜胚移植组,但促性腺激素用药天数和用药剂量却显著低于对照组,分析可能的原因在于促排卵方案的不同:在我院生殖中心,根据个体化用药原则,年龄越大或卵巢储备功能越差,偏向于改良短方案或克罗米芬微刺激方案促排卵,而对于相对较年轻或卵巢储备功能好的患者一般采用标准的短效长方案。而短效长方案患者相应的用药天数和用药量会高于改良短方案和微刺激方案的患者。本文中冻胚移植组促排卵方案中:长方案36周期(24.5%),短方案32周期(21.8%),微刺激方案及黄体期促排卵共72周期(50.0%),超长方案7周期(4.8%);而鲜胚移植组中长方案804周期(88.4%),短方案83周期(9.1%),超长方案23周期(2.5%)。冻胚移植组以微刺激方案促排卵为主,而鲜胚移植组主要以长方案促排卵为主,因此冻胚移植组的用药剂量及用药天数会明显少于对照组。虽然冻胚移植组患者年龄大于鲜胚移植组,但平均获卵数相似,而平均可移植胚胎数和优质胚胎数均高于鲜胚移植组,可能的原因在于用药剂量相对较少,减少了药物对卵母细胞发育的影响,因而能获得更多的优质胚胎,从而获得更好的临床妊娠结局。
大量研究已证实,单胎妊娠围产期并发症及预后优于多胎妊娠。为降低母儿围产期并发症,改善临床妊娠结局,降低多胎妊娠率,我中心从2010年开始减少了胚胎移植数目,不论年龄大小,平均移植胚胎不超过2个,因此本研究中两组平均移植胚胎数较少(1.95±0.49vs.1.96±0.51)。可以明显看出,不论是冻胚移植组还是鲜胚移植组,双胎新生儿妊娠周数及出生体重均明显低于单胎新生儿。
虽然本研究结果表明高龄患者行全胚冷冻后行冻胚移植能获得与鲜胚移植相似甚至优于鲜胚移植的临床结局,同时围产期结局明显优于鲜胚移植组,但全胚冷冻后再行冻胚移植不论在时间上还是经济上都增加了患者的负担,目前不适合全面推广,尚需经过大样本的前瞻性研究来进一步证实。
[1] ESHRE Capri Workshop Group,Fertility and ageing[J].Hum Reprod Update,2005,11:261-276.
[2] Egbert RV,Peter LP.The variability of female reproductive ageing[J].Hum Reprod Update,2002,8:141-154.
[3] Roque M,Lattes K,Serra S,et al.Fresh embryo transfer versus frozen embryo transfer in in vitro fertilization cycles:a systematic review and meta-analysis[J].Fertil Steril,2013,99:156-162.
[4] Aflatoonian A,Oskouian H,Ahmadi S,et al.Can fresh embryo transfers be replaced by cryopreserved-thawed embryo transfers in assisted reproductive cycles? A randomized controlled trial[J].J Assist Reprod Genet,2010,27:357-363.
[5] Shapiro BS,Daneshmand ST,Garner FC,et al.Evidence of impaired endometrial receptivity after ovarian stimulation for in vitro fertilization:aprospective randomized trial comparing fresh and frozen-thawed embryo transfer in normal responders[J].Fertil Steril,2011,96:344-348.
[6] Shapiro BS,Daneshmand ST,Garner FC,et al.Evidence of impaired endometrial receptivity after ovarian stimulation for in vitro fertilization:aprospective randomized trial comparing fresh and frozen-thawed embryo transfers in high responders[J].Fertil Steril,2012,96:516-518.
[7] Ulla-Britt W,Anna-Karina AH,Liv Bente R,et al.Perinatal outcomes of children born after frozen-thawed embryo transfer:a Nordic cohort study from the CoNARTaS group[J].Hum Reprod,2013,28:2545-2553.
[8] 杨美琼,马文敏,罗国群,等.全胚冷冻患者行解冻胚胎移植结局分析[J].广东医学,2013,34:1865-1867.
[9] 李攀,姜宏,陈京京,等.全胚冷冻后冻融周期移植的临床结局分析[J].实用医学杂志,2014,30:2580-2582.
[10] Eric SS,Laura JM,Marc GG,et al.Ovarian hyperstimulation syndrome and prophylactic human embryo cryopreservation:analysis of reproductive outcome following thawed embryo transfer[J].J Ovarian Res,2008,1:1-6.
[11] Srinivasan V,Tommy T,Azza F,et al.Elective cryopreservation of embryos at the pronucleate stage in women at risk of ovarian hyperstimulation syndrome may affect the overall pregnancy rate[J].Fertil Steril,2006,86:1773-1775.
[12] Anthony N,Awoniyi O,Anjali K,et al.Elective cryopreservation of all embryos with subsequent cryothaw embryo transfer in patients at risk for ovarian hyperstimulation syndrome reduces the risk of adverse obstetric outcomes:a preliminary study[J].Fertil Steril,2013,99:168-173.
[13] Pelkonen S,Koivunen R,Gissler M,et al.Perinatal outcome of children born after frozen and fresh embryo transfer:the finnish cohort study 1995-2006[J].Hum Reprod,2010,25:914-923.
[14] Shih W,Rushford DD,Bourne H,et al.Factors affecting low birthweight after assisted reproduction technology:difference between transfer of fresh and cryopreserved embryos suggests an adverse effect of oocyte collection[J].Hum Reprod,2008,23:1644-1653.
[15] Pinborg LA,Aaris Henningsen AK,Rasmussen S,et al.Infant outcome of 957singletons born after frozen embryo replacement:the Danish National Cohort Study 1995-2006[J].Fertil Steril,2010,94:1320-1327.
[16] Sazonova A,Kallen K,Thurin-Kjellberg A,et al.Obstetric outcome in singletons after in vitro fertilization with cryopreserved/thawed embryos[J].Hum Reprod,2012.27:1343-1350.
