脱氢表雄酮预处理对卵巢低反应患者体外受精-胚胎移植结果的影响
2015-12-24宋晖武雁田国华李砚滑玮黄艳红
宋晖,武雁,田国华,李砚,滑玮,黄艳红
(第四军医大学西京医院妇产科生殖中心,西安 710032)
卵巢低反应(POR)是卵巢对促性腺激素刺激(超促排卵)反应不良的病理状态,其发生率约占接受促性腺激素释放激素激动剂(GnRH-a)卵巢刺激或体外受精(IVF)治疗妇女的9%~24%并呈逐年增加趋势[1]。尽管临床上采取了一系列应对策略,如增加促性腺激素(Gn)用量、使用不同的降调节方案,然而临床妊娠率依旧低,周期取消率高。近年来,多项研究发现:脱氢表雄酮(Dehydroepiandrosterone,DHEA)能够有效改善卵巢储备功能,提高妊娠率,降低流产率[2-3]。但是由于缺乏大样本的研究,DHEA 对POR 患者的临床作用仍有争论。本研究旨在探讨使用DHEA 预处理对POR 患者卵巢功能及体外受精-胚胎移植结果的影响,为提高POR 患者辅助生殖治疗效果提供新思路。
资料和方法
一、研究对象
按照自愿原则选择2012年1月至2013年9月在本院妇产科生殖中心接受短方案体外受精-胚胎移植/卵胞浆内单精子注射(IVF-ET/ICSI)治疗的符合诊断标准及剔除标准的POR 患者共112例,年龄30~44岁,平均37.5岁;不育年限4~8年,平均5.5 年。按Doll’s临床病例随机表法,将患者随机分为DHEA 预处理的研究组和未用DHEA 处理的对照组,每组各56例;两组在年龄、不育年限、基础卵泡数等方面均无显著性差异,具有可比性(P>0.05)(表1)。
表1 两组一般情况比较(±s)
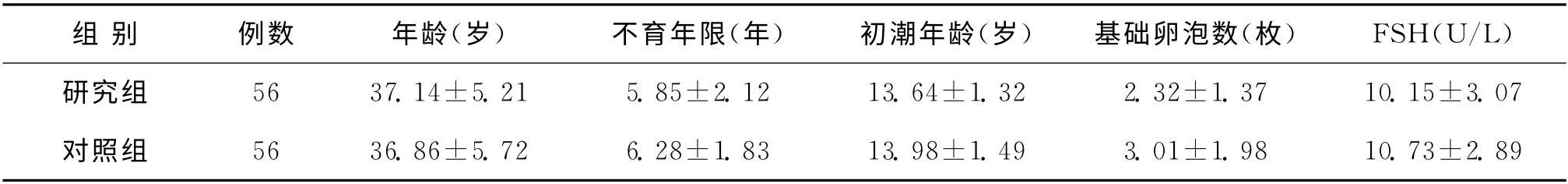
表1 两组一般情况比较(±s)
组 别 例数 年龄(岁) 不育年限(年) 初潮年龄(岁) 基础卵泡数(枚) FSH(U/L)研究组 56 37.14±5.21 5.85±2.12 13.64±1.32 2.32±1.3 7 10.15±3.07对照组 56 36.86±5.72 6.28±1.83 13.98±1.49 3.01±1.9 8 10.73±2.89
二、诊断标准
根据2011博格尼亚标准(Bologna criteria)[4],确定至少满足以下3 项中的2 项即可诊断POR:(1)女性高龄(≥40岁)或有其他POR 的危险因素;(2)曾有POR(常规卵巢刺激方案获卵≤3 个)史;(3)卵巢储备实验[如窦卵泡数(AFC)5~7个或抗苗勒管激素(AMH)为0.5~1.1ng/ml]异常。经过两个最大的卵巢刺激方案都出现卵巢低反应者也可认定为POR。
三、研究方法
1.方法:本研究为随机对照研究。将112例符合卵巢低反应诊断标准使用短方案进行IVF-ET/ICSI的患者随机分为经DHEA 预处理的研究组和未用DHEA 处理的对照组,每组各56例。研究组患者行降调节治疗前接受DHEA(25 mg/片,Lab Hercules,美国)25 mg,口服,tid,疗程为3 个月。经阴道B 超定期监测两组卵泡生长情况,并依据卵泡生长情况调整Gn 的用量。当双侧卵巢内至少有2个直径大于18mm 的卵泡时,给予人绒毛膜促性腺激素(HCG)6 000~10 000U。在注射HCG 36h左右取卵,根据男方精液情况,采用IVF或ICSI授精。在取卵后第3天进行胚胎移植,移植后给予黄体支持。移植后14d,检测血β-HCG>3U/L 诊为妊娠。移植后30d超声见妊娠囊、卵黄囊为临床妊娠。
2.观察指标:服药前后分别于月经第3 天测FSH 值、E2值,并经阴道B 超计数双侧卵巢内的基础卵泡数。对照组仅促排前于月经第3 天测FSH值、E2值,并经阴道B 超计数双侧卵巢内的基础卵泡数。比较研究组服用DHEA 后较对照组IVF 周期治疗参数的变化:Gn总量、获卵数、卵裂率、受精率、优质胚胎率、胚胎种植率、临床妊娠率、周期取消率及流产率。
四、统计学处理
数据均采用SPSS12.0统计软件包处理,计量资料用均数±标准差(±s)表示,组间比较用t 检验;计数资料用率(%)表示,组间比较用χ2检验;P<0.05为差异有统计学意义。
结 果
一、研究组用药前后卵巢储备功能比较
研究组服用DHEA 后FSH 值、E2值下降,窦卵泡数较用药前增加,差异有统计学意义(P <0.05)。用药后FSH/LH 值较用药前有所下降,但差异无统计学意义(P>0.05)(表2)。
表2 研究组用药前后卵巢储备功能参数的比较(±s)

表2 研究组用药前后卵巢储备功能参数的比较(±s)
注:与处理前比较 *P<0.05
例数 FSH(U/L) E2(pmol/L) FSH/LH 基础卵泡数(枚)DHEA 处理前 56 10.15±3.07 252.06±129.12 4.38±3.23 2.32±1.37 DHEA 处理后 56 7.43±3.04* 172.57±90.99* 4.21±2.77 4.68±2.12*
二、研究组服用DHEA 后与对照组相比
Gn 总量呈降低趋势但无统计学差异(P >0.05)、获卵数显著增加(P<0.05),卵裂率、受精率呈升高趋势但无统计学差异(P>0.05),优质胚胎率、胚胎种植率、临床妊娠率显著升高(P<0.05),周期取消率显著降低(P<0.05),而流产率无统计学差异(P>0.05)(表3)。
表3 两组患者IVF周期治疗结果的比较[(±s),n(%)]
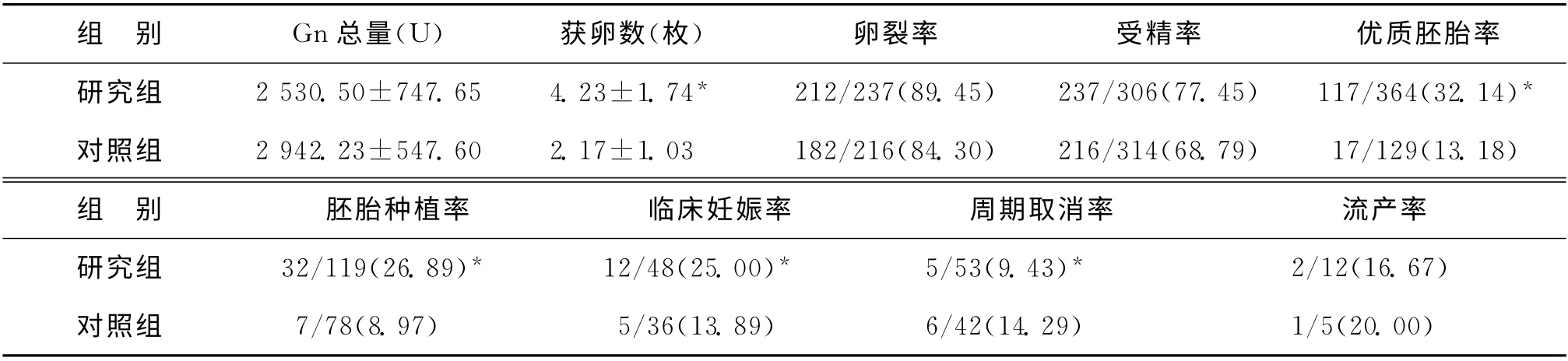
表3 两组患者IVF周期治疗结果的比较[(±s),n(%)]
注:与对照组比较 *P<0.05
组 别 Gn总量(U) 获卵数(枚)卵裂率 受精率 优质胚胎率研究组 2 530.50±747.65 4.23±1.74* 212/237(89.45) 237/306(77.45) 117/364(32.14)*对照组 2 942.23±547.60 2.17±1.03 182/216(84.30) 216/314(68.79) 17/129(13.18)组 别 胚胎种植率 临床妊娠率 周期取消率 流产率研究组 32/119(26.89)* 12/48(25.00)* 5/53(9.43)* 2/12(16.67)对照组 7/78(8.97) 5/36(13.89) 6/42(14.29) 1/5(20.00)
讨 论
DHEA 最先是由诺贝尔化学奖得主Butenadnt分离提取出来的一种不稳定的雄激素,在体内大部分以硫酸盐形式存在。近年来,多项研究发现DHEA 能够有效改善卵巢储备功能,提高妊娠率,降低流产率。Barad等[5]对POR 患者添加DHEA的病例-对照研究结果显示:DHEA 组临床妊娠率较对照组显著升高;周期取消率、流产率较对照组降低,但无统计学差异;认为DHEA 对POR 患者的临床妊娠率有所提高。Mamas等[6]报道5 名卵巢早衰(POF)患者经过3~7个月的DHEA 治疗后,均自然 妊 娠,只 有1 例 流 产。多 项 研 究[7-10]指 出DHEA 能改善卵巢储备功能低下患者的卵巢储备,提高其IVF-ET 的成功率。
本研究结果也显示:经DHEA 预处理的观察组用药后FSH 值、E2值下降,窦卵泡数较用药前增加(P<0.05);与对照组比较,治疗周期相关参数:Gn总量呈降低趋势、获卵数显著增加(P<0.05),卵裂率、受精率呈升高趋势,优质胚胎率、胚胎种植率、临床妊娠率显著升高(P<0.05),周期取消率显著降低(P<0.05),而流产率无统计学差异(P>0.05)。但是由于缺乏大样本的研究,DHEA 对DOR 患者的临床作用仍有争论,作用机制尚不明确。目前主要有以下几种推测:(1)雄激素可诱导颗粒细胞卵泡刺激素受体(FSHR)的生成,促进卵泡募集,增加可募集的卵泡数目[11];(2)DHEA 是类固醇激素合成必需的底物,雄激素是雌二醇的前体物质,DHEA异常低下可导致这些与卵泡生长和成熟有重要作用关系的激素含量低下[12];(3)DHEA 可降低胚胎非整倍体率,这至少可以部分解释胚胎质量提高和妊娠率增加[13];(4)DHEA 可改善卵巢功能低下患者的卵巢微环境,使其功能更年轻化,这可能与其改善卵母细胞、胚胎质量、增加妊娠率和降低流产率相关[14]。
国内外的多项研究及本研究结果提示:对卵巢低反应患者使用DHEA 预处理能有效改善其卵巢储备功能,增强促排卵效果,提高优质胚胎率和胚胎种植率,进而提高IVF-ET 的临床妊娠率。但是最近的Meta分析显示,尚无充足的证据证明DHEA或其他雄激素的有效性[15]。另外DHEA 的作用原理、不良反应以及远期影响都需要进一步研究。因此,今后还需进行大样本随机对照试验为临床应用DHEA 提供更有力的证据,其治疗的临床适应证、有效的给药方案、最佳的给药方式等还有待进一步研究探索。
[1] Ubaldi FM,Rienzi L,Ferrero S,et a1.Management of poor responders in IVF[J/OL].Reprod Biomed Online,2005,10:235-246.
[2] Wiser A,Gonen O,Ghetler Y,et al.Addition of dehydroepiandrosterone(DHEA)for poor-responder patients before and during IVF treatment improves the pregnancy rate:A randomized prospectivestudy[J].Hum Reprod,2010,25:2496-2500.
[3] 贾悦,潘芹芹,崔毓桂,等.脱氢表雄酮在骨质代谢中的作用[J].生殖医学杂志,2004,13:183-185.
[4] Ferraretti AP,La Marca A,Fauser BC,et al.ESHRE working group on poor ovarian response definition.ESHRE consensus on the definition of‘poor response’to ovarian stimulation for in vitro fertilization:the Bologna criteria[J].Hum Reprod,2011,26:1616-1624.
[5] Barad D,Gleicher N.Effect of dehydroepiandrosterone on oocyte and embryo yields,embryo grade and cell number in IVF[J].Hum Reprod,2006,21:2845-2849.
[6] Mamas L,Mamas E.Premature ovarian failure and dehydroepiandrosterone[J].Fertil Steril,2009,91:644-646.
[7] Sonmezer M,zmen B,Cil AP,et al.Dehydroepiandrosterone supplementation improves ovarian response and cycle outcome in poor responders[J/OL].Reprod Biomed Online,2009,19:508-513.
[8] Gleicher N,Weghofer A,Barad DH.The role of androgens in follicle maturation and ovulation induction:friend or foe of infertility treatment?[J].Reprod Biol Endocrinol,2011,9:116.
[9] Yakin K,Urman B.DHEA as a miracle drug in the treatment of poor responders;hype or hope?[J].Hum Reprod,2011,26:1941-1944.
[10] 安锦霞,王琰.脱氢表雄酮(DHEA)预治疗在体外受精-胚胎移植周期中的应用[J].生殖与避孕,2013,2:89-92.
[11] Nielsen ME,Rasmussen IA,Kristiansen SG,et al.In human granulosa cells from small antral follicles,androgen receptor mRNA and androgen levels in follicular fluid correlate with FSH receptor mRNA[J].Mol Hum Reprod,2011,17:63-70.
[12] McNatty KP,Makris A,Reinhold VN,et al.Metabolism of androstenedione by human ovarian tissues in vitro with particular reference to reductase and aromatase activity[J].Steroids,1979,34:429-443.
[13] Gleicher N,Weghofer A,Barad DH.Dehydroepiandrosterone(DHEA)reduces embryo aneuploidy:Direct evidence from preimplantation genetic screening(PGS)[J].Reprod Biol Endocrinol,2010,8:140.
[14] Barad D,Brill H,Gleicher N.Update on the use of dehydroepiandrosterone supplementation among women with diminished ovarian function[J].Assist Reprod Genet,2007,24:629-634.
[15] Bosdou JK,Venetis CA,Kolibianakis EM,et al.The use of androgens or androgen-modulating agents in poor responders undergoing in vitro fertilization:a systematic review and metaanalysis[J].Hum Reprod Update,2012,18:127-145.
