高效液相色谱-紫外检测器法测定高脂饮食小鼠血清中槲皮素含量
2015-12-21边会喜吴泽宇
边会喜,蔡 静,吴泽宇,张 弦,刘 健
(1.合肥工业大学生物与食品工程学院,安徽 合肥 230009;2.合肥工业大学 农产品生物化工教育部工程研究中心,安徽 合肥 230009)
高效液相色谱-紫外检测器法测定高脂饮食小鼠血清中槲皮素含量
边会喜1,蔡 静1,吴泽宇2,张 弦1,刘 健1
(1.合肥工业大学生物与食品工程学院,安徽 合肥 230009;2.合肥工业大学 农产品生物化工教育部工程研究中心,安徽 合肥 230009)
目的:建立用高效液相色谱-紫外检测器检测法测定饮食诱导的肥胖小鼠血清中槲皮素含量的方法。方法:色谱柱:Eclipse XDB-C18柱(4.6 mm×250 mm,5 μm);流动相:乙腈-0.2%甲酸溶液(40∶60,V/V);检测波长:360 nm;柱温:30 ℃;流速:0.50 mL/min。结果:槲皮素在2.5~40 μg/mL质量浓度范围内呈良好的线性关系(r=0.999 1),平均回收率为96.0%,相对标准偏差为10.98%(n=5)。结论:该方法具有良好的回收率和重复性。可以对血清中的槲皮素实现简便、快速、准确的检测。
高效液相色谱法;紫外检测器;高脂饮食;血清;槲皮素
槲皮素是一种典型的黄酮类物质,并且广泛分布在植物中,大多以甙的形式存在,经水解后可得槲皮素[1-2]。目前已经证实槲皮素具有多种对人体健康有益的生物功能,包括抗炎、抗氧化、抗肿瘤、抗血小板凝集等活性[3-7]。有体外实验证明槲皮素能够有效地改善肥胖和相关的胰岛素抵抗[8-10],另有研究证实槲皮素可以改善饮食诱导的肥胖模型、基因缺陷肥胖模型、化学诱导的糖尿病动物模型中胰岛素敏感性[11-13]。因此,在研究槲皮素对饮食诱导的肥胖小鼠作用机制的过程中,为了对槲皮素进行质量浓度控制和稳定性研究,本实验采用高效液相色谱紫外检测器法对高脂饮食添加槲皮素喂养的小鼠血清中槲皮素的质量浓度进行检测。
1 材料与方法
1.1 材料与试剂
槲皮素标准品(标准品号:Sigma-Q4951,≥95%,HPLC)、β-葡萄糖醛酸酶(标准品号:Type HP-2);乙酸乙酯、甲醇、乙腈为色谱纯、甲酸为分析纯,水为高纯水。
1.2 仪器与设备
1260 Infinity高效液相色谱仪(配有紫外检测器、ChemStation工作站)、Eclipse XDB-C18(4.6 mm×250 mm,5 μm)色谱柱 美国安捷伦公司;QT-1型旋涡混合器 上海琪特分析仪器有限公司;PURELAB Classic纯水仪 英国Elga公司;CT14RD高速冷冻离心机 上海天美生化仪器设备工程有限公司;MTN-2800D氮吹浓缩装置 天津奥特赛恩斯仪器有限公司;DHG-9101-2SA型电热恒温鼓风干燥箱 上海三发科学仪器有限公司;FA1204B型电子天平 上海精密科学仪器有限公司;DK-8D型电热恒温水槽 上海一恒科技有限公司。
1.3 动物培养及样品采集
将5 周龄的C57BL/6小鼠分为两组,每组8 只,分别喂养高脂饮食和添加0.1%槲皮素的高脂饮食,喂养12周。饮食配方如表1所示,其中高脂饮食基于“Research Diets D12451”,包含4.73 kcal/g和45%脂肪能量。在此基础上配制高脂饮食添加0.1%槲皮素的饲料。
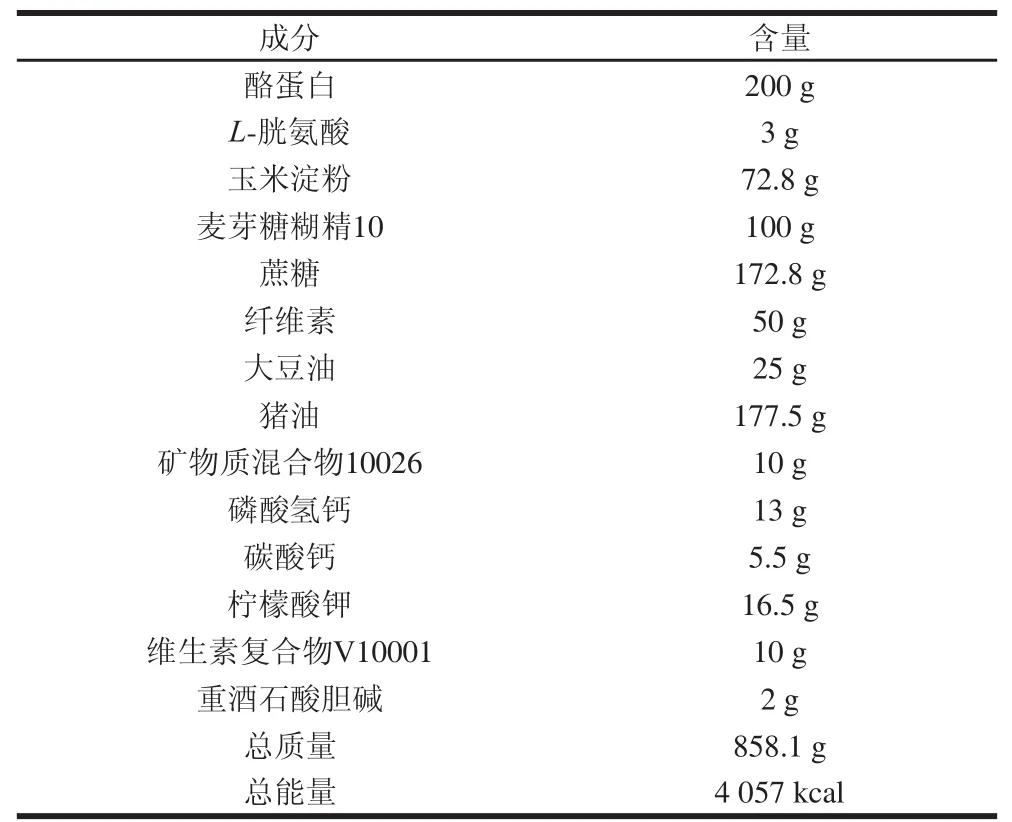
表1 实验动物饮食配方表Table1 The composition of experimental diet
所有的小鼠都在SPF级动物房中饲养,温度维持在25 ℃,并且循环维持12 h的光照和12 h的黑暗环境。小鼠可以自由的摄取水和食物。12 周以后小鼠禁食过夜,然用CO2窒息处死。血液从心脏中取出,4 ℃静置过夜,然后在5 000×g离心15 min收集血清,于-80 ℃储存备用。
1.4 方法
1.4.1 色谱条件
色谱柱:Eclipse XDB-C18柱(4.6 mm×250 mm, 5 μm);流动相:乙腈-0.2%甲酸溶液(40∶60,V/V);流速:0.5 mL/min;检测波长:360 nm;柱温:30 ℃;进样量:20 μL。
1.4.2 对照品溶液的配制
准确称取槲皮素对照品10.0 mg置于50 mL容量瓶中,用甲醇使其溶解并定容至刻度,摇匀,得200 μg/mL槲皮素对照品溶液。使用时根据需要稀释至质量浓度2.5、5.0、10.0、20.0、40.0 μg/mL。
1.4.3 样品溶液的配制
将血清从-80 ℃取出,在室温条件下融解,每个样品取样100 μL,加入10 μL抗坏血酸(0.1 mol/L)、100 μL高纯水及250 μL醋酸钠缓冲液(100 mmol/L,pH 5.0),简单混合后加入β-葡萄糖醛酸酶(HP-2型)(10 000 U),使用旋涡混合器混匀,置于37 ℃水浴中培养6 h。再使用2 mL的乙酸乙酯反复萃取3次。取乙酸乙酯部分并吹干,再用80 μL的95%的甲醇溶解,旋涡振荡。5 000 r/min离心6 min后待测。
2 结果与分析
2.1 检测波长的确定
槲皮素在360 nm波长条件下色谱峰的峰形和检测灵敏度符合检测要求,结合参考文献[14-15],最终确定360 nm作为检测波长。
2.2 流动相的选择
分别采用不同比例的甲醇-乙腈-磷酸、甲醇-乙腈-水-磷酸、乙腈-磷酸、乙腈-甲酸溶液为流动相[16-19],对样品的分离情况进行考察,当乙腈-0.2%甲酸(40∶60,V/V)时,槲皮素峰形较好。标准品色谱图如图1所示。
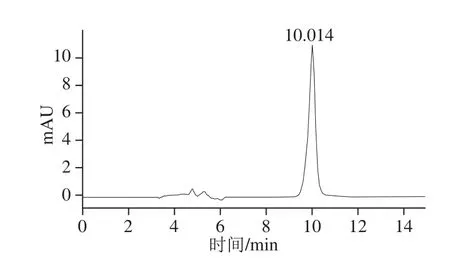
图1 槲皮素标准溶液色谱图Fig.1 HPLC-UV chromatogram of quercetin standard solution
2.3 线性关系和精密度实验
分别精密吸取5 组混合标准溶液20 μL,从低质量浓度到高质量浓度进样,每组重复3 次,按色谱条件测定其峰面积,以对照品在混合标液中的质量浓度(μg/mL)为横坐标、峰面积为纵坐标,得到的线性回归方程、相关系数、线性范围、检测限(RSN=3)、定量限(RSN=10)见表2。从标准溶液中取槲皮素质量浓度为10 μg/mL的一组溶液进行了3 次重复测定,结果表明槲皮素的相对标准偏差为3.96%。

表2 线性回归方程、相关系数、线性范围、检测限、定量限Table2 Linear equation with correlation coeffi cients and linear ranges, and limits of detection and quantitation
2.4 稳定性
取20 μg/mL标准溶液,在6 h内每2 h进样1 次,进样量20 μL,测定槲皮素的峰面积的相对标准偏差为0.93%。结果表明:供试品溶液在6 h内基本稳定。
2.5 加标回收率
取采用高脂饮食未添加槲皮素喂养的小鼠血清,分别添加不同量的槲皮素标准溶液,按照1.4.3节方法制备加标样品溶液,按规定的色谱条件进行测定,测定结果见表3。槲皮素平均回收率为96.0%,相对标准偏差为10.98%(n=5)。
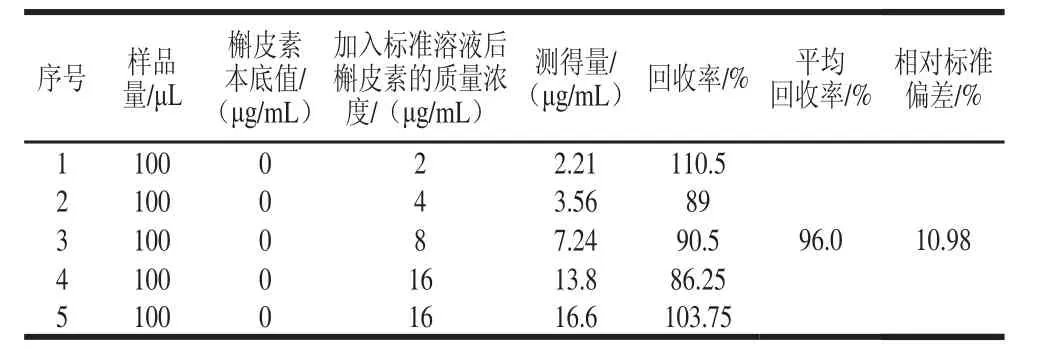
表3 方法回收率和精密度(n=5)Table3 Recovery and precision of the method (n = 5)
2.6 样品含量测定结果
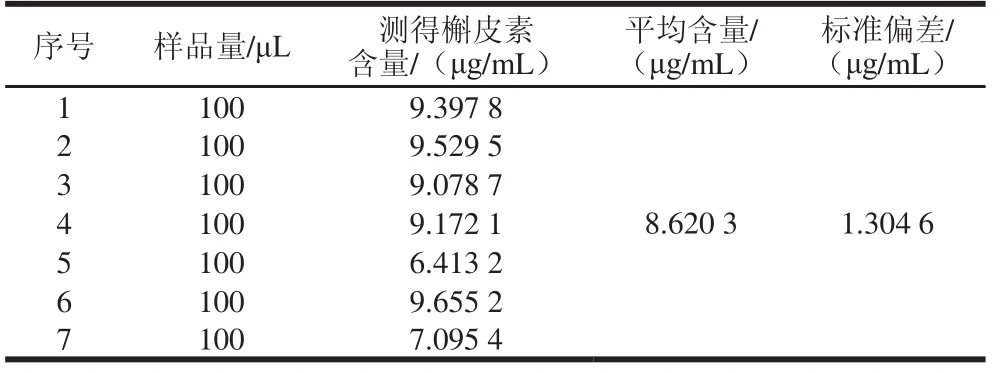
表4 高脂饮食添加槲皮素喂养的小鼠血清中槲皮素的测定结果(n=7)Table4 Contents of quercetin in serum of high fat diet (HFD)-fed mice ((n = 7))

图2 小鼠血清色谱图Fig.2 HPLC-UV chromatograms of mouse sera
将7 只高脂饮食添加槲皮素喂养的小鼠血清样本制备好,手动进样,并按色谱条件平行进行3 次测定,外标法计算样品中槲皮素的含量。测定结果见表4,样品色谱图见图2。测定结果表明该方法具有良好的回收率和重复性,可以对血清中的槲皮素实现简便、快速、准确的检测。
3 讨 论
本实验将高脂饮食诱导肥胖的小鼠饲料中添加槲皮素进行喂养,采集血清,对其中的槲皮素含量进行检测。在制备样品的过程中,为了防止槲皮素的氧化,加入抗坏血酸,并迅速检测[20-21]。槲皮素作为一种醇溶性物质,由于其结构上具有酚羟基,可能会导致酚羟基电离成苷元阴离子造成峰拖尾现象,因此流动相应偏酸性,以抑制离解,使色谱峰的峰形得到改善,因此流动相中加入甲酸[22-23]。有研究报道,大鼠灌胃槲皮素后的血浆中检测不到槲皮素原形药,而经过彻底的酸水解后可检测到槲皮素、异鼠李素等[24]。Graf等[25]发现,槲皮素经过大鼠体内代谢,血浆中产生大量的硫酸化的甲基槲皮素葡萄糖苷酸,说明血浆中的槲皮素以结合物的形式存在。因此采用β-葡萄糖醛酸酶水解后进行检测。而最终检测样品中目标峰的拖尾现象应该与槲皮素代谢物的水解有关,可用质谱做进一步的确认。
本实验建立了用高效液相色谱-紫外检测器检测法测定添加槲皮素的高脂饮食小鼠的血清中槲皮素的方法,并对其血清中所含的槲皮素含量进行了测定。结果表明,与相关报道的槲皮素质量浓度在同一数量级内[6-7]。本实验考察了色谱检测条件,同时对方法的精密度、稳定性及加标回收率等进行了考察,结果表明该方法相对准确、简便易行。
[1] 李素云, 李峥, 李敬来, 等. 槲皮素及其糖苷衍生物的研究进展[J].解放军药学学报, 2011(6): 540-543.
[2] 阿布拉江·克依木. 黄酮苷类天然产物的质谱分析方法研究[D]. 北京: 中国协和医科大学, 2006.
[3] 王艳芳, 王新华, 朱宇同. 槲皮素药理作用研究进展[J]. 天然产物研究与开发, 2003(2): 171-173.
[4] JAN A T, KAMLI M R, MURTAZA I, et al. Dietary flavonoid quercetin and associated health benefi tsan overview[J]. Food Reviews International, 2010, 26(3): 302-317.
[5] 周进, 方丽, 姚文秀, 等. 细胞培养氨基酸稳定同位素标记-质谱技术测定槲皮素对人肝癌细胞热休克蛋白表达的影响[J]. 中华肿瘤杂志, 2011, 33(10): 737-741.
[6] KOBORI M, MASUMOTO S, AKIMOTO Y, et al. Dietary quercetin alleviates diabetic symptoms and reduces streptozotocin-induced disturbance of hepatic gene expression in mice[J]. Molecular Nutrition and Food Research, 2009, 53(7): 859-868.
[7] STEWART L K, SOILEAU J L, RIBNICKY D, et al. Quercetintransiently increases energy expenditure but persistently decreases circulating markers of infl ammation in C57BL/6J mice fed a high-fat diet[J]. Metabolism, 2008, 57(7): 39-46.
[8] OVERMAN A, CHUANG C C, MCINTOSH M. Quercetin attenuates inflammation in human macrophages and adipocytes exposed to macrophage-conditioned media[J]. International Journal of Obesity, 2011, 35(9): 1165-1172.
[9] YANG Lei, LI Xiaofan, GAO Lei, et al. Suppressive effects of quercetin-3-O-(6’-feruloyl)-beta-D-galactopyranoside on adipogenesis in 3T3-L1 preadipocytes through down-regulation of PPARgamma and CEBPalpha expression[J]. Phytotherapy Research, 2012, 26(3): 438-444.
[10] AHN J, LEE H, KIM S, et al. The anti-obesity effect of quercetin is mediated by the AMPK and MAPK signaling pathways[J]. Biochemical and Biophysical Research Communications, 2008, 373(4): 545-549.
[11] KOBORI M, MASUMOTO S, AKIMOTO Y, et al. Chronic dietary intake of quercetin alleviates hepatic fat accumulation associated with consumption of a Western-style diet in C57BL6J mice[J]. Molecular Nutrition and Food Research, 2011, 55(4): 530-540.
[12] KIM J H, KANG M J, CHOI H N, et al. Quercetin attenuates fasting and postprandial hyperglycemia in animal models of diabetes mellitus[J]. Nutrition Research and Practice, 2011, 5(2): 107-111.
[13] JEONG S M, KANG M J, CHOI H N, et al. Quercetin ameliorates hyperglycemia and dyslipidemia and improves antioxidant status in type 2 diabetic dbdb mice[J]. Nutrition Research and Practice, 2012, 6(3): 201-207.
[14] 许春莲, 胡晓鹃, 邱奇琦, 等. 小鼠血浆中槲皮素脂溶性及水溶性代谢产物的分离与测定[J]. 食品科学, 2012, 33(6): 132-136.
[15] 陈燕. 荞麦蜂花粉中槲皮素、异鼠李素含量的测定[J]. 食品科技, 2009, 34(9): 267-269.
[16] 曾诚, 宓穗卿, 罗颂平, 等. 菟丝子灌胃大鼠槲皮素含量测定及药代动力学研究[J]. 中医药学刊, 2004(6): 1148-1150.
[17] 曾诚, 罗颂平, 宓穗卿, 等. 菟丝子活性成分槲皮素含量测定中HPLC方法的建立[J]. 中国中医药信息杂志, 2004(8): 701-703.
[18] 甘盛, 施晓光, 韩婷, 等. 高效液相色谱法同时测定葡萄籽中芦丁、槲皮素与异槲皮素的含量[J]. 中南药学, 2011(12): 894-897.
[19] 张丽华, 张阳德, 张洋, 等. 高效液相色谱法测定大鼠血浆中槲皮素的含量[J]. 中国现代医学杂志, 2011(5): 549-551.
[20] 王增仙. 高效液相色谱-质谱法测定血浆中槲皮素及其主要代谢产物[J]. 中成药, 2012(4): 750-753.
[21] ERLUND I, MARNIEMI J, HAKALA P, et al. Consumption of black currants, lingonberries and bilberries increases serum quercetin concentrations[J]. European Journal of Clinical Nutrition, 2003, 57(1): 37-42.
[22] 洪叶岚, 马骥, 肖娅萍, 等. 反相高效液相色谱法对秦岭21 种蕨类植物中槲皮素与山柰酚含量的测定[J]. 分析测试学报, 2010(3): 294-297.
[23] 董文庚, 邓晓丽, 苗凤智, 等. HPLC法测定银杏叶中黄酮的含量[J].理化检验: 化学分册, 2005(8): 563-565.
[24] 陈峰, 符乃光, 任守忠, 等. 液相色谱-质谱联用法测定大鼠血浆中的槲皮素代谢物[J]. 中国药学杂志, 2008(3): 225-227.
[25] GRAF B A, AMEHO C, DOLNIKOWSKI G G, et al. Rat gastrointestinal tissues metabolize quercetin[J]. The Journal of Nutrition, 2006, 136(1): 39-44.
Determination of Quercetin in Serum of High Fat Diet-Fed Mice by HPLC-UV
BIAN Huixi1, CAI Jing1, WU Zeyu2, ZHANG Xian1, LIU Jian1
(1. School of Biotechnology and Food Engineering, Hefei University of Technology, Hefei 230009, China; 2. Engineering Research Center of Bio-process, Ministry of Education, Hefei University of Technology, Hefei 230009, China)
The quercetin content of serum from diet-induced obese mice was determined by high-performance liquid chromatography fi tted with an ultraviolet detector (HPLC-UV) and an Agilent Eclipse XDB-C18column (4.6 mm × 250 mm, 5 μm). The mobile phase was a mixture of acetonitrile-0.2% formic acid (40:60, V/V) with a fl ow rate of 0.5 mL/min, and the detection wavelength was 360 nm. There was a good linear relationship for quercetin in the range of 2.5-40 μg/mL (r = 0.999 1). The average recovery rate for quercetin was 96.0% with relative standard deviation (RSD) of 10.98% (n = 5). This method could be used to determine quercetin in serum with good recovery rate and repeatability. It was a simple, rapid and accurate analytical method.
high performance liquid chromatography; ultraviolet detector; high fat diet; serum; quercetin
O657
A
1002-6630(2015)20-0086-04
10.7506/spkx1002-6630-201520015
2015-01-13
国家自然科学基金面上项目(31171315);中央高校基本科研业务费专项(2013HGQC0040)
边会喜(1983—),男,博士研究生,研究方向为食品生物技术。E-mail:bhx1983@163.com
