毛细管电泳法快速检测白酒中四种塑化剂研究
2015-12-20薛洪宝
张 晖 薛洪宝
(蚌埠医学院化学教研室 安徽蚌埠 233030)
塑化剂能够引起动物存活率下降、肝肾功能降低、体重减轻、红细胞减少和致癌性[1];它还能够引起动物更加严重的后果,如脊柱畸形、仔胎腭裂、眼睛缺陷、心脏变形等,接受塑化剂试验的小鼠睾丸体积可萎缩大约一半[2-6]。据统计资料表明,目前我国的塑化剂危害已经到了无处不在的程度,其使用范围之广,污染面积之大,影响人数之多,比农药、其它食品添加剂等更让人担心,而更令人忧虑的是,现在很少人能够意识到它的危害[7,8]。
塑化剂中以邻苯二甲酸酯类为主,其分子结构如图1所示。在我国该类塑化剂以邻苯二甲酸二丁酯(DBP)和邻苯二甲酸二辛酯(DNOP)居多[9]。
少量塑化剂添加到白酒中可使白酒的粘性增强,醇香长久,表面上提高了白酒的品质和档次。一般情况下,白酒产品中的塑化剂属于特定迁移,主要来源于酒泵进出乳胶管、塑料输酒管、塑料接酒桶、成品酒塑料内盖、封酒缸塑料布、成品酒塑料瓶包装、成品酒塑料袋包装或成品酒塑料桶包装等[10,11]。为了保证白酒饮用安全,很有必要建立一种快速、简便、灵敏的检测其中塑化剂的方法。
目前,白酒中塑化剂的检测方法主要有气相色谱法[12]、高效液相色谱法[13]、色谱-质谱联用法[14,15]等,这些方法不仅检测时间长、步骤复杂,而且对设备要求较高,不便于推广。但用毛细管电泳法检测白酒中的塑化剂鲜有报道。本研究旨在建立基于毛细管电泳法的4种邻苯二甲酸酯类塑化剂—邻苯二甲酸二异丁酯(DBP)、邻苯二甲酸苄基丁基酯(BBP)、邻苯二甲酸二异辛酯(DIOP)和邻苯二甲酸二异癸酯(DIDP)的检测方法,并以市售白酒为试验样品,验证该方法的可行性,为快速检测白酒中上述4种塑化剂提供快速、简便、灵敏的新方法。
一、实验部分
(一) 仪器与试剂。P/ACETMMDQ毛细管电泳系统(BeckmanCoulter,Fullerton,CA,USA),32Karat电泳分析软件及二极管阵列检测器(PDA)和未涂层熔融石英毛细管(75μmi.d.×50cm,有效长度40cm,河北永年锐沣色谱器件有限公司);FA/JA系列精密电子天平(精度:0.0001g,天津天马衡基仪器有限公司);KQ-100DE型数控超声波清洗器(昆山市超声仪器有限公司);pHS-3C酸度计(上海科学仪器有限公司)。
植酸钠,三羟甲基氨基甲烷(Tris),磷酸钠,十二烷基苯磺酸钠(SDBS),硼酸钠,十二烷基硫酸钠(SDS),无水乙醇,盐酸,氢氧化钠,甲醇,邻苯二甲酸二异丁酯(DBP),邻苯二甲酸苄基丁基酯(BBP),邻苯二甲酸二异辛酯(DIOP),邻苯二甲酸二异癸酯(DIDP)等,所用试剂均为国产分析纯;五种品牌白酒(购于本地超市);所用蒸馏水为双蒸水。
(二)塑化剂溶液及电泳缓冲溶液的配制。移取一定体积的DBP、BBP、DIOP和DIDP于50mL容量瓶里,加35mL无水乙醇溶解,再用双蒸水定容,摇匀。即得塑化剂混合溶液,备用。
分别配制0.1000mol·L-1植酸钠溶液(A);0.0500mol·L-1的Tris-HCl溶液(B)、磷酸钠溶液(C)、SDBS溶液(D)、硼酸钠溶液(E);10g·L-1SDS溶液(F),上述溶液以及无水乙醇(G)、双蒸水(H)按表1各溶液体积比要求混合即分别制得植酸钠、Tris-HCl、磷酸钠、SDBS、硼酸钠五个系列缓冲溶液,如C:D:F=0.5:1:0.5表示由C、D、F三种溶液按0.5:1:0.5的体积比混合制得的一种缓冲溶液。
(三)实验方法。
1.电泳分析条件。电泳毛细管:未涂层熔融石英毛细管75μmi.d.×50cm,有效长度40cm;缓冲溶液:0.0150mol·L-1的硼酸钠溶液,pH9.00;分离电压:+16kV;进样压力:0.5psi(3.45kPa);进样时间3.0s;分离温度:25℃;二极管阵列检测器。毛细管冲洗程序:0.1mol·L-1NaOH溶液冲洗2min;0.1 mol·L-1HCl溶液冲洗2min;双蒸水冲洗1min;缓冲溶液冲洗1min。每一次样品分析前运行上述冲洗程序。
2.塑化剂溶液及样品分析。分别以表1所示溶液为缓冲溶液,配制的塑化剂溶液为分析样品进样分析,得到相应的电泳图。根据电泳图选择合适的缓冲溶液和缓冲溶液的浓度,接着确定适宜的缓冲溶液pH和分离电压,即确定最佳电泳分析条件。最后按该电泳条件对塑化剂溶液和白酒样品进行分析。

表1 电泳缓冲溶液
二、 结果与讨论
(一)电泳条件的优化。
1.缓冲溶液及其浓度的选择。缓冲溶液及其浓度对毛细管电泳分离效果有相当明显的影响。分别考察了表1中植酸钠、Tris-HCl等五个系列缓冲溶液体系的分离情况,部分电泳图如图2所示。结果表明,硼酸钠缓冲溶液系列中硼酸钠溶液背景噪音及干扰影响较小,DBP等塑化剂的检测灵敏度较高,所以选用硼酸钠溶液为最佳缓冲体系;其它缓冲体系或者背景噪音较大,或者干扰影响较大,或者峰形展宽,或者塑化剂的检测灵敏度较低等原因不宜采用。
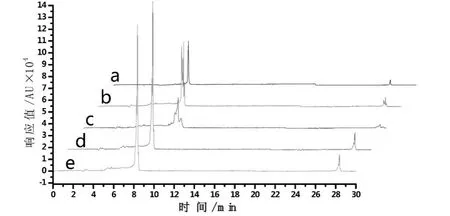
图2 不同缓冲溶液电泳图
在毛细管电泳中,缓冲溶液的浓度比较大时电流会比较大,产生比较多的焦耳热,使峰形变差;浓度较小时,电流信号较小,灵敏度较低。为获得良好的检测灵敏度和分离度,考察了硼酸钠溶液浓度分别为0.0075mol·L-1、0.0100mol·L-1、0.0150mol·L-1、0.0200mol·L-1、0.0300mol·L-1、0.0350mol·L-1对分离效果的影响,电泳图如图3所示。图3表明,0.0150mol·L-1硼酸钠溶液的迁移时间较短、分离效果较好、峰形较理想。因此,选用0.0150mol·L-1作为硼酸钠缓冲溶液的最佳浓度。

图3 不同硼酸钠浓度电泳图
2.分离电压的选择。在毛细管电泳分离过程中,电压对分离有较大影响。电压影响电渗流强弱及带电粒子迁移速率,从而决定组分迁移时间。本实验考察了不同电压(+8kV~+24kV)对各组分迁移的影响,电泳图如图4所示。由图4可知,电压小于+16kV时,迁移时间延长,电压过低时伴有管壁吸附现象,导致峰型变宽;电压大于+16kV时,迁移时间缩短,但基线噪声较大,电泳体系运行不稳定;电压等于+16kV时,信噪比较高,分离效果比较好,分析速度较快。综合考虑迁移时间、灵敏度、峰形和噪音等因素,选择+16kV作为最佳分离电压。
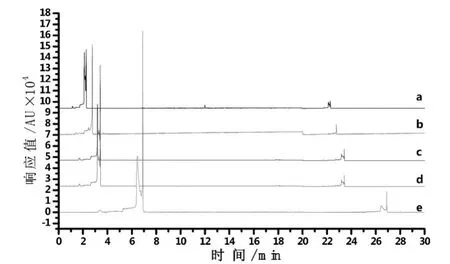
图4 不同电压条件的电泳图
3.缓冲溶液pH值的选择。pH值不仅对缓冲溶液中微粒所带电荷起决定作用,而且对电泳淌度也有影响,是毛细管电泳分离效果的关键因素。调节浓度为0.0150mol·L-1的硼酸钠缓冲溶液的pH值分别为:8.00、8.50、9.00、9.50和10.00,按上述实验方法进样分析,发现当缓冲溶液pH8.00、8.50时,毛细管内壁吸附性强,拖尾严重,重现性较差;当pH9.50、10.00时,电离作用强,电泳电流较大,焦耳热效应明显,分离效率降低;当缓冲液pH9.00时峰形较好,噪音小,分离效果最佳,并且电流适中。故选择pH9.00浓度为0.0150mol·L-1的硼酸钠缓冲溶液为最佳运行缓冲溶液。
通过对电泳缓冲溶液类型和浓度、分离电压、缓冲溶液pH等电泳因素进行考察,确立了电泳的最佳条件为:缓冲溶液为0.0150mol·L-1的硼酸钠溶液,pH9.00,分离电压为大于+16kV。
(二)方法重现性实验。在分析的最佳实验条件下,将DBP等塑化剂混合溶液平行进样4次,电泳图如图5所示。根据图5可得,DBP、BBP、DIOP和DIDP的峰面积的相对标准偏差(RSD)分别为9.02%、6.38%、3.48%和9.82%,如表2所示。
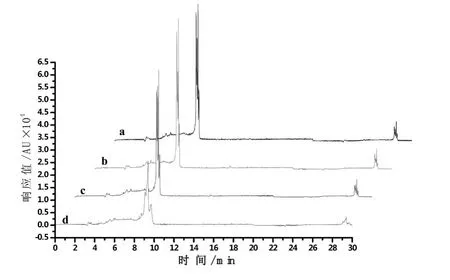
图5 重现性电泳图(n=4)

表2 重现性实验结果
(三)塑化剂混合溶液和白酒样品检测。在最佳电泳条件下分别将塑化剂混合溶液和白酒样品进样检测,电泳图如图6和图7所示。

图6 四种塑化剂的电泳图
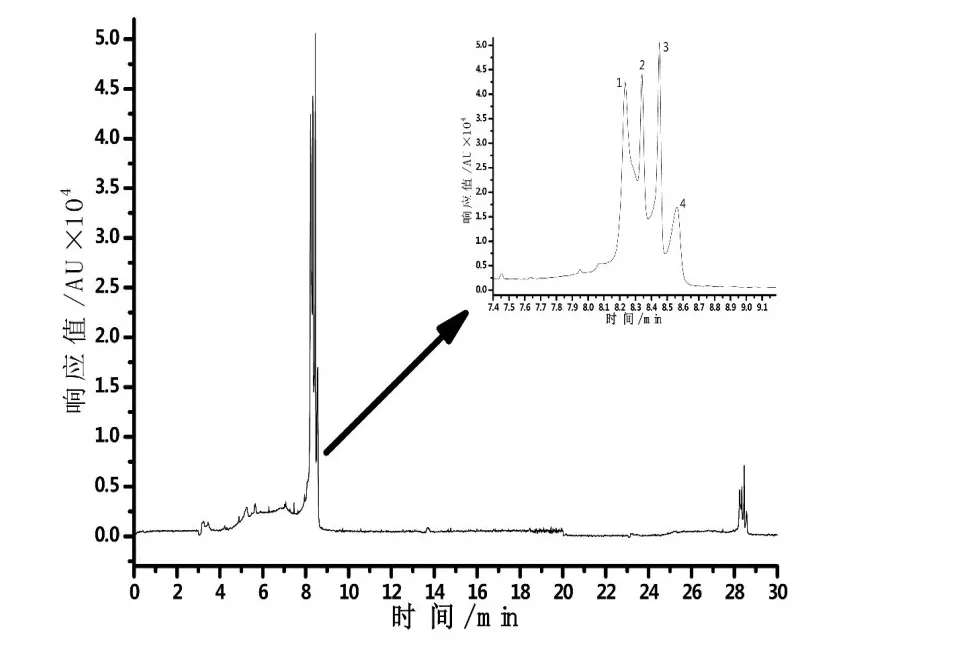
图7 五种白酒样品的电泳图
由图6和图7可知,白酒样品a含有DIOP;b含有BBP和DIOP;c含有DBP,但含量很低;d含有DBP和BBP;e含有DIOP和DIDP。
三、 结论
本实验采用毛细管电泳法建立了白酒中4种塑化剂检测方法。其最佳电泳分析条件为:缓冲溶液:0.0150mol·L-1的硼酸钠溶液,pH9.00;分离电压:+16kV;进样压力:0.5psi(3.45kPa);进样时间3.0s;分离温度:25℃;二极管阵列检测器。在该条件下对塑化剂溶液和当地超市的五种品牌白酒进行检测分析,根据电泳图可得出白酒样品中DBP等四种塑化剂的定性分析结果。
[1]Van Wezel A P, Van Vlaardingen, Posthumus R, et al.Environmental risk limits for two phthalates,with special emphasis on endocrine disruptive properties [J]. Ecotoxic Environ Safety,2000:46.
[2]孙利,陈志锋,雍伟等.与食品接触的塑料成型品中邻苯二甲酸酯类增塑剂迁移量的测定[J]. 中国卫生检验杂志,2008(3).
[3]顾钧,余雯静.食品塑料内衬中邻苯二甲酸二辛酯的HPLC 分析[J].苏州大学学报:自然科学版,2004(2).
[4]张娜,刘欣.邻苯二甲酸酯类化合物的研究进展[J].环境科学导刊,2009(3).
[5]JoseF,JimenezL,Rubios,etal.Determinationofphthalate esters in sewage by hemimicelles-based soild-phase extraction and liquid chro-matography-mass spectrometry[J].Analytica Chi mica Acta,2005:551.
[6]Li X.J,Zeng Z.R,Chen Y,et al.Determination of phthalate acid esters plasticizers in plastic by ultrasonic solvent extraction combined with solid-phase microextraction using calyx arene fiber[J].Talanta,2004:63.
[7]杨艳伟,朱英.化妆品中10 种邻苯二甲酸酯类化合物的高效液相色谱测定法[J].环境与健康杂志,2006(4).
[8]任仁.警惕邻苯二甲酸酯污染[J].大学化学,2003(6).
[9]胡晓宇,张克荣,孙俊红.中国环境中邻苯二甲酸酯类化合物污染的研究[J].中国卫生检验杂志,2003(1).
[10]曹国庆.白酒中塑化剂的危害与检测方法概述[J].科技资讯,2012(36).
[11]刘强.中国酒业协会声明:白酒中基本上都含塑化剂成分[N].生活晨报,2012-11-21.
[12]张前龙,王宇等.食品塑料包装中酞酸醋酯类环境污染物气相色谱测定方法的研究[J].中国卫生检验杂志,2009(12).
[13]黄丽雪,刘丽霞等.高效液相色谱法测定3 种邻苯类增塑剂检测条件的研究[J].包装工程,2012(17).
[14]邵栋梁.GC-MS 法测定白酒中邻苯二甲酸酯残留量[J].化学分析计量,2010(6).
[15]刘杰,郁宏燕等.液相色谱-串联质谱法测定饮料中16 种邻苯二甲酸酯[J].食品科学,2012(18).
