用盐酸浸出含钛高炉渣富集钛的试验研究
2015-12-16马光强
马光强,邹 敏
(攀枝花学院 生物与化学工程学院,四川 攀枝花 617000)
攀钢每年产出高炉渣约320万t,已累积6 000多万t,渣中TiO2质量分数为20%~23%,除少量用作混凝土填料外,其余大部分都露天堆放在渣场[1-2]。因此,研究含钛高炉渣的综合利用有重要的经济效益和社会效益。用硫酸浸出攀钢高炉渣,可以提取二氧化钛及三氧化二钪,但该法耗酸量大,生产成本高,对环境有一定污染[3];在1 200~1 300℃下,用NaOH改变含钛高炉渣的物相组成,然后可用水富集氧化钛,但该工艺烧碱用量大,成本高,且因硅酸钠的团聚造成钛的富集效果不理想[4];攀钢钢铁研究院将高炉渣高温选择性碳化,低温氯化制备TiCl4,但碳粉损失大,电极易断裂,氯化残渣难以处理[5];隋智通等[6]研究了含钛型高炉渣选择性浸出有价组分,工艺清洁,成本低,处理能力大,但因钙钛矿晶粒大小不一,以及与尖晶石共生,单体解离效果差,选别困难,且钙钛矿富钛料直接利用价值低,还需进一步去除氧化钙等杂质。
试验采用盐酸浸出法去除高炉渣中的酸溶性组分来富集钛。初步研究结果表明,该方法可选择性浸出钙、镁、铝、铁等组分,同时将绝大部分钛留于滤渣中,经固液分离后,滤渣中二氧化钛质量分数提升到40%以上,有望为高炉渣中钛资源的富集和综合开发利用提供一种新途径。
1 试验部分
1.1 试验原料、试剂与仪器
原料:高炉渣取自四川攀枝花钢铁集团公司巴关河渣场,经破碎、球磨、筛分,取粒度小于100目的炉渣备用,其化学成分见表1。
试剂:分析纯盐酸(科龙化学试剂公司)。
设备:JH-720可见光分光光度计(上海菁华公司),SX-1200℃箱式电炉(绵阳金冠公司),101-3BS型恒温鼓风干燥箱(常州科林公司)。
1.2 试验方法
根据计算的酸渣体积质量比,将一定体积和浓度的盐酸加入到反应装置中,加热至设定温度,再加入一定量高炉渣,搅拌反应一定时间后取出浆料,固液分离后,用去离子水洗涤,滤渣分析各元素质量分数,并进行XRD表征。
1.3 分析与表征
采用硫酸高铁铵标准溶液滴定法[7]测定高炉渣中的二氧化钛,采用EDTA络合滴定法测定钙、镁[8],采用邻二氮菲分光光度计法测定铁[9],采用二甲酚橙分光光度法测定铝。

表1 高炉渣化学成分 %
采用D/max-2500/PC型转靶X射线衍射仪进行XRD表征。
2 试验结果与讨论
盐酸与高炉渣中的各组分反应如下:
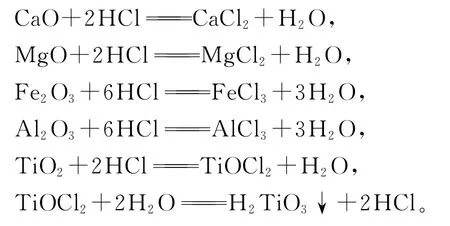
2.1 反应温度对各组分浸出率的影响
盐酸浓度6mol/L,酸渣体积质量比1.2∶1,反应时间5h,反应温度对高炉渣中各组分浸出率的影响试验结果如图1所示。
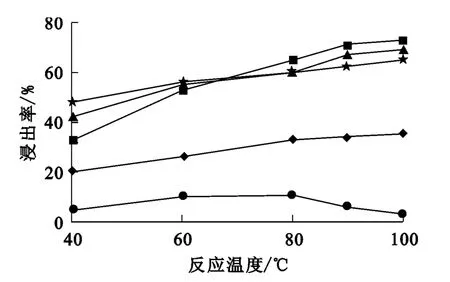
图1 反应温度对各组分浸出率的影响
由图1看出:随反应温度升高,Mg、Al、Fe浸出率急剧升高,温度升至90℃时趋于稳定;Ca浸出率随温度升高变化不大,因为钙钛矿与酸的反应活性较差;Ti浸出率随温度升高先增大后减小,因为随温度升高,进入溶液中的Ti4+易水解生成沉淀,致使滤渣中TiO2含量逐渐增加,90℃时达到40%。综合考虑,反应温度以控制在90℃较为适宜。
2.2 酸渣体积质量比对各组分浸出率的影响
酸渣体积质量比高,耗酸量大,且反应后产生的废酸多,处理成本高;酸渣比低,酸解不充分,因此选择合适的酸渣体积质量比非常重要。反应温度90℃,盐酸浓度6mol/L,反应时间5h,酸渣体积质量比对高炉渣中各组分浸出率的影响试验结果如图2所示。
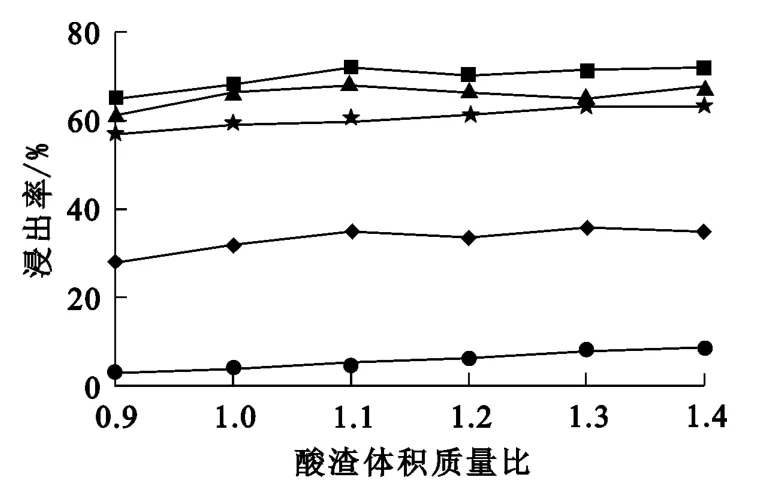
图2 酸渣体积质量比对各组分浸出率的影响
从图2看出,在酸足量前提下,酸渣体积质量比对各组分浸出率的影响较小,各组分浸出率均维持在较高水平,滤渣中TiO2含量也变化不大。考虑到成本及后续处理的便利,确定酸渣体积质量比以1.1∶1为宜。
2.3 反应时间对各组分浸出率的影响
反应温度90℃,酸渣体积质量比1.1∶1,盐酸浓度6mol/L,反应时间对各元素浸出率的影响试验结果如图3所示。

图3 反应时间对各组分浸出率的影响
从图3看出,随反应时间延长,Ca、Mg、Al、Fe浸出率增大;5h左右反应趋于平稳,各元素浸出率达到最高。Ti浸出率随浸出的进行而降低,这是由于随反应时间延长,液相中盐酸浓度逐步降低,溶液中TiCl4逐步水解,在反应5h后,Ti的浸出与水解趋于平衡,滤渣中TiO2含量达到最高。综合考虑,确定反应时间以5h为宜。
2.4 盐酸浓度对各组分浸出率的影响
反应温度90℃,酸渣体积质量比1.1∶1,反应时间5h,盐酸浓度对高炉渣中各组分浸出率的影响试验结果如图4所示。

图4 盐酸浓度对各组分浸出率的影响
从图4看出,盐酸浓度对各组分浸出率的影响比较明显:随酸浓度增大,Ca、Mg、Al、Fe浸出率显著增大,盐酸浓度>6mol/L后趋于平稳;而Ti浸出率总体上处于较低水平,仅略有增大,这是由于较高的盐酸浓度会逐步抑制溶液中TiCl4的水解,使得TiO2浸出率稍有提高。综合考虑,盐酸浓度以控制在5~6mol/L为宜。
2.5 综合试验
根据上述试验结果,在优化条件(温度90℃,反应时间5h,盐酸浓度6mol/L,酸渣体积质量比1.1∶1)下进行综合试验,结果Ca、Mg、Al、Fe浸出率分别为30%、71%、68%、65%。Ti浸出率小于6%,滤渣中TiO2质量分数最大为40%,钛得到初步富集。此外,酸浸得到含Ca、Mg、Al、Fe废液,可采用分步沉淀法及萃取法分离。
2.6 XRD分析
图5为含钛高炉渣浸出前后的XRD衍射图。可以看出:炉渣中的钛元素主要以钙钛矿(CaTiO3)和少量钛铁矿(FeTiO3)形式存在,其余主要物相为镁铝尖晶石(MgAlO2)和透辉石(CaMg(SiO3)2);盐酸浸出后,镁铝尖晶石和钛铁矿物相峰强明显减弱,而钙钛矿和透辉石的峰强无明显变化,说明酸浸过程中,Mg、Al已大部分转入到溶液中,而转入溶液中的Ti是以钛铁矿物相存在的那部分;此外出现偏钛酸(H2TiO3)物相的特征峰,说明钛在浸出过程中也同时水解生成偏钛酸。
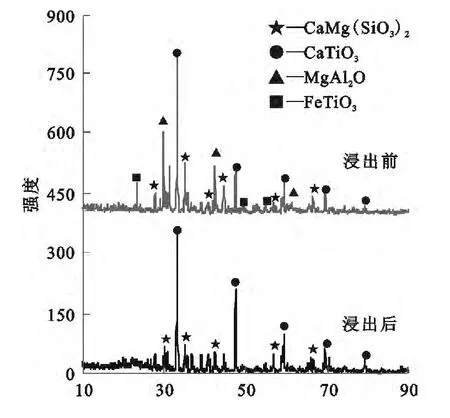
图5 高炉渣浸出前后的XRD图谱
3 结论
用盐酸浸出含钛高炉渣,可将TiO2富集到超过40%。适宜的酸浸条件为:反应温度90℃,酸渣体积质量比1.1∶1,反应时间5h,盐酸浓度5~6mol/L。在此条件下,Mg、Al、Fe浸出率在65%以上,Ti浸出率低于6%。酸浸过程中,镁铝尖晶石和钛铁矿大部分进入溶液,钙钛矿和透辉石浸出的较少。
[1]孟炳辰,张朝晖,巨建涛.高炉渣资源化循环利用现状及新途径[J].湿法冶金,2011,30(1):6-10.
[2] 曾丹林,刘胜兰,龚晚君,等.高炉尘泥渣综合利用研究现状[J].湿法冶金,2014,33(2):94-96.
[3]陈启福,张燕秋,方民宪.攀钢高炉渣提取二氧化钛及三氧化二钪的研究[J].钢铁钒钛,1991,12(3):30-35.
[4]周志明,张丙怀,朱子宗.高钛型高炉渣的渣钛分离试验[J].钢铁钒钛,1999,20(4):36-38.
[5]黄家旭,杨仰军,陆平,等.攀钢碳化高炉渣低温氯化试验研究[J].钢铁钒钛,2011,32(1):12-15
[6]隋智通,郭振中,张 力,等.含钛高炉渣中钛组分的绿色分离技术[J].材料与冶金学报,2006,5(2):93-97.
[7]周满秀,王晓霞.高炉渣中二氧化钛测定方法的研究[J].天津冶金,2005(5):35-37.
[8]郑小敏,汪雪梅,杨平,等.硫酸高铁铵滴定法测定制备金属钛的电解质熔盐中 Ti2+和 Ti3+[J].冶金分析,2011,31(10):29-33.
[9]陆娜萍,年季强,朱春要,等.微波消解-邻二氮菲分光光度法测定高炉渣中的全铁[J].光谱实验室,2012,29(5):3043-3045.
