髓样来源的抑制细胞在舌癌小鼠中的表达及意义
2015-12-16储眉廖贵清唐文周媛苏宇雄梁玉洁
储眉 廖贵清 唐文 周媛 苏宇雄 梁玉洁
1.广州市第八人民医院口腔科,广州 510440;2.中山大学光华口腔医学院·附属口腔医院口腔颌面外科,广州 510055;3.香港大学牙医学院口腔颌面外科,香港 999077
口腔鳞状细胞癌(oral squamous cell carcinoma,OSCC)是常见的头颈部恶性肿瘤,目前治疗以手术和放化疗为主,但患者5年生存率无明显提高[1]。OSCC患者存在着较严重的免疫缺陷,因此近年来提高机体免疫系统对抗肿瘤的免疫治疗成为研究热点[2-3]。在肿瘤浸润的白细胞中,髓样来源的抑制细胞(myeloid-derived suppressor cell,MDSC)是免疫抑制作用网络中的重要成员[4],构成了有着不成熟状态和抑制T细胞增殖作用的髓样细胞的异质群体。本研究建立4-硝基喹啉-1-氧化物(4-nitroquinoline-1-oxide,4NQO)舌癌小鼠模型,观察MDSC在舌癌小鼠中的表达,并探讨其在口腔癌中的意义。
1 材料和方法
1.1 4NQO舌癌模型建立
36只雌性4~6周龄的C57BL/6小鼠及标准固体饲料均由中山大学实验动物中心提供。在无特异病原体条件下饲养,室温18~25 ℃,湿度30%~50%,24 h光暗循环条件下,标准饲料经钴60辐照后喂养。4NQO用双蒸水配制成0.5 g·L-1母液。实验组24只小鼠用避光瓶喂养,4NQO母液用灭菌普通自来水配成50 mg·L-1工作液,每周更换4NQO水,连续饮用16周后,改为饮用普通灭菌自来水至第28周。对照组12只小鼠饮用普通灭菌自来水28周。
1.2 取材及组织病理学观察
在第16、20、24及28周时,6只实验组小鼠及3只对照组小鼠予4%水合氯醛镇静后经眼眶取外周血,处死后取全舌标本。舌标本一半立即冰冻固定用于实时定量聚合酶链反应(quantitative real timepolymerase chain reaction,qRT-PCR)或后续免疫组织化学染色,另一半立即固定于10%中性甲醛缓冲液中,24 h后乙醇梯度脱水,石蜡包埋,4 μm切片,常规苏木精-伊红(hematoxylin-eosin,HE)染色。
1.3 免疫组织化学染色
根据组织学结果,实验分为3组:正常对照组12只,异常增生组9只,OSCC组12只。采用葡聚糖聚合物法(labelled dextran polymer method,LDP),切片经脱蜡、修复抗原、灭活内源性过氧化物酶及室温封闭后,滴加anti-Ki67单抗4 ℃孵育过夜。加入二抗室温孵育,二氨基联苯胺(3,3'-diaminobenzidine,DAB)染色,苏木素复染。阴性对照省略一抗孵育步骤。光学显微镜400倍视野下观察切片并计数,计算阳性细胞百分比,每个样本取10个视野,计算均值,表示为标记指数(labeling indices,LI)。
1.4 流式细胞学分析
根据前述组织学结果分为3组的小鼠,再行流式细胞学分析。每只小鼠血液分为两份样本,分别加入30 μL血,一份用抗CD11b和粒性白细胞分化抗原-1(granulocyte-differentiation antigen-1,Gr-1)抗体,另一份用抗CD3、抗CD4和CD8抗体,进行荧光标记并染色。两份标本分别加入红细胞裂解液100 μL,室温裂解并PBS洗涤后进行流式细胞仪检测。
1.5 小鼠病变组织免疫组织化学染色
优化的切片温度(optimal cutting temperature,OCT)包埋的组织制成4 μm冰冻切片,冰丙酮固定,灭活内源性过氧化物酶,室温封闭后,Gr-1单抗1︰10后的切片4 ℃孵育过夜。加入生物素化二抗室温孵育,再加高灵敏度的链霉亲和素(high sensitivity streptavidin,HSS)-辣根过氧化物酶室温孵育后DAB染色,苏木素复染。阴性对照省略一抗孵育步骤。光镜下观察切片。
1.6 qRT-PCR
分组同前述。采用Trizol法提取舌病变组织内总RNA,将提取的总RNA逆转录为cDNA用于聚合酶链反应(polymerase chain reaction,PCR)扩增。实验引物如下。精氨酸酶1(arginase 1,ARG-1)上游引物序列:5'-GAAGAACCCACGGTCTGTGG-3',下游引物序列:5'-TCCAACTGCCAGACTGTGGTC-3'; 甘油醛-3-磷酸脱氢酶(glyceraldehyde-3-phosphate dehydrogenase,GAPDH)上游引物序列:5'-CGTGTTCCTACCCCCAATGT-3',下游引物序列:5'-TGTCATCATACTTGGCAGGTTTCT-3'。PCR反应条件:93 ℃ 3 min,93 ℃ 30 s,55 ℃ 45 s,共40个循环。将每个样本mRNA水平与相应GAPDH表达水平之比得到目的基因的标准化表达水平,再与正常小鼠的表达水平相比较,计算出表达倍数。
1.7 统计学分析
采用SPSS 16.0软件进行统计学分析,所得数据用均数±标准差表示。MDSC的数值是占外周血细胞的百分比,CD3+CD4+和CD3+CD8+的数值是占淋巴细胞总数的百分比。组间差异的比较采用ANOVA分析。Spearman相关系数用于评价两个指标间的相关性。P<0.05认为差异有统计学意义。
2 结果
2.1 4NQO诱导小鼠舌组织癌变
在第28周观察期结束时,每只实验组小鼠口腔黏膜都出现一个或以上病变,病变部位多位于舌背黏膜,呈现乳头状或菜花状新生物,伴轻微糜烂现象。随时间延长,实验组小鼠出现了由正常黏膜,经上皮单纯性增生,到异常增生,最终发展成早期浸润癌的组织学变化过程。第16周时6只4NQO诱导(实验组)小鼠有3只(50%)出现异常增生,3只(50%)出现单纯性增生;20周时6只实验组小鼠有4只(67%)出现异常增生,2只(33%)出现浸润癌;24周时6只实验组小鼠有2只(33%)出现异常增生,4只(67%)出现浸润癌;28周时6只(100%)实验组小鼠出现浸润性癌(图1)。同时间点的3只对照组小鼠均未发现异常增生、上皮层次紊乱等变化。根据组织学结果,后续实验分为3组:异常增生组9只,OSCC组12只,正常对照组12只。

图1 小鼠舌黏膜的染色结果 HE × 200Fig 1 Staining results in tongue mucosa of mice HE × 200
2.2 Ki67免疫组织化学染色
正常舌黏膜基底层细胞胞核呈现Ki67阳性染色,LI为20.31%±2.42%;在上皮单纯性增生时,Ki67表达不仅位于基底细胞层,有的甚至累及基底细胞上层,LI为25.08%±2.14%;在上皮异常增生区域,阳性表达进一步增加,LI为31.11%±3.58%;Ki67在OSCC中呈弥散性表达,LI为46.75%±3.46%。单纯增生组、异常增生组和OSCC组LI明显高于正常组(图2)。
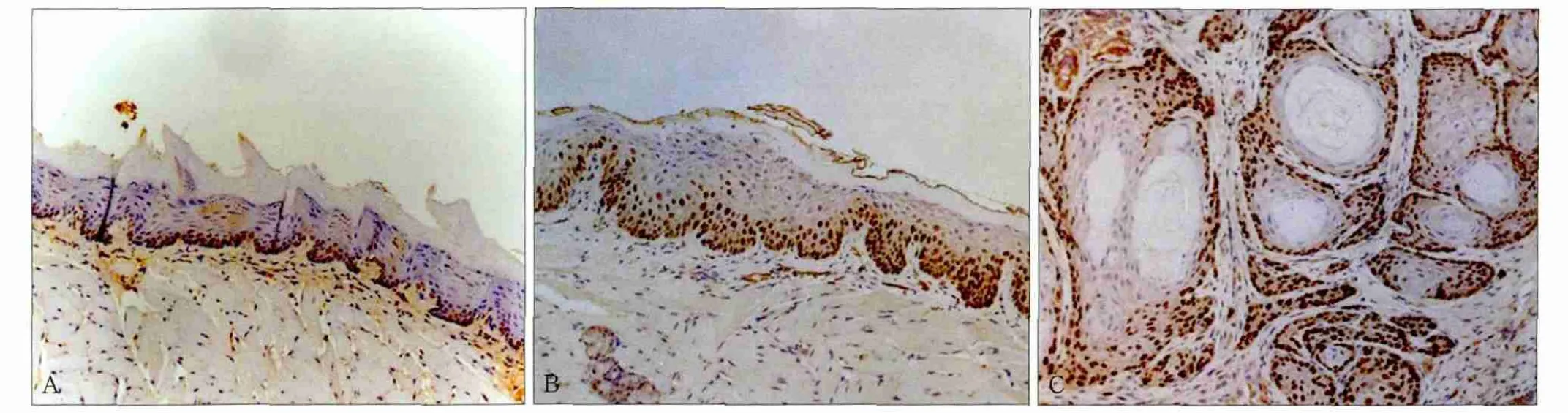
图2 小鼠舌黏膜Ki67免疫组织化学染色结果 LDP × 200Fig 2 Ki67 immunohistochemical staining in tongue mucosa of mice LDP × 200
2.3 MDSC细胞和T细胞亚群在外周血的变化
在肿瘤进展过程中,从正常对照组到异常增生和OSCC组,外周血MDSC细胞持续显著增加(P<0.01)。OSCC组CD3+CD8+细胞百分比较正常对照组与异常增生组明显升高(P<0.01),但正常对照组与异常增生组间无明显变化(P=0.062)。当3组比较时,CD4+/CD8+比差异有统计学意义(P<0.01)。配对比较发现各组之间差异均有统计学意义(P<0.05),然而,CD3+CD4+细胞未发现明显增加(P=0.534)(表1、图3)。
2.4 小鼠外周血中MDSC细胞与T细胞亚群及CD4+/CD8+比相关性分析结果
相关性分析发现,MDSC细胞与CD3+CD8+细胞呈现正相关(r=0.772,P<0.01),MDSC细胞比例与CD4+/CD8+比呈现负相关(r=-0.830,P<0.01),但MDSC细胞与CD3+CD4+细胞无明显相关(r=0.181,P>0.05)。

表1 不同病理分级时小鼠外周血细胞亚群的比例Tab 1 Frequency of peripheral blood cell subsets in mice with different pathological classification
2.5 MDSC细胞在病变组织中的表达
在实验组小鼠的舌黏膜中,表达阳性Gr-1的免疫细胞(MDSC细胞)的细胞膜呈棕黄色(图4)。异常增生区域的MDSC细胞较正常对照组有所增加,在OSCC区域的肿瘤组织内及与正常组织的交界处,均浸润了大量的MDSC细胞。

图3 外周血中MDSC细胞和T细胞亚群细胞流式分析结果Fig 3 Flow cytometric analysis of MDSC and T cell subsets in peripheral blood
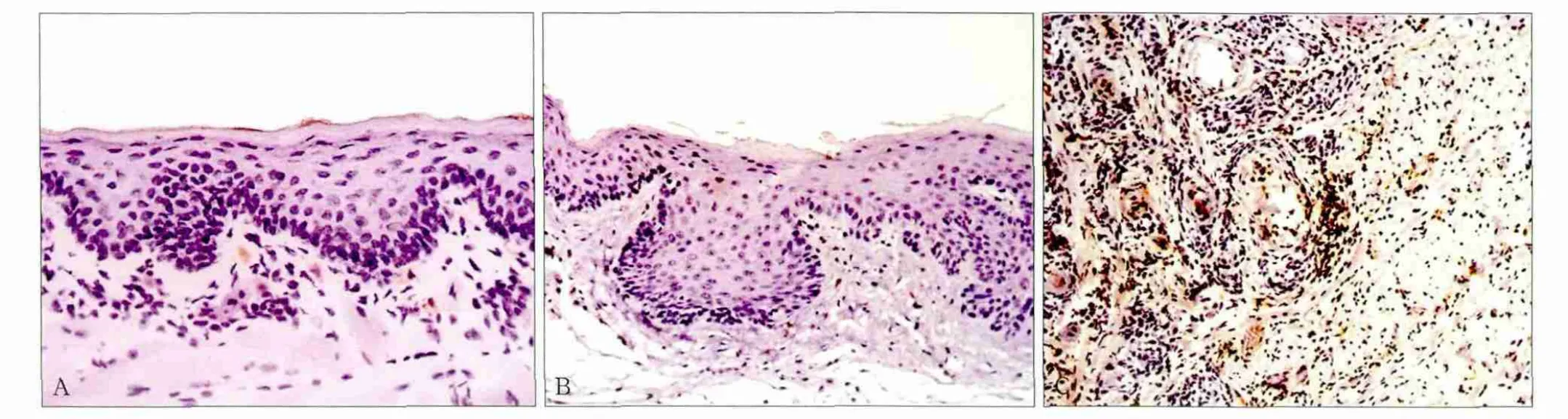
图4 MDSC细胞在小鼠舌黏膜中的表达 LSAB × 200 Fig 4 MDSC expression in tongue mucosa of mice LSAB × 200
2.6 口腔病变对酶类基因表达的影响
检测了ARG-1在正常舌黏膜和4NQO诱导的舌黏膜病变部位的表达水平。qRT-PCR结果显示,ARG-1 mRNA在异常增生组织中的表达高于在正常舌黏膜中的表达,而在OSCC中的表达高于正常舌黏膜和异常增生组织中的表达(P<0.05)。其中,OSCC小鼠舌癌部位ARG-1 mRNA表达水平较正常小鼠舌黏膜显著升高(4.80±1.46)倍(P=0.01)。因此,ARG-1 mRNA的表达是随着肿瘤进展而增加。
3 讨论
舌癌的发生发展是一个多步骤复杂的过程。4NQO作用于口腔黏膜上皮,可能是通过引起DNA的损伤和诱发基因突变,诱导了舌癌的发生发展[5-6]。本研究组织病理学发现4NQO作用后,小鼠的舌黏膜出现了由正常黏膜向癌前病变和鳞癌转变的过程。Ki67免疫组织化学染色结果也同样证实了该过程。Ki67是一种与细胞周期相关的核蛋白,作为增殖标志物常用于检测增殖细胞的表达,其表达量与肿瘤的恶性程度相关[7-8]。
髓细胞生成的异常是肿瘤免疫逃逸的重要原因[9]。这群细胞的增长可诱导T淋巴细胞对抗原刺激的无应答[9-10],因此被命名为MDSC细胞。MDSC细胞在肿瘤状态下可大量积蓄[2,11-12]。笔者发现4NQO诱导的小鼠随病变进展,外周血中Gr-1+CD11b+MDSC比例逐渐增加,明显高于对照组。这说明MDSC的扩增可能是促肿瘤发展环节中的重要一步。
CD4+和CD8+T细胞在介导抗肿瘤免疫应答中有重要作用[13-14]。本研究发现,随肿瘤进展,外周血中CD3+CD8+T细胞比例逐渐升高,CD4+/CD8+比降低,与正常对照组相比,差异有统计学意义。随肿瘤进展,CD4+/CD8+比的减少可能是由于CD3+CD8+T细胞的扩增所致,这也提示了荷瘤小鼠免疫功能逐渐减弱。Gannot等[15]也发现肿瘤负荷可影响系统免疫应答。本研究还发现MDSC比例与CD3+CD8+T细胞比例存在正相关性,与CD4+/CD8+比显示负相关关系。这提示机体可能通过降低CD4+/CD8+比和提高MDSC比例来影响抗肿瘤免疫应答。这些发现提示MDSC的扩增与肿瘤进展及机体免疫力低下有关。
MDSC在小鼠体内的表型定义为Gr-1+CD11b+的细胞群。OSCC的临床行为可能与肿瘤侵袭前沿浸润炎性细胞的类型有关。Yang等[16]对小鼠乳腺癌组织MDSC采用Gr-1抗体标记后发现,在肿瘤与腺体组织的交界处即肿瘤侵袭前沿浸润了大量的MDSC。本研究免疫组织化学也发现,肿瘤组织中散在分布的MDSC在侵袭前沿表达较丰富,而在正常舌和异常增生舌黏膜区域表达较少。异常增生小鼠的外周血中MDSC较正常小鼠显著增高,然而在舌病变部位异常增生区域表达较少,可能由于异常增生区域诱导分泌的细胞因子和趋化因子较少,造成了MDSC在局部微环境中的变化与循环中的变化的差别。
ARG-1可能参与MDSC诱导的免疫抑制作用[9,17]。本研究发现随舌癌进展,ARG-1 mRNA水平逐渐升高。这提示ARG-1基因水平的上调可能参与了口腔癌MDSC的扩增。在肿瘤微环境中,MDSC中ARG-1的过表达,消耗了局部微环境中L-精氨酸的水平,导致T细胞受体信号通路的失调,使CD8+T细胞无应答[18]。这提示MDSC浸润至肿瘤组织,创造了一个有利于肿瘤进展的微环境,并且可能通过ARG-1发挥免疫抑制作用。
综上所述,本研究显示荷瘤小鼠的舌黏膜出现OSCC时,舌和外周血的MDSC水平显著升高,并与病变部位ARG-1的表达呈正相关关系。这提示MDSC的扩增有可能是肿瘤进展的重要原因,ARG-1基因水平的上调可能参与了这一过程。MDSC可能是口腔癌免疫治疗的新靶点。
[1]Wolff KD, Follmann M, Nast A. The diagnosis and treatment of oral cavity cancer[J]. Dtsch Arztebl Int, 2012, 109(48):829-835.
[2]Weed DT, Vella JL, Reis IM, et al. Tadalafil reduces myeloidderived suppressor cells and regulatory T cells and promotes tumor immunity in patients with head and neck squamous cell carcinoma[J]. Clin Cancer Res, 2015, 21(1):39-48.
[3]邬腊梅, 杨宏宇, 罗娟, 等. 4-1BBL-B7-H3基因对免疫重建重症联合免疫缺陷荷瘤鼠的抑瘤作用[J]. 华西口腔医学杂志, 2014, 32(2):190-195.
[4]Gabrilovich DI, Nagaraj S. Myeloid-derived suppressor cells as regulators of the immune system[J]. Nat Rev Immunol,2009, 9(3):162-174.
[5]Tang XH, Knudsen B, Bemis D, et al. Oral cavity and esophageal carcinogenesis modeled in carcinogen-treated mice[J]. Clin Cancer Res, 2004, 10(1 Pt 1):301-313.
[6]Okazaki Y, Tanaka Y, Tonogi M, et al. Investigation of environmental factors for diagnosing malignant potential in oral epithelial dysplasia[J]. Oral Oncol, 2002, 38(6):562-573.
[7]Deyhimi P, Torabinia N, Torabinia A. A comparative study of histological grade and expression of Ki67 protein in oral squamous cell carcinoma in young and old patients[J]. Dent Res J: Isfahan, 2013, 10(4):514-517.
[8]Klimowicz AC, Bose P, Petrillo SK, et al. The prognostic impact of a combined carbonic anhydrase IX and Ki67 signature in oral squamous cell carcinoma[J]. Br J Cancer, 2013,109(7):1859-1866.
[9]Shi M, Li M, Cui Y, et al. Gr-1 Ab administered after bone marrow transplantation plus thymus transplantation sup-presses tumor growth by depleting granulocytic myeloidderived suppressor cells[J]. PLoS ONE, 2014, 9(5):e97908.
[10]Xia S, Sha H, Yang L, et al. Gr-1+CD11b+myeloid-derived suppressor cells suppress inflammation and promote insulin sensitivity in obesity[J]. J Biol Chem, 2011, 286(26):23591-23599.
[11]Diaz-Montero CM, Salem ML, Nishimura MI, et al. Increased circulating myeloid-derived suppressor cells correlate with clinical cancer stage, metastatic tumor burden,and doxorubicin-cyclophosphamide chemotherapy[J]. Cancer Immunol Immunother, 2009, 58(1):49-59.
[12]Chi N, Tan Z, Ma K, et al. Increased circulating myeloidderived suppressor cells correlate with cancer stages, interleukin-8 and -6 in prostate cancer[J]. Int J Clin Exp Med,2014, 7(10):3181-3192.
[13]Monu NR, Frey AB. Myeloid-derived suppressor cells and anti-tumor T cells: a complex relationship[J]. Immunol Invest,2012, 41(6/7):595-613.
[14]Nagaraj S, Gabrilovich DI. Regulation of suppressive function of myeloid-derived suppressor cells by CD4+T cells[J].Semin Cancer Biol, 2012, 22(4):282-288.
[15]Gannot G, Buchner A, Keisari Y. Interaction between the immune system and tongue squamous cell carcinoma induced by 4-nitroquinoline N-oxide in mice[J]. Oral Oncol, 2004,40(3):287-297.
[16]Yang L, Huang J, Ren X, et al. Abrogation of TGF beta signaling in mammary carcinomas recruits Gr-1+CD11b+myeloid cells that promote metastasis[J]. Cancer Cell, 2008,13(1):23-35.
[17]Li RJ, Liu L, Gao W, et al. Cyclooxygenase-2 blockade inhibits accumulation and function of myeloid-derived suppressor cells and restores T cell response after traumatic stress[J]. J Huazhong Univ Sci Technol Med Sci, 2014, 34(2):234-240.
[18]Rodriguez PC, Quiceno DG, Zabaleta J, et al. ArginaseⅠproduction in the tumor microenvironment by mature myeloid cells inhibits T-cell receptor expression and antigenspecific T-cell responses[J]. Cancer Res, 2004, 64(16):5839-5849.
