NKA-Ⅱ树脂富集纯化银杏叶聚戊烯醇
2015-12-13刘玉桃杨小明
刘玉桃,杨小明*
(江苏大学食品与生物工程学院,江苏 镇江 212013)
NKA-Ⅱ树脂富集纯化银杏叶聚戊烯醇
刘玉桃,杨小明*
(江苏大学食品与生物工程学院,江苏 镇江 212013)
从8种树脂中筛选出对银杏叶聚戊烯醇(polyprenols,PPs)有较大吸附率的NKA-Ⅱ树脂。研究PPs在NKA-Ⅱ树脂上的吸附特性,确定分离PPs适宜工艺参数。动力学数据研究表明,PPs在NKA-Ⅱ树脂上的吸附过程符合一级吸附动力学方程,控速步骤以液膜扩散为主;吸附等温曲线服从Langmuir和Freundlich等温吸附方程。NKA-Ⅱ树脂固定床纯化PPs的操作条件:上样质量浓度0.73 mg/mL、流速2 mL/min;以流速1 mL/min的正己烷-丙酮(80∶20,V/V)洗脱,用量5 BV。经NKA-Ⅱ树脂固定床纯化后,PPs含量从33.85%提高到71.54%,回收率为88.76%。树脂柱再生第6次时,对PPs的分离纯化能力才明显降低,表现出良好的再生使用性。
大孔树脂;吸附;聚戊烯醇
银杏叶聚戊烯醇(polyprenols,PPs)是含有2 个反式和12~20 个顺式异戊烯基、两端分别为ω端基和不饱和α端基[1-4]的化合物,具有促进机体造血机能、改善再生障碍性贫血的功效[5-7],对高血压、高血脂、糖尿病等都具有明显的治疗作用[8-10]。
近年来,国内外关于银杏叶PPs的纯化有许多报道,孙磊等[11]采用硅胶柱层析多次反复分离银杏叶石油醚提取物后,得到含量为90%的PPs,但该方法耗时,有机溶剂消耗量大,效率低下。王成章[12]采用有机溶剂粗提-碱水解-冷冻除蜡,最后通过分子短程蒸馏得到纯度为70%的PPs产品。此方法克服了反复过硅胶柱的缺陷,但生产条件要求高,耗能大,馏出温度最高达300 ℃,可能会对PPs的结构 有影响。杨克迪等[13]建立了甲醇溶液-银离子配位体系,通过银离子与PPs的不饱和键形成π络合,有选择性地分离PPs类化合物,使得产品纯度有明显提高。该方法在较温和的条件下进行,操作简单,但是PPs在有机相中与甲醇-水萃取相中银离子接触困难、操作时间长,且甲醇饱和蒸汽压较高,挥发严重,导 致银离子浓度难以控制。因此需要一种稳定、可重复使用、生产周期短的材料来分离纯化PPs。
大孔吸附树脂是一类有机高聚物吸附剂,它具有理化性质稳定、选择性较好、生产周期短、树脂再生方便、可重复使用等优点,因而天然产物的分离纯化中被广泛应用[14-16]。本实验以PPs吸附率为指标,从8种大孔树脂中筛选出具有良好吸附和解吸性能的树脂,并对该树脂吸附PPs的热力学和动力学过程进行探讨。
1 材料与方法
1.1 材料与试剂
银杏叶采自江苏大学校园,60 ℃烘干,粉碎备用;银杏叶PPs标准品由本试验室自制,色谱纯度大于95%;各种型号的大孔树脂均购自郑州勤实科技有限公司。
异丙醇、正己烷、甲醇(均为色谱纯) 国药化学试剂有限公司;液相色谱分析用水为娃哈哈纯净水;其他试剂均为分析纯 上海化学试剂有限公司;其他用水为双蒸水。
1.2 仪器与设备
1260高效液相色谱仪(包括G1322A在线脱气、G1312C二元泵、G1329B自动进样器、G1314B紫外检测器、Chemstation工作站) 安捷伦科技有限公司;Shim-pack VP-ODS色谱柱(250 mm×4.6 mm) 日本岛津公司;SHA-B水浴恒温振荡器 江苏金坛市中大仪器厂。
1.3 方法
1.3.1 PPs含量的测定
PPs含量的测定采用高效液相色谱(high performance liquid chromatogrophy,HPLC)外标法[17],色谱条件:柱温30 ℃,检测波长215 nm,流动相为异丙醇-正己烷-甲醇-水(体积比54∶16∶27∶3),流速1 mL/min,进样量10 μL。分别准确称取PPs标准品配成不同质量浓度的标准品溶液进行HPLC分析,以PPs标准品的质量浓度为横坐标(x),以有效组分的峰面积之和为纵坐标(y),得PPs标准曲线为y=22 131x-54.49,线性范围:0.023~0.74 mg/mL,相关系数R2=0.999。
1.3.2 PPs原料的制备
称取100 g干燥的银杏叶粉,按1∶6(g/mL)的料液比加入石油醚(沸程60~90 ℃),在70 ℃条件下热回流提取4 h,重复3 次,抽滤,合并滤液,减压浓缩后得到石油醚浸膏。称取上述石油醚浸膏2.0 g,用50 mL石油醚溶解,加入等体积5% NaOH的甲醇溶液,于50 ℃条件下搅拌3 h。反应完成后静置分层,取出上层石油醚相减压浓缩后得到银杏叶PPs浸膏。称取上述浸膏1.5 g用硅胶柱(400 mm×20 mm,装100~200 目硅胶50 g)纯化,以石油醚-乙酸乙酯(90∶10,V/V)洗脱液洗脱400 mL,减压浓缩后用正己烷定容至100 mL,密封冷冻保存备用[18]。
1.3.3 树脂预处理
将树脂用去离子水浸泡5 min,除去上漂的树脂后无水乙醇浸泡24 h,充分溶胀后于50 ℃条件下烘干,存于干燥器内备用。
1.3.4 树脂对PPs平衡吸附量测定
准确称取处理好的树脂各0.20 g,置于100 mL具塞三角瓶内,加入一定质量浓度的PPs正己烷溶液20 mL,于25 ℃恒温水浴中振荡,充分吸附后,分离树脂和溶液,采用1.3.1节方法测定平衡吸附后溶液中PPs的含量,根据公式(1)、(2)计算平衡吸附量和吸附率;树脂则用正己烷快速洗涤3 次,加入正己烷-丙酮(8∶2,V/V)[19],于25 ℃条件下恒温振荡,充分解吸后,按1.3.1节方法测定液相中PPs的含量,根据公式(3)计算解吸率。

式(1)~(3)中:qe为平衡吸附量/(mg/g);E和D分别为平衡吸附率和解吸率/%;ρ0、ρe和ρd分别为PPs起始质量浓度、平衡质量浓度、在解吸液中的质量浓度/(mg/mL);Vi和Vd分别为起始溶液的体积和解吸液的体积/mL;M为树脂干质量/g。
1.3.5 静态吸附动力学
准确称取NKA-Ⅱ树脂0.20 g,置于100 mL具塞三角瓶内,加入质量浓度为0.446 0 mg/mL的PPs正己烷溶液,于25 ℃条件下恒温振荡,每隔0.5 h测定液相中PPs质量浓度,按式(4)计算吸附量。

式中:qt和ρt分别为对应吸附时间t时的吸附量/(mg/g)和PPs在溶液中的质量浓度/(mg/mL);Vi为起始溶液的体积/mL;M为树脂干质量/g。
1.3.6 静态吸附等温线
准确称取8 份NKA-Ⅱ树脂,每份0.20 g,置于1 0 0 m L具塞三角瓶内,分别加入质量浓度为0.45 mg/mL的PPs正己烷溶液10、13、16、19、22、25、28、31 mL,于15、25、35 ℃恒温水浴中充分振荡,计算树脂的平衡吸附量。每个温度重复做3 次。
1.3.7 固定床吸附分离
NKA-Ⅱ树脂湿法装柱,柱床体积22 mL,柱高28 cm。将一定质量浓度的PPs正己烷溶液在恒温条件下以一定流速连续流过树脂柱,测定流出液中PPs的质量浓度,分析料液质量浓度、流速对穿透曲线的影响。
固定床吸附结束后,以3 BV的丙酮冲洗柱子,去除残留的脂溶性杂质后,依次以正己烷-丙酮(60∶40、80∶20、100∶0,V/V)溶液梯度洗脱,每个梯度3 BV。测定洗脱液中PPs质量浓度,考察洗脱剂组成及流速对洗脱曲线的影响。
2 结果与分析
2.1 树脂的筛选
8 种不同类型树脂对PPs的平衡吸附量、平衡吸附率见表1。
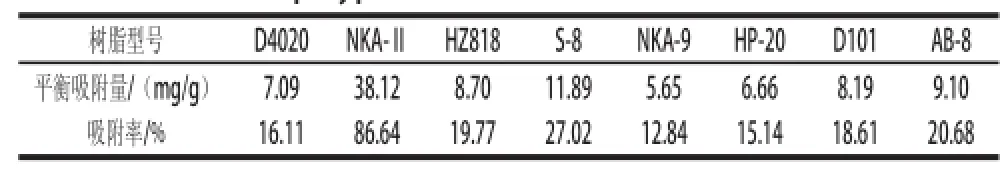
表1 不同类型树脂对PPs的平衡吸附量和吸附率(25 ℃)Table1 Equilibrium adsorption amounts and adsorption ratios for
由表1可见,树脂NKA-Ⅱ对PPs的平衡吸附量为38.12 mg/g,平衡吸附率达86.64%,而所选的其他树脂的吸附率均低于30%。用正己烷-丙酮(8∶2,V/V)对NKA-Ⅱ树脂解吸,解吸率97.87%。因此,选择树脂NKA-Ⅱ进行静态、动态吸附研究。
2.2 NKA-Ⅱ树脂吸附动力学
25 ℃条件下,分别测定了不同吸附时间NKA-Ⅱ树脂对PPs的吸附量,作出PPs在NKA-Ⅱ上的静态吸附动力学曲线和一级速率方程拟合 曲线见图1。
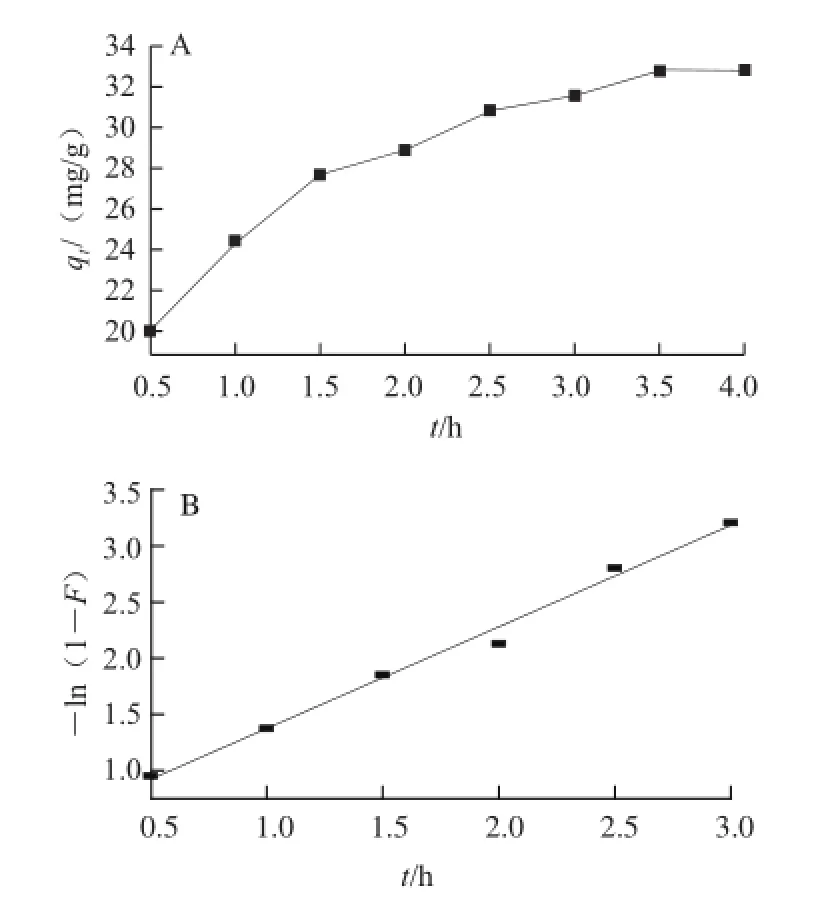
图1 PPs在NKA-Ⅱ上的吸附动力学曲线 (A)及一级速率方程拟合曲线 (B) BFig.1 Adsorption kinetic curve of PPs on NKA-Ⅱ (A) and fitting curve of first-order rate equation (B)
图1A显 示,PPs在树脂NKA-Ⅱ上的吸附量随吸附时间的延长逐渐增加,大约4 h后达到吸附平衡。在吸附3 h时,吸附量已经达到了平衡吸附量的 96%。分别利用一级、二级和准二级动力学模型对吸附速率进行拟合[20],结果发现,采用二级和准二级动力学方程拟合的相关系数均小于一级动力学方程,故PPs在NKA-Ⅱ上的静态动力学吸附特性最符合一级吸附动力学特征(图1B)。由图1B可知,前3 h内-ln(1-F)与时间t呈现良好的线性关系(R2=0.996 0),表明PPs在大孔树脂NKA-Ⅱ上的动力学吸附符合一级速率方程。这说明在所研究的条件下PPs在大孔树脂上的吸附过程主要受液膜扩散控制[21]。
在吸附过程中,吸附剂颗粒内部的内扩散亦为速率控制步骤[22]。采用基于单分子层吸附的Bangham速率方程 lnqt= lnkB+m−1lnt对吸附动力学数据进行拟合分析,从R2=0.992 5看,吸附前期(前3 h),PPs在NKA-Ⅱ树脂上的吸附动力学行为基本遵循Bangham速率方程的规律。
由以上分析可知,一级动力学的拟合结果优于Bangham速率方程,表明PPs在NKA-Ⅱ树脂上的吸附主要受液膜扩散控制,但颗粒内扩散对吸附过程也有一定的影响。
2.3 NKA-Ⅱ对PPs的静态吸附等温曲线
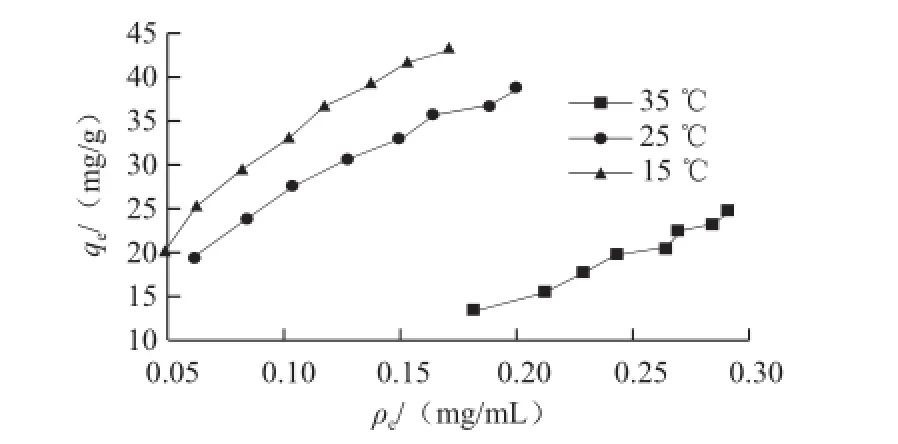
图2 PPs在树脂NKA-Ⅱ上的吸附等温线Fig.2 Adsorption isotherms of PPs on resin NKA-Ⅱ
为考察NKA-Ⅱ树脂对PPs的吸附行为,测定了不同温度条件下NKA-Ⅱ树脂对PPs的吸附。由图2可知,随着吸附温度升高,NKA-Ⅱ树脂对PPs的吸附量逐渐降低,说明PPs在NKA-Ⅱ树脂上吸附属于放热过程,升高温度不利于吸附过程进行[23]。
在吸附平衡模型中, Langmuir等温吸附方程和Freundlich等温吸附方程是应用最为广泛的等温吸附方程,方程分别如下:

式(5)、(6)中:qm为最大饱和吸附量/(mg/g),KL为结合常数/(mL/mg);n、KF为等温吸附特征常数。
分别用Langmuir和Freundlich等温吸附方程对以上3 个温度条件下的等温吸附数据进行拟合,拟合结果及相关参数见表2。

表2 银杏叶PPs的静态等温吸附拟合结果Table2 Fitting results for static adsorption isotherms of polyprenols
由表2可知,Langmuir等温吸附模型相对于Freundlich等温吸附模型能较好地描述PPs在NKA-Ⅱ树脂上的静态吸附特性。表明此质量浓度条件下,PPs在NKA-Ⅱ树脂上的吸附趋近单分子层吸附。Langmuir拟合结果中可以看出,随温度的升高,树脂的饱和吸附量qm减小,与实验结果相对应。Freundlich方程拟合结果中n值可以看作是吸附优惠性的体现,在较低温度条件下拟合得到的n值均大于1,表明是优惠吸附。
2.4 操作条件对固定床穿透曲线的影响
NKA-Ⅱ树脂固定床吸附纯化PPs时,当流出液的PPs质量浓度达到其上样液的5%时即认为PPs已穿透[23,25]。同一上样流速(Q =2.0 mL/min),样品初始质量浓度对固定床穿透曲线的影响见图3。
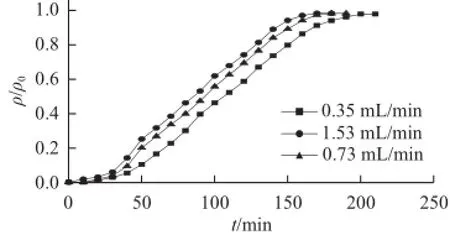
图3 银杏叶PPs质量浓度对穿透曲线的影响Fig.3 Effect of PPs concentration on breakthrough curves
由图3可以看出,上样质量浓度为1.53、0.73 mg/mL和0.35 mg/mL时PPs的穿透点分别为30、35 min和40 min,树脂达到完全饱和吸附时的时间分别为180、190 min和210 min。可见,流速一定时,上样质量浓度越高,穿透点和饱和吸附点越靠前,达到饱和吸附的时间越短。因此,提高上样质量浓度有利于提高树脂的使用效率。然而,由图3可见,与上样质量浓度0.73 mg/mL相比,1.53 mg/mL的效果不是太明显,并且上样质量浓度过高时,在一定流速条件下,物质和树脂的接触时间变短,造成吸附量的降低,损失率变大,不利于生产。因此确定0.73 mg/mL为适宜的上样质量浓度。
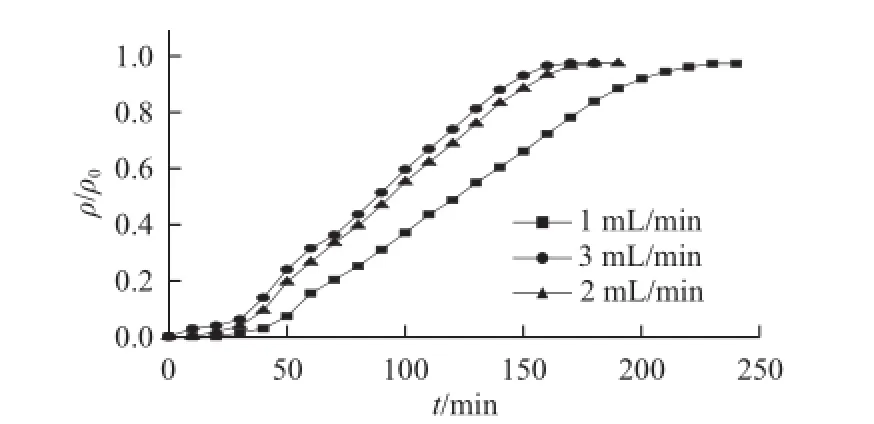
图4 上样流速对穿透曲线的影响Fig.4 Effect of sample loading flow rate on breakthrough curves
固定上样质量浓度为0.73 mg/mL,分析上样流速对固定床穿透曲线的影响,结果见图4。与上样流速为1 mL/min时的穿透曲线相比,流速为2 mL/min和3 mL/min时的穿透点都比较提前,穿透曲线也较陡,这是因为流速加快将直接缩短固液两相的接触时间,致使传质区加长。但是,由于流速由2 mL/min增加至3 mL/min时,洗脱效果不是太明显,且流速增加造成溶剂和原料的浪费。综上所述,确定2 mL/min为适宜的上样流速。

表3 不同条件下固定床吸附PPs的穿透时间与模型计算结果Table3 Comparison of the experimental and calculated breakthrough time of PPs Ps
通过Bohart-Adams数学模型ln(ρ0/ρ−1)=A−Kρ0t对上述数据进行拟合,得到穿透时间的理论数值,将其与实验测得数据进行对比。结果如表3所示,理论值与实验值相差较小,所以Bohart-Adams能够较好地拟合该操作数据。综上所述选择以质量浓度0.73 mg/g、流速2.0 mL/min作为固定床上样条件。
2.5 固定床洗脱
NKA-Ⅱ树脂固定床吸附PPs后,按照1.3.7节中的方法进行梯度洗脱,每个梯度为3 BV,0.5 BV接一个流分,并用HPLC法检测其中的PPs质量浓度,考察洗脱剂组成对洗脱效果的影响,结果见图5。

图5 银杏叶PPs的梯度洗脱曲线Fig.5 Elution curve of polyprenols
由图5可见,当洗脱剂为正己烷-丙酮(8∶2,V/V)时,洗脱峰窄且集中,被解吸的PPs主要集中于6.5~9 BV段,且3 BV的解吸剂可将吸附的PPs几乎完全洗脱。因此,确定洗脱溶液为正己烷-丙酮(8∶2,V/V),用量5 BV。
质量浓度为0.727 4 mg/mL的PPs正己烷溶液以2 mL/min的流速上样,待NKA-Ⅱ树脂固定床吸附饱和后,以正己烷-丙酮(80∶20,V/V)为洗脱剂,分别以1 mL/min和1.5 mL/min的流速洗脱,每10 min接一个流分,测定各流分中的PPs质量浓度直至几乎检测不到,绘制PPs的洗脱曲线见图6。
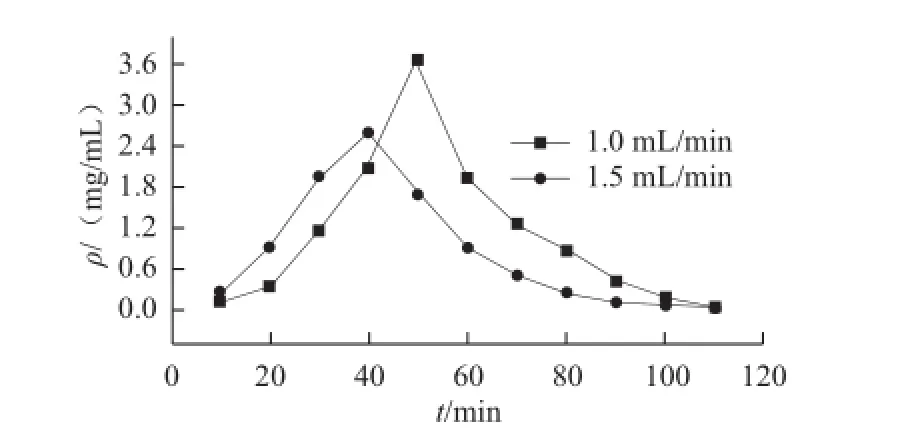
图6 流速对银杏叶PPs洗脱曲线的影响Fig.6 Effect of elution flow rate on elution curves of polyprenols
图6 显示,洗脱流速较大时,洗脱峰较提前,拖尾现象也较明显。洗脱峰提前是流速加快导致树脂表面液膜变薄,使传质系数增大,从而增大传质速率所致;洗脱曲线出现拖尾原因是流速较快时,交换带也相应较长。从图6还可以看出,洗脱流速越慢,洗脱峰越集中,但流速太慢,生产周期延长,因此选择在1 mL/min流速条件下进行洗脱。
最后,在上述条件下经NKA-Ⅱ树脂固定床富集后,分离物中PPs含量由浸膏中的33.85%提高到71.54%,PPs的回收率达到了88.76%。采用梯度洗脱的方法对树脂固定床进行再生,再生的树脂固定床连续使用3 次,吸附量未有明显下降,再生第6次时才有明显下降,表明该树脂有较好的再生使用性。
3 结 论
从8 种不同型号的大孔树脂中筛选出对银杏叶PPs有较大吸附量的NKA-Ⅱ树脂。采用3种动力学模型分析出PPs在NKA-Ⅱ上的动力学吸附符合一级速率方程;两个等温吸附方程对比,Langmuir等温吸附模型能较好地描述PPs在NKA-Ⅱ树脂上的静态吸附平衡,且该吸附过程是能够自发进行的放热过程。同时对NKA-Ⅱ树脂固定床纯化PPs工艺进行探讨,优化得到NKA-Ⅱ大孔树脂对PPs动态吸附的工艺参数为:上样流速2 mL/min、上样质量浓度0.73 mg/mL;优化得到NKA-Ⅱ大孔树脂对PPs动态解吸的工艺参数为:流速1 mL/min、洗脱剂正己烷-丙酮(80∶20,V/V)、用量5 BV。PPs含量从树脂柱纯化前的33.85%提高到71.54%,回收率为88.76%。树脂柱再生第6次时,对PPs的分离纯化能力才有明显降低,表现出较好的再生使用性。
[1] 徐宏彬, 李玲. 植物聚戊烯醇研究概述[J]. 中国药师, 2008, 11(8): 977-979.
[2] SWIEZEWSKA E, SASAK W, MANKOWSKI T, et al. The research for plant polyprenols[J]. Acta Biochimica Polonica, 1994, 41: 221-260.
[3] TAKIGAWA T, IBATA K, MIZUNO M. Synthesis of mammalian dolichols from plant polyprenols[J]. Chemistry and Physics of Lipids, 1989, 51(3): 171-182.
[4] VAN HOUTE H A, BUSSON R H, PARMENTIER G G, et al. Synthesis of [1-14C] dolichol acid[J]. Chemistry and Physics Lipids, 1994, 72: 103-107.
[5] 杨克迪, 陈钧, 欧阳臻, 等. 高效液相色谱/大气压化学电离质谱分析银杏叶中聚戊烯醇化合物[J]. 分析化学研究简报, 2003, 31(8): 937-940.
[6] 杨克迪, 陈钧, 童张法. 反相高效液相色谱法制备银杏叶中聚戊烯醇同系物单体[J]. 色谱, 2003, 21(1): 49-51.
[7] 杨克迪, 刘自力, 童张法, 等. 银杏叶聚戊烯醇类化合物分离工艺研究[J]. 广西大学学报: 自然科学版, 2002, 27(2): 136-139.
[8] 孙磊, 李春斌, 范圣第. HPLC测定银杏叶中聚戊烯醇的含量[J]. 华西医学杂志, 2006, 21(3): 297-299.
[9] 王成章. 银杏叶聚戊烯醇的化学, 纯化和药效研究[J]. 天然产物研究与开发, 2001, 13(2): 43-45.
[10] DANILOY L L, MALTSEY S D, DEYEYA A V, et al. Phosprenyl: a novel drug with antiviral and immunomodulatory activity[J]. Archivum Immunologiae et Therapiae Experimentalis, 1995, 44(5/6): 395-400.
[11] 孙磊, 李春斌, 白静, 等. 正交设计法在银杏叶聚戊烯醇提取工艺中的应用[J]. 中国现代应用药学杂志, 2006, 23(5): 361-363.
[12] 王成章. 银杏叶聚戊烯醇(GP)的分离和衍生物合成机理及生物活性研究[D]. 北京: 中国林业科学研究院, 2007: 43-45.
[13] 杨克迪, 陈钧, 杨小明, 等. 银离子配位萃取银杏叶中多萜长链化合物的研究[J]. 无机化学学报, 2006, 22(2): 243-247.
[14] 付玉杰, 刘晓娜, 侯春莲, 等. 大孔吸附树脂分离纯化异甘草素的研究[J]. 离子交换与吸附, 2006, 22(4): 315-322.
[15] 朱洪梅, 韩永斌, 顾振新, 等. 大孔树脂对紫甘薯色素的吸附与解吸特性研究[J]. 农业工程学报, 2006(5): 153-156.
[16] 贾雁高, 杜爱玲, 谷成燕, 等. AB8大孔树脂吸附与硅胶层析法分离姜酚的对比研究[J]. 山东大学学报: 工学版, 2010(2): 121-125.
[17] 李洁, 杨小明, 王云飞, 等. 响应面法优化银杏叶聚戊烯乙酸酯水解工艺[J]. 食品工业科技, 2013, 34(7): 256-259.
[18] 翁娜, 陈剑锋, 郑晨晖, 等. 银杏叶聚戊烯醇的分离纯化[J]. 现代化工, 2007, 27(增刊2): 373-376.
[19] SWIEZEWSKA E, DANIKIEWICZB W. Polyisoprenoids: structure, biosynthesis and function[J]. Progress in Lipid Research, 2005, 44(4): 235-258.
[20] 付杰, 李燕虎, 叶长燊, 等. DMF在大孔吸附树脂上的吸附热力学及动力学研究[J]. 环境科学学报, 2012, 32(3): 639-644.
[21] 黄永春, 杨锋, 马月飞, 等. 860021大孔树脂吸附茶多糖的研究[J].现代化工, 2007, 27(增刊2): 220-224.
[22] YU Ying, ZHUANG Yuanyi, WANG Zhonghua. Adsorption of water-soluble dye onto functionalized resin[J]. Journal of Colloid and Interface Science, 2001, 2: 288-293.
[23] DING Yan, YANG Xiaoming, PAN G, et al. Adsorption and enrichment of alkalids from areca nut by means of macroporous resins[J]. Adsorption Science and Technology, 2012, 30(3): 193-204.
[24] 谷芳芳, 任凤莲, 吴梅林. X-5大孔树脂吸附熊果酸的动力学与热力学特性研究[J]. 广州化学, 2006(3): 15-19.
[25] 朱静, 陆晶晶, 袁其朋. 大孔吸附树脂对石榴皮多酚的分离纯化[J].食品科技, 2010, 35(1): 188-193.
Enrichment and Purification of Ginkgo biloba Leaf Polyprenols by NKA-Ⅱ Macroporous Resin
LIU Yutao, YANG Xiaoming*
(School of Food and Biological Engineering, Jiangsu University, Zhenjiang 212013, China)
Resin NKA-Ⅱ was selected as the best one among eight kinds of macroporous resins for the purification of polyprenols (PPs) from Ginkgo biloba leaves in terms of its highest adsorption rate for PPs. The adsorption behavior of PPs on NKA-Ⅱ resin was further investigated and optimum parameters for adsorption and desorption were procured. The data showed that the adsorption behavior of PPs on NKA-Ⅱ resin followed the first order kinetic equation. The adsorption process was mainly affected by film diffusion. The adsorption isothermal curve obeyed both Freundlich and Langmuir isotherm equations. PPs were separated by a fixed bed packed with NKA-Ⅱ resin under the operating conditions as follows: 0.73 mg/mL of the sample was loaded onto the column at a flow rate of 2 mL/min and eluted with 5 BV of hexane-acetone (80:20, V/V) at a flow rate of 1 mL/min. Under these conditions, the content of PPs increased from 33.85% to 71.54%, and the recovery was 88.76%. After the sixth regeneration, its separation capacity for PPs began to significantly decrease, showing a good regenerability.
macroporous resin; adsorption; polyprenols
TS218
A
1002-6630(2015)04-0063-05
10.7506/spkx1002-6630-201504012
2014-07-21
镇江市工业攻关项目(GY2011015)
刘玉桃(1988—),女,硕士研究生,研究方向为天然产物的分离纯化。E-mail:512075928@qq.com
*通信作者:杨小明(1963—),女,教授,博士,研究方向为天然产物研发。E-mail:XM_Yang1963@126.com
