肝功能正常患者Gd-EOB-DTPA增强MRI肝胆期延迟时间的研究
2015-12-13丁丁陆健黎美玲张学琴张涛杜圣徐晓莉姜吉锋杨雪飞
丁丁,陆健,黎美玲,张学琴,张涛,杜圣,徐晓莉,姜吉锋,杨雪飞
南通大学附属南通第三医院影像科,南通 226001
钆塞酸二钠(Gadolinium ethoxybenzyl diethylenetriaminepentaacetic acid,Gd-EOB-DTPA)是一种肝细胞特异性磁共振成像(magnetic resonance imaging,MRI)对比剂,它既有细胞外间隙对比剂的特点,又可被正常肝细胞特异性摄取,是一种可以在一次检查中同时获取动态增强和肝胆期影像的新型双功能MRI对比剂[1-2]。药品说明书推荐肝胆期延迟20 min扫描,相对普通对比剂,Gd-EOB-DTPA存在检查时间长的缺点,部分患者不能忍耐长时间的检查,限制了其在临床的应用推广。本研究纳入38例存在肝脏局灶性病变的肝功能正常病例,通过比较分析注射Gd-EOB-DTPA后10 min与20 min肝脏的信号强度和病灶的显示情况,评价延迟10 min的肝胆期是否能够满足病灶的检出和诊断。
1 材料和方法
1.1 临床资料
病例纳入标准:患者肝功能正常、存在肝脏局灶性病变。病例排除标准:(1)肝脏存在弥漫性病变(如肝硬化、脂肪肝等);(2)曾接受肝脏手术或介入治疗;(3)肝肾功能不全。
2011年9月至2014年9月共计38例患者纳入研究,年龄24~80岁,平均(58±13)岁,共有肝脏局灶性病变46个,其中15个经手术病理证实,31个临床及影像资料典型、随访表现符合证实:25个良性(血管瘤7个,炎症3个,肝脏局灶性结节增生6个,囊肿7个,炎性假瘤2个),21个恶性(转移瘤12个,肝癌7个,胆管癌2个)。其中良性病灶最大径范围1~4 cm,恶性病灶最大径范围1~5 cm。
1.2 方法
MRI扫描技术:使用美国GE公司1.5 T HDE磁共振扫描仪。扫描体位取仰卧位,头先进。扫描参数:呼吸触发FSE T2WI+FS:TR=2~3呼吸周期,TE=80 ms,层厚6 mm,层间距1.5 mm,FOV 40 cm×30 cm,矩阵320×224,NEX 2.00;FSPGR T1W 同反向位:TR=120~250 ms,TE=2.25/4.5 ms,层厚6 mm,层间距1.5 mm,FOV 40 cm×36 cm,矩阵256×170,NEX 1.00;单次激发SE-EPI DWI:TR=5000 ms,TE=75.40 ms,层厚6 mm,层间距1.5 mm,FOV 40 cm×38 cm,矩阵128×128,NEX 8.00;肝脏容积快速采集序列(LAVA)三维动态增强扫描:TR=5.14 ms,TE=2.30 ms,扫描层厚5 mm,层间距-2.50 mm,FOV 40 cm×36 cm,矩阵288×192。
MR对比剂及注射方法:Gd-EOB-DTPA,商品名普美显,德国拜耳医药公司生产,以1.0 ml/s速率按0.1 ml/kg体重经肘静脉团注,随后以2 ml/s速率注射20 ml生理盐水。分别于注射对比剂后25 s、60 s、180 s行动态增强扫描,延迟10 min和20 min行肝胆期扫描。
1.3 图像分析。
由2名具有5年以上MRI经验的影像医师在PACS工作站共同阅片,观察38例患者的所有MRI图像,测量肝脏、病灶及竖脊肌的信号强度(signal intensity,SI)和相应层面背景噪声标准差(standard deviation of noise,SD噪声)。肝脏及竖脊肌SI测量感兴趣区(region of interest,ROI)大小约100 mm2,避开血管、胆管、病变、伪影及异常灌注区。分别测量肝脏左外叶、左内叶、右前叶及右后叶SI,取平均值代表该患者肝脏SI(SI肝脏)。病灶SI只测量一次,ROI尽可能包含病灶并避开坏死和出血区域。不同时间肝脏、病灶及竖脊肌的信号强度测量均在相同层面上。SD噪声ROI放置于肝脏沿体部相位编码方向腹侧(面积500 mm2)。计算动态增强各期及肝胆期SI肝脏相对增加率(liver ratio)、竖脊肌SI相对增加率(muscle ratio)、肝脏与竖脊肌SI比值(liver-muscle ratio)、肝脏和病灶的信号噪声比(signal to noise ratio, SNR)及病灶对比噪声比(contrast to noise ratio,CNR),计算公式如下:SI相对增加率肝脏/竖脊肌=[( SI增强后-SI增强前)/SI增强前]×100%;肝脏与竖脊肌SI比值=( SI肝脏/SI竖脊肌)×100%;SNR=SI肝脏或病灶/SD噪声;CNR=|SI病灶-SI肝脏|/SD噪声。分别记录对比剂进入胆总管的时间。
1.4 统计学分析
采用SPSS 16.0软件处理分析数据。计量资料以均值±标准差表示。10 min与20 min肝胆期数据比较采用配对t检验进行统计学分析。P<0.05为差异有统计学意义。
2 结果
注射Gd-EOB-DTPA 后,不同扫描时间肝脏、竖脊肌SI相对增加率及肝脏与竖脊肌SI比值见图1。相对于动态增强,肝实质信号在10 min肝胆期明显增加,随后趋于稳定。
10 min和20 min肝胆期肝脏、竖脊肌SI相对增加率及肝脏与竖脊肌SI比值比较见表1。注射Gd-EOB-DTPA 后10 min与20 min肝胆期之间,肝脏SI相对增加率、竖脊肌SI相对增加率及肝脏与竖脊肌SI比值差异均有统计学意义。
注射Gd-EOB-DTPA 后10 min与20 min肝胆期肝实质SNR、病灶SNR及CNR比较见表2。注射Gd-EOB-DTPA后10 min与20 min肝胆期之间,肝脏SNR差异无统计学意义,肝胆期低信号病灶SNR差异无统计学意义,肝胆期高信号病灶SNR差异有统计学意义,肝胆期低信号及高信号病灶CNR差异均无统计学意义(图2、3)。
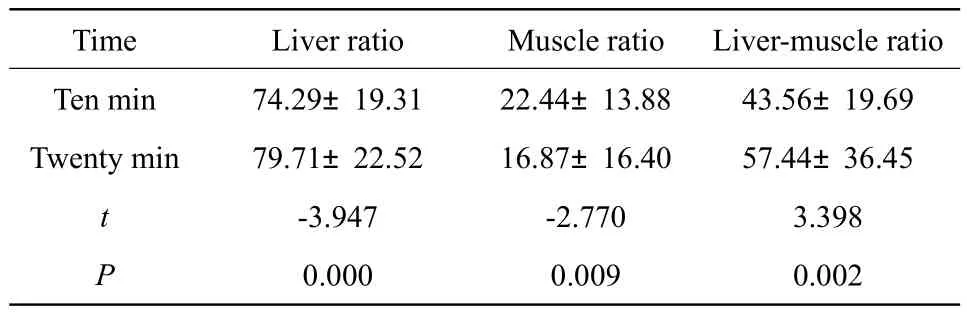
表1 10 min与20 min肝脏、竖脊肌SI相对增加率及肝脏与竖脊肌SI比值比较(%)Tab.1 Comparison of liver ratio,muscle ratio,liver-muscle ratio between ten and twenty min(%)
注射Gd-EOB-DTPA 后,26例10 min胆道可见对比剂排泄,占68.42%,20 min时所有病例胆道均可见对比剂排泄。

表2 10 min和20 min肝胆期肝实质SNR、病灶SNR及CNR比较Tab.2 Comparison of liver SNR,lesion SNR and CNR between 10 and 20 min hepatobiliary phases
3 讨论
Gd-EOB-DTPA是一种肝细胞特异性MRI对比剂,越来越多的研究[3-8]表明,Gd-EOB-DTPA增强MRI既提高了肝脏病灶的检出率,又为肝脏病灶的诊断及鉴别诊断提供了重要信息。肝脏Gd-EOB-DTPA增强MRI分动态期和肝胆期。动态期即从注射对比剂开始至3 min,其强化特点类似细胞外间隙对比剂;对比剂在细胞外间隙扩散,被肝细胞特异性摄取并逐渐排泄到胆道系统中,此即肝胆期[2,9]。延迟10min的肝胆期是否能够满足肝脏病灶的检出和诊断,目前尚存在争议。Motosugi U等[10]研究显示,延迟10 min的肝胆期可以满足高达61%的患者病灶的检出和诊断,但是并没有指出如何在10 min与20 min之间做选择;C.S.van Kessel等[1]认为,肝胆期延迟10 min能够满足肝功能正常患者已知病灶的诊断。

图1 不同扫描时间肝脏、竖脊肌SI相对增加率及肝脏与竖脊肌SI比值(%)Fig.1 Liver ratio,muscle ratio and liver-muscle ratio at different time(%)

图2 肝右后叶转移瘤。A~D:病灶平扫呈低信号,动脉期强化呈高信号,门脉期呈等信号,延迟3 min呈稍低信号;E~F:肝实质信号在10 min肝胆期(E)明显升高,10 min及20 min肝胆期病灶显示清晰,均呈明显低信号 图3 肝左内叶FNH。A~D:病灶平扫呈等信号,动脉期强化呈高信号,门脉期及延迟3 min呈稍高信号;E~F:肝实质信号在10 min肝胆期(E)明显升高,10 min及20 min肝胆期病灶均呈高信号Fig.2 Liver metastase at right posterior segment.A—D:Lesion was hypointense,hyperintense,isointense and mild-hypointense at pre-contrast,arterial phase,portal phase and delay 3 min imaging respectively; E—F:Liver signal intensity increased signifi cantly at 10 min hepatobiliary phase.Lesion was hypointense at both 10 and 20 min hepatobiliary phases imaging,visible distinctly.Fig.3 Liver focal nodular hyperplasia at left medial segment.A—D:Lesion was isointense,hyperintense at pre-contrast and arterial phase imaging,mild-hyperintense at portal phase and delay 3 min imaging respectively; E—F:Liver signal intensity increased signifi cantly at 10 min hepatobiliary phase.Lesion was hyperintense at both 10 and 20 min hepatobiliary phases imaging.
本研究显示,肝实质信号在两个时间段内上升明显,第一个为动态增强门静脉期,这是由于Gd-EOB-DTPA具有普通对比剂的特性,可以反映组织的血流灌注信息,另一个为10 min肝胆期,这是由于肝细胞能特异性摄取对比剂,使肝实质信号明显升高。肝实质信号在10 min肝胆期之后趋于稳定,20 min肝胆期肝脏信号上升幅度明显变小,且有68.42%的患者10 min可见胆道对比剂排泄,说明10 min时肝细胞摄取对比剂趋于饱和。10 min与20 min肝胆期之间,肝脏SI相对增加率、肝脏与竖脊肌SI比值差异有统计学意义,20 min时肝实质信号进一步升高,而竖脊肌信号在20 min时已降低,使肝脏与不含有肝细胞的肌肉组织之间形成明显的信号强度差异,表明肝胆期延迟20 min可能提高肝实质与不含正常肝细胞的病变组织之间的信号强度差异。而注射Gd-EOB-DTPA后10 min与20 min肝脏SNR差异无统计学意义,即经过噪声校正的肝脏信号强度10 min与20 min之间并无明显差异,可见在肝实质信号进一步升高的同时,背景噪声也进一步增高。
10 min与20 min肝胆期低信号病灶SNR及CNR差异均无统计学意义,说明10 min肝胆期能够满足肝胆期低信号病灶的检出和诊断。对于肝胆期高信号病灶,延迟20 min SNR进一步提高,差异有统计学意义,提示该类型病灶组织可能包含功能性肝细胞,和正常肝细胞一样,在20 min肝胆期能够继续摄取对比剂使病灶信号进一步升高。此类病灶与肝实质在20 min时都有信号的进一步升高,导致10 min与20 min肝胆期CNR并无显著变化,差异无统计学意义,因此20 min肝胆期并没有为肝胆期高信号病灶的检出和诊断提供更多有价值的信息。
综上所述,Gd-EOB-DTPA 增强MRI延迟10 min的肝胆期能够满足肝功能正常患者肝脏局灶性病变的检出和诊断。
值得一提的是,Gd-EOB-DTPA增强MRI肝胆期肝实质的信号强度同时取决于肝细胞对对比剂的摄取和排泄[3,11-12]。有研究[13-16]发现,Gd-EOB-DTPA增强MRI肝胆期肝实质的信号强度与其功能状态有关,而肝实质信号强度的改变可能会导致肝胆期病灶与肝实质间对比度改变,进而影响病灶的检出和诊断。本研究只纳入肝脏功能正常患者,对于肝功能降低患者肝胆期的最佳延迟时间还有待进一步研究。
[References]
[1]van Kessel CS,Veldhuis WB,van den Bosch MA,et al.MR liver imaging with Gd-EOB-DTPA:a delay time of 10 minutes is suffi cient for lesion characterisation.Eur Radiol,2012,22(10):2153-2160.
[2]Zhang T,Lu J,Zhang XQ,et al.Diagnostic value of hepatobiliary phase imaging with GD-EOB-DTPA for hepatocellular carcinomas in cirrhosis.Natl Med J China,2014,94(7):517-520.张涛,陆健,张学琴,等.钆塞酸二钠MR肝胆期对肝硬化背景下肝癌的诊断价值.中华医学杂志,2014,94(7):517-520.
[3]Kim HY,Choi JY,Kim CW,et al.Gadolinium ethoxybenzyl diethylenetriamine pentaacetic acid-enhanced magnetic resonance imaging predicts the histological grade of hepatocellular carcinoma only in patients with Child-Pugh class A cirrhosis.Liver Transpl,2012,18(7):850-857.
[4]Zech CJ,Grazioli L,Breuer J,et al.Diagnostic performance and description of morphological features of focal nodular hyperplasia in Gd-EOB-DTPA-enhanced liver magnetic resonance imaging:results of a multicenter trial.Invest Radiol,2008,43(7):504-511.
[5]Bashir MR,Gupta RT,Davenport MS,et al.Hepatocellular carcinoma in a North American population:does hepatobiliary MR imaging with Gd-EOB-DTPA improve sensitivity and confi dence for diagnosis?.J Magn Reson Imaging,2013,37(2):398-406.
[6]Löwenthal D,Zeile M,Lim WY,et al.Detection and characterisation of focal liver lesions in colorectal carcinoma patients:comparison of diffusion-weighted and Gd-EOB-DTPA enhanced MR imaging.Eur Radiol,2011,21(4):832-840.
[7]Liang CH.Magnetic resonance imaging contrast agents:an update on their clinical application.Chin J Magn Reson Imaging,2014,5(S1):37-42.梁长虹.磁共振对比剂临床应用及进展.磁共振成像,2014,5(S1):37-42.
[8]Jiang HY,Liu XJ,Song B.Progresses in magnetic resonance imaging of hepatocellular Carcinoma.Chin J Magn Reson Imaging,2015,6(2):91-97.蒋涵羽,刘曦娇,宋彬.磁共振成像技术在肝细胞癌中的应用进展.磁共振成像,2015,6(2):91-97.
[9]Choi JY,Lee JM,Sirlin CB.CT and MR imaging diagnosis and staging of hepatocellular carcinoma:part I.Development,growth,and spread:key pathologic and imaging aspects.Radiology,2014,272(3):635-654.
[10]Motosugi U,Ichikawa T,Tominaga L,et al.Delay before the hepatocyte phase of Gd-EOB-DTPA-enhanced MR imaging:is it possible to shorten the examination time?.Eur Radiol,2009,19(11):2623-2629.
[11]Tajima T,Takao H,Akai H,et al.Relationship between liver function and liver signal intensity in hepatobiliary phase of gadolinium ethoxybenzyl diethylenetriamine pentaacetic acid-enhanced magnetic resonance imaging.J Comput Assist Tomogr,2010,34(3):362-366.
[12]Cruite I,Schroeder M,Merkle EM,et al.Gadoxetate disodiumenhanced MRI of the liver:part 2,protocol optimization and lesion appearance in the cirrhotic liver.AJR Am J Roentgenol,2010,195(1):29-41.
[13]Tamada T,Ito K,Higaki A,et al.Gd-EOB-DTPA-enhanced MR imaging:evaluation of hepatic enhancement effects in normal and cirrhotic livers.Eur J Radiol,2011,80(3):e311-e316.
[14]Okada M,Ishii K,Numata K,et al.Can the biliary enhancement of Gd-EOB-DTPA predict the degree of liver function?.Hepatobiliary Pancreat Dis Int,2012,11(3):307-313.
[15]Takao H,Akai H,Tajima T,et al.MR imaging of the biliary tract with Gd-EOB-DTPA:effect of liver function on signal intensity.Eur J Radiol,2011,77(2):325-329.
[16]Nilsson H,Blomqvist L,Douglas L,et al.Gd-EOB-DTPA-enhanced MRI for the assessment of liver function and volume in liver cirrhosis.Br J Radiol,2013,86(1026):20120653.
