舒肝解郁胶囊治疗成年癫痫合并轻中度抑郁的疗效及安全性
2015-12-06黄雨兰
黄雨兰,喻 良,黄 颐△
1.四川大学华西医院 心理卫生中心(成都 610041);2.四川省医学科学院·四川省人民医院 神经内科(成都 610072)
近年来大样本量流行病学研究[1]显示,情绪障碍尤其是抑郁障碍是癫痫最常见的合并症,患病率5.9%~64.1%。抑郁可加重癫痫发作,而癫痫患者患抑郁的风险较正常人群和其他神经系统疾病患者高5~20倍,二者相互影响[1-3]。因此,控制癫痫发作的同时,治疗患者合并的抑郁更加利于癫痫发作本身的控制,促进患者康复。但是由于抗抑郁西药有导致惊厥的副作用,多数医生因担心其可能导致癫痫发作或加重而忽略对抑郁的治疗[4-6],从而影响癫痫患者的预后。中药通常具有副作用小的特点,因此从中药中寻找有效的抗抑郁药物对癫痫患者合并抑郁的治疗可能更为有效。研究[7-11]表明,舒肝解郁胶囊具有抗抑郁作用,近年来已成为临床治疗抑郁症的重要药物。目前国内外尚无舒肝解郁胶囊治疗癫痫合并抑郁的研究报道,本研究拟使用舒肝解郁胶囊治疗癫痫合并轻中度抑郁的患者,以观察其疗效及安全性。
1 资料与方法
1.1 临床资料
选取2013年8月至2014年4月四川省人民医院神经内科门诊及住院的癫痫患者共63例。纳入标准:1)所有患者均符合1981年国际抗癫痫联盟制定的癫痫诊断标准及1989年国际抗癫痫联盟公布的癫痫发作及分类标准;2)年龄≥18岁;3)患者健康问卷抑郁量表(patient health questionnaire 9-item depression scale,PHQ-9)[12]评分在5~14分;4)入组前至少使用1种抗癫痫药物3个月以上;5)既往没有使用过抗抑郁治疗;6)无药物滥用;7)所有患者签署知情同意书。排除标准:1)观察期间出现癫痫持续状态;2)并发抑郁之外的其他精神疾病;3)未服用抗癫痫药或长期使用对癫痫发作有影响的其他药物或服用其他对中枢神经系统有影响的药物者;4)患有严重的心、肝、肾疾病及神经系统退行性疾病;5)不愿签署知情同意书者。
将63例符合入组排除标准的患者随机分为观察组和对照组。其中,观察组32例,男18例,女14例;年龄18~65岁,平均(31.23±11.71)岁;病程1~12年,平均(6.57±3.74)年;部分性发作20例,全身性发作12例。对照组31例,男17例,女14例;年龄19~71岁,平均(30.72±12.45)岁;病程1~13年,平均(6.04±4.04)年;部分性发作18例,全身性发作13例。两组在年龄、性别、病程和发作类型等方面比较,差异无统计学意义(P>0.05)。
1.2 治疗方法
观察组除接受相应的抗癫痫药物治疗外,同时加用舒肝解郁胶囊(1.44g/d,分两次服用,成都康弘制药有限公司)抗抑郁治疗;对照组只接受抗癫痫药物治疗,观察期3个月。观察期内患者服用抗癫痫药物及抗抑郁药物的种类和剂量维持不变,并排除其他抗抑郁治疗方法。
1.3 测评工具
PHQ-9是拥有9个条目的抑郁自评问卷,评估受试者过去2周的感受。9个条目反应的是DSMIV标准中的抑郁症,每个条目分为0~3分4级评分。问卷总分为9个条目的评分总和,得分0~27分,分值5、10、15和20分别代表轻、中、中重和重度抑郁分界值,得分越高表示抑郁症状越严重。PHQ-9已经被翻译成中文,在中国成年人群中具有很高的信度和效度[13-14],尤其在癫痫后抑郁诊断中与抑郁症经典诊断量表汉密尔顿抑郁量表(HAMD)的一致性达到94%[15],因此,目前已成为癫痫后抑郁的常用诊断工具。
癫痫患者的生活质量量表(quality of life in epilepsy inventory-31,QOLIE-31)是评价癫痫患者生活质量的专用量表。该表涵盖了癫痫患者日常生活中最重要的生活质量问题31个,包括发作担忧、综合生活质量、情感健康、精力、认知功能、药物影响和社会功能等7个方面维度。各分项以百分制计分,乘以各自的权重分,相加得到总分,查表得到T分,分值越高,生活质量越好。
1.4 观察指标
两组患者以日志的形式记录癫痫发作情况。分别记录入组前1个月(基线期)以及观察期3个月内的癫痫发作次数,同时评定治疗前及治疗3个月后的PHQ-9评分及QOLIE-31评分,并观察治疗前后患者的血、尿常规、肝肾功能及心电图变化情况。
1.5 统计学方法
采用SPSS 17.0统计软件包进行分析。计量资料用均数±标准差(±s)表示,计数资料采用百分比表示。组间计数资料比较采用χ2检验,每组患者治疗前后比较采用配对t检验,两组间计量资料比较采用独立样本t检验,以P<0.05为差异有统计学意义。
2 结果
2.1 两组患者治疗前后抑郁情况(PHQ-9)比较
观察组与对照组在治疗前PHQ-9评分比较,差异无统计学意义(P>0.05)。治疗3个月后,观察组PHQ-9评分较治疗前显著降低(P<0.05),对照组PHQ-9评分与治疗前比较,差异无统计学意义(P>0.05),观察组PHQ-9评分较对照组显著降低(P<0.05)(表1)。
表1 两组患者治疗前后PHQ-9评分比较(±s)

表1 两组患者治疗前后PHQ-9评分比较(±s)
观察时点 观察组(n=32)对照组(n=31)t值 p值8.71±2.81 8.43±2.64 0.196 0.848治疗3个月后 3.00±1.15 7.86±2.27 -5.050 0.000 t值 8.402 1.922 p值治疗前0.000 0.103
2.2 两组患者治疗前后生活质量(QOLIE-31)比较
两组患者治疗前QOLIE-31评分比较,差异无统计学意义(P>0.05)。治疗3个月后,观察组QOLIE-31评分较治疗前显著增加(P<0.05),对照组QOLIE-31评分较治疗前显著降低(P<0.05),观察组QOLIE-31评分较对照组显著增加(P<0.05)(表2,表3和表4)。
2.3 两组患者治疗前后癫痫发作情况比较
两组患者治疗前癫痫发作次数比较,差异无统计学意义(P>0.05)。治疗3个月后,两组患者癫痫发作次数均显著减少(P<0.05),但观察组较对照组减少更显著,差异有统计学意义(P<0.05)(表5)。
表2 观察组治疗前后生活质量(QOLIE-31)比较(n=32)(±s)

表2 观察组治疗前后生活质量(QOLIE-31)比较(n=32)(±s)
观察时点 对发作担心 生活满意度 情绪 精力/0±10.35治疗3个月后 62.20±11.61 70.60± 8.93 56.00±12.94 52.80±8.35 65.60±7.30 57.60±4.93 57.00±10.93 63.60± 9.37 t值 -12.649 -4.579 -9.731 -7.661 -3.303 -4.053 -3.929 -7.102 p 值 0.000 0.010 0.001 0.002 0.030 0.015 0.017 0.002疲乏 认知功能 药物影响 社会功能 总体健康治疗前 50.20±12.32 60.00±12.79 42.80±10.35 44.20±6.72 59.60±9.86 44.00±8.86 46.80±11.76 50.2
表3 对照组治疗前后生活质量(QOLIE-31)比较(n=31)(±s)
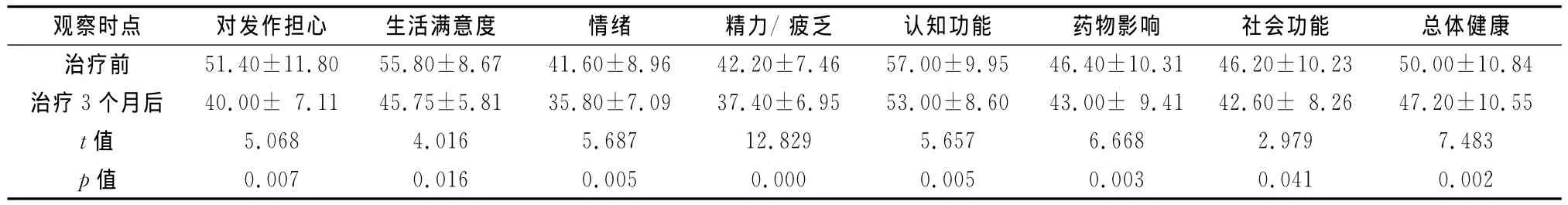
表3 对照组治疗前后生活质量(QOLIE-31)比较(n=31)(±s)
观察时点 对发作担心 生活满意度 情绪 精力/±10.84治疗3个月后 40.00± 7.11 45.75±5.81 35.80±7.09 37.40±6.95 53.00±8.60 43.00± 9.41 42.60± 8.26 47.20±10.55 t值 5.068 4.016 5.687 12.829 5.657 6.668 2.979 7.483 p 值 0.007 0.016 0.005 0.000 0.005 0.003 0.041 0.00疲乏 认知功能 药物影响 社会功能 总体健康治疗前 51.40±11.80 55.80±8.67 41.60±8.96 42.20±7.46 57.00±9.95 46.40±10.31 46.20±10.23 50.00 2
表4 两组患者治疗前后生活质量(QOLIE-31)比较(±s)

表4 两组患者治疗前后生活质量(QOLIE-31)比较(±s)
0±10.35对照组(n=31)51.40±11.80 55.80± 8.67 41.60± 8.96 42.20±7.46 57.00±9.95 46.40±10.31 46.20±10.23 50.00±10.84 t值 -0.157 0.608 0.196 0.445 0.415 -0.395 0.086 0.030 p 值 0.879 0.560 0.850 0.668 0.689 0.703 0.934 0.977治疗3个月后 观察组(n=32)62.20±11.61 70.60±8.93 56.00±12.94 52.80±8.35 65.60±7.30 57.60±4.93 57.00±10.93 63.60± 9.37对照组(n=31)40.00± 7.11 45.75±5.81 35.80± 7.09 37.40±6.95 53.00±8.60 43.00±9.41 42.60± 8.26 47.20±10.55 t值 3.648 5.205 3.061 3.170 2.497 3.074 2.350 2.600 p 值 0.007 0.001 0.016 0.013 0.037 0.015 0.047 0.03疲乏 认知功能 药物影响 社会功能 总体健康治疗前 观察组(n=32)50.20±12.32 60.00±12.79 42.80±10.35 44.20±6.72 59.60±9.86 44.00± 8.86 46.80±11.76 50.2观察时点 对发作担心 生活满意度 情绪 精力/2
表5 两组患者治疗前后癫痫发作情况比较(次/月,±s)
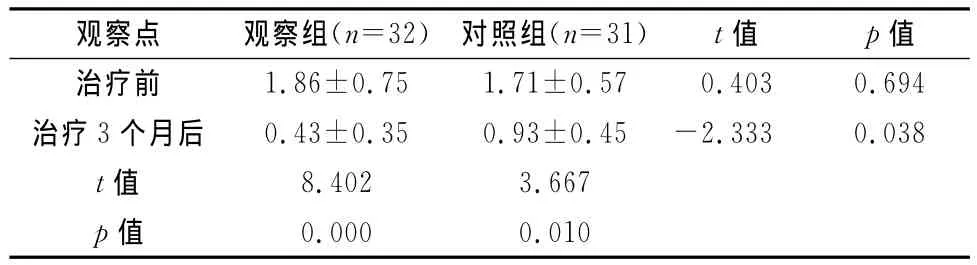
表5 两组患者治疗前后癫痫发作情况比较(次/月,±s)
观察点 观察组(n=32)对照组(n=31)t值 p值1.86±0.75 1.71±0.57 0.403 0.694治疗3个月后 0.43±0.35 0.93±0.45 -2.333 0.038 t值 8.402 3.667 p值治疗前0.000 0.010
2.4 不良反应发生情况
观察组不良反应发生率为9.38%(3/32),主要表现为恶心、头晕及腹泻等,对照组不良反应发生率为6.45%(2/31),主要表现为头晕、嗜睡等,两组不良反应轻,均未做特殊处理。两组患者不良反应的发生率及治疗前后的心电图、血常规、尿常规和肝肾功能等各项指标比较,差异无统计学意义(P>0.05)。两组均无癫痫加重病例。
3 讨论
舒肝解郁胶囊主要由贯叶金丝桃和刺五加等组成。贯叶金丝桃抗抑郁机制可能为抑制中枢的5-HT、DA和NE等神经递质的再摄取,使突触间隙的单胺递质浓度升高,以及对单胺氧化酶的抑制作用而产生抗抑郁效果。刺五加具有镇静、抗疲劳、促进细胞免疫和体液免疫作用,影响可溶性黏附因子附着蛋白及受体,促进囊泡转运、停泊、融合和释放,增加突触间隙神经递质水平,二者合用具有很好的抗抑郁疗效[9-10]。本研究结果表明,舒肝解郁胶囊治疗3个月后,其PHQ-9评分较治疗前显著降低(P<0.05),而未经舒肝解郁胶囊治疗的对照组治疗前后PHQ-9评分比较,差异无统计学意义(P>0.05),同时观察组PHQ-9评分较对照组显著降低(P<0.05),说明舒肝解郁胶囊对癫痫合并的轻中度抑郁具有良好疗效。治疗组癫痫发作次数较对照组减少更显著,差异有统计学意义(P<0.05),提示在治疗癫痫的同时治疗抑郁,对癫痫的控制更加有利。
癫痫治疗的最终目标之一就是提高患者的生活质量。本研究结果表明,治疗3个月后,治疗组QOLIE-31评分较治疗前及对照组显著增加(P<0.05),提示舒肝解郁胶囊还可以改善癫痫患者的生活质量。研究[16-17]表明,癫痫发作的频率、抑郁、焦虑和抗癫痫药物的副作用等是影响癫痫患者生活质量下降最主要的预测因素,因此,推测舒肝解郁胶囊提高癫痫患者生活质量的机制可能与其改善了患者的抑郁,并协同减少了癫痫发作次数等有关。
本研究表明,舒肝解郁胶囊治疗组的不良反应与对照组比较,差异无统计学意义,无癫痫加重病例,提示舒肝解郁胶囊治疗癫痫合并的抑郁安全性良好,与既往的研究[9-11]一致。
综上所述,舒肝解郁胶囊治疗癫痫合并轻中度抑郁症安全有效,癫痫发作无加重,可以用于癫痫合并轻中度抑郁症的治疗。但由于本研究样本量较少,观察时间较短,因此,需扩大样本量并延长观察期后,进一步评价舒肝解郁胶囊治疗癫痫合并轻中度抑郁症的疗效及安全性。
[1]Catena-Dell'Osso M,Caserta A,Baroni S,et al.The relationship between epilepsy and depression:an update[J].Current Medicinal Chemistry,2013,20(23):2861-2867.
[2]Kanner AM.Depression and epilepsy:a bidirectional relation[J].Epilepsia,2011,52(1):21-27.
[3]Kanner AM.Depression and epilepsy:a review of multiple facets of their close relation[J].Neurologic Clinics,2009,27(4):865-880.
[4]Cotterman-Hart S.Depression in epilepsy:Why aren't we treating?[J].Epilepsy & Behavior,2010,19:419-421.
[5]De Oliveira GN,Kummer A,Salgado JV,et al.Psychiatric disorders in temporal lobe epilepsy:an overview from a tertiary service in Brazil[J].Seizure,2010,19(8):479-484.
[6]Gilliam F,Penovich PE,Eagan CA,et al.Conversations between community-based neurologists and patients with epilepsy:results of an observational linguistic study[J].Epilepsy & Behavior,2009,16(2):315-320.
[7]Sarris J,Kavanagh DJ.Kava and St.John’s Wort:current evidence for use in mood and anxiety disorders[J].Journal of Alternative and Complementary Medicine,2009,15(8):827-836.
[8]Kasper S,Gastpar M,Möller HJ,et al.Better tolerability of St.John’s wort extract WS 5570compared to treatment with SSRIs:a reanalysis of data from controlled clinical trials in acute major depression [J]. International Clinical Psychopharmacology,2010,25(4):204-213.
[9]姚军,李清伟,季建林,等.不同剂量舒肝解郁胶囊治疗轻中度抑郁症的多中心、随机、开放、对照研究[J].中国新药与临床杂志,2014,33(8):568-572.
[10]孙新宇,陈爱琴,许秀峰,等.舒肝解郁胶囊治疗轻中度抑郁症的随机双盲安慰剂对照研究[J].中国新药杂志,2009,18(5):413-416.
[11]黄玲,陈路佳,刘立立,等.舒肝解郁胶囊治疗轻、中度抑郁的疗效与安全性的系统评价[J].中国药房,2013,24(32):73-76.
[12]Kroenke K,Spitzer RL.The PHQ-9:a new depression diagnostic and severity measure[J].Psychiatr Ann,2002,32(9):509-515.
[13]Zhang YL,Liang W,Chen ZM,et al.Validity and reliability of Patient Health Questionnaire-9and Patient Health Questionnaire-2to screen for depression among college students in China[J].Asia-Pacific Psychiatry,2013,5(4):268-275.
[14]Lai BP,Tang AK,Lee DT,et al.Detecting postnatal depression in Chinese men:a comparison of three instruments[J].Psychiatry Res,2010,180(2-3):80-85.
[15]伍文清,肖玉莲,陈葵.盐酸帕罗西汀治疗癫痫并发抑郁的临床研究[J].中国康复理论与实践,2012,18(2):169-171.
[16]Shubham M,Alok T,Richa T,et al.Study of Interrelationship of Depression,Seizure Frequency and Quality of Life of People with Epilepsy in India[J].Ment Illn,2014,6(1):5169.
[17]Lee SJ,Kim JE,Seo JG,et al.Predictors of quality of life and their interrelations in Korean people with epilepsy:a MEPSY study[J].Seizure,2014,23(9):762-768.
