纳米、微米一水草酸钙和二水草酸钙对非离子表面活性剂NP-40的吸附差异
2015-12-01温小玲甘琼枝欧阳健明
温小玲 甘琼枝 欧阳健明
(暨南大学生物矿化与结石病防治研究所,暨南大学化学系,广州510632)
纳米、微米一水草酸钙和二水草酸钙对非离子表面活性剂NP-40的吸附差异
温小玲 甘琼枝 欧阳健明*
(暨南大学生物矿化与结石病防治研究所,暨南大学化学系,广州510632)
为探究CaOx结石的形成机理,测定了不同浓度NP-40(cNP-40)存在下各尺寸COM或COD晶体的吸附量;采用X射线衍射和红外光谱研究吸附前后晶体是否发生晶相改变;采用ζ电位仪测定吸附后晶体表面的ζ电位随cNP-40的变化。结果表明:不同尺寸COM、COD对NP-40的吸附能力大小顺序为:50 nm>100 nm>1 μm>>3 μm>10 μm;相同尺寸的晶体,COM的吸附量大于COD。随着cNP-40增加,3 μm和10 μm的COM、COD晶体的吸附曲线为S型,而50 nm、100 nm、1 μm的COM、COD晶体的吸附曲线为直线型。加入NP-40后,ζ电位绝对值与各晶体的吸附密度成正相关。提出了草酸钙晶体吸附NP-40的分子模型。晶体尺寸越小,对NP-40的吸附量越大。非离子表面活性剂虽然自身不带电荷,但吸附到COM、COD晶体表面后可以通过位阻斥力来增加晶体悬浮液的稳定性,有利于抑制草酸钙结石的形成。
草酸钙;晶体尺寸;非离子表面活性剂;表面吸附;吸附模型
0 前言
泌尿系结石已经成为威胁人类健康的一种常见病和多发病,目前还没有十分有效的预防方法,80%以上的尿结石患者病因不清[1-2]。导致尿石形成的主要因素包括尿液中成石物质的过饱和,晶体成核、聚集和生长,抑制剂减少或促进剂增多以及肾小管上皮细胞的受损。尿液组分和尿微晶性质与结石的形成密切相关[3-4]。研究表明,尿液中含有许多可以吸附在晶体表面的物质,虽然它们在尿液中的含量非常低,对尿石盐的过饱和度影响较小,但能改变晶体表面的荷电性质,从而改变晶体生长习性和聚集速度[5]。人体尿液中存在的蛋白质、氨基酸、胆汁盐等在处于等电点时会具有非离子表面活性剂的性质[6-7]。
草酸钙有3种水合物形式,即一水草酸钙(COM)、二水草酸钙(COD)和三水草酸钙(COT),其中COM是热力学最稳定的形式,COD次之,COT热力学最不稳定,在尿石中也很少见。COT很容易在溶液中发生晶相转变;相比之下,COM和COD是肾结石的主要成分[8]。
表面活性物质的类型和浓度均会影响尿石盐如草酸钙(CaOx)晶体的生长动力学过程和晶体的最终形貌。例如,阳离子表面活性剂十六烷基三甲基溴化铵(CTAB)能影响COM晶体的形貌,生成蝴蝶状的COM晶体[9],且随CTAB浓度的增加,生成的晶体尺寸会减小;而阴离子表面活性剂十二烷基磺酸钠(SDS)不仅能影响草酸钙的形貌,还能诱导亚稳态的COD的形成。二辛基磺基琥珀酸钠(AOT)可以优先吸附在一水草酸钙(COM)的(101)和(010)晶面上,改变COM晶体的形貌,生成的COM晶体变得更薄、更长[10],并能抑制或延缓COM晶体的生长,同时促进COD晶体的形成。在阴、阳离子混合表面活性剂形成的囊泡体系中制备的COM为十二面体和星形[11],且比没有添加表面活性剂时的尺寸更大。
与阴离子表面活性剂相比,非离子表面活性剂乳化能力更高,且在水中不发生电离,因而具有离子型表面活性剂所不具有的某些特性,如在水中和有机溶剂中都有较好的溶解性,在溶液中稳定性高,不会影响溶液的离子强度,也不易受强电解质(如无机盐、酸、碱)的影响。因此,近年来越来越多的人研究非离子表面活性剂。Sharma等[12]研究了非离子表面活性剂九乙二醇单十二醚(C12E9)在SiO2纳米粒子表面的吸附,加入C12E9后可以使SiO2的团聚成为一个可逆的过程,而SiO2在水溶液中的团聚是不可逆的。加入非离子表面活性剂六乙二醇单十二醚(C12E6)后,SiO2的稳定性也会随C12E6的浓度增大而增大[13]。Paria等[14]研究了4个壬基酚聚氧乙烯醚(NP)系列的非离子表面活性剂在砂上的吸附动力和吸附平衡,发现NP的吸附量大小与非离子表面活性剂的头部面积和乙二醇(EO)的数量有关。非离子表面活性剂Tween 80可以吸附在草酸钙表面,阻碍草酸钙的团聚,从而抑制草酸钙的沉积[15]。C16E8能聚集草酸根离子,从而促进COM的成核和初期生长,当晶体生长到临界大小,由于表面活性剂的吸附,进一步的增长会减缓[9]。可见,非离子表面活性剂与尿液中微晶的吸附有可能影响尿结石的形成。
我们的前期研究[16-17]表明,尿液中既存在微米级的晶体,也存在纳米级的晶体。由于晶体尺寸的不同会导致晶体比表面积、表面能和ζ电位等存在差异,因而影响其与尿液中存在的各种物质(如蛋白质、葡胺聚糖等大分子和表面活性剂等小分子)的吸附能力,使得尿微晶的生长、聚集及其与肾上皮细胞的粘附受到影响,并最终影响结石的形成。但目前已有的报道主要是针对微米级的草酸钙晶体,对纳米尺寸草酸钙晶体的吸附研究未见报道。此外,各尺寸草酸钙晶体与非离子表面活性剂的作用存在怎样的差异还不清楚。基于此,本文选取纳米、微米COM和COD为研究对象,研究了NP-40对不同尺寸COM、COD的吸附特性。
1 实验材料与方法
1.1 试剂与仪器
壬基酚聚氧乙烯醚(NP-40,Aladdin公司)为分析纯试剂,氯化钙(CaCl2)、草酸钾(K2Ox)、碘化钾(KI)、柠檬酸三钠(Na3cit)、硫酸镁(MgSO4)和氯化钾(KCl)等均为分析纯试剂。试验用水均为二次蒸馏水。
Varian Cary 500型紫外可见分光光度计(美国Varian公司)。Nicolet 6700型傅里叶变换红外光谱仪(美国Nicolet公司)。Zetasizer Nano-ZS型纳米粒度-Zeta电位分析仪(英国Malvem公司)。D/ max2400X射线粉末衍射仪(日本理学)。
1.2 不同尺寸COM、COD晶体的合成、表征
通过改变反应物浓度、反应温度、搅拌速度、滴加方式和溶剂,可以控制COM和COD的尺寸。例如,反应物浓度越大,反应温度越低,搅拌速度越快,生成的晶体尺寸越小。具体制备过程如下。
COM晶体:不同尺寸的COM晶体由CaCl2溶液与K2Ox溶液直接反应获得。以无水乙醇-水混合溶液(VH2O∶V乙醇=1∶1)为溶剂,将浓度均为100 mmol· L-1的CaCl2和K2Ox溶液各50 mL在25℃快速混合,高速搅拌(1 250 r·min-1)反应6 min后离心,产物用无水乙醇超声洗2次,抽滤,干燥,得到尺寸50 nm的COM晶体。以水为溶剂,改变反应物浓度为300 mmol·L-1,得到尺寸100 nm的COM晶体。改变反应物浓度为20 mmol·L-1,升高温度至60℃,得到尺寸1 μm的COM晶体。降低反应物浓度至5 mmol·L-1,升高温度至75℃,混合方式改为逐滴滴加,得到尺寸3 μm的COM晶体。COM-10 μm制备方法同COM-3 μm,仅减慢滴加速度和搅拌速度。晶体后处理方法均同50 nm的COM晶体。
COD晶体:不同尺寸COD晶体的制备需要加入pH=6.8的缓冲溶液,其组成为:19.26 mmol·L-1Na3cit、23.1 mmol·L-1MgSO4和12.7 mmol·L-1KCl。将4 mol·L-1的CaCl2溶液12 mL加入188 mL缓冲溶液(pH=6.8)中,在5℃、快速搅拌(1 250 r·min-1)下直接倒入50 mL 5℃的250 mmol·L-1K2Ox溶液,反应5 min后离心,二次水洗2次,无水乙醇洗2次,抽滤,干燥,得到尺寸50 nm的COD晶体。COD-100 nm的制备方法同COD-50 nm,仅将反应温度由5℃增加到25℃。将CaCl2和K2Ox的浓度分别降低至14.8 mmol·L-1和3.8 mmol·L-1,反应温度降低至5℃,搅拌速度降低至500 r·min-1,得到尺寸1 μm的COD晶体。COD-3 μm的制备方法同COD-1 μm,仅将反应温度及陈化温度由5℃增加至25℃。CO D-10 μm的制备方法同COD-1 μm,但反应物最终浓度为cCaCl2=12.5 mmol·L-1,cK2Ox=6.4 mmol·L-1,反应温度为25℃。
X射线粉末衍射(XRD)和红外光谱(FTIR)表明合成的晶体为纯的目标产物。采用Image Pro Plus 5.02图像软件(Media Cybernetics,USA)分析晶体的数量和尺寸,得出各晶体的平均尺寸分别为50 nm、200 nm、1 μm、3 μm和10 μm。为了方便起见,我们采用上述整数表示。
各晶体的比表面(SBET)和孔径测定在全自动比表面积及孔隙度分析仪(Tristar 3000,Micromeritics, USA)上进行,以He作为载气,N2为被吸附气体。仪器自动对数据进行BJH(Barrett-Joyner-Halenda)方法处理,得到晶体的孔容、孔径和比表面积。
1.3 NP-40吸附实验
用移液管移取不同体积的NP-40溶液于100 mL的容量瓶,加入二次蒸馏水定容,配置成起始浓度(C0)分别为0、30、60、90、120、150、180、210、250、300、350、400、450 mg·L-1的NP-40标准溶液。准确称取13份50 mg的COM和13份50 mg的COD分别置于26个25 mL的烧杯中,分别加入上述NP-40标准溶液15 mL。超声10 min使晶体完全分散后,放入37℃恒温干燥箱中,吸附24 h后取出离心,取上清液测定剩余的NP-40浓度ceq,同时测量悬浮液的ζ电位。根据公式计算出晶体对NP-40的吸附量Qads。以c0为横坐标,Qads为纵坐标绘制吸附等温线。NP-40的浓度(cNP-40)测定参照文献[18],其标准曲线线性方程为y=0.007 2x-0.010 4,R2=0.998 5。
1.4 吸附前后晶体的XRD和FTIR表征
尺寸50 nm、100 nm、1 μm、3 μm和10 μm的COM、COD晶体与NP-40吸附24 h后,将各悬浮液离心,去除上清液,晶体涂抹在洁净的石英片上,放入55℃烘箱中,干燥后进行XRD和FTIR测试。
1.5 草酸钙晶体的稳定性实验
称取5 mg的COM或COD晶体于2个25 mL的烧杯中,分别加入浓度为0和150 mg·L-1的NP-40溶液,超声10 min至完全分散。用UV-Vis分光光度计在波长620 nm处测定COM、COD悬浊液在静置不同时间后的光密度(At)。并参照文献[19-20]中聚集系数的计算方法,将静置时间t的光密度(At)与静置前(t=0)的光密度(A0)的差值称为沉降系数(SC),即:SC=(A0-At)×100,式中100是为了使SC由小数转化为整数,SC越大表示悬浊液中晶体的沉降程度越大。
2 结果与讨论
2.1 不同尺寸COM对NP-40的吸附曲线
图1A为不同尺寸COM晶体对NP-40的吸附曲线,出现2种情况:对于3种尺寸较小的COM晶体,即COM-50 nm、COM-100 nm和COM-1 μm晶体,其对NP-40的吸附量随cNP-40的增加几乎呈直线增加(图1a-1c);而对于2种大尺寸COM,即COM-3 μm和COM-10 μm,其吸附曲线为S型(图1d, 1e),且其吸附量小于3个小尺寸的COM。各尺寸COM对NP-40的吸附能力为:50 nm>100 nm>1μm>>3 μm>10 μm。
(1)COM-3 μm和COM-10 μm对NP-40的吸附曲线为S型吸附曲线,可大致分为3个阶段:
在浓度较低的阶段1,即在cNP-40<60 mg·L-1时,晶体表面的吸附量随cNP-40增加而缓慢增加。此时主要是由范德华力(归因于非离子表面活性剂的高极性和高的分子质量)产生的单层吸附,此时NP-40分子间无相互作用。在阶段1开始时,COM晶体表面吸附的NP-40分子很少(图2a);而阶段1完成时,晶体表面基本被平躺的NP-40分子铺满(图2b)。阶段1基本不涉及表面活性剂的性质和晶体表面的性质。
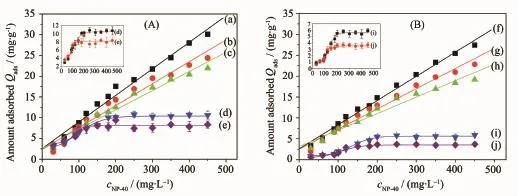
图1 不同尺寸COM、COD晶体的吸附量随NP-40浓度的变化Fig.1Absorption amount change of various sizes of COM and COD crystals with the concentration of NP-40

表1 不同尺寸COM和COD的比表面积以及对NP-40的最大吸附量和吸附密度Table 1Specific surface area of COM and COD with different sizes as well as the maximum adsorption quantity and adsorption density of NP-40
在阶段2中,即60 mg·L-1<cNP-40<180 mg·L-1时,吸附量迅速增加(见图1A中插图)。在阶段2刚开始时,NP-40分子的亲水基团与COM表面有很强的吸引力,使得疏水烷基链慢慢翘向上面(图2c);随着cNP-40增加,被吸附的NP-40分子中的烷基链逐渐聚集在一起(图2d),但亲水基仍平躺于界面上,分子紧密有序排列。当cNP-40继续增加时,新增的NP-40分子烷基链会与已经吸附在晶体表面的NP-40分子外露的烷基链相互作用,形成双分子层(图2e),或NP-40分子通过聚集优化表面的总曲率,来减小表面活性剂极性链间的空间排斥,形成胶束(图2f)。
阶段3中,即cNP-40>180 mg·L-1时,吸附量达到饱和稳定阶段。此时,随着非离子表面活性剂浓度的增加,溶液中会继续形成胶束或半胶束,但不会吸附在晶体表面(图2g)。

图2 NP-40分子吸附在COM-3 μm或COM-10 μm晶体表面的结构示意图Fig.2Structural diagrams of NP-40 molecules adsorbed on surface of COM-3 μm or COM-10 μm
(2)COM-50 nm、COM-100 nm和COM-1 μm对NP-40的吸附曲线为直线型
一般而言,当非离子表面活性剂通过亲水基吸附在固体表面,其吸附曲线为S型;而当其通过疏水基吸附在固体表面时,吸附曲线为Langmuir型,即L型。虽然3和10 μm的COM晶体与NP-40的吸附曲线属于S型归因于NP-40的亲水基与COM吸附,但3个小尺寸COM晶体(50 nm、100 nm和1 μm)与NP-40的吸附曲线为直线型却并不是因为NP-40通过疏水基吸附在晶体表面,而是归因于小尺寸晶体的吸附能力很强,在本实验的NP-40浓度范围内(<450 mg·L-1),吸附还没有达到饱和所致。
随着晶体尺寸的不断减小,其比表面积显著增加(表1),吸附位点增加,晶体表面能及表面结合能都迅速增大,因此对表面活性剂的吸附量显著增加。此外,晶体尺寸越小,处在表面的原子数越多,这些表面原子周围缺少相邻的原子,有许多悬空键,具有不饱和性质,易与其它原子相结合而稳定下来,故具有很大的化学活性。例如当粒径尺寸为1 nm时,其表面原子数可达到总原子数的99%[21]。因此,在最大实验浓度cNP-40=450 mg·L-1时,3个小尺寸COM晶体的吸附仍然没有达到平衡状态(即它们还可以进一步吸附NP-40)。从表1中各尺寸COM晶体的吸附密度亦可以看出,在最大浓度cNP-40=450 mg·L-1时,3个小尺寸COM的吸附密度(1.12~1.62 N·nm-2)远小于2个大尺寸的COM晶体(6.24~9.81 N·nm-2),这也间接说明了小尺寸COM晶体在cNP-40=450 mg· L-1时还未达到饱和。
2.2 不同尺寸COD对NP-40的吸附曲线
不同尺寸COD晶体与NP-40的吸附曲线(图1B)与COM晶体的相似。对于3种小尺寸晶体(COD-50 nm、COD-100 nm和COD-1 μm),其吸附曲线亦为直线型,且在cNP-40=450 mg·L-1时均未达到吸附饱和。而对于2种大尺寸晶体(COD-3 μm、COD-10 μm),其吸附曲线为S型,且吸附量均小于3个小尺寸的COD,归因于其比表面积小于3个小尺寸的COD所致(表1)。各尺寸COD对NP-40的吸附能力为:50 nm>100 nm>1 μm>>3 μm>10 μm。
2.3 吸附NP-40后COM和COD晶体的ζ电位变化
为了表征各尺寸COM和COD吸附NP-40后晶体表面的电荷变化,测定了他们的ζ电位。根据各尺寸晶体的吸附曲线类型(图1),分别选取50 nm和3 μm的COM、COD作为代表,其结果如图3所示。可以看出,ζ电位随cNP-40变化呈现2种不同情况:
对于微米级的COM-3 μm和COD-3 μm晶体,在浓度较低时,其ζ电位绝对值随着cNP-40增加而迅速增加,并在cNP-40=180 mg·L-1时达到最大。这是因为大尺寸COM晶体对NP-40的吸附量先随着cNP-40增加而增加,然后达到了吸附饱和。可见,悬浮液中晶体ζ电位的变化情况与晶体对NP-40吸附量的变化趋势(图1)基本一致,这也进一步验证了晶体对于NP-40的吸附。
对于纳米级的COM-50 nm和COD-50 nm晶体,随着cNP-40不断增加,其ζ电位均不断缓慢变负,因为纳米晶体对NP-40的吸附量随cNP-40的增大而不断增大(图1)。
加入中性NP-40后,ζ电位变化本应不大,但是ζ电位绝对值随cNP-40增大而增大,说明吸附在COM、COD表面的NP-40提供了足够的空间稳定性来保持COM、COD悬浮液的稳定,这是因为NP-40醚键的氧原子(-O-)可与草酸钙表面的钙离子形成了配位键,提供位阻斥力,从而改变ζ电位和晶体的电荷面密度所致。NP-40结构式如图4b所示,其分子量为616.82,吸附在COM、COD表面的NP-40分子占据了较大的空间,在晶体周围提供的一层空间屏障,可阻止颗粒相互团聚,使颗粒分散,增加颗粒的稳定性[23]。Katepalli等[24]与Han等[25]的研究结果表明,如果吸附的非离子表面活性剂能够增加粒子的稳定性,则ζ电位会变负[25];若不能增加粒子的稳定性,则ζ电位变化不大[24]。表2为cNP-40=150 mg·L-1时COM和COD晶体的吸附密度和晶体表面ζ电位变化值,两者呈正相关。例如,COM-3 μm的吸附密度最大(5.31 N·nm-2),NP-40提供的位阻斥力最明显,所以ζ电位的变化值最大。正因为在相同的cNP-40时微米级晶体对NP-40的吸附密度大于纳米级晶体,因此,在相同cNP-40时,微米晶体的ζ电位绝对值大于纳米晶体。
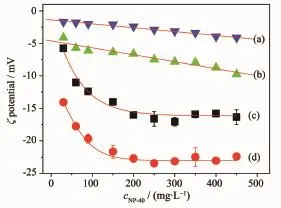
图3 不同尺寸COM和COD晶体表面ζ电位随NP-40浓度的变化Fig.3ζ potential change of different sizes of COM and COD crystals with concentration of NP-40

表2 在cNP-40=150 mg·L-1时微/纳米COM和COD晶体的ζ电位和吸附密度Table 2ζ potential and adsorption density of micron/nano COM and COD in presence of 150 mg·L-1NP-40
2.4不同尺寸COM、COD晶体对NP-40的吸附量比较
比较图1A与图1B可以看出,在相同条件下,COD的吸附量均小于相应的COM晶体。在cNP-40= 450 mg·L-1时各晶体的吸附量见表1。这一方面是因为在制备COD时必须加入缓冲溶液,从而引入了Mg2+和柠檬酸根离子,使得COD表面可能吸附了少量的Mg2+和柠檬酸根离子[6]。柠檬酸根含有3个非平面的羧基和1个羟基,能分别与草酸钙晶体表面的钙离子和草酸根离子形成配位键和氢键[26],从而降低了NP-40与COD晶体表面的作用位点。另一方面是因为COM和COD的表面离子结构不一样,COD晶面暴露大量草酸根离子和水分子[23],增加了COD的亲水性,掩蔽了其表面的其他吸附。
尿液中的大分子(如蛋白质)与草酸钙晶体之间存在相互作用。疏水作用、静电作用、化学作用和氢键作用均可促进表面活性剂的吸附[27]。蛋白质分子可以通过静电作用与荷电表面结合;通过疏水作用与疏水表面结合;或通过氢键作用与亲水表面结合[28]。Farmanesh等[29]指出,富含酸性基团(如-COO-)的晶体生长抑制剂通过钙桥与草酸钙晶体表面的Ca2+离子连接,形成“(COM)COO-……Ca2+……-OOC(抑制剂)”,而阳离子基团(如-NH3+)则通过静电作用与与晶体表面带负电荷的草酸根结合,形成“(COM)COO-……+H3N(抑制剂)”。由于草酸钙是亲水的,而NP-40不带电荷,因此草酸钙与NP-40的吸附不可能通过疏水作用和静电作用。文献[30]报道乙氧基化表面活性剂可通过氢键吸附到二氧化硅表面,因此可以推测,NP-40分子中的羟基可以与草酸钙表面的草酸根形成氢键(图4),而NP-40中的醚键氧原子(-O-)还可以与晶体表面的钙离子形成配位键,这导致了吸附NP-40后晶体表面的ζ电位下降(图3)。
由于不同尺寸的COM和COD晶体吸附NP-40后可以稳定晶体在尿液中的存在,这提示尿液中不带电荷的物质(如处于等电点的蛋白质、氨基酸)也可以吸附到晶体表面,通过位阻斥力来增强尿微晶的稳定性,从而抑制草酸钙结石的形成。

图4 草酸钙晶体吸附NP-40的分子模型(a)和NP-40的分子结构(b)Fig.4Schema of NP-40 adsorbed on calcium oxalate crystal(a)and the molecular structure of NP-40(b)
2.5 NP-40对COM、COD悬浮液稳定性的影响
2.5.1 悬浮液的沉降
图5为COM和COD分散在NP-40的水溶液中后溶液光密度值随时间的变化情况。加入NP-40后,晶体悬浮液的沉降系数(SC)减小,表明晶体的沉降变慢,即NP-40能增加草酸钙晶体悬浮液的稳定性。这与晶体吸附NP-40后的ζ电位变化结果(图3)一致。晶体吸附NP-40后,其表面的ζ电位绝对值增大,晶体间排斥力增大,使得晶体的沉降速度变慢。由于3 μm的晶体重力较大,其沉降速度大于50 nm的晶体。从图5可以看出,COM-3 μm和COD-3 μm在t=30 min时就已经沉降完全,SC亦不再改变;而COM-50 nm和COD-50 nm在t=30 min时还在继续沉降,SC绝对值继续增大。
2.5.2 吸附后晶体的FTIR谱与XRD图
各尺寸COM和COD晶体吸附NP-40后的XRD图和FTIR谱如图6和7所示。在XRD图中,COM晶体(图6A)均检测到晶面间距d=0.593、0.365、0.296和0.235 nm归属于COM晶体(101)、(020)、(202)和(130)晶面的衍射峰(PDF卡号:20-231)[31]。而各尺寸的COD晶体(图6B)均检测到d= 0.618、0.442、0.277和0.224 nm依次归属于COD晶体(200)、(211)、(411)和(213)晶面的衍射峰(PDF卡号:17-541)[31],但是在COD晶体中也检测到了晶面间距d=0.593、0.365、0.296和0.235 nm归属于COM晶体(101)、(020)、(202)和(130)晶面的衍射峰。说明部分COD晶体会转化为COM晶体,这主要是由于COD晶体不如COM晶体稳定,处于亚稳定状态[1]。Cody等[32]研究表明COD表面单位面积内所具有的吸附位点最少,吸附能力最弱,所以抑制剂要想找到这些位点,必须增加抑制剂的浓度。由于NP-40通过氢键和配位键与COD的吸附位点键合,键合能力不强[27],所以对晶相转化的抑制能力没有阴离子表面活性剂的强,会有部分COD转化成COM。

图5 纳米、微米COM、COD晶体悬浊液在纯水和150 mg·L-1NP-40溶液中放置不同时间后的沉降系数Fig.5Sedimentation coefficient of suspensions of nano-/micron-sized COM and COD crystals in pure water and in presence of 150 mg·L-1NP-40 after placed at different times

图6 吸附NP-40后不同尺寸COM和COD的XRD图Fig.6XRD patterns of COM and COD with different sizes after absorbed NP-40
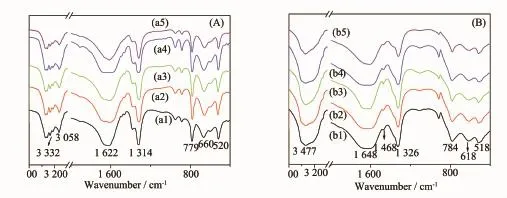
图7 不同尺寸COM和COD晶体吸附NP-40后的红外谱图Fig.7FTIR spectra of COM and COD with different sizes after absorbed NP-40
在FTIR谱中,COM和COD晶体均在3 485~3 047 cm-1处有一个宽的归属于结晶水O-H键的伸缩振动峰,差别在于COM在此区间内分裂成5个吸收峰,而COD只有一个宽的吸收峰[33]。COM晶体中羧基(COO-)的不对称伸缩振动和对称伸缩振动分别在1 622和1 314 cm-1附近,而COD晶体的分别在1 648 cm-1和1 326 cm-1附近。
FTIR谱没有检测到NP-40的吸收峰,归因于NP-40在COM和COD的吸附量很少,NP-40的吸收峰被草酸钙的吸收峰所掩盖。例如,COM-50 nm对NP-40最大吸附量(30.1 mg·g-1)也只占晶体的3.01%,因此,红外难以检测到NP-40的吸收峰。
3 结论
尺寸分别为50 nm、100 nm、1 μm、3 μm和10 μm的COM和COD晶体均可对非离子表面活性剂NP-40进行吸附。晶体尺寸越小,比表面积越大,对NP-40的吸附量越大。NP-40可以通过配位键或氢键吸附到COM、COD晶体表面,导致ζ电位绝对值增大,晶体悬浮液稳定性增加,沉降速度减慢,这有利于抑制草酸钙结石的形成。
[1]Zhao Z,Xia Y,Xue J,et al.Cryst.Growth Des.,2013,14(2): 450-458
[2]Prywer J,Sadowski R R,Torzewska A.Cryst.Growth Des., 2015,15:1446-1451
[3]Hussein N S,Sadiq S M,Kamaliah M D,et al.Saudi J. Kidney Diseases Transplantation,2013,24(3):630
[4]Farmanesh S,Ramamoorthy S,Chung J,et al.J.Am.Chem. Soc.,2014,136(1):367-376
[5]Hess B,Kok D J.Kidney Stones:Mesical and Surgical Management.Philadelphia:Lippincott-RavenPublishers, 1996:3-32
[6]SikiriM,Filipovi-Vincekovi N,Babi-Ivani V,et al.J.Colloid Interface Sci.,1999,212(2):384-389
[7]Saso L,Grippa E,Gatto M T,et al.Int.J.Urol.,2001,8(3): 124-127
[8]Zhang D,Qi L,Ma J,Cheng H.Chem.Mater.,2002,14(6): 2450-2457
[9]Wei X,Yang J,Li Z,et al.Collodis Surf.A,2012,401:107-115
[10]Sikiri M D,Füredi-Milhofer H.Adv.Colloid Interface Sci., 2006,128:135-158
[11]Dong R,Weng R,Dou Y,et al.J.Phys.Chem.B,2010,114 (6):2131-2139
[12]Sharma K P,Aswal V K,Kumaraswamy G.J.Phys.Chem. B,2010,114(34):10986-10994
[13]Thwala J M,Goodwin J W,Mills P D.Colloids Surf.A,2008, 331(3):162-174
[14]Paria S,Yuet P K.Ind.Eng.Chem.Res.,2007,46(1):108 -113
[15]Berezin M B,Kustov A V,Smirnova N L,et al.Russ.J. Inorg.Chem.,2011,56(1):139-140
[16]Gao J,Xue J F,Xu M,et al.Int.J.Nanomed.,2014,9:4399 -4409
[17]LIU Yi-Ming(柳一鸣),XIA Zhi-Yue(夏志月),OUYANG Jing-Ming(欧阳健明),et al.Chinese J.Inorg.Chem.(无机化学学报),2013,29(5):903-909
[18]Brown D G,Jaffe P R.Environ.Sci.Technol.,2001,35: 2022-2025
[19]Kulaksizoglu S,Sofikerim M,Cevik C.Int.J.Urol.,2007,14 (3):214-218
[20]Christmas K G,Gower L B,Khan S R,et al.J.Colloid Interface Sci.,2002,256(1):168-174
[21]LI Quan(李泉),ZENG Guang-Fu(曾广赋),XI Shi-Quan (席时权).Chemistry(化学通报),1995(6):29-34
[22]Fuangswasdi A,Charoensaeng A,Sabatini D A,et al.J. Surfactants Deterg.,2006,9(1):21-28
[23]Tunik L,Füredi-Milhofer H,Garti N.Langmuir,1998,14 (12):3351-3355
[24]Katepalli H,John V T,Bose A.Langmuir,2013,29(23): 6790-6797
[25]Han Z,Zhang F,Lin D,et al.Environ.Sci.Technol.,2008, 42(18):6869-6875
[26]Qiu S R,Wierzbicki A,Salter E A,et al.J.Am.Chem. Soc.,2005,127:9036-9044
[27]Zhang R,Somasundaran P.Adv.Colloid Interface Sci.,2006, 123:213-229
[28]Shemetov A A,Nabiev I,Sukhanova A.ACS Nano,2012,6 (6):4585-4602
[29]Farmanesh S,Chung J,Sosa R D.J.Am.Chem.Soc.,2014, 136(36):12648-12657
[30]Nevskaia D M,Guerrero-Ru A,López-González J D.J.Colloid Interface Sci.,1998,205(1):97-105
[31]King M,Mcclure W F,Andrews L C.International center for diffraction data:Newtown Square,PA,1992.
[32]Cody A M,Cody R D.J.Cryst.Growth,1994,135(1):235-245 [33]Yao X Q,Ouyang J M,Peng H,et al.Carbohydr.Polym., 2012,90(7):392-398
Adsorption of Nonionic Surfactant NP-40 on Micron/Nano Calcium Oxalate Monohydrate and Dihydrate Crystals
WEN Xiao-LingGAN Qiong-ZhiOUYANG Jian-Ming*
(Institute of Biomineralization and Lithiasis Research,Jinan University,Guangzhou 510632,China)
In order to study the formation mechanism of calcium oxalate(CaOx)stones,the adsorption amount of COD and COM with different sizes to NP-40 was detected by UV-Vis spectroscopy.Crystal phase transformation before and after adsorption was analyzed by XRD and FT-IR.ζ potential of crystals after the adsorption of various concentration of NP-40(cNP-40)was measured by ζ potential analyzer.The adsorption capacity of COM and COD with different size to NP-40 was:50 nm>100 nm>1 μm>>3 μm>10 μm.The adsorption quantity of COM was greater than COD of the same size.The adsorption curves of COM and COD with size of 3 μm and 10 μm are S-type,while the curves of COM and COD with size of 50 nm,100 nm and 1 μm were linear-type.The absolute values of ζ potential of crystals were positively related to the adsorption density to NP-40.The molecular model of NP-40 adsorbed on CaOxcrystals was proposed in this study.The smaller the crystal size is,the greater the adsorption amount of CaOxcrystals to NP-40 possess.Although nonionic surfactant itself is uncharged,it can be adsorbed onto COM and COD crystals and increase the stability of crystals suspension by steric hindrance,which is conducive to inhibiting the formation of CaOxstones.
calcium oxalate;crystal size;nonionic surfactant;surface adsorption;adsorption model
R69;R329;O614.23+1
A
1001-4861(2014)10-2021-09
10.11862/CJIC.2015.266
2015-03-24。收修改稿日期:2015-08-26。
国家自然科学基金(No.21371077)资助项目。
*通讯联系人。E-mail:toyjm@jnu.edu.cn
