医疗器械通用标准体系研究
2015-12-01肖忆梅李军中国食品药品检定研究院北京市100050
【作 者】肖忆梅,李军中国食品药品检定研究院,北京市,100050
医疗器械通用标准体系研究
【作 者】肖忆梅,李军
中国食品药品检定研究院,北京市,100050
通过对医疗器械通用标准的分类研究,根据这些标准的作用及适用范围,将通用标准分为二级,提出通用标准体系结构设置,并对通用标准体系建设提出意见和建议。
医疗器械;通用标准体系
随着国家对医疗器械标准化工作的日益重视,医疗器械标准的数量快速增长,截止到2014年6月我国已有医疗器械标准1 246项,初步形成了医疗器械标准体系。为了进一步做好标准体系建设工作,完善标准体系结构,更好地发挥标准的技术规范作用,我们对医疗器械标准体系开展了理论研究,通过对现有标准在体系中的地位和适用范围的分析,将现有标准分为通用标准和专用标准,明确提出了医疗器械通用标准体系的概念,并尝试提出通用标准体系建设思路,为进一步完善医疗器械标准体系,理顺结构,优化功能提供技术依据。
1 通用标准的概念
1.1 通用标准的划分
2009年国家标准化管理委员会(SAC)开展的国家标准化体系建设工程将标准划分为基础通用标准、产品标准、方法标准和管理标准[1]等四类标准。国际标准化组织(ISO)将医疗器械标准划分为基础标准、类标准和产品标准[2]等三类。借鉴这两种标准分类方法,结合医疗器械领域特点,我们对医疗器械标准划分为两类:通用标准和专用标准。
医疗器械通用标准是适用于医疗器械全领域,或者多个技术领域并广泛被其他标准所引用的标准,基本对应国家标准化体系建设工程中的基础通用标准、管理标准和部分方法标准;基本对应国际标准中的基础标准和类标准。
医疗器械标准体系中通用标准以外的标准统称为专用标准,是在针对特定的或一族产品、过程或服务的标准,对应国家标准化体系建设工程中的产品标准和部分方法标准,和国际标准的产品标准,具体对应关系见图1。
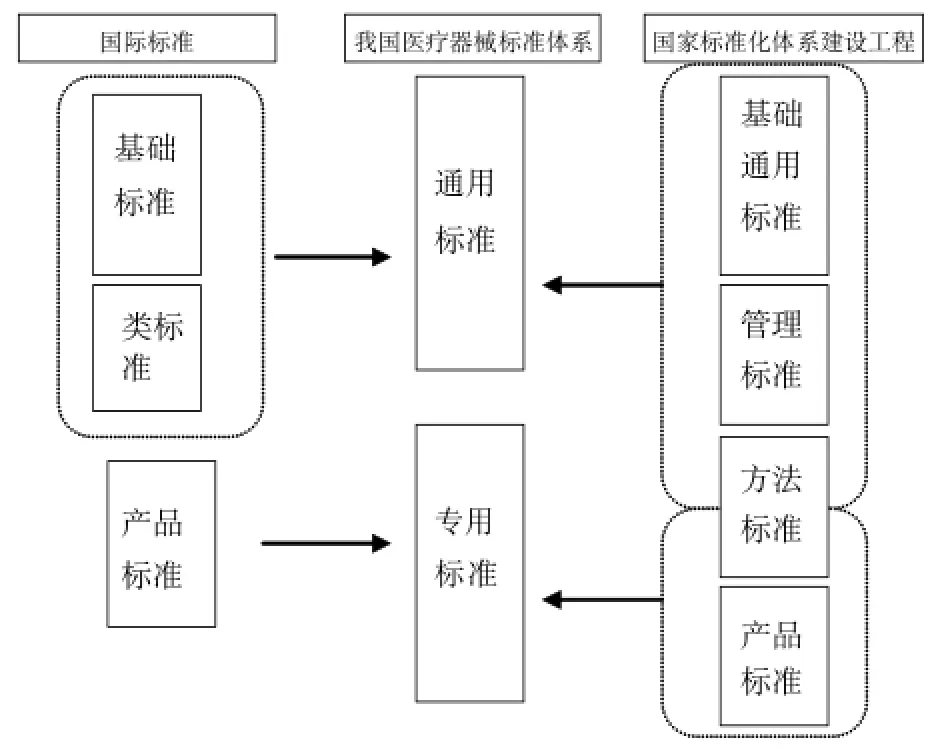
图1 各类标准的对应关系Fig.1 Relationship between different standards
1.2 通用标准的特点
由于医疗器械通用标准是针对基本概念、通用要求、共性技术的标准,是覆盖医疗器械全部技术领域或多个技术领域的。因此,通用标准在整个标准体系中应属于顶层标准或称横向标准;专用标准是下层标准或称纵向标准。
通用标准具有“大而窄”的特点。“大”是指适用的领域大,“窄”是指规范的内容相对窄,往往只包括一个技术方面,如质量体系标准等。而专用标准,更多的是产品标准,特点则是“小而全”,“小”是指标准只覆盖一个具体的产品,“全”是指标准内容涉及到具体产品的所有技术方面。
在标准体系结构中,通用标准宜被专用标准(产品标准)广泛引用,专用标准是对通用标准在特殊产品要求中的补充。
1.3 通用标准的作用
通用标准适用于全部医疗器械,基本满足了医疗器械安全及基本性能要求,是保证医疗器械安全有效的最基本的技术门槛。考虑到医疗器械是技术密集、创新集中的领域,所以医疗器械通用标准更加适宜指导规范创新医疗器械产品,也可满足监管保障安全的要求。
另一方面,通过鼓励制定和使用通用标准,可有效降低快速增长的标准数量,并可防止制定出不协调的标准或相互矛盾的标准,并达到行业与监管部门对于技术要求一致性,有效利用相关资源,实现标准社会及经济效益最大化。
2 通用标准体系的研究
2.1 通用标准体系的概念
根据GB/T 13016标准,标准体系是一定范围内的标准按其内在联系形成的科学的有机整体[3]。因此,由通用标准组成的结构化、层次化的体系是医疗器械通用标准体系。由于通用标准的重要地位,通用标准体系在整个标准体系中应具有举足轻重的作用,是医疗器械标准体系的重要基础。
2.2 我国通用标准体系现状
对我国现有的1 246项医疗器械标准进行归类,其中约有154项标准可以归于通用标准,约占总数的12.4%。现有的通用标准主要包括,YY/T 0287《医疗器械 质量管理体系 用于法规的要求》、YY/T 0316《医疗器械 风险管理对医疗器械的应用》、GB 9706有关电气安全系列标准、GB/T 16886医疗器械生物学评价系列标准、以及医疗器械的灭菌、包装或标签标记等标准。
这些标准主要是由全国医疗器械质量管理和通用要求技术委员会(SAC/TC221)、全国医疗器械生物学评价技术委员会(SAC/TC248)、全国消毒技术与设备技术委员会(SAC/TC200)、全国医用电器标准化技术委员会(SAC/TC10)、全国外科植入物技术委员会(SAC/TC110)等专业标准化技术委员会制定。
2.3 国际通用标准体系情况
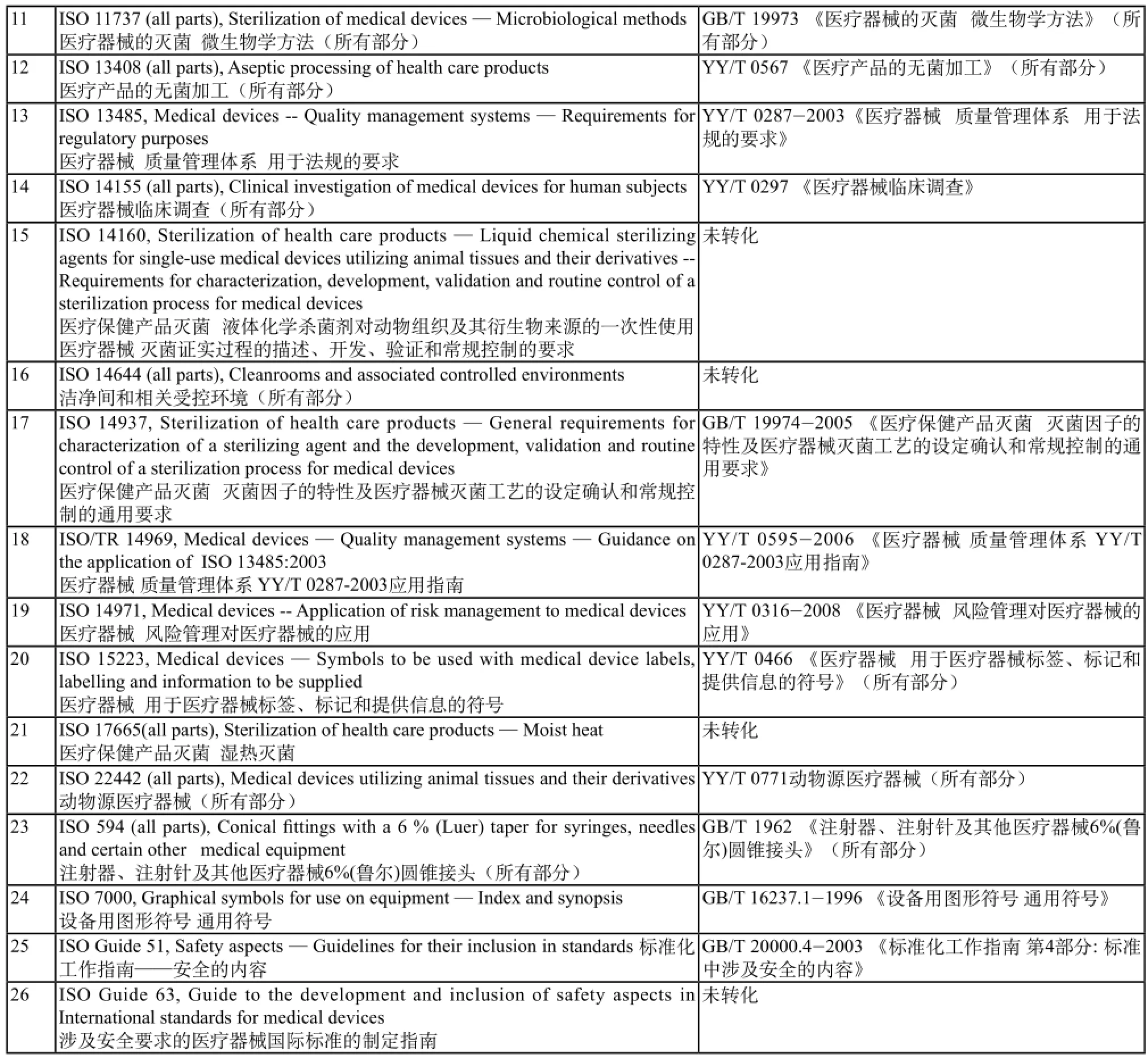
我们对医疗器械国际标准中的通用标准进行研究,目前国际通用标准主要涉及以下领域,对应标准已转化为国标/行标的情况如表1所示。
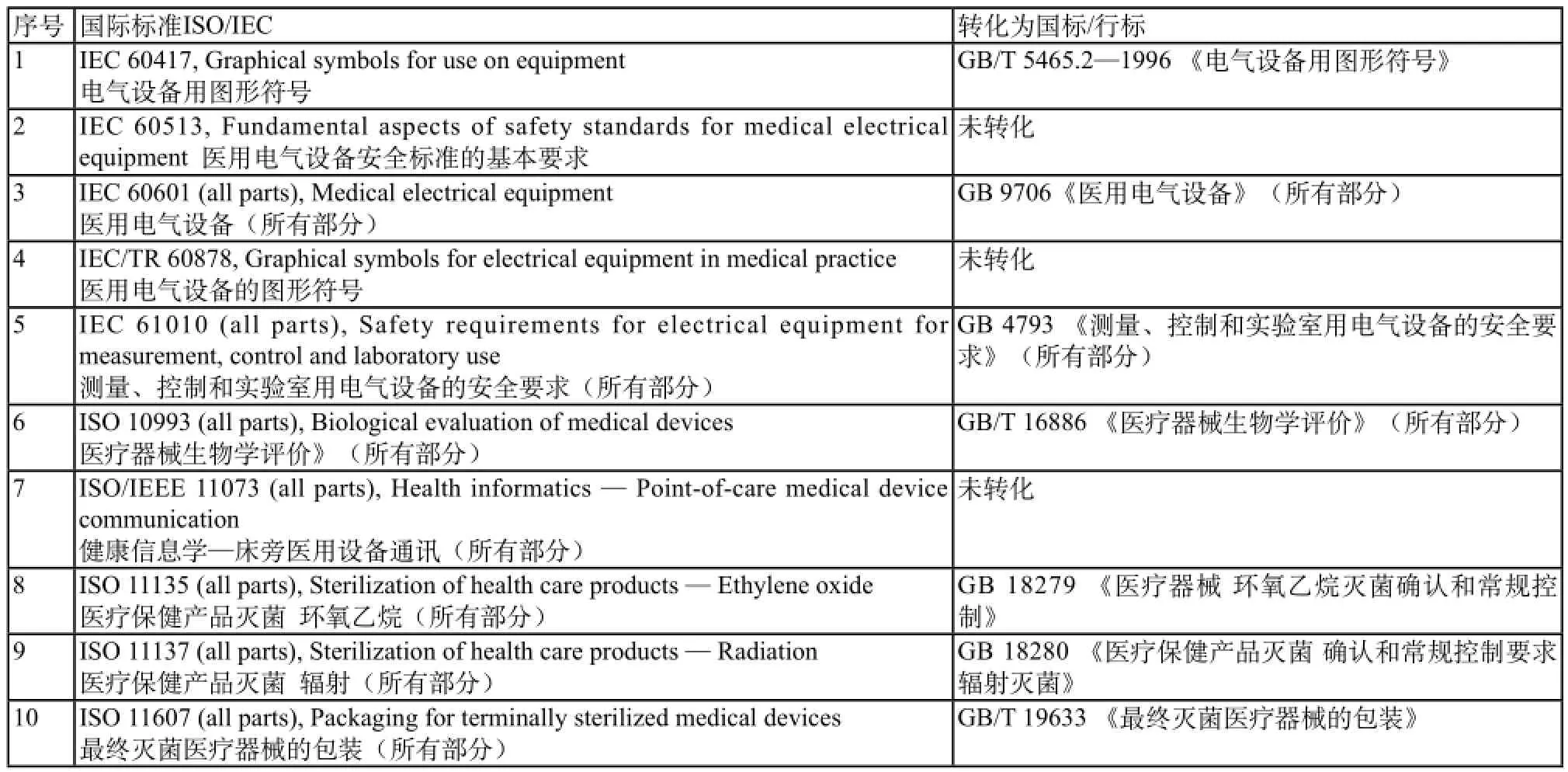
表1 国际通用标准转换为国标/行标情况汇总Tab.1 Situation of international univered standards transforming to national standards or industry standards
2.4 现有通用标准体系存在的主要问题
2.4.1 通用标准体系地位不凸显
由于多年来缺乏对标准体系的研究,并未对标准进行合理划分,未区分通用标准与专用标准,且通用标准的制修订工作多为相关标准化技术委员会根据自身需求和技术水平转化国际标准而来,转化、制修订工作随意性较大,且通用标准与产品技术要求相关性不强,往往制定积极性不高,影响了我国通用标准体系的发展。
2.4.2 通用标准技术覆盖面不完整
在与国际医疗器械通用标准进行逐一比对后,发现我国在健康信息学、医用电气安全标准要求、洁净间控制等领域的通用标准尚未转化或转化不全,造成我国通用标准体系无法有效覆盖医疗器械全领域,造成通用标准体系整体性不强。
2.4.3 通用标准层次不清晰
对通用标准体系的结构进行分析,发现现有通用标准中存在层次上的混乱,有些通用标准是国家标准,有些通用标准却为行业标准,通用标准体系结构不甚清晰,影响了对通用标准的识别和应用。
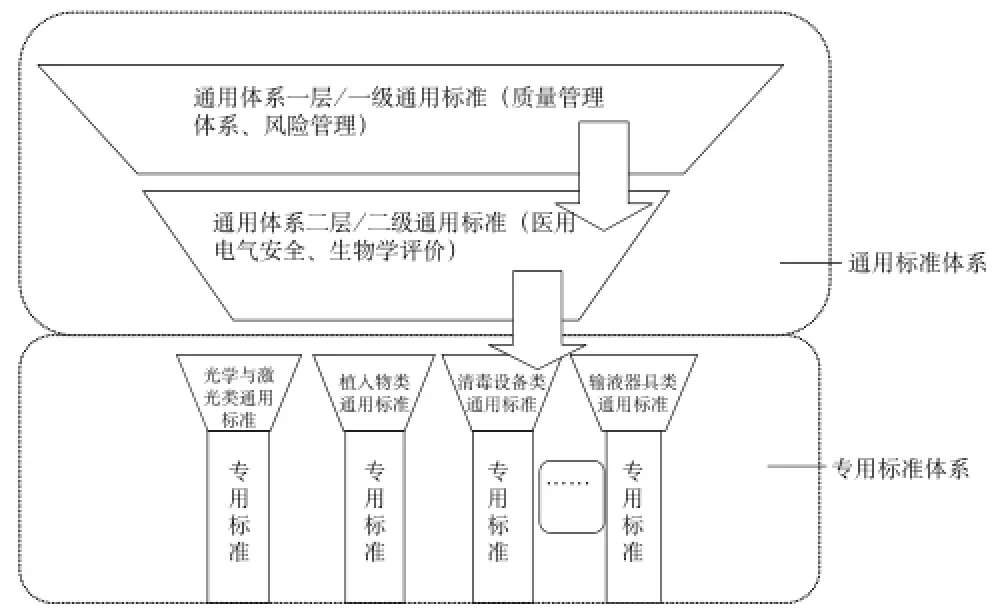
图2 各级通用标准的关系Fig.2 Relationship between general levels standards
由于在标准体系中对通用标准与专用标准没有清晰区分,使得通用标准对专用标准的指导作用相对薄弱,通用标准间、通用标准与专用标准间协调性不强,影响了整个医疗器械标准体系的整体功能,不利于医疗器械标准的健康发展。
3 对通用标准体系建设的思路及建议
3.1 突出通用标准体系的地位
根据标准适用范围的不同,强化医疗器械标准的分类,区分通用标准与专用标准,并在医疗器械标准体系中突出通用标准体系的地位和作用,并针对通用标准体系开展系统研究,制定通用标准体系建设规划。可参照国际标准化组织的做法,制定适合我国医疗器械通用标准技术指导文件,指导医疗器械研发、生产及监督等部门科学地使用医疗器械标准。
3.2 补充完善通用标准体系的技术领域
国际标准化组织确定了质量管理体系、风险管理、生物学评价、健康信息学等13个领域,涉及约26类的通用标准(包括系列标准)。通过对比,我国现有的通用标准体系中仍有些是空白,如健康信息学领域。因此,建议尽快组织对空白领域的专题研究,及时结合我国医疗器械产业和监管的需求,转化和建立相关标准,填补空白,完善通用标准体系。
3.3 构建层次清晰的通用体系结构
通过对国内通用体系的研究,考虑通用标准的适用性差异,我们归纳提出以下通用标准体系的二级结构。
3.3.1 一级通用标准
医疗器械最基础的标准,即适用于所有医疗器械领域的基本原则应位于通用体系的最高层,结合医疗器械,考虑有三个领域:
(1) 管理体系标准,例如质量管理体系、风险管理[4];
(2) 基本安全标准或规定过程要求的标准,例如医疗器械临床调查、可用性;
(3) 其他相关标准,例如医疗器械行业标准的制定。
3.3.2 二级通用标准
覆盖多个医疗器械的专业领域,但不覆盖整个医疗器械领域应位于通用体系第二层,大致可分为十类:
(1) 基本安全类标准,例如医用电气安全、微生物控制、家用医疗设备(增补);
(2) 生物学评价标准;
(3) 医疗器械灭菌(技术)标准;
(4) 包装运输标准;
(5) 原材料标准;
(6) 零配件标准;
(7) 生物相容性标准;
(8) 过程控制标准;
(9) 医学实验室管理标准;
(10) 健康信息学类标准(增补)。
以上二级结构是根据通用标准的适用性、标准的技术要求,结合医疗器械专用标准体系提出的,是对通用标准体系结构、层次的设置原则,是通用标准体系的框架。
4 结语
通过对医疗器械标准体系的研究,分析体系存在的主要问题,明确通用标准的划分原则,提出通用标准体系概念、通用体系建设思路和建议,以期通过研究,更好地规划标准化工作,做好标准体系的顶层设计,对健全医疗器械标准体系,更好地发挥标准规范产业,服务监管的作用提供一定的理论研究基础。
[1] 国家标准化管理委员会. 国家标准化体系建设工程指南[Z]. 国标委综合[2009]40号 附件.
[2] ISO/TR 16142: 2006 Medical devices -- Guidance on the selection of standards in support of recognized essential principles of safety and performance of medical devices[S].
[3] GB/T 13016-2009标准体系表编制原则和要求[S].
[4] ISO/TR 16142: 2006 Medical devices -- Guidance on the selection of standards in support of recognized essential principles of safety and performance of medical devices[S].
Research on Universal Standard System of Medical Device
【Writers】XIAO Yimei, LI Jun
National Institute for Food and Drug Control, Beijing, 100050
By research on the universal standards classification of medical device, according to their functions and scope of application, they are divided into two levels, universal standard architecture is proposed, to provide opinions and suggestions for standard system construction of medical devices.
medical device, universal standard architecture
F203
A
10.3969/j.issn.1671-7104.2015.02.014
1671-7104(2015)02-0128-04
2014-09-02
李军,E-mail: xiaoyuan1976@vip.sina.com
