镁二次电池正极材料纳米Fe3S4的电化学性能
2015-11-30张若然吴晓梅曾小勤邹建新丁文江
张若然吴晓梅曾小勤 邹建新 丁文江
镁二次电池正极材料纳米Fe3S4的电化学性能
张若然吴晓梅*曾小勤 邹建新 丁文江
(上海交通大学材料科学与工程学院,金属基复合材料国家重点实验室,上海200240)
首次将尖晶石相的纳米Fe3S4材料用作镁二次电池的正极材料。采用水热法一步合成了具有纳米结构的Fe3S4材料,并采用XRD、SEM测试手段对产物的物相、形貌进行了表征。实验结果表明,在160℃能够合成纯相的Fe3S4材料,该材料具有银耳状纳米结构。电化学测试结果显示,水热法合成的纳米Fe3S4材料能够在镁二次电池体系中进行有效的可逆充放电,放电平台电压为0.9 V,首次放电容量高达267 mAh·g-1,50次循环后衰减至110 mAh·g-1。电化学交流阻抗测试结果表明镁离子能够在Fe3S4晶格中扩散。
镁电池;正极材料;Fe3S4;纳米材料
自2000年以色列科学家Aurbach在Nature上发表了关于镁二次电池的研究[1]以来,镁二次电池便引起了研究者的广泛关注。相比于研究成熟的锂电池,镁二次电池具更高的体积比容量(金属镁3 833 mAh·cm-3,金属锂2 061 mAh·cm-3)[2],而且镁在大部分有机电解液中不易形成枝晶[3],使用安全性更高;此外,金属镁还有操作安全性高,储量丰富,价格低廉,环境友好等优势[2,4-5]。然而,镁离子和锂离子离子半径相当,却具有更高的电荷量,所以镁离子具有更强的极化作用,难以嵌入大部分基质材料中[6-7],给正极材料的选择带来很大困难。目前,只有Chevrel相MxMo6T8(M=主族或过渡金属,T=S,Se;x=1,2)化合物用作镁二次电池正极材料时具有良好的电化学性能[1,8-10]。新型正极材料的开发是镁二次电池研究的热点,其研究主要集中于过渡金属氧化物(如V2O5[11-12],MoO3[13],MnO2[14]等),过渡金属硫化物(如TiS2[15],MoS2[16-18]等),聚阴离子型磷酸盐材料[19]和硅酸盐材料(如MgxFeSiO4[20-23])等。本文对价格低廉、环境友好的Fe3S4材料在镁二次电池中的电化学性能进行了初步探索。
Fe3S4作为一种具有尖晶石结构的磁性材料和生物材料而被人们熟知[24-26],它被选作镁离子可逆嵌入/脱出的基质材料的原因如下:首先,尖晶石相的Fe3S4具有AB2S4型晶体结构(图1a),能够提供二价阳离子的嵌入位置。Fe3S4的AB2S4结构中,四面体间隙A位置被三价铁离子占据(占据率0.125),八面体间隙B位置由二价和三价铁离子共同占据(占据率0.25)[26-27],研究表明Ni2+、Ti2+等二价阳离子能够嵌入Fe3S4的晶体结构的A位置和B位置[28-29]。其次,Fe3S4的晶体结构允许电子在二价和三价铁离子间跃迁,因此该材料具有高于半导体材料的半金属性的导电性[30-31],这一特性使得嵌入电荷的再分布变得更容易,可以减弱客体离子嵌入/脱出造成的材料结构的变化。再者,相对于氧化物材料,硫化物材料中化学键的离子性较弱,客体离子嵌入过程受到的阻力较小[5]。最后,Paolella等曾成功将Fe3S4应用到锂离子电池中[32],促使我们对Fe3S4在镁二次电池中的电化学性能进行探索。相对研究成熟的Chevrel相正极材料,Fe3S4的相对分子质量更低,能够提供更高的理论比容量(C=nF/M);而且铁元素的储量远高于钼,这使得Fe3S4的价格更为低廉;能够在低温下合成的Fe3S4材料,相对于只能在高温下合成的Chevrel相材料能耗更低。
纳米结构的电极材料一般具有较大的比表面积,有利于电解液和活性材料的有效接触[33];而且纳米材料颗粒较小,能够有效缩短离子/电子的扩散程,因而能提高插层材料的电化学性能[34]。本文采用水热法一步合成了具有纳米结构的Fe3S4材料,并对其在镁二次电池中的电化学性能进行了初步研究。
1 实验部分
1.1 Fe3S4材料的合成和表征
纳米Fe3S4材料的合成参考文献[25]的合成方法:将8 mmol FeSO4·7H2O和32 mmol L-半胱氨酸(L-cysteine)溶解于160 mL去离子水中,剧烈搅拌30 min后,将液体转移到容量为200 mL的具有聚四氟乙烯内衬的水热反应釜中。将密封的水热反应釜加热到140~180℃,保温12 h,随炉冷却至室温,离心分离,用无水乙醇和去离子水将固体产物反复洗涤,随后在80℃真空条件下烘干10 h,得到黑灰色粉末。水热反应产物的物相和形貌分别采用X射线衍射仪(XRD,D/max 2550VL/PCX)和场发射扫描电镜(FESEM,JSM7600F)进行表征。XRD使用Cu靶Kα(λ=0.154 nm)射线源,管电压为40 kV,扫描步长0.01°,扫描速率4°·min-1。
1.2 电池的组装和电化学性能测试
将水热反应产物、导电剂(super-P碳粉)、粘结剂(聚偏二氟乙烯(PVDF))按照质量比8∶1∶1混合,充分研磨后,加入适量N-甲基吡咯烷酮(NMP)溶剂,充分搅拌制得均一的黏胶,均匀涂覆在直径为15 mm的圆形碳纸上,60℃真空干燥5 h,制得工作电极。采用打磨光亮的金属镁片(纯度99.9%)作为对电极,0.25 mol·L-1Mg(AlCl2EtBu)2/THF[1]溶液为电解液,Celgard 2400隔膜,与工作电极一起在手套箱中组装扣式电池(CR2032),室温陈化12 h后进行电化学测试。手套箱水氧含量均低于0.1μL·L-1。
所有电化学性能测试均在室温下进行。恒流充放电测试在Land电池测试系统上进行,充放电电流密度为20 mA·g-1,充放电截止电压分别为0.3和2.0 V。循环伏安测试(CV)和电化学交流阻抗测试(EIS)在CHI660E电化学工作站上完成。电池陈化12 h后直接进行CV测试,扫描速率为0.1 mV·s-1,扫描电压范围为0.3~2.0 V。EIS测试扫描频率范围为100 kHz~1 MHz。
材料结构稳定性测试:在完全放电状态下停止充放电测试,静置20 min后,在手套箱中拆开电池,取出正极片用四氢呋喃多次冲洗;在手套箱中自然晾干后,轻轻刮下活性物质,封入特制的XRD样品台中进行XRD测试,测试条件与1.1部分相同。
2 结果与讨论
2.1 水热法合成的纳米Fe3S4材料的表征
不同温度下合成的Fe3S4材料的XRD图如图1b所示,从中可以看出,140℃温度下合成的产物中含有FeS杂质相,180℃合成的材料中含有FeS2杂质相,而160℃水热反应产物的所有XRD衍射峰都对应于立方Fe3S4相(JCPDS No.89-1998),没有杂质峰出现,表明该温度下的水热反应产物是纯相的Fe3S4。可见,温度过高或过低都会有杂质相生成,只有在160℃温度下能够获得纯相的Fe3S4材料。Fe3S4具有如图1a所示的尖晶石相晶体结构,类似于常用作锂离子电池正极材料的尖晶石相LiMn2O4材料[35],Fe3S4也能提供A-B-A类型的离子扩散通道,我们推测在电化学作用下比Ni2+、Ti2+等半径更小的Mg2+应该能够可逆的嵌入Fe3S4的框架结构中。
160℃水热反应合成的Fe3S4材料的微观形貌如图2所示。从图2a可以看出,水热法合成的Fe3S4具有银耳状的微观形貌,这种多孔结构有利于电解液的渗透,而且能够提供较高的表面积从而提高Fe3S4材料的电化学活性。从高倍扫描照片(图2b)中可以看出,Fe3S4材料银耳状的结构是由厚度约30 nm的片状纳米结构相互交叉组成的,这种较薄的片状纳米结构能够大幅缩短离子扩散程,从而提高Fe3S4材料的电化学性能。
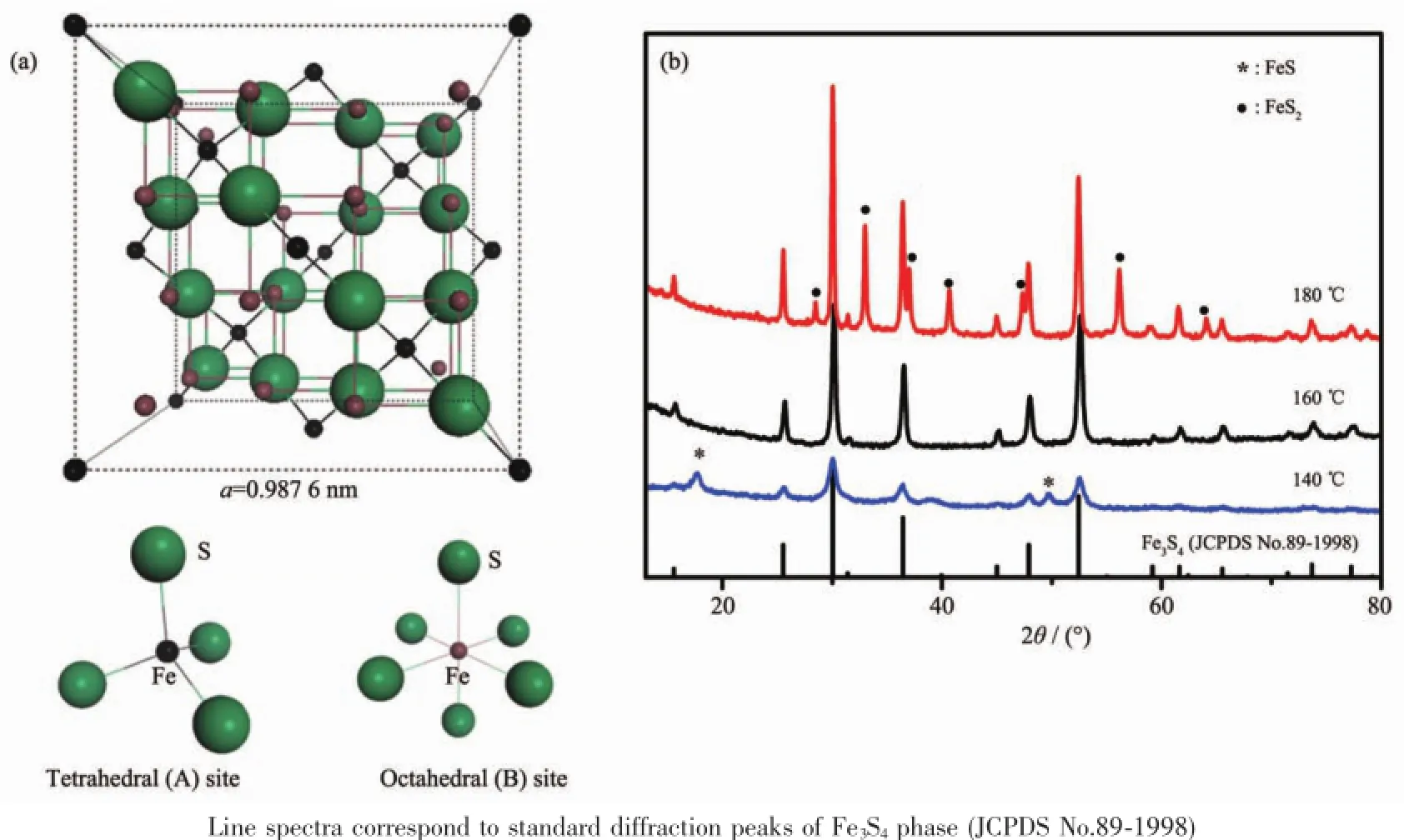
图1 (a)Fe3S4的晶体结构示意图;(b)不同温度下合成的Fe3S4材料的XRD图Fig.1(a)Schematic crystal structure of Fe3S4;(b)XRD patterns of the Fe3S4products prepared by hydrothermal method at different temperatures

图2 (a)160℃水热法合成的Fe3S4材料的SEM图;(b)高倍SEM图Fig.2(a)low and(b)high magnification SEM images of the Fe3S4product prepared by hydrothermal method at 160℃
2.2 纳米Fe3S4材料的电化学性能研究
160℃水热反应合成的纳米Fe3S4材料在镁二次电池中的CV曲线如图3所示。首次阴极极化扫描过程中,在1.3 V处出现还原峰;从0.9 V起还原电流迅速增加,在0.5 V处达到最大值,并保持该电流至0.3 V。在第二、三次循环中,1.3 V的还原峰消失,0.9~0.3 V电流增加到极值的现象也不再出现,这是由于首次阴极极化过程中在Fe3S4电极上发生了不可逆的电化学反应,该现象类似于K-α-MnO2(potassium-stabilized manganese dioxide)正极材料在镁二次电池体系中首次放电过程形成表面膜((Mg, Mn)O化合物)的现象[14]。在之后的循环扫描中,2个氧化峰先后出现在1.3和1.8 V;与之对应的2个还原峰相互重合,出现在0.75 V位置。随着循环次数增加,2个氧化峰都向低电压方向偏移,而还原峰的位置不变,氧化峰和还原峰的电压差变小,说明随着循环次数增加,电化学反应的可逆性增加。根据Haider等[28]的研究,Fe3S4晶格的A位置和B位置都能够被二价阳离子嵌入,因此,CV曲线中的两对可逆的氧化还原峰是对应于镁离子在A位置和B位置的嵌入/脱出。宽化的氧化还原峰是由材料的纳米效应造成的,较薄的纳米片能够大幅短离子扩散程,使离子嵌入脱出更加容易,导致CV曲线中的峰形不够尖锐[32,36]。
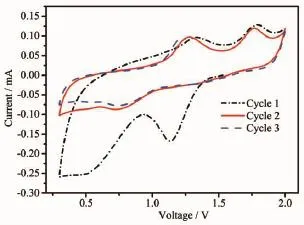
图3 纳米Fe3S4材料的循环伏安曲线Fig.3 Cyclic voltammograms of the fresh cell fabricated with Fe3S4working electrode
纳米Fe3S4材料的恒流充放电曲线和循环-放电比容量曲线如图4所示。电池经12 h陈化后,开路电压仍然保持在1.5 V左右。从图4a的恒流充放电曲线中可以看出,首次放电过程中,在1.3 V处出现了明显的电压平台,电压降至0.9 V时,电压下降斜率明显降低;之后的充放电循环中,1.3 V处的放电平台消失,在0.9 V出现放电平台,充电平台出现在1.3和1.8 V。这一现象和CV测试结果一致,首次放电过程发生了不可逆的表面化学反应,之后的充放电过程对应于镁离子在Fe3S4晶格中嵌入和脱出。从图4b的放电比容量-循环曲线可以看出:首次循环放电容量高达267 mAh·g-1,第二次循环降低到215 mAh·g-1,放电比容量在后续的循环中缓慢衰减,50次循环后衰减至110 mAh·g-1,库仑效率约90%。镁二次电池的研究还处于初期阶段,相对于其他大量新型正极材料[37-39],Fe3S4材料具有较高的首次放电比容量和比较好的循环稳定性。造成可嵌入电极材料容量衰减的原因主要有[40-41]:活性材料的相转变,活性材料的溶解,电解液的分解,电极表面钝化膜的形成等。本文对充放电循环中电极材料的物相变化进行了分析,如图5所示,可以看出材料的结构没有发生显著变化。从充放电曲线(图4a)还可以看出,多次充放电循环中电压平台位置没有明显变化,从另一角度反映了活性材料在循环过程中结构稳定性。所以本实验中造成电池容量衰减的原因并不是活性材料的相转变,可能是活性材料的溶解,电解液的分解,钝化膜的形成等原因。
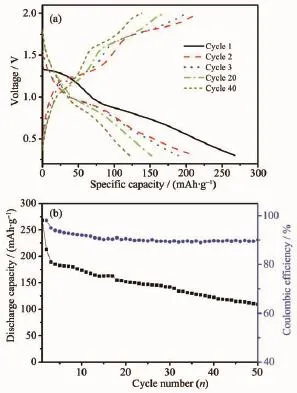
图4 (a)纳米Fe3S4材料在不同循环中的充放电曲线; (b)纳米Fe3S4材料的恒流充放电循环-放电比容量曲线Fig.4(a)Selected galvanostatic charge-discharge voltage profiles of nanostructured Fe3S4;(b)Galvanostatic charge-discharge cycling profiles ofFe3S4electrode
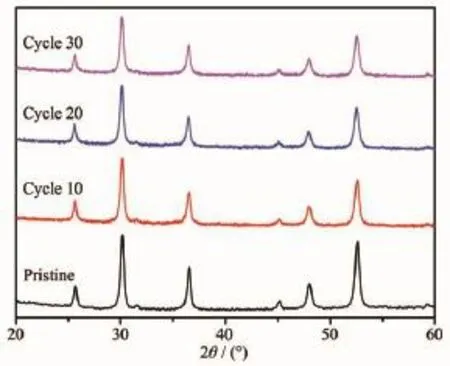
图5 Fe3S4电极在不同循环中的XRD图Fig.5 XRD patterns of the Fe3S4electrode in the selected cycles
交流阻抗测试是一种常用的探究电极电化学反应的测试方法,Fe3S4材料在镁二次电池中的电化学交流阻抗谱如图6所示。陈化12 h的新鲜电极和第二次循环放电至1.5 V的电极Nyquist图形状和锂离子电池相似[42-45]:由代表电荷转移阻抗的中高频半圆和代表扩散阻抗的低频斜线组成。图5也给出了和阻抗谱对应的等效电路图,其中Rs代表溶液阻抗,(QRct)i(i=1、2、3)代表在电极表面多层膜中的电荷转移阻抗[46-48](Q为固定相角元素,Rct为电荷转移电阻),W代表离子固态扩散的Warburge阻抗。等效电路能够很好的拟合实验结果,表明Fe3S4电极上的电化学反应过程包括:镁离子在电解液中迁移,镁离子在电极表面多层膜中的电荷转移以及镁离子在Fe3S4晶格中的固态扩散。从图5可以看出新鲜电极的电荷转移阻抗值大于经过一次充放电循环后的电极的电荷转移阻抗值,说明首次放电过程形成表面膜后,电极表面的电荷转移过程更加容易。新鲜电极的Warburge阻抗为4Ω,经过一次充放电循环后,Warburge阻抗增加为1 282Ω。这一结果表明电极表面膜形成过程中,离子的固态扩散并不是主要的反应过程,仅有微量的镁离子嵌入到Fe3S4晶格中所以Warburge阻抗值极小;经过一次充放电循环之后,Warburge阻抗值有了显著的增加,表明镁离子能够在Fe3S4晶格中进行有效的扩散。
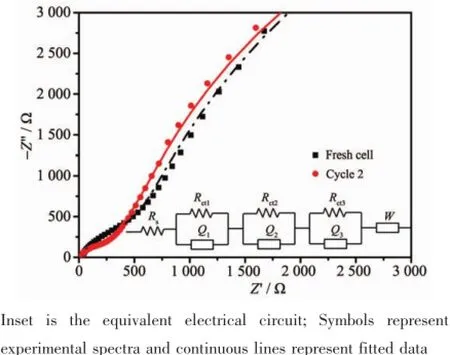
图6 新鲜Fe3S4电极和第二次放电至1.5 V的电极的Nyquist图和模拟电路图Fig.6 Nyquist plots of the fresh Fe3S4electrode and the electrode discharged to 1.5 V in the second cycle
3 结论
本文采用水热法合成了Fe3S4纳米材料,并对其在镁二次电池中的电化学性能进行研究,得到如下结论:
(1)采用水热法在160℃可一步合成纯相的Fe3S4材料,该材料具有银耳状纳米结构,片层厚度约为30 nm。
(2)纳米Fe3S4正极材料能够在镁二次电池中进行可逆的充放电循环,放电电压平台为0.9 V,电化学阻抗测试表明镁离子能够在Fe3S4晶格中扩散。
(3)Fe3S4正极材料的首次放电容量高达267 mAh·g-1,50次循环后衰减至110 mAh·g-1。纳米Fe3S4作为镁二次电池正极材料,具有较高的首次放电比容量和较好的循环稳定性。
[1]Aurbach D,Lu Z,Schechter A,et al.Nature,2000,407:724-727
[2]Saha P,Datta M K,Velikokhatnyi O I,et al.Prog.Mater. Sci.,2014,66:1-86
[3]Muldoon J,Bucur C B,Oliver AG,et al.Energy Environ. Sci.,2012,5:5941-5950
[4]SHEN Jian(沈健),PEN Bo(彭博),TAO Zhan-Liang(陶占良), et al.Prog.Chem.(化学进展),2010,22(2/3):515-521
[5]Yoo H D,Shterenberg I,Gofer Y,et al.Energ.Environ.Sci., 2013,6:2265-2279
[6]Levi E,Levi M D,Chasid O,et al.J.Electroceram.,2009, 22:13-19
[7]Levi E,Gofer Y,Aurbach D.Chem.Mater.,2010,22:860-868
[8]Levi E,Mitelman A,Aurbach D,et al.Chem.Mater.,2007, 19:5131-5142
[9]Levi E,Mitelman A,Aurbach D,et al.Inorg.Chem.,2007, 46:7528-7535
[10]Levi E,Gershinsky G,Aurbach D,etal.Chem.Mater.,2009, 21:1390-1399
[11]Imamura D,Miyayama M.Solid State Ionics,2003,161:173-180
[12]Gershinsky G,Yoo H D,Gofer Y,et al.Langmuir,2013,29: 10964-10972
[13]JIAO Li-Fang(焦丽芳).Thesis for the Doctorate of Nankai University(南开大学博士论文).2005.
[14]Arthur T S,Zhang R,Ling C,et al.Acs.Appl.Mater.Inter., 2014,6:7004-7008
[15]Tao Z L,Xu L N,Gou X L,et al.Chem.Commun.,2004, 18:2080-2081
[16]Liang Y,Feng R,Yang S,et al.Adv.Mater.,2011,23:640-643
[17]Liu Y,Jiao L,Wu Q,et al.Nanoscale,2013,5:9562-9567
[18]Liu Y,Jiao L,Wu Q,et al.J.Mater.Chem.A,2013,1:5822 -5826
[19]Huang Z D,Masese T,Orikasa Y,et al.RSC Adv.,2015,5: 8598-8603
[20]Nuli Y N,Yang J,Wang J L,et al.J.Phys.Chem.C,2009, 113:12594-12597
[21]NuLi Y N,Zheng Y,Wang F,et al.Electrochem.Commun., 2011,13:1143-1146
[22]Sun J Z.Asian J.Chem.,2012,24(5):1909-1911
[23]Sun J Z.Monatsh.Chem.,2014,145:103-106
[24]Spender M R,Coey J M D,Morrish A H.Can.J.Phys., 1972,50:2313-2326
[25]Cao F,Hu W,Zhou L,et al.Dalton Trans.,2009,42:9246-9252
[26]Chang L,Rainford B D,Stewart J R,et al.J.Geophys.Res., 2009,114:B07101
[27]Coey J,Spender M,Morrish A.Solid State Commun.,1970, 8:1605-1608
[28]Haider S,Grau-Crespo R,Devey A J,et al.Geochim. Cosmochim.Acta,2012,88:275-282
[29]Martic M,Jakab-Simon I N,Haahr L T,et al.J.Biol.Inorg. Chem.,2013,18:261-276
[30]Roberts A P,Chang L,Rowan C J,et al.Rev.Geophys., 2011,49:RG1002
[31]Dekkers M J,Passier H F,Schoonen M A.Geophys.J.Int., 2000,141:809-819
[32]Paolella A,George C,Povia M,et al.Chem.Mater.,2011,23: 3762-3768
[33]Guo Y G,Hu J S,Wan L J.Adv.Mater.,2008,20:2878-2887
[34]Devan R S,Patil R A,Lin J H,et al.Adv.Funct.Mater., 2012,22:3326-3370
[35]Tarascon J M.J.Electrochem.Soc.,1987,134(6):1345-1351 [36]Reddy M V,Yu T,Sow C H,et al.Adv.Funct.Mater., 2007,17(15):2792-2799
[37]Mizuno Y,Okubo M,Hosono E,et al.J.Mater.Chem.A, 2013,1:13055-13059
[38]Zhang R,Yu X,Nam K W,et al.Electrochem.Commun., 2012,23:110-113
[39]Yu L,Zhang X.J.Colloid Interface Sci.,2004,278:160-165
[40]TANG Zhi-Yuan(唐致远),RUAN Yan-Li(阮艳莉).Prog. Chem.(化学进展),2005,17(1):1-7
[41]MA Ling(马苓),DU Guang-Yuan(杜光远),XU Qiang(徐强), et al.Chinese J.Power Sources(电源技术),2014,38(3):553-556
[42]ZHUANG Quan-Chao(庄全超).Thesis for the Doctorate of Xiamen University(厦门大学博士论文).2007.
[43]WANG Lian-Liang(王连亮),SUN Zhi-Zhong(孙志中),YI Wen-Tao(伊文涛),et al.J.Salt Lake Res.(盐湖研究),2008, 16(4):21-26
[44]ZHUANG Quan-Chao(庄全超),XU Shou-Dong(徐守冬),QIU Xiang-Yun(邱祥云),et al.Prog.Chem.(化学进展),2010, 22:1044-1057
[45]QIU Xiang-Yun(邱祥云).Thesis for the Doctorate of China University of Mining(中国矿业大学博士论文).2013.
[46]Aurbach D,Levi M D,Levi E.Solid State Ionics,2008,179: 742-751
[47]Aurbach D,Gofer Y,Schechter A,et al.J.Power Sources, 2001,97:269-273
[48]Levi M D,Gizbar H,Lancry E,et al.J.Electroanal.Chem., 2004,569:211-223
Electrochemical Properties of Nanostructured Greigite(Fe3S4) as a Cathode Material in Rechargeable Magnesium Battery
ZHANG Ruo-Ran WU Xiao-Mei*ZENG Xiao-Qin ZOU Jian-Xin DING Wen-Jiang
(State Key Laboratory of Metal Matrix Composites,School of Materials Science and Engineering,Shanghai Jiao Tong University,Shanghai 200240,China)
Nanostructured greigite(Fe3S4)prepared by hydrothermalmethod was firstly used as a cathode material for rechargeable magnesium battery.The as-synthesized samples were characterized by X-ray diffraction(XRD) and scanning electron microscope(SEM).Cyclic voltammetry and galvanostatic charge-discharge cycling tests showed that the obtained Fe3S4could be reversibly cycled in rechargeable magnesium battery.The discharge voltage plateau located at 0.9 V.The nanostructured Fe3S4electrode exhibited a high capacity of 267 mAh·g-1during the first discharge process,then the capacity gradually dropped to 110 mAh·g-1after 50 cycles. Electrochemicalimpedance spectroscopy tests showed that Mg2+can diffuse in the lattice of Fe3S4.
magnesium battery;cathode material;Fe3S4;nanostructured material
6.21;O614.81+1
A
1001-4861(2015)07-1351-06
10.11862/CJIC.2015.182
2015-02-06。收修改稿日期:2015-04-28。
国家自然科学基金(No.51274140)资助项目。
*通讯联系人。E-mail:wuxiaomei@sjtu.edu.cn
