八元瓜环对1,1'-亚乙基-2,2'-联吡啶及金刚烷胺的分子识别作用研究*
2015-11-22宋桂先张建新薛赛凤祝黔江
宋桂先,唐 青,黄 英*,张建新,陶 朱,薛赛凤,祝黔江
(1.贵州大学 大环化学及超分子化学重点实验室,贵州 贵阳 550025;2.贵州大学 生化工程中心,贵州 贵阳 550025;3.贵州省天然产物重点实验室,贵州 贵阳 550009)
分子识别就是主体(或受体)对客体(或底物)选择性结合并产生某种特定功能的过程,是组装及组装功能的基础,是酶和受体选择性的根基[1]。近年来,超分子化学及其应用研究越来越受到科学家的重视,尤其是受体分子的设计合成引起了世界化学家的普遍关注[2],且发现客体分子与瓜环形成超分子自组装体系后,其理化性质、光学性质及生物活性等发生了不同程度的改变[3-6]。瓜环[7-9](Cucurbit[n]urils,Q[n]),具有较强的结构刚性,能根据自身空腔的大小,选择性地容纳尺寸、形状相匹配的客体分子,形成了特有的瓜环主客体化学[10-14]。对于八元瓜环(Q[8])或十元瓜环(Q[10])来说,常可通过引入富电子客体与缺电子客体通过竞争或协同作用形成主客体包结配合物。1,1'-亚乙基-2,2'-联吡啶(1,1'-Ethylene-2,2'-bipyridinium,EB)为季铵盐类化合物,能与瓜环形成稳定的配合物[15-16]。因此,本文拟选用金刚烷胺(1-Adamantanamine,AD)为竞争客体,研究Q[8]与AD 及EB 之间的分子识别作用(图1),探讨三元主客体作用体系的作用机制、作用模式等,为瓜环的应用提供理论依据。

图1 Q[8]与EB 和AD 的可能作用模式图
1 实验部分
1.1 试剂与仪器
VARIAN INOVA-400M 核磁共振仪(VARIAN,America),Agilent 8453 型紫外-可见分光光度计(Agilent,America),Cary Eclipse 荧光光谱仪(Agilent,America),Nano ITC 等温滴定量热仪(TA,America)。八元瓜环由实验室按文献[17-18]制备,1,1'-亚乙基-2,2'-联吡啶、金刚烷胺购自阿拉丁,水为二次蒸馏水。
1.2 紫外吸收光谱及荧光发射光谱测定
EB、AD 分别配成1.00× 10-3mol/L 母液,Q[8]配成1.00×10-4mol/L 母液备用。固定客体EB 的浓度为2×10-5mol/L,采用摩尔比法改变瓜环的浓度(0~6)×10-5mol/L 分别配制一系列不同物质的量之比的溶液;测定Q[8]与EB 在水溶液中的紫外可见吸收光谱,并以激发波长为309 nm,激发狭缝5 nm,发射狭缝5 nm 测定体系的荧光发射光谱。此后,固定Q[8]/EB 体系浓度为2.00×10-5mol/L,加入AD,分别以上述相同条件测定三者紫外吸收光谱与荧光发射光谱。
1.3 等温量热测定
EB、AD 分别配成1.00× 10-3mol/L 母液,Q[8]配成1.00×10-4mol/L 母液备用。取Q[8]母液稀释至浓度为5×10-5mol/L,在水溶液中用EB 及AD 滴定Q[8],采用Nano ITC 等温滴定量热仪测定主客体Q[8]/EB、Q[8]/AD 在25℃时的热力学平衡常数及其他热力学参数,样品池体积为960 μL,搅拌速度为250 r/min,4 μL/滴,间隔时间150 s。以水为参比,此后,另固定Q[8]/EB 体系浓度为5.00× 10-5mol/L,用AD 母液滴定滴Q[8]/EB,相同条件测定三者作用热力学平衡常数及其他热力学参数。
1.4 1H NMR 测定
1H NMR 谱在25 ℃下用VARIAN INOVA-400 MHZ 核磁共振仪测定,溶剂为氘代水。
2 结果与讨论
2.1 Q[8]/EB 及Q[8]/AD 体系的主客体相互作用研究
EB为季铵盐类化合物,在水溶液中以离子形式存在。水溶液中EB 在λ=309 nm 处有最大吸收峰,而Q[8]在此波长处无吸收,当在EB 中加入Q[8](浓度为:(a)0;(b)4.0;(c)8.0;(d)12.0;(e)16.0;(f)20.0;(g)24.0;(h)28.0;(i)32.0;(j)36.0;(k)40.0;单位:μM)后,体系的紫外可见吸收强度随着Q[8]浓度的增加而降低,在321 nm有等吸收点,且在CQ[8]/CEB≈1 时也出现平台(图2(A)),表明Q[8]与EB 形成了1∶1的主客体配合物,用软件ReactLab EQUILIBRIA 计算平衡常数K=(7.66 ±0.55)×105L/mol。类似地,EB 的最大荧光发射波长为351 nm,而Q[8]在此波长处无荧光,当在EB 中加入Q[8]后,体系的荧光强度随着Q[8]浓度的增加而降低,且在CQ[8]/CEB≈1 时也出现平台(图2(B)),通过对测量数据的拟合得到Q[8]/EB 主客体配合物的平衡常数K=(4.38 ±0.22)×105L/mol[19]。
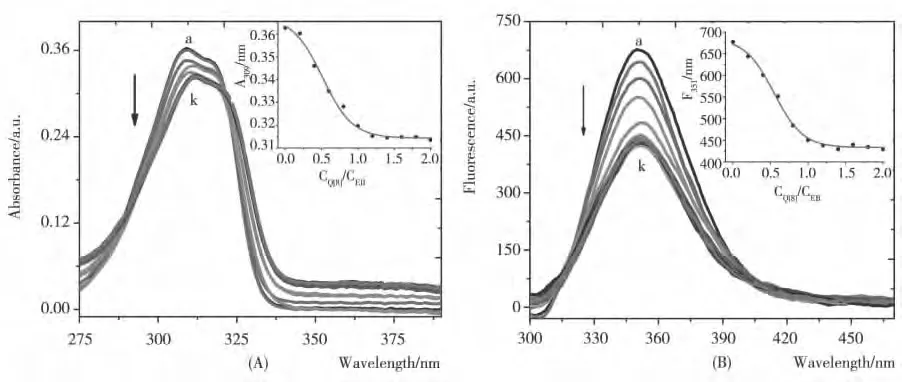
图2 Q[8]/EB 的紫外吸收光谱图(A)与荧光光谱图(B)
等温量热滴定法(ITC)提供了Q[8]/EB 及Q[8]/AD 体系的热力学常数(图3)。Q[8]与EB作用如图3(A)的热力学平衡常数为Ka=(5.20 ±0.74)×105L/mol,反应计量比n 约为1;Q[8]与AD 作用如图3(B)的热力学平衡常数为Ka=(1.74 ±0.82)×107L/mol,反应计量比n 约为1。该数据显示Q[8]与EB 及Q[8]与AD 均形成了包结计量比为1∶1主客体配合物。由图中的热力学数据也可知,对于Q[8]/EB 及Q[8]/AD 体系,其ΔH <0,表明上述超分子体系是放热体系。
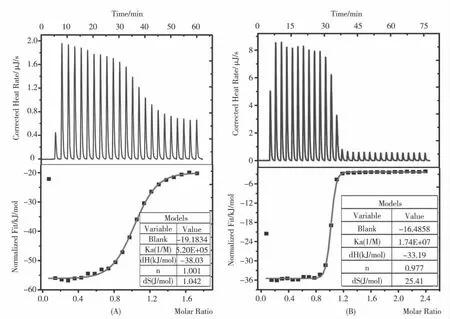
图3 25 ℃时Q[8]与EB 在水溶液中等温量热滴定图(A)以及Q[8]与AD 在水溶液中等温量热滴定图(B)
2.2 AD 与Q[8]/EB 的相互作用研究
由于AD 独特的结构(图1)表明其无光谱特征。当在Q[8]/EB 体系中逐渐滴加AD(浓度为:(a)0;(b)4.0;(c)8.0;(d)12.0;(e)16.0;(f)20.0;(g)24.0;(h)28.0;(i)32.0;(j)36.0;(k)40.0;单位:μM)时,体系的紫外吸收强度和荧光发射强度均随着AD 浓度的增加而逐渐增强(如图4),且在CAD/CQ[8]/EB≈1 时也出现平台,通过计算得平衡常数分别为KUV=(1.46 ± 0.37)× 107L/mol,KIF=(2.93 ±0.51)×107L/mol。该实验结果表明AD 能竞争与Q[8]作用形成稳定包合物,使EB 被挤出Q[8]内腔。

图4 AD 与Q[8]/EB 的紫外吸收光谱图(A)及荧光光谱图(B)
AD 滴定Q[8]/EB 的ITC 滴定数据如图5(A)及表1 所示,结果显示反应计量比n 约为1,因此可推断,AD 与Q[8]/EB 作用比为1∶1,由表1的热力学数据可看出,对于Q[8]/EB,Q[8]/AD及Q[8]/EB/AD 体系来说,其ΔH <0,表明上述超分子体系均是放热体系。从表1 数据还可知,KQ[8]/AD>KQ[8]/EB,据此可推测当在Q[8]/EB 体系中逐渐滴加AD 时,AD 与EB 竞争着与Q[8]作用,随着AD 浓度的增加,EB 逐渐被挤出瓜环的内腔,而AD 与Q[8]形成Q[8]/AD 稳定的二元包合物。
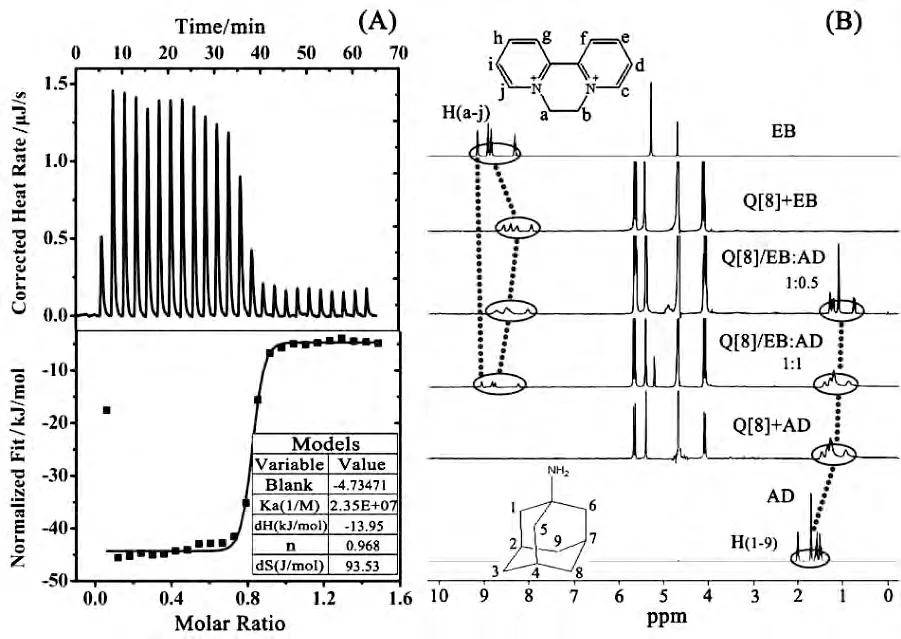
图5 25 ℃的水溶液中AD 与Q[8]/EB 的等温量热滴定图(A)以及AD 与Q[8]及EB 的氢核磁共振图谱(B)

表1 Q[8]与EB 及AD 相互作用的热力学参数
Q[8]/EB/AD 相互作用共存体系在水溶液中的1H NMR 谱图进一步验证了AD 竞争与Q[8]作用形成稳定配合物(如图5(B))。核磁图谱显示,相对于游离EB 及AD 来说,加入Q[8]后,EB 中Ha-j质子共振峰均向高场移动,说明EB 进入了Q[8]的空腔而受到了屏蔽作用;AD 结构中H1-9质子共振峰也均向高场移动,且峰变宽,说明AD也进入Q[8]的空腔受到了屏蔽作用。当在Q[8]/EB体系加入AD 时,EB 的H 质子共振峰会随着AD 的增加而逐渐移向低场,当AD∶Q[8]∶EB达到1∶1∶1时,EB 的H 质子共振峰会移到游离客体H 质子共振峰位置,说明AD 将EB 挤出了Q[8]的空腔而与Q[8]形成了稳定的Q[8]/AD 主客体配合物。其原因可能是由于AD为富电子客体,其与Q[8]具有较强的结合力,当将AD 加入Q[8]/EB体系后,通过竞争作用将EB 挤出Q[8]空腔,其可能作用模式如图1 所示。
3 结论
本文利用紫外吸收光谱、荧光光谱、核磁技术、等温量热滴定仪等分析测试手段考察了Q[8]与EB 及AD 间的相互作用,结果表明Q[8]与EB 及AD 均形成了包结计量比为1∶1的主客体配合物。当在Q[8]/EB 体系加入AD 时,由于AD 与Q[8]结合力较强,能竞争Q[8]内腔,使EB 被挤出Q[8]内腔,导致客体光谱性质和热力学性质均发生了改变。
[1]张中强,涂华民.超分子化学的研究和进展[J].河北师范大学学报:自然科学版,2006,30(4):453.
[2]张来新,杨琼,赵卫星.超分子化学研究的新进展[J].应用化工,2010,39(11):1758.
[3]Del P.M.,Hernandez L.,Quintana C..A selective spectrofluorimetric method for carbendazim determination in oranges involving inclusion-complex formation with cucurbit[7]uril[J].Talanta,2010,81:1542.
[4]Del P.M.,Alonso M.,Hernandez L.,et al.An Electrochemical Approach for the Cucurbit[7]uril/Carbendazim Supramolecular Inclusion Complex.Application to Carbendazim Determination in Apples[J].Electroanalysis,2011,23(1):189.
[5]Kim H.J.,Heo J.,Jeon W.S.,et al.Selective Inclusion of a Hetero-Guest Pair in a Molecular Host:Formation of Stable ChargeTransfer Complexes in Cucurbit[8]uril[J].Angew Chem Int.Ed,2001,40(8):1526.
[6]Apurba L.,Indraji K.,Saleh N.G..Supramolecular encapsulation of benzimidazolederived drugs by cucurbit[7]uril[J].Can J.Chem,2011,89:139.
[7]Ling Y.h.,Joel T.,Mague,Angel E.,et al.Inclusion Complexation of Diquat and Paraquat by the Hosts Cucurbit[7]uril and Cucurbit[8]uril[J].Chem Eur.J.,2007,13:7908.
[8]Behrend R.,Meyer E.,Rusche F..Mitthelungen aus dem organisch-chemischen aboratorium der technischen hochschule zu hannover[J].Liebigs Ann Chem.,1905,339:1.
[9]Freeman W.A.,Mock W.L.J..Cucurbituril[J].Am Chem.Soc,1981,103(24):7367.
[10]Kim J.,Jung L.S.,Kim S.Y.,et al.New Cucurbituril Homologues:Syntheses,Isolation,Characterization,and X-ray Crystal Structures of Cucurbit[n]uril (n=5,7,and 8)[J].J Am.Chem Soc,2000,122(3):540.
[11]Xu ZH.Q.,Yao X.Q.,Xue S.F..Investigation of structures of the self-assembled pseudorotaxane of cucurbiturils with some alkyldiamines[J].Acta Chimica Sinica,2004,62(19):1927.
[12]Xu L.,Liu S.M.,Wu C.T..Separation of positional isomers by cucurbit[7]uril-mediated capillary electrophoresis[J].Electrophoresis,2004,25:3300.
[13]Liu S.M.,Li X.,Wu C.T..Preparation and characterization of perhydroxyl-cucurbit[6]uril bonded silica stationary phase for hydrophilic-interaction chromatography[J].Talanta,2004,64:929.
[14]ZHao J.,Kim H.J..Cucurbit[n]uril derivatives soluble in water and organic solvents[J].Angew Chem Int Ed,2001,40:4233.
[15]Sindelar V.,Cejas M.A.,Raymo F.R.,et al.Supramolecular Assemblyof 2,7-Dimethyldiazapyrenium and Cucurbit[8]uril:A New Fluorescent Host for Detection of Catechol and Dopamine[J].Chew Eur.J.,2005,11:7054.
[16]Ling Y.,Wang W.,Angel E.Kaifer.A new cucurbit[8]urilbased fluorescent receptor for indole derivatives[J].Chem Commun,2007:610.
[17]Kim J.,Jung I.S.,Kim S.Y.,et al.New Cucurbituril Homologues:Syntheses,Isolation,Characterization,and X-ray Crystal tructures of Cucurbit[n]uril (n=5,7,and 8)[J].J.Am.Chem.Soc.2000,122(3):540.
[18]Day A.I.,Blanch R.J.,Arnold A.P.,et al.A cucurbiturilbased gyro-scane:A new supramolecular form[J].Angew Chem.Int.Ed,2002,41(2):275.
[19]ZHang H.M.,Yang J.Y.,Du L.M..Determination o f sotalol by fluorescence quenching Method[J].Anal.Methods,2011,3:1156.
