紫归子妇炎康泡腾栓5种活性成分的含量测定
2015-11-11武静莲姜林芬吴红梅胡林海胡芳弟
武静莲,姜林芬,吴红梅,胡林海,胡芳弟
(1.甘肃省第三人民医院,甘肃兰州 730000;2.甘肃省中医学校,甘肃兰州 730050;3.嘉峪关市第一人民医院,甘肃嘉峪关 730000;4.兰州大学药学院,甘肃兰州 730000)
紫归子妇炎康泡腾栓5种活性成分的含量测定
武静莲1,姜林芬2,吴红梅2,胡林海3,胡芳弟4*
(1.甘肃省第三人民医院,甘肃兰州 730000;2.甘肃省中医学校,甘肃兰州 730050;3.嘉峪关市第一人民医院,甘肃嘉峪关 730000;4.兰州大学药学院,甘肃兰州 730000)
目的探讨紫归子妇炎康泡腾栓中5种活性成分的含量测定方法,并测定5批自制紫归子妇炎康泡腾栓中5种活性成分的含量。方法采用高效液相色谱法,以KromasiL C18柱(250 mm×4.6 mm,5 μm),分别以甲醇-水(82∶18)和甲醇-0.5%醋酸(32∶68)为流动相,测定该制剂中左旋紫草素和阿魏酸的含量。以甲醇-0.02%三乙胺水溶液(53∶47)为流动相,测定该制剂中苦参碱和氧化苦参碱的含量。以KromasilODS保护柱(4.6 mm×10mm,5 μm),以甲醇-0.1%三乙胺水溶液(80∶20)为流动相,测定该制剂中β,β-二甲基丙烯酰的含量。结果实验室自制的5批紫归子妇炎康泡腾栓中阿魏酸、左旋紫草素、β,β-二甲基丙烯酰、苦参碱、氧化苦参碱的平均含量分别为0.31 mg/枚、0.14 mg/枚、0.28 mg/枚、19.80mg/枚、1.69 mg/枚。结论使用的紫归子妇炎康泡腾栓中阿魏酸、左旋紫草素、β,β-二甲基丙烯酰、苦参碱、氧化苦参碱的高效液相色谱含量测定方法简单易行,可以用于紫归子妇炎康泡腾栓的质量控制。
紫归子妇炎康泡腾栓;含量测定;质量控制;活性成分
紫归子妇炎康泡腾栓是在传统中医理论的指导下,针对现代妇科中药研究领域学术热点,从当归、紫草、苦豆子3味妇科良药中提取与治疗阴道炎相关的活性成分,即具有清热解毒、祛风除湿、活血化瘀、杀虫止痒功效的活性组分,采用现代技术制成的妇科用栓剂。该制剂中的主要抗炎活性成分包括阿魏酸[1]、左旋紫草素[2]、β,β-二甲基丙烯酰[3]、苦参碱和氧化苦参碱[4]。为了全面系统地控制该制剂的质量,本文采用HPLC(高效液相色谱)方法,对该制剂中的左旋紫草素、β,β-二甲基丙烯酰、阿魏酸、苦参碱及氧化苦参碱5种成分进行含量测定方法研究。
1 试剂与仪器
1.1 试剂
左旋紫草素(中国药品生物制品检定所提供,批号769-9001);β,β-二甲基丙烯酰(中国药品生物制品检定所提供,批号116-200503);苦参碱(中国药品生物制品检定所提供,批号0805-9804);氧化苦参碱(中国药品生物制品检定所提供,批号0780-9703);阿魏酸(中国药品生物制品检定所提供,批号110773-200611);甲醇(山东禹王集团化工分公司生产,色谱纯);高效液相色谱用三重蒸馏水(经0.45 μm微孔滤膜过滤);氯仿(天津市星月化工有限公司,分析纯);三乙胺(天津市凯通,分析纯);磷酸二氢钾(北京化工厂,分析纯);氢氧化钠(天津市德恩化学试剂有限公司,分析纯);溴麝香草酚蓝(中国公司合营新中化学厂,分析纯);紫草、苦豆子和当归药材购自兰州黄河药市。
1.2 仪器
戴安μltimate3000型高效液相色谱仪,Kromasil C18柱(250 mm×4.6 mm,5 μm),二极管阵列检测器(DAD),紫外分光光度计1700型(苏州市莱顿科学仪器有限公司),RE-52A型旋转蒸发仪(上海亚荣生化仪器厂),KQ-400DB型超声波清洗器(昆山市超声仪器有限公司),DHG-9075A型烘箱(上海一恒有限公司),BS224S型万分之一电子分析天平(德国Sartoriμs赛多利斯),MillinnceQ超纯水机。
2 实验方法
2.1 对照品溶液的配置
(1)精密称取阿魏酸对照品6.32 mg,用甲醇定容制成0.06 mg/mL阿魏酸对照品储备溶液。
(2)精密称取左旋紫草素对照品12.78 mg,用甲醇定容制成0.51 mg/mL左旋紫草素对照品储备溶液。
(3)精密称取苦参碱对照品13.13 mg,用甲醇定容制成0.525 mg/mL的苦参碱对照品储备溶液。
(4)精密称取氧化苦参碱对照品1.01 mg,用甲醇定容制成0.521 mg/mL的氧化苦参碱对照品储备溶液。
(5)精密称取β,β-二甲基丙烯酰4.72 mg,用甲醇配制成0.472 mg/mL的β,β-二甲基丙烯酰对照品储备溶液。
2.2 含量测定
2.2.1 制剂中左旋紫草素的含量测定(1)色谱条件:色谱柱:Kromasil C18柱(250 mm×4.6 mm,5 μm);流动相:甲醇-水(82∶18);流速:1.0 mL/min;二极管阵列检测器(DAD);检测波长:516 nm;柱温:30°C;进样量:10 μL。
(2)标准曲线的绘制:精密吸取0.51 mg/mL的左旋紫草素对照品溶液0.25 mL、1 mL、2 mL、4 mL、8 mL,稀释至10 mL,分别吸取10 μL,注入高效液相色谱仪,按2.2.1项下的色谱条件进行测定。以峰面积为纵坐标(Y),以左旋紫草素浓度为横坐标(X),得回归方程:Y=0.257 6X-0.233 5,相关系数R=0.999 9,在12.55~408.80 μg/mL范围内,线性关系良好。
(3)制剂中左旋紫草素的含量测定:精密称取紫归子妇炎康泡腾栓2枚,加40 mL 1 mol/L的NaOH溶液,超声溶解30分钟,静置,离心(转速4 000转/分)10分钟,取上清液,用1 mol/L的HCL调节pH值至5.0~6.0,适当搅拌,放置,析出红色固体物质,抽滤,滤饼干燥(40℃)至恒重后,置于5 mL容量瓶中,加甲醇溶解,定容,用0.45 μm微孔滤膜过滤,即得。精密吸取样品10 μL,进样,测定。
2.2.2 制剂中β,β-二甲基丙烯酰的含量测定(1)色谱条件:色谱柱:Kromasil ODS保护柱(4.6 mm×10 mm,5 μm);流动相:甲醇-0.1%三乙胺水溶液(80∶20),用磷酸调节pH=3;流速:1.0 mL/min;检测波长:516 nm;柱温:30°C;进样量:10 μL。
(2)标准曲线的绘制:精密吸取0.472 mg/mL的β,β-二甲基丙烯酰对照品溶液0.25mL、1mL、2mL、4mL、8mL,稀释至10mL,分别吸取10 μL注入高效液相色谱仪,按2.2.2项下的色谱条件进行测定。以峰面积为纵坐标(Y),β,β-二甲基丙烯酰浓度为横坐标(X),得回归方程:Y=4.75×105X-8.06×105,相关系数R=0.999 9,在11.80~70.80 μg/mL范围内,线性关系良好。
(3)制剂中β,β-二甲基丙烯酰的测定:样品处理方式同2.2.1项。
2.2.3 制剂中阿魏酸的含量测定(1)色谱条件:色谱柱:Kromasil C18柱(250 mm×4.6 mm,5 μm);流动相:甲醇-0.5%醋酸(32∶68);流速:1.0 mL/min;二极管阵列检测器(DAD);检测波长:316 nm;柱温:35°C;进样量:10 μL。
(2)标准曲线的绘制:精密吸取0.06 mg/mL的阿魏酸对照品溶液0.5 mL、1 mL、2 mL、4 mL、8 mL,加5%的甲酸甲醇稀释至10 mL,分别吸取10 μL,注入高效液相色谱仪,按2.2.3项下的色谱条件进行测定。以峰面积为纵坐标(Y),以阿魏酸浓度为横坐标(X),得回归方程:Y=838.58X-0.022 8,相关系数R= 0.999 9,在3.11~49.84 μg/mL范围内,线性关系良好。
(3)样品中阿魏酸的含量测定:精密称取紫归子妇炎康泡腾栓2枚,置于10 mL容量瓶中,加甲醇,超声溶解30分钟,补足重量,用0.45 μm微孔滤膜过滤,即得。精密吸取样品10 μL,进样,测定。
2.2.4 制剂中苦参碱和氧化苦参碱的含量测定(1)色谱条件:色谱柱:Kromasil C18柱(250 mm×4.6 mm,5 μm);流动相:甲醇-0.02%三乙胺水溶液(53∶47);流速:1.0 mL/min;二极管阵列检测器(DAD);检测波长:205 nm;柱温:30℃;进样量:10 μL。
(2)标准曲线的绘制:精密吸取0.525mg/mL的苦参碱对照品溶液0.5 mL、1 mL、2 mL、4 mL、8 mL,加甲醇稀释至10 mL,分别吸取10 μL,注入高效液相色谱仪,按2.2.4项下的色谱条件进行测定。以峰面积为纵坐标(Y),以苦参碱浓度为横坐标(X),得回归方程:Y=2.100 1X-0.391 2,相关系数R=0.999 9,在26.25~420.00 μg/mL范围内,线性关系良好。精密吸取0.521 mg/mL的氧化苦参碱对照品溶液0.5 mL、1 mL、2 mL、4 mL、8 mL,加甲醇稀释至10 mL,分别吸取10 μL,注入高效液相色谱仪,按2.2.4项下的色谱条件进行测定。以峰面积为纵坐标(Y),以氧化苦参碱浓度为横坐标(X),得回归方程:Y=1.723 6+3.460 2,相关系数R=0.999 5,在26.05~416.08 μg/mL范围内,线性关系良好。
(3)样品中苦参碱和氧化苦参碱的含量测定:精密称取紫归子妇炎康泡腾栓2枚,置于10 mL容量瓶中,加甲醇,超声溶解30分钟,补足重量,用0.45 μm微孔滤膜过滤,即得。精密吸取样品10 μL,进样,测定。
2.3 方法学实验
2.3.1 稳定性实验取同一批自制紫归子妇炎康泡腾栓,分别在0小时、3小时、6小时、9小时、12小时、18小时、24小时进样20 μL,记录峰面积。苦参碱、氧化苦参碱、阿魏酸、左旋紫草素和β,β-二甲基丙烯酰的RSD分别为2.08%、1.33%、1.89%、1.50%、1.57%。
2.3.2 精密度实验精密吸取一定浓度的苦参碱、氧化苦参碱、阿魏酸、左旋紫草素和β,β-二甲基丙烯酰对照品溶液20 μL,连续进样5次,记录峰面积。苦参碱、氧化苦参碱、阿魏酸、左旋紫草素和β,β-二甲基丙烯酰RSD分别为0.74%、0.63%、0.34%、1.26%、1.53%。
2.3.3 重复性实验取同一批自制紫归子妇炎康泡腾栓供试品5份,按样品测定方法测定。供试品中苦参碱、氧化苦参碱、阿魏酸、左旋紫草素和β,β-二甲基丙烯酰RSD分别为1.96%、1.62%、2.61%、1.41%、2.38%。
2.3.4 回收率实验精密称取已知含量的紫归子妇炎康泡腾栓制剂5份,每份1.25 g,分别加入苦参碱对照品储备溶液9.95 mL、氧化苦参碱对照品储备溶液1.32 mL、阿魏酸对照品储备溶液0.755 mL、左旋紫草素对照品储备溶液0.206 mL、β,β-二甲基丙烯酰对照品储备溶液0.292 mL。按上述方法进行处理和测定,计算紫归子妇炎康泡腾栓中5种活性成分的回收率平均为99.78%,RSD为3.12%。
3 含量测定结果
5批制剂样品中左旋紫草素、β,β-二甲基丙烯酰、阿魏酸、苦参碱、氧化苦参碱的含量测定结果见表1。
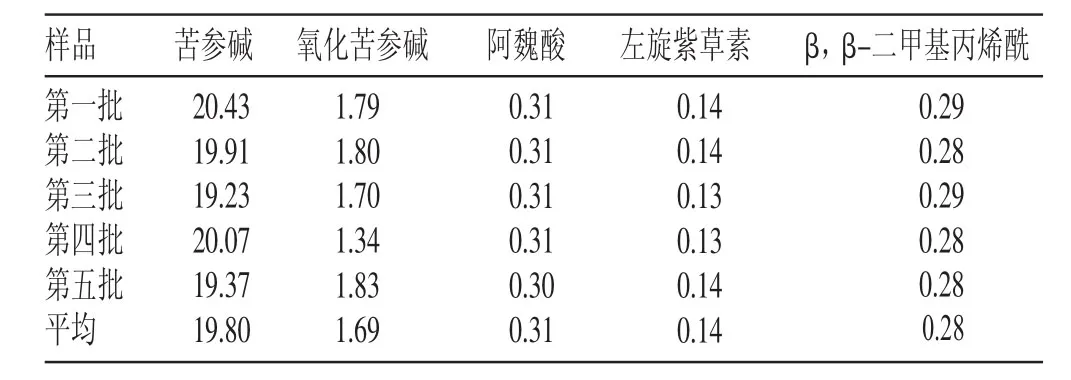
表1 样品中5种活性成分的含量(mg/枚)
4 结语
本文采用高效液相色谱法测定了自制紫归子妇炎康泡腾栓中5种活性成分的含量,所采用的方法简单易行。为全面高效地控制制剂的质量提供了保证。实验室自制的5批紫归子妇炎康泡腾栓中阿魏酸、左旋紫草素、β,β-二甲基丙烯酰、苦参碱、氧化苦参碱的平均含量分别为0.31 mg/枚、0.14 mg/枚、0.28 mg/枚、19.80 mg/枚、1.69 mg/枚。
[1]蒋伟,王长虹,王峥涛.当归水溶性成分研究[J].中国药学杂志,2010,45(2):101-103.
[2]徐新刚,王宝珍,孙志蓉,等.新疆紫草的主要化学成分[J].吉林大学学报,2010,48(2):319-322.
[3]林建峰,吴珊.紫云金的抗炎镇痛作用[J].海峡药学,2000,12(1):25-27.
[4]胡慧香,张智敏.复方苦豆子栓剂的制备及临床应用[J].山西中医,2009,25(5):50-51.
(*通讯作者:胡芳弟)
R28
B
1671-1246(2015)24-0151-03
甘肃省卫生厅2013年资助中医药科研课题(GZK-2012-15)
