邻香草醛缩胱氨酸双Schiff碱的合成及其对粟酒裂殖酵母细胞生长代谢的热动力学研究
2015-11-08蒋建宏谷惠文肖圣雄胡钞粟肖碧源汤蒋莹王文轩邓媚莹李强国
蒋建宏,李 旭,谷惠文,肖圣雄,胡钞粟,肖碧源,汤蒋莹,王文轩,邓媚莹,李强国
邻香草醛缩胱氨酸双Schiff碱的合成及其对粟酒裂殖酵母细胞生长代谢的热动力学研究
蒋建宏1,2,李 旭1,2,谷惠文3,4,肖圣雄1,2,胡钞粟1,2,肖碧源1,2,汤蒋莹1,2,王文轩1,2,邓媚莹1,2,*李强国1,2
(1. 湘南学院化学与生命科学系,湖南,郴州 423043;2. 湘南稀贵金属化合物及其应用湖南省重点实验室,湖南,郴州423043;3. 湖南大学化学化工学院,湖南,长沙 410082;4. 化学生物传感与计量学国家重点实验室,湖南,长沙 410082)
用摩尔比为2:1的邻香草醛(C8H8O3)与L-胱氨酸(C6H12N2O4S2)反应,合成了一种新的双Schiff碱化合物--双{2-[(3-巯基丙酸钠)-2-亚胺基-甲基]-6-甲氧基-苯酚} (OVCS)。通过元素分析、红外光谱、核磁共振等手段对其组成和结构进行了表征, 确定其化学式为Na2(C22H22N2O8S2),采用TAM air微量热仪测定了新合成的Schiff碱化合物(OVCS)在305.15 K时对粟酒裂殖酵母细胞作用的产热曲线;根据产热曲线计算了在OVCS作用下,粟酒裂殖酵母细胞生长代谢的最大发热功率P、速率常数、传代时间t、抑制率和半抑制浓度C等热动力学参数。通过实验可以发现随着OVCS浓度的增加,粟酒裂殖酵母细胞的生长代谢速率常数、生长代谢的总热效应Q、最大发热功率P均减小,抑制率、达到生长代谢最大功率所需时间t、传代时间t均增加等规律,半抑制浓度C为35.99 mg/L(或9.62×10-2mol/L)。实验结果表明,OVCS对粟酒裂殖酵母细胞有抑制作用,且浓度越大,抑制作用越强。
邻香草醛;L-胱氨酸;热动力学参数;粟酒裂殖酵母细胞
一直以来,席夫碱抗菌活性方面都是人们关注和研究的重点[1]。而邻香草醛具有较好的抗癌抗菌活性,且邻香草醛席夫碱要比其它席夫碱(如水杨醛类席夫碱)抗菌抗癌活性更好[2-4]。此外,L-胱氨酸与L-硫氢化氨基丙酸相同, 它广泛地应用于医药、食品、化妆品等方面[5],具有调节人体营养平衡、促进新陈代谢、抗癌、抗病毒等功能。有关邻香草醛席夫碱化合物抗癌抗菌的报道已有很多,但邻香草醛与L-胱氨酸双席夫碱化合物的合成与生物活性还未见报道。将两种具有抗菌活性的物质结合起来,预测可以加强抗菌效果,对探究新的高效抗菌药物具有重要意义。
用微量热法已经得到了很多关于药物对微生物作用的相关信息[6-7],用微量热法研究双{2-[(C3-巯基丙酸钠)-2-亚胺基-甲基]-6-甲氧基-苯酚}(OVCS)对粟酒裂殖酵母细胞的作用还未见报道。本研究通过微量热法来探究在305.15 K时OVCS对粟酒裂殖酵母细胞生长代谢的影响。通过对TAM air微量热仪的数据进行一系列的处理和分析,进一步了解OVCS对细胞的作用机理,为探究邻香草醛类席夫碱的药理和探求高效低毒的抗菌抗癌药物提供理论基础。
1 实验部分
1.1 仪器与试剂
1.1.1 仪器
实验采用3116-2/3239TAM Air 八通道热导式等温微量热仪(瑞典Thermometric AB公司)。描述热导式热量计量热的基本方程是建立在Newton冷却定律基础之上的Tian方程(Eq. 1)[8]。
(d/d)t=Cd()d+Ck(∆T) (1)
式中C∆T项表示热量积累,C为量热计量热皿的热容,CkD(∆T)项表示热量的散失。由于量热计的环境温度恒定,当量热皿外部区域为高热容材料(如铝散热片)时,即C>>C,则几乎没有热量在量热皿积累,热的传导接近完全,此时Eq.1 变为:()(CkD) =∆T→0。即在热导式热量计中温升非常小,要求检测系统有较高的灵敏度。
Bruker 400MHz Advance(瑞士Bruker公司),氘代DMSO做溶剂。
PE-2400元素分析仪(美国Perkin Elmer公司)。
1.1.2 材料
邻香草醛[纯度≥ 99.0%,北顺(北京)化学科技有限公司];L-胱氨酸(纯度≥ 99.0%,天津市光复精细化工研究所);其余试剂均为分析纯;实验用水为三重蒸馏水。
粟酒裂殖酵母细胞(Schizosaccharomyces pombe)由西班牙萨拉曼卡大学(University of Salamanca)Faustino Mollinedo 教授惠赠;YES培养基:5.000 g酵母粉+30.000 g葡萄糖+0.225 g亮氨酸+0.225 g腺嘌呤+0.225 g赖氨酸+0.225 g尿嘧啶+0.225 g组氨酸,溶于1000 mL三次蒸馏水中,于120 ℃高压灭菌30 min后备用。
1.2 实验过程
1.2.1 OVCS的合成
称取0.4 g(10 mmol)氢氧化钠溶于60 mL无水乙醇中,加入1.2015 g(5 mmol)白色粉末状L-胱氨酸,搅拌溶解,转入三颈烧瓶中,再将含有1.5215 g (10 mmol)邻香草醛20 mL无水乙醇溶液逐滴加入到三颈烧瓶中,40 ℃搅拌加热回流半小时,抽滤,再用无水甲醇溶解,抽滤提纯,将抽滤后溶液进行蒸馏浓缩至出现结晶产物、产品抽滤,用无水乙醇洗涤数次后,真空干燥,得到黄色固体粉末。
1.2.2 粟酒裂殖酵母细胞及其在OVCS作用下生长代谢热的测定
采用TAM Air热导式等温微量热仪测定,实验方法和操作步骤参见文献[9]。
2 结果与讨论
2.1 OVCS的性质、组成及结构
2.1.1 OVCS的性质及元素分析
OVCS为黄色固体粉末,在空气中极不稳定,极易水解,不溶于乙醇、乙醚,易溶于甲醇、乙氰、丙酮和二甲亚砜等溶剂。对其进行元素分析,数据表明:测量值与理论值基本一致(结果见表1)。

表1 OVCS的元素分析
2.1.2 OVCS的红外光谱测定
从图1的红外光谱图可知:-vanillin中出现的1632.95 cm-1处的C=O伸缩振动峰和L-cystine中出现的1590.24 cm-1处的-NH2基团的面内变形振动峰,在OVCS中均消失了,而出现了1636.68 cm-1处的C=N基团的特征吸收峰,发生了蓝移,说明C=O键与-NH2发生了反应,形成了C = N键,确定生成了OVCS化合物。此外,在L-cystine中出现的675.00 cm-1处的C-S吸收峰在OVCS的673.42 cm-1处出现,在L-cystine中540.51 cm-1处出现的S-S伸缩振动峰在OVCS的541.14 cm-1处出现,且Ph-O的伸缩振动峰在-vanillin的1295.51 cm-1处和OVCS的1296.59 cm-1处出现,峰值几乎相同,说明酚羟基没有发生变化,而在OVCS中找不到羧基峰,羧基峰已经改变,这些均与元素分析结论相同。

波长(cm-1)
2.1.3 OVCS的核磁谱图
从图2的核磁谱图分析数据如下(结构式见图3):9.96 (s, 2H, 苯环上酚羟基-OH), 8.40 (s, 2H, 9号位上氢-N=CH), 6.81-6.99 (m, 4H, 苯环3、5号位上氢), 6.60 (d,= 6.4 Hz, 2H, 苯环4号位上氢), 6.00 (t,= 7.7 Hz, 2H, 11号位上氢=N-CH), 3.73 (dd,= 7.6, 4.4 Hz, 4H, 13号位上氢-CH2), 3.64 (s, 6H, 苯环上甲氧基-OCH3),而羧基应该是以羧酸盐-COO-形式存在[10],不是-COOH,故核磁数据里面没有对应的-COOH的质子信号。OVCS中共有22个H。
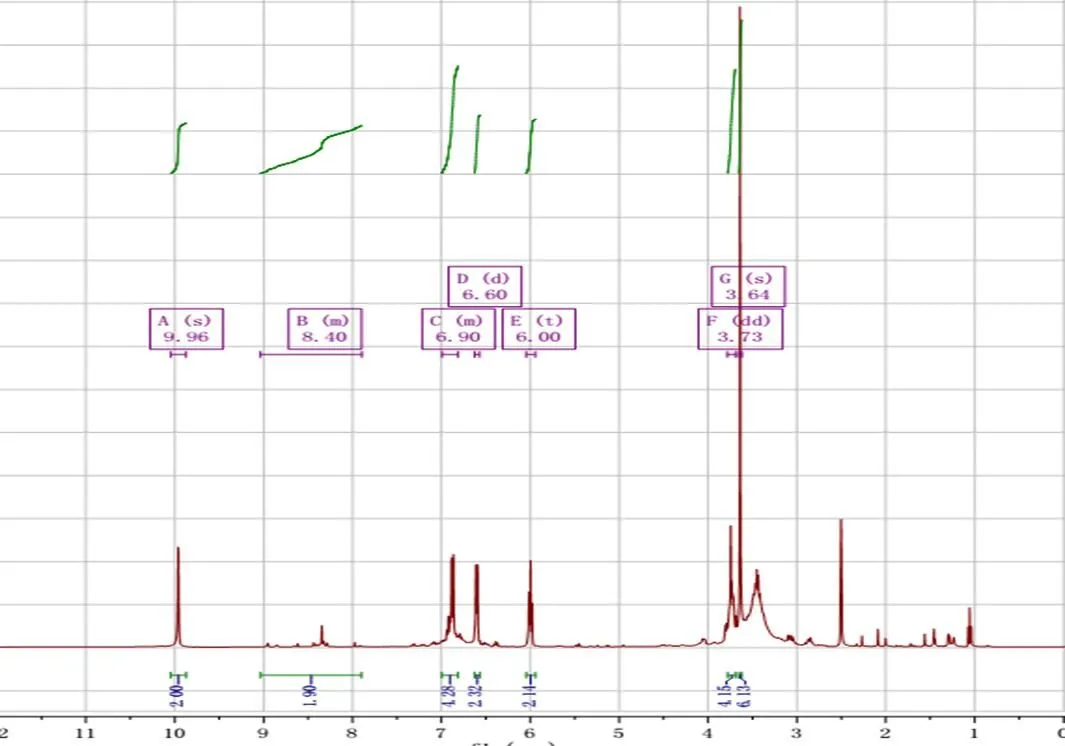
图2 OVCS的核磁图谱
2.1.4 OVCS的结构式
结合元素分析、红外谱图分析结果,可确定产物的结构式如下:
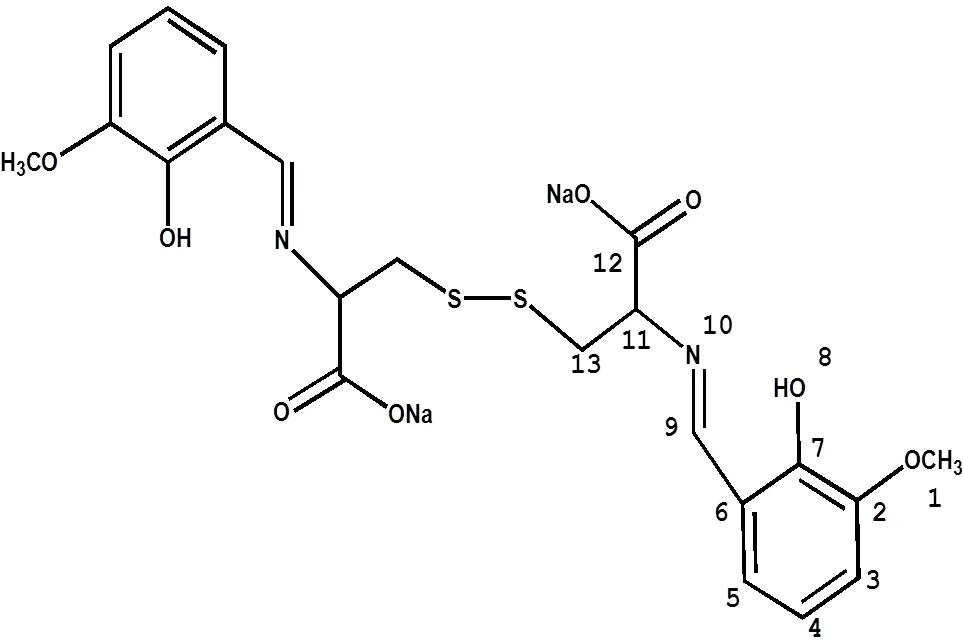
图3 OVCS的结构式
2.2 生物量热实验结果与数据处理
2.2.1 粟酒裂殖酵母细胞的生长代谢热曲线
在305.15 K时,保持其它条件不变的情况下,依次加入不同浓度的OVCS溶液到5 mL培养基中,来测定粟酒裂殖酵母细胞的正常生长代谢热谱曲线,热谱曲线如图4所示。

a, 0 mg/L; b, 11.20 mg/L; c, 14.56 mg/L; d, 17.92 mg/L; e, 21.28 mg/L; f, 24.64 mg/L; g, 28.00 mg/L;h, 41.44 mg/L
2.2.2 粟酒裂殖酵母细胞的生长速率常数和传代时间t
从图4的生长代谢热曲线可以看出,粟酒裂殖酵母细胞的的生长期包括停滞期、指数生长期、稳定期和衰减期等阶段。在粟酒裂殖酵母细胞的指数生长期[11]内,其数量增长的数学表达式为:
lnp=lnp-kt+(2)
式中,p为粟酒裂殖酵母细胞在时刻的热输出功率;为粟酒裂殖酵母细胞在某条件下指数生长期内的生长数速率常数,其值越大,细胞的生长代谢速率越快。将生长代谢热曲线上指数生长期阶段的曲线,用计算机进行线性拟合,可得到在不同OVCS浓度作用下粟酒裂殖酵母细胞的传热速率常数,又由公式t=(2)/,可以算出粟酒裂殖酵母细胞在不同OVCS浓度作用下的传代时间t(见表2)。
2.2.3 粟酒裂殖酵母细胞的抑制率和半抑制浓度C50
药物对细菌生长代谢过程的抑制率的公式为:
=(K-K)/K×100% (3)
式中K0为粟酒裂殖酵母细胞未受到药物作用时生长速率常数,K为粟酒裂殖酵母细胞受到浓度为的药物作用时的生长速率常数。半抑制浓度C,即当抑制率为50%时所对应的药物浓度。
由公式(3)可计算出粟酒裂殖酵母细胞在不同OVCS浓度作用下的抑制率和抑制率为50%时的生长速率常数(见表2)。再由与的关系,求出半抑制浓度C。半抑制浓度的大小表明了药物对粟酒裂殖酵母细胞的抑制效果。C越小,药物对粟酒裂殖酵母细胞抑制效果越好,抗菌活性越强。OVCS对粟酒裂殖酵母细胞的半抑制浓度为35.99 mg/L。
2.2.4 粟酒裂殖酵母细胞生长的最大产热功率P,最大产热功率时间t和总放热量Q
从图4的生长代谢产热曲线可以读出最大产热功率P以及最大产热功率时间t(见表2),它们的大小实际上代表了粟酒裂殖酵母细胞生长获得最大活性时的产热功率以及获得最大活性所需的时间。总放热量Q可直接通过对每条生长代谢产热曲线的积分得到(见表2),它的大小反映了不同OVCS浓度作用下,粟酒裂殖酵母细胞生长代谢的强弱情况,Q越小,说明该浓度下,OVCS对细胞生长代谢的抑制作用越强。
2.2.5 生长速率常数与浓度的关系
粟酒裂殖酵母细胞生长代谢速率常数对OVCS浓度进行Logistic曲线拟合, 得到如图5所示关系。由图可知,随着OVCS浓度的增加,粟酒裂殖酵母细胞的生长速率常数呈S型曲线逐渐减小,表明OVCS对粟酒裂殖酵母细胞有抑制作用。得到曲线方程为:
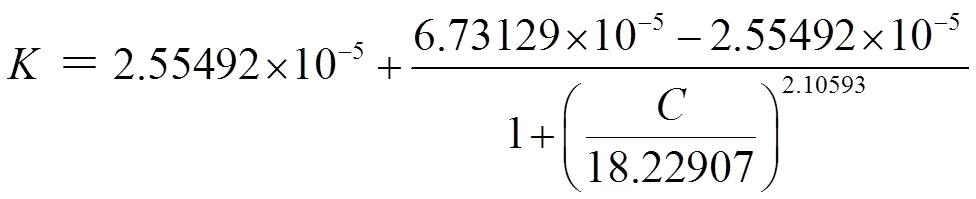
[0 ≤(OVCS)≤ 41.44 mg/L];相关系数=0.99737。

表2 305.15 K时,粟酒裂殖酵母细胞在不同药物浓度作用下生长期的热动力学参数
(mg/L), 配合物浓度;(S−1)生长速率常数;(%),抑制率;Q(w),总放热量;P(w),最大发热功率;t(S),达到最大发热功率所需时间;t(min),传代时间;线性匹配相关系数。
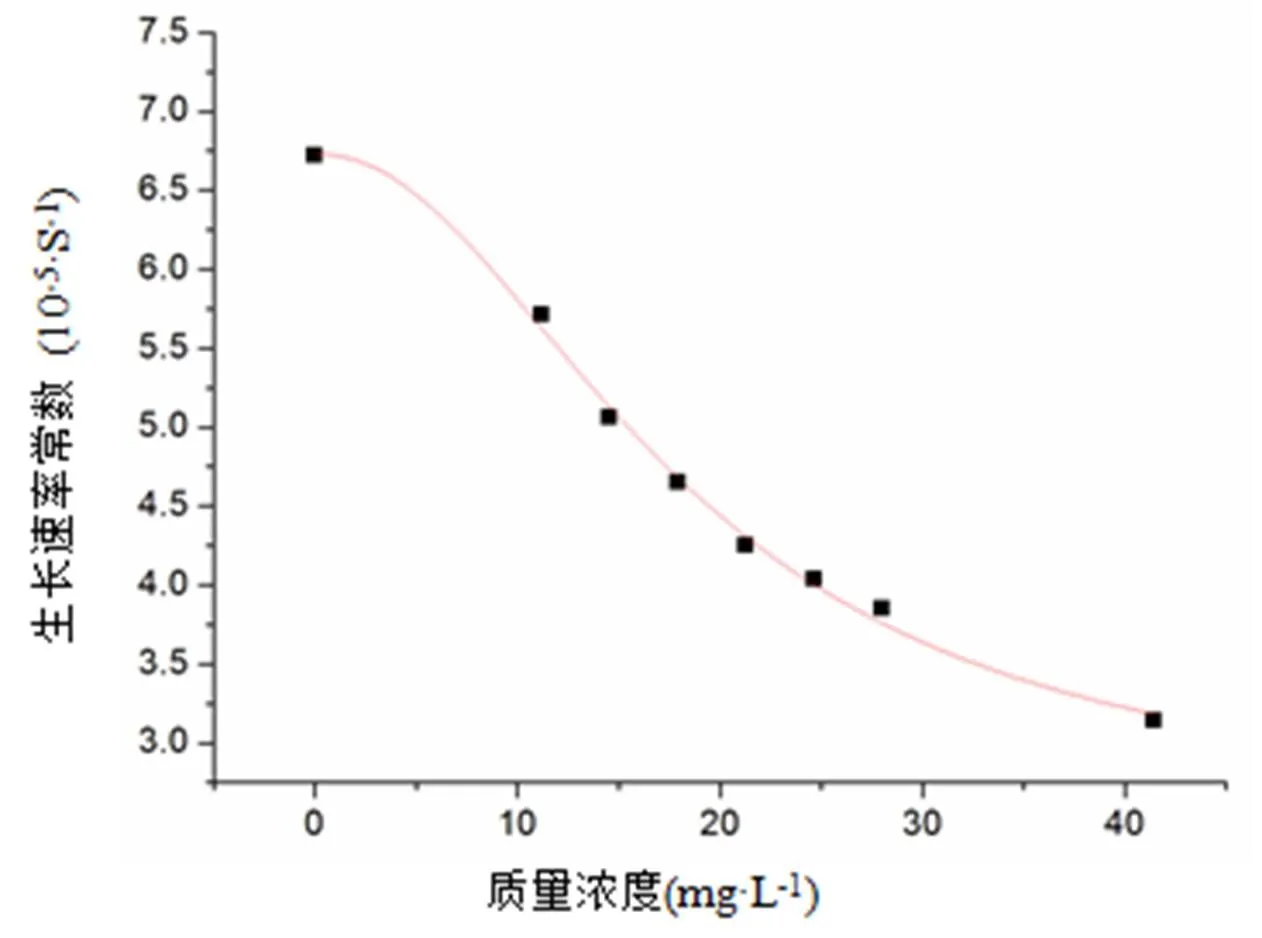
图5 粟酒裂殖酵母细胞的生长速率常数k与OVCS浓度c的关系
2.2.6 抑制率与浓度的关系
OVCS对粟酒裂殖酵母细胞抑制率与它的浓度的进行Logistic曲线拟合,得到如图6所示关系。由图可知,随着OVCS浓度的增加,OVCS对粟酒裂殖酵母细胞的抑制率呈S曲线增加,表示OVCS浓度越大,抑制作用越强。得到曲线方程为:
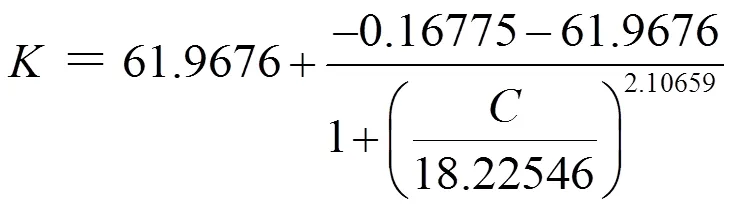
[0 ≤(OVCS)≤ 41.44 mg/L];相关系数=0.99737。
图6 OVCS对粟酒裂殖酵母细胞的抑制率与它浓度的关系
Fig.6 Inhibitive rate () ofwith different concentrations of OVCS()
2.2.7 生长代谢的总热效应total与浓度的关系
粟酒裂殖酵母细胞生长代谢的总热效应Q对OVCS浓度进行Logistic曲线拟合,得到如图7所示关系。由图7可知,随着OVCS浓度的增加,粟酒裂殖酵母细胞生长代谢的总热效应Q呈S曲线逐渐减小,表明OVCS浓度越大,对粟酒裂殖酵母细胞的抑制作用就越大。得到曲线方程为:
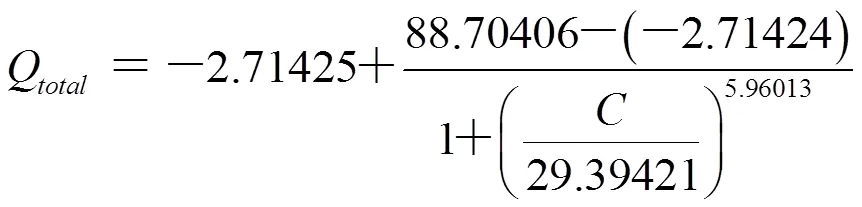
[0 ≤(OVCS)≤ 41.44 mg/L];相关系数=0.99962。
图7 粟酒裂殖酵母细胞生长代谢的总热效应Q与OVCS浓度的关系
Fig.7 The total thermal effect (Q) ofwith different concentrations of OVCS()
2.2.8 最大发热功率P与浓度的关系
粟酒裂殖酵母细胞的最大发热功率P与OVCS浓度的关系,如图8所示。由图8可知,OVCS浓度的增加,使粟酒裂殖酵母细胞的最大发热功率P呈下降趋势,表明OVCS对粟酒裂殖酵母细胞有抑制作用。
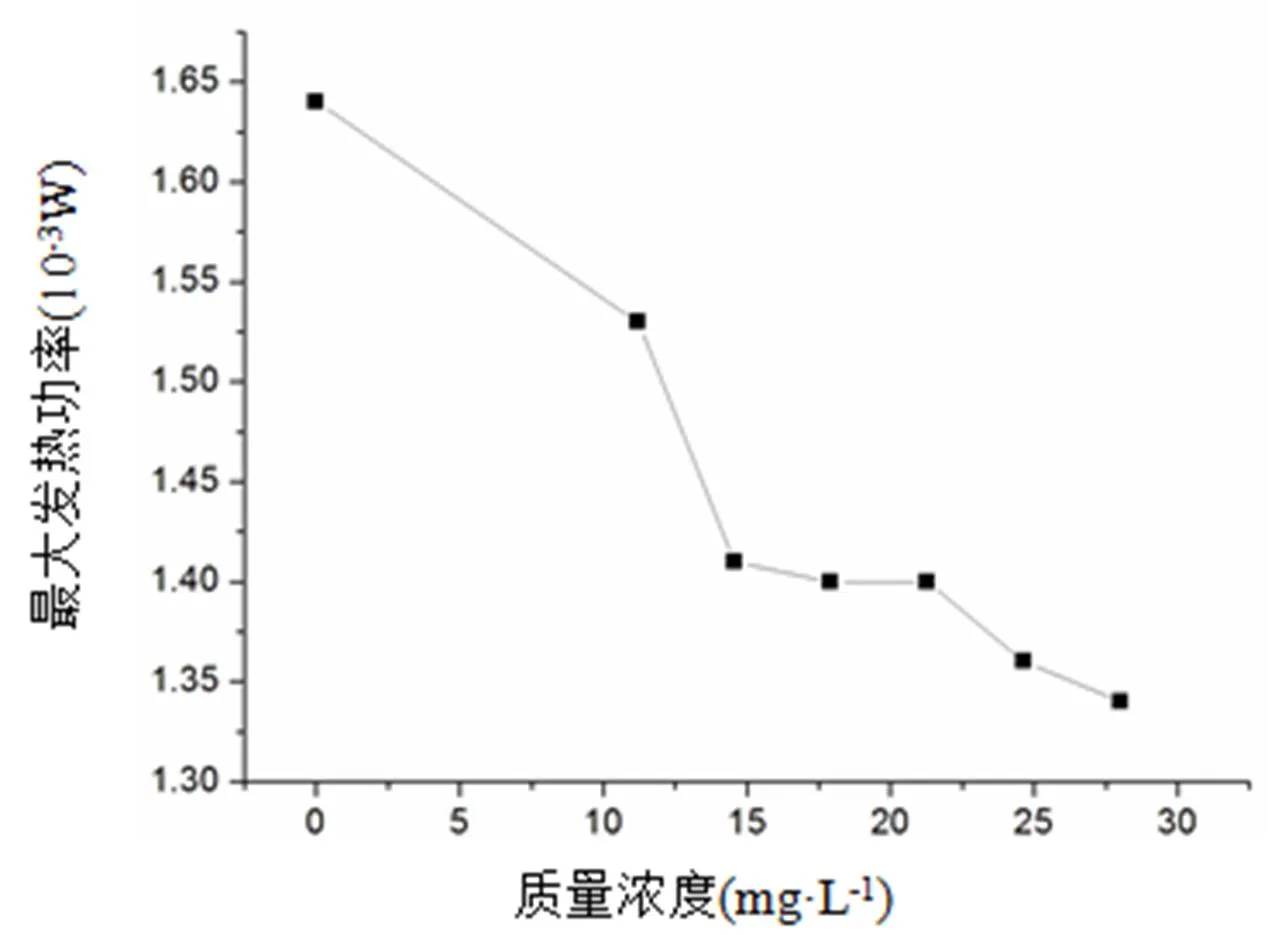
图8 粟酒裂殖酵母细胞的最大发热功率Pmax与浓度c的关系
2.2.9 达到生长代谢最大功率所需时间t与浓度的关系
粟酒裂殖酵母细胞达到生长代谢最大功率所需时间t与OVCS浓度进行Logistic曲线拟合,如图9所示关系。由图9可知,随着OVCS浓度的增加,粟酒裂殖酵母细胞达到生长代谢最大功率所需时间t呈S型曲线增大。得到曲线方程为:

[0 ≤(OVCS)≤ 41.44 mg/L];相关系数=0.99949。
图9 粟酒裂殖酵母细胞生长代谢最大功率所需时间t与OVCS浓度的关系
Fig.9 The maximum power required to achieve the growth metabolism timetofwith different concentrations of OVCS()
2.2.10 传代时间t与浓度的关系
粟酒裂殖酵母细胞传代时间t与OVCS浓度进行Logistic曲线拟合,得到如图10所示关系。由图10可知,随着OVCS浓度的增加,粟酒裂殖酵母细胞传代时间t呈S曲线增加,表明OVCS浓度越大,抑制作用增强。得到曲线方程为:
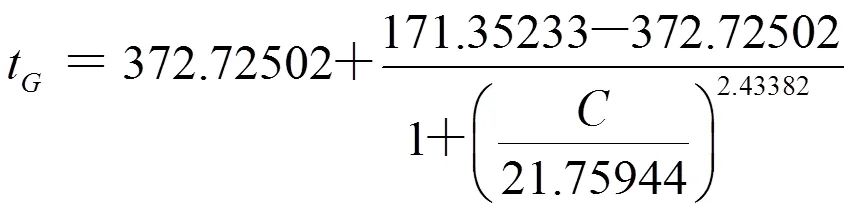
[0 ≤(OVCS)≤ 41.44 mg/L];相关系数=0.99908。
图10 粟酒裂殖酵母细胞传代时间t与OVCS浓度的关系
Fig.10 The generation time (t)ofwith different concentrations of OVCS()
3 结论
用摩尔比为2:1的邻香草醛与L-胱氨酸反应,合成了一种新的双Schiff碱化合物——双{2-[(3-巯基丙酸钠)-2-亚胺基-甲基]-6-甲氧基-苯酚}(OVCS),其分子式为Na2(C22H22N2O8S2)。用TAM air微量热仪探究了新合成的Schiff碱化合物(OVCS)在305.15 K时对粟酒裂殖酵母细胞生长代谢的影响。根据得到的产热曲线进行的一系列分析,结果显示:随着OVCS浓度的增加,生长速率常数、总热效应Q、最大发热功率P均减小,而抑制率、最大功率的时间t、传代时间t均增加。
实验表明:在所研究的浓度范围内,OVCS对粟酒裂殖酵母细胞的生长都起抑制作用,且随着浓度的增大,其抑制作用越强,而抑制作用的机理还有待进一步探究。
参考文献:
[1] 蒋建宏, 李旭, 肖圣雄, 等. 2-{[4-氨基-5-(3,4,5-三甲氧基-苄基)-嘧啶-2-亚胺基]-甲基}-6-甲氧基-苯酚与酵母细胞和牛血清白蛋白的相互作用[J].高等学校化学学报, 2014, 35 : 831-838.
[2] Prabhakaran R,Geetha A, Thilagavathi M, et al. Synthesis, characterization, EXAFS investigation and antibacterial activities of new ruthenium(III) complexes containing tetradentate Schiff base[J]. Inorg Biochem, 2004, 98(12) : 2131-2140.
[3] Assegid G, Lamprecht I. Microcalorimetric investigations on the influence of propolis on the bacterium micrococcus luteus[J]. Thermochim. Acta, 1997, 290(2) : 155-166.
[4] Jeewoth T,Bhowon M G,Wah H L K.Synthesis, characterization and antibacterial properties of Schiff bases and Schiff base metal complexes derived from 2,3-diamino- pyridine[J]. Transit. Met. Chem. 1999, 24(4) : 445-448.
[5] 刘善斌. 新型过渡金属配合物的合成、表征及应用研究[D]. 青岛:中国海洋大学, 2011.
[6] 何笃贵,李强国,杨德俊,等. RE(C7H5O3)2(C9H6NO)配合物抗真菌作用的热动力学研究[J]. 中国稀土学报, 2007, 25 : 107.
[7] 肖圣雄,李强国,李旭,等. 镨配合物的热化学及其对酵母菌作用的热动力学研究[J]. 中国科学: 化学, 2010, 40(9) : 1422-1429.
[8] 张信连,杨维东,刘洁生,等. 稀土元素生物效应中的Hormesis现象[J]. 生物技术, 2004, 14 : 82-84.
[9] 杨德俊,李旭,胡吉林,等.烟酸锰配合物[Mn(C6H4NO2)2]·2H2O(s)的合成、生成焓及其对粟酒裂殖酵母细胞生长代谢的微量热法研究[J].化学学报, 2010, 68 : 2373-2380.
[10] 李艳,孙绍发,吴鸣虎.过渡金属胱氨酸水杨醛Schiff碱配合物的合成及抑菌活性[J].化学研究,2010,21(6) : 26-33.
[11] 蒋建宏,肖圣雄,王艳兰,等. 1,3-二氨基硫脲对粟酒裂殖酵母细胞作用的热动力学研究[J]. 山东化工, 2014, 43(11) : 1-3.
Synthesis and thermokinetic study on the S.growth metabolism of a novel bis-Shciff base derived from-vanillin and L-cystine
JIANG Jian-hong1,2, LI Xu1,2, GU Hui-wen3,4, XIAO Sheng-xiong1,2, HU Chao-su1,2, XIAO Bi-yuan1,2,TANG Jiang-ying1,2,WANG Wen-xuan1,2, DENG Mei-ying1,2,*LI Qiang-guo1,2
(1.Department of Chemistry and Life Science, Xiangnan University, Chenzhou, Hunan 423043, China;2. Hunan Provincial Key Laboratory of Xiangnan Rare-Precious Metals Compounds and Applications,Chenzhou,Hunan 423043,China;3.School of Chemistry and Chemical Engineering, Hunan University, Changsha, Hunan 410082, China; 4. State Key Laboratory of Chemo/Biosensing and Chemometrics, College of Chemistry and Chemical Engineering, Changsha, Hunan 410082, China)
A novel Schiff base named Bis{2-[(3-mercapto propionic acid sodium-2-ylimino)-methyl]-6- methoxy-phenol}(abbreviated as OVCS) was synthesized using 2:1 molar ratio of-vanillin (C8H8O3) and L-cystine (C6H12N2O4S2). Elemental analysis, IR and NMR spectroscopy were employed to characterize the composition and structure of OVCS. The analytical results show that the molecular formula of the Schiff base is Na2(C22H22N2O8S2). The thermokinetic properties of the action of OVCS on the growth metabolism ofwere investigated by a TAM air isothermal calorimetry at 305.15 K. Some thermokinetic parameters of growth metabolism of, such as the maximum heating power (P), growth rate constant (), generation time (t), inhibition rate () and half inhibitory concentration (C) were calculated. Experimental results indicate that the values of, QandPofdecrease, while the value of,tandtofincreased with the increase of the concentrations of OVCS. TheCvalue of OVCS was found to be 35.99 mg/L (or 9.62×10-2mol/L). From this work, one can reach a conclusion that OVCS possesses inhibitory effect on the growth metabolism of, and the greater the concentration, the stronger the inhibition.
-vanillin; L-cystine; thermokinetic property;cell
1674-8085(2015)06-0029-07
O641;O633.12
A
10.3969/j.issn.1674-8085.2015.06.007
2015-06-06;修改日期:2015-09-08
国家自然科学基金项目(21273190);湖南省科技计划项目(2013FJ3033, 2012TP4021-6, 2010FJ3053);湘南学院科研基金项目(2013YJ36;2014XJ52);湘南学院大学生研究性学习和创新性实验计划项目(校发[2013]15号)
蒋建宏(1984-),男,湖南邵阳人,助教,硕士,主要从事生物热化学研究(Email:jiangjianhong927@163.com);
李 旭(1980-),男,湖南郴州人,实验师,硕士,主要从事热化学研究(Email: 51571435@163.com );
谷惠文(1987-),男,湖南衡阳人,博士生,主要从事分析化学研究(Email: gruyclewee@hnu.edu.cn );
肖圣雄(1975-),男,湖南郴州人,副教授,硕士,主要从事热化学研究(Email:54xsx@163.com);
胡钞粟(1991-),女,湖南益阳人,湘南学院化学与生命科学系应用化学专业2011级本科生(E-mail:huchaosu@163.com);
肖碧源(1994-),女,湖南邵阳人,湘南学院化学与生命科学系应用化学专业2012级本科生(E-mail:1586769784@qq.com);
汤蒋莹(1995-),女,浙江宁波人,湘南学院化学与生命科学系应用化学专业2013级本科生(E-mail:615874992@qq.com);
王文轩(1995-),女,湖南浏阳人,湘南学院化学与生命科学系药学专业2013级本科生(E-mail:1352645558@qq.com);
邓媚莹(1995-),女,湖南湘潭人,湘南学院化学与生命科学系药学专业2013级本科生(E-mail 1416146668@qq.com);
*李强国(1963-),男,湖南郴州人,二级教授,主要从事生物热化学研究(Email:liqiangguo@163.com).
