CT引导下125I放射性粒子植入联合化疗对中晚期胰腺癌的疗效
2015-10-28伦俊杰赵俊玲孙建业胡效坤殷好治
伦俊杰,赵俊玲,孙建业,胡效坤,殷好治
CT引导下125I放射性粒子植入联合化疗对中晚期胰腺癌的疗效
伦俊杰,赵俊玲,孙建业,胡效坤,殷好治
目的探讨CT引导下125I放射性粒子植入联合吉西他滨和替吉奥(GS)化疗方案治疗中晚期胰腺癌的疗效及安全性。方法将68例无手术指征的中晚期胰腺癌患者随机分为两组。A组38例接受125I粒子植入联合GS化疗方案,B组30例接受GS化疗方案。比较两组近期疗效、中位无进展生存时间(mPFS)、中位生存时间(mOS)和不良反应。结果A组客观有效率、疾病控制率和临床受益率(ORR、DCR和CBR)分别为57.9%、73.7%、84.2%,B组分别为26.7%、46.7%、60.0%,两组比较差异均有统计学意义(P<0.05);A组mPFS、mOS分别为8.0、11.8个月,高于B组5.6、10.4个月,差异有统计学意义(P<0.05);消化道反应、血液毒性及肝毒性等不良反应,差异无统计学意义(P>0.05)。结论对于中晚期胰腺癌患者,CT引导下125I放射性粒子植入联合GS方案是一种安全、有效的治疗手段。
胰腺癌;125I粒子;吉西他滨;替吉奥
胰腺癌是常见的消化道恶性肿瘤之一。其发病隐匿,大部分患者在确诊时处于中晚期,已失去手术切除机会。放疗、化疗成为其主要治疗手段,但疗效不尽人意[1-2]。随着研究的深入,125I放射性粒子植入已成为中晚期胰腺癌的重要治疗手段,并取得较好成效[3-4]。本研究回顾性分析68例中晚期胰腺癌患者的临床资料,分析125I放射性粒子植入联合吉西他滨和替吉奥(GS)方案治疗患者的疗效及不良反应,以期为中晚期胰腺癌患者提供一种安全、有效的治疗手段。
1 材料与方法
1.1材料
1.1.1一般资料收集2009年10月至2012年1月期间入住我科、临床资料完整的、无法手术切除的中晚期胰腺癌患者68例,患者术前均经CT平扫、增强和(或)MRI检查,以及CT引导下穿刺活检,经病理和细胞学明确诊断。其中男41例,女27例;年龄39~80岁,中位年龄49岁;胰头癌57例,胰体癌7例,胰尾癌4例;按国际抗癌联盟(UICC)临床分期法:Ⅲ期22例,Ⅳ期46例;肿瘤最大直径均≤6 cm,患者既往均未接受放疗、化疗及其他综合治疗,KPS评分≥60分,无严重的心肺肾等脏器病变。分成A组(125I粒子植入联合GS组)与B组(GS组),两组患者的一般临床特征具有可比性,预计生存期>3个月。
1.1.2仪器与设备德国西门子公司生产的64排螺旋CT扫描仪,放射性粒子植入治疗计划系统(TPS)由珠海和佳医疗股份有限公司提供,粒子植入器和植入针(18 G带刻度)为美国Radio-nuclear公司生产的Mick枪,125I放射性粒子由北京智博有限公司制造,为圆柱形外包钛合金密封结构,长4.5 mm、直径0.8 mm,平均能量为27~35 KeV,组织穿透能力1.7 cm,放射活度为0.50~0.82 mCi,初始剂量率7 cGy/h,半衰期59.46 d。
1.2方法
1.2.1治疗方法A组患者术前均签署相关知情同意书,术前计划将胰腺CT图像传入TPS,勾画靶区,给出处方剂量,计算靶区体积、匹配周边剂量(match peripheral dose,MPD),绘出等剂量曲线、粒子放射性活度、所需粒子的空间分布,确定进针的路径、植入针数及粒子数。术前2 d行流质饮食,术前24 h禁饮食,术前12 h服用导泻药,术前半小时注射止血针。
术时患者取仰卧位,常规消毒、铺巾,局麻下在CT引导下,利用Mick粒子植入枪后退式植入125I粒子。确保进针深度达病灶的最深处(距肿瘤边缘约1 cm、回吸无出血、胰漏),植入粒子间隔0.5~1 cm,避免损伤胰管和大血管。A组38例,共植入粒子1 232枚,每例患者植入中位粒子数32枚(16~68枚),肿瘤MPD为90~140 Gy。术中行CT扫描进行验证,如出现粒子分布不均或有遗漏等情况,在剂量缺损区立即补植,见图1。

图1 胰头癌125I粒子植入治疗过程
1.2.2术后处理术后卧床休息且禁食水24 h,并给予预防感染、止血、止痛、抑制胰酶分泌、营养支持等治疗。在粒子植入后5~10 d内依据患者体质恢复情况行GS方案化疗,术后1个月复查CT,行剂量验证,确定是否需要补植粒子。
1.2.3GS方案化疗具体方案如下:吉西他滨(Gem)1 000 mg/m2,静脉滴注,每日1次,滴注30 min,d 1,8;替吉奥(S-1)40 mg/m2,餐后口服,每日2次,d 1~14,每3周为1疗程。入组患者至少完成2个疗程化疗。复查项目:血常规、生化、CA199、X线胸片、CT平扫+增强、MRI等。
1.2.4疗效及不良反应评价标准每2个疗程化疗按实体瘤疗效评价标准(RECIST1.1)判定近期疗效:完全缓解(CR)、部分缓解(PR)、疾病稳定(SD)、病变进展(PD),客观有效率(ORR)=(CR+PR)/(CR+PR+SD+PD),疾病控制率(DCR)=(CR+PR+ SD)/(CR+PR+SD+PD)。临床受益率(CBR)评定标准:依据1997年Burris等根据患者疼痛缓解、KPS评分改善和体重增加3项指标制定的CBR标准进行评定。无进展生存期(PFS)指从接受治疗开始至疾病进展或死亡时间,生存期(OS)指从接受治疗开始至死亡或末次随访日或随访截止日。根据美国肿瘤放射治疗年会(RTOG)推荐标准评价粒子植入后不良反应,根据国立癌症研究所的常规毒性判定标准(NCI CTCAE3.0)评价不良反应。
1.3随访及统计学方法
采用门诊或电话随访,随访3年,截至时间为2014年7月31日,采用SPSS 17.0统计软件分析,近期疗效、不良反应采用χ2检验,Kaplan-Meier法行生存分析,Log rank公式进行检验,P<0.05为差异有统计学意义。
2 结果
2.1近期疗效评价
68例患者均可评价疗效,A组38例患者中CR 7例,PR 15例,SD 6例,PD 10例;B组30例中CR 2例,PR 6例,SD 6例,PD 16例;两组ORR分别为57.9%、26.7%(χ2=6.631,P=0.010),DCR分别为73.7%、46.7%(χ2=5.182,P=0.023),CBR分别为84.2%(32/38)、60.0%(18/30)(χ2=5.049,P=0.025),差异有统计学意义。
2.2中位无进展生存时间(mPFS)及生存期(mOS)2.2.1mPFSA组为8个月(95%CI 5.485~9.915),高于B组5.63个月(95%CI 1.781~7.686),经Logrank检验,差异有统计学意义(χ2=3.997,P=0.046)。2.2.2mOSA组为11.84个月(95%CI 8.297~15.436)高于B组10.40个月(95%CI 6.89~12.45),经Long-rank检验,差异有统计学意义(χ2=4.116,P= 0.042),见图2。
2.3不良反应
粒子植入及化疗顺利,根据RTOG和NCI CTCAE 3.0标准,患者均未出现治疗相关性死亡及Ⅳ度严重不良反应。术后部分患者出现穿刺局部疼痛,对症处理后症状消失,患者均未发生胰漏、出血、胰腺炎、放射性肠炎、腹膜炎以及腹腔脓肿、肺栓塞等严重并发症,随访中发现2例患者粒子迁移到肝脏内,肝功检查未见明显异常。主要不良反应为消化道反应、血液毒性及肝毒性,2组比较差异无统计学意义(P>0.05)。(见表1)
3 讨论
研究表明,大约85%胰腺癌患者在确诊时已处于中晚期,失去手术根治机会[5]。因此,为提高患者生活质量和延长生存时间,以放疗、化疗为主的综合治疗就成为中晚期胰腺癌的主要手段。
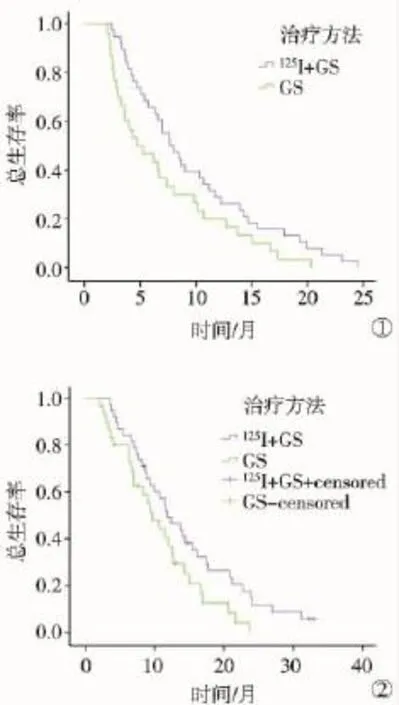
图2 2组中晚期胰腺癌患者的PFS和OS曲线

表1 2组中晚期胰腺癌患者治疗后的不良反应n(%)
近年来,粒子组织间植入放疗逐渐受到重视,其持续放射低剂量γ射线,使DNA分子链中单链断裂、双键断裂;电离水分子产生自由基,引起肿瘤细胞水肿、变性、坏死,最终导致肿瘤细胞凋亡。粒子组织间植入放疗具有以下优势:①放射源射线射程短、穿透力低,肿瘤可以得到较高的剂量,周围正常组织受量低而得到保护;②为持续低剂量照射,最大程度杀伤肿瘤;③不受呼吸运动和腹腔脏器移动影响。常用的核素粒子有125I、198AU、103Pd、169Y[6]。因125I粒子能量较低、半衰期长、易防护,便于运输,成为目前永久性植入方式最常用的核素粒子。125I放射性粒子组织间植入放疗已用于实体肿瘤临床治疗,并取得较好成效[7-9]。最近国内外应用125I粒子植入治疗中晚期胰腺癌已成为热点,研究表明125I粒子植入将成为中晚期胰腺癌安全、有效、并发症少的新型治疗方法[3-4]。近年来,国内外研究表明,吉西他滨与替吉奥胶囊联合(GS)较吉西他滨单药更能改善中晚期胰腺癌患者的预后[10-11]。125I粒子植入和GS化疗治疗胰腺癌已得到国内外广泛应用。
基于以上研究背景,我科在CT引导下125I粒子植入联合GS方案对中晚期胰腺癌患者进行疗效分析,本研究结果显示,对于中晚期胰腺癌患者,125I粒子植入联合GS化疗组的ORR、DCR和CBR明显高于单独GS化疗组(P<0.05)。说明125I放射性粒子植入可持久地缓解疼痛,改善患者生活质量,这可能与125I粒子持久地杀伤肿瘤细胞,减轻内部张力,解除或缓解肿瘤对腹腔神经丛的压迫或侵犯有关。在不良反应的发生率上,A组未高于B组,差异无统计学意义(P>0.05),说明125I粒子植入并没有增加胰腺癌患者不良反应,进一步说明125I粒子植入对于患者是安全的。在远期疗效上,A组mPFS和mOS明显高于单独GS化疗组且差异具有统计学意义(P<0.05),这可能与GS化疗增敏作用促使125I粒子持续杀灭肿瘤细胞,抑制肿瘤生长,延长患者mPFS和mOS,提高生存率有关。为验证125I粒子植入联合GS方案治疗中晚期胰腺癌的确切疗效,尚需要扩大样本容量行多中心对照研究。
总之,对于中晚期胰腺癌患者,CT引导下125I粒子植入联合GS化疗方案能显著缓解疼痛、改善患者生活质量、延长生存时间,是目前中晚期胰腺癌患者一种简单、安全、有效的治疗方案,值得进一步深入研究。
[1]Nakai Y,Isayama H,Sasaki T,et al.A multicentre randomised phaseⅡtrial of gemcitabine alone vs gemcitabine and S-1 combination therapy in advanced pancreatic cancer:GEMSAP study[J].Br J Cancer,2012,106:1934-1939.
[2]Ikeda M,Ioka T,Ito Y,et al.A multicenter phaseⅡtrial of S-1 with concurrent radiation therapy for locally advanced pancreatic cancer[J].Int J Radiat Oncol Biol Phys,2013,85:163-169.
[3]Wang H,Wang J,Jiang Y,et al.The The investigation of125I seed implantation as a salvage modality for unresectable pancreatic carcinoma[J].J Exp Clin Cancer Res,2013,32:106.
[4]吴普照,张跃伟.胰腺癌综合性介入治疗进展[J].介入放射学杂志,2014,23:452-455.
[5]Witkowski ER,Smith JK,Tseng JF.Outcomes following resection of pancreatic cancer[J].J Surg Oncol,2013,107:97-103.
[6]杨文魁,陈勇,王磊,等.CT引导下125I粒子植入联合GP方案治疗局部进展期胰腺癌[J].世界华人消化杂志,2014,22:1455-1459.
[7]彭晶晶,谭勇,谭艳,等.125I粒子植入治疗结肠直肠癌肝转移[J].介入放射学杂志,2012,21:773-776.
[8]Peng S,Yang QX,Zhang T,et al.Lobaplatin-TACE combined with radioactive125I seed implantation for treatment of primary hepatocellular carcinoma[J].Asian Pac J Cancer Prev,2014,15: 5155-5160.
[9]Zhang SC,Zheng YH,Yu PP,et al.The combined treatment of CT-guided percutaneous I-125 seed implantation and chemothe rapy for non-small-cell lung cancer[J].J Cancer Res Clin Oncol,2011,137:1813-1822.
[10]Iida T,Nakabayashi Y,Okui N,et al.Successful management of metachronouslivermetastasisafterpancreaticoduodectomy forpancreaticductalcarcinomausinghepatectomyand chemotherapy:a case report[J].Anticancer Res,2014,34:2417-2420.
[11]Song H,Han B,Park CK,et al.PhaseⅡtrial of gemcitabine and S-1 for patients with advanced pancreatic cancer[J].Cancer Chemother Pharmacol,2013,72:845-852.
CT-guided125I radioactive seed interstitial implantation combined with chemotherapy for advancedpancreatic carcinoma:analysis of therapeutic efficacy
LUN Jun-jie,ZHAO Jun-ling,SUN Jian-ye,HU Xiao-kun,YIN Hao-zhi.Department of Oncology,Changle County People's Hospital,Weifang,Shandong Province 262400,China
YIN Hao-zhi,E-mail:sdyhz@163.com
ObjectiveTo evaluate the efficacy and safety of CT-guided125I radioactive seed implantation combined with gemcitabine and Gio(gemcitabine and S-1,GS scheme)chemotherapy in treating advanced pancreatic carcinoma.MethodsSixty-eight patients with inoperable advanced pancreatic carcinoma were randomly divided into two groups.Patients in group A(n=38)were treated with CT-guided125I radioactive seed implantation combined with GS chemotherapy scheme,while patients in group B(n=30)received GS chemotherapy scheme only.The short-term effect,the median progression-free survival time,the median survival time and adverse reactions of the two groups were determined,and the results were compared between the two groups.ResultsThe objective response rate(ORR),disease control rate(DCR)and clinical benefit rate(CBR)of the group A were 57.9%,73.7%and 84.2%respectively,while those of group B were 26.7%,46.7%and 60.0%respectively.The differences between the two groups were statistically significant(P<0.05).In group A the median progression-free survival time and the median survival time were 8.00 months and 11.84 months respectively,which were strikingly higher than those in group B(5.63 months and 10.40 months respectively),the differences between the two groups were statistically significantly(P<0.05). No significant differences in gastrointestinal reactions,blood toxicity,liver toxicity and other adverse reactions existed between the two groups(P>0.05).ConclusionFor advanced pancreatic carcinoma,CT-guided125I radioactive seed implantation combined with GS program is a safe and effective treatment.(J Intervent Radiol,2015,24:494-497)
pancreatic carcinoma;125I seed;gemcitabine;Gio
R735.9
A
1008-794X(2015)-06-0494-04
2014-10-30)
(本文编辑:俞瑞纲)
10.3969/j.issn.1008-794X.2015.06.007
昌乐县科技发展计划项目(乐科字第201424号)
262400山东省昌乐县人民医院肿瘤科(伦俊杰、赵俊玲、孙建业、殷好治);青岛大学附属医院介入医学中心(胡效坤)
殷好治E-mail:sdyhz@163.com
