高效液相色谱法测定葡萄酒中苋菜红的不确定度评定
2015-10-25李小佳崔萌萌马联弟
马 康,李小佳,崔萌萌,马联弟
(1.中国计量科学研究院,北京 100029;2.北京科技大学化学与生物工程学院,北京 100083;3.北京化工大学化学理学院,北京 100029)
高效液相色谱法测定葡萄酒中苋菜红的不确定度评定
马 康1,李小佳2,崔萌萌3,马联弟1
(1.中国计量科学研究院,北京100029;2.北京科技大学化学与生物工程学院,北京100083;3.北京化工大学化学理学院,北京100029)
通过对高效液相色谱法测定葡萄酒中合成色素苋菜红质量浓度的全过程分析,确定了测定结果不确定度的来源。采用计量学不确定度传递模型,对引入的不确定度分量进行评定,确定了葡萄酒中苋菜红质量浓度标准不确定度由标准物质、标准溶液配制、标准曲线拟合、样品制备、测量重复性和回收率等6部分不确定度合成得到。2个不同质量浓度样品测定结果不确定度被评定,其相对扩展不确定度分别为2.6%和2.2%(k=2),由不确定度评价结果分析得到,样品重复性测定和标准溶液配制是测定结果不确定度的主要来源。
计量学;苋菜红;葡萄酒;高效液相色谱;不确定度
1 前 言
葡萄酒是由新鲜葡萄或葡萄汁经发酵而成的饮料,富含有机酸、糖类、黄酮类、酚类和原花青素等功能成分,适量饮用能预防多种疾病[1,2]。随着我国人民生活水平的提高,葡萄酒的消费量呈现了快速增长的趋势。为了保障葡萄酒的饮用安全,相关国家标准对葡萄酒中允许添加的食品添加剂种类和浓度作了明确规定,其中规定不允许添加合成着色剂[3~5],但一些不法生产者向葡萄酒中添加合成着色剂(苋菜红、胭脂红、柠檬黄、日落黄、亮蓝)的情况却时有发生。其中苋菜红是非法添加频率较高的合成着色剂[6]。为了保证葡萄酒的产品质量,防止假冒伪劣产品以次充好和保护大众健康,需要对葡萄酒中苋菜红等着色剂进行测量,为了保证测量结果的准确、可靠和可信,需要对测量结果的不确定度进行评价。
不确定度是与测量结果相关联的参数,表征合理地赋予被测量的分散性[7]。它是考察一种测量方法能力优劣的指征,是对检测数据进行客观真实的表述。近年来检验分析工作对测量结果的不确定度评定工作越来越重视,不确定度评价结果的可信性、可比性和可接受性的主要指标,同时各实验室及时总结与评定分析结果的不确定度,对实验室分析数据的汇总整合具有科学的评价意义[8,9]。本文针对高效液相色谱法测量其他着色剂组分可依此方法进行类似计算。
2 实验部分
2.1仪器与试剂
UFLC-20A液相色谱仪-二极管阵列检测器(UFLC-PDA,日本岛津公司)。苋菜红溶液标准物质(中国计量科学研究院);甲醇(色谱纯)、乙酸铵(优级纯)、柠檬酸(优级纯)购自百灵威公司;氨水和聚酰胺粉购自北京化学试剂公司。
2.2试验条件
色谱柱:ODS-C18,4.6 mm×250 mm×5 μm(日本GL Science公司);柱温:35℃;流量:1.0mL/ min;进样量:20 μL。
流动相:流动相A为甲醇;流动相B为0.10 mol/L乙酸铵水溶液。
梯度程序:0~6 min,90%A;6~12 min,(90% ~55%)A;12~13 min,(55%~90%)A;13~15 min,90%A。
检测器:二极管阵列波长190~700nm,苋菜红波长521nm。
2.3分析流程
准确称取葡萄酒5.0 g,柠檬酸水溶液补足约20mL,60℃聚酰胺粉吸附约1 h,然后用pH=4的柠檬酸水溶液、60∶40的甲醇-甲酸溶液、纯净水各洗3次,最后用乙醇-氨水-水溶液(7∶2∶1)洗脱目的物,旋蒸近干,纯水定容25mL,经0.45 μm的滤膜。葡萄酒中苋菜红组分测试流程见图1。

图1 葡萄酒样品中苋菜红组分液相色谱测试流程
2.4测定结果的数学模型
本文研究的基质为葡萄酒,采用高效液相色谱法测量葡萄酒中4种着色剂组分的质量浓度,计算式为

式中,X为样品中着色剂的质量浓度,mg/L;C为由标准曲线所得样液中着色剂的质量浓度,mg/L;V为样品最终定容体积,mL;m为最终定容体积所代表的样品量,g;R为方法的回收率,%。
3 测定不确定度来源
苋菜红组分质量浓度测量结果的不确定度由二部分组成:第一部分是通过测量数据的标准偏差、测量次数及所要求的置信水平按统计方法直接求得(A类不确定度);第二部分是通过对测量影响参数和影响函数的分析,估计出其大小,同时考虑样品不均匀性和有效期内的变动性等其它因素所引起的不确定度(B类不确定度)。对式(1)做全微分并除以X,则得

因此,不确定度的来源因素包括:标准物质、工作标准溶液配制、最小二乘法拟合标准曲线、回收率、样品制备(天平、容量和温度),分析过程引入的不确定度通过加标回收率估计,见图2。
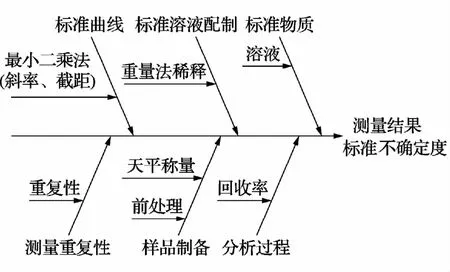
图2 葡萄酒中苋菜红测定不确定度的来源
4 结果与讨论
4.1不确定度分量评定
4.1.1标准物质引入的不确定度
苋菜红溶液标准物质GBW(E)100 002 a,特性量值500 μg/mL,相对扩展不确定度1%(k=2),则标准物质的不确定度为

4.1.2工作标准溶液配制引入的不确定度
工作标准溶液至少需要配制5个质量浓度,用上述的苋菜红溶液标准物质进行逐级得到,质量浓度分别为5 μg/mL、10 μg/mL、25 μg/mL、50 μg/mL 和100 μg/mL的工作标准溶液。稀释过程的数学模型为

其引入的不确定度的计算式为

式中,Ci为稀释得到苋菜红工作标准溶液质量浓度,μg/mL;C0为苋菜红溶液标准物质质量浓度,μg/mL;V0为移取标准溶液的体积,mL;Vi为苋菜红工作标准溶液定容体积,mL。
以50 μg/mL的工作标准溶液为例说明。移取体积V0引入的不确定度主要由移液器的重复性、校准规范[12]中的最大允差和移取溶液的温度差引入的。采用1mL 3次水充满移液器,用0.1mg的天平连续称量6次(1.0001g;1.0015g;1.0010g;0.9997 g;1.0008 g;0.9995 g),称量结果的6次测量的标准偏差为移液器的重复性0.00079mL;根据JJG646—2006中1mL移液器的最大允差为0.008mL,取三角分布,此项引入的不确定度为0.008/=0.0033mL;工作标准溶液配制温度与校准时温度不同,结合实验室的温度设置要求,温差不超过4℃,水体积膨胀系数为0.000 21 L/℃,温度引入体积变化为0.00021×0.001×4×1 000mL=0.000 84mL,假定温度变化为矩形分布,则标准不确定度为0.000 84mL/=0.00049mL。

容量瓶定容体积Vi不确定度来源:(1)容量瓶校准对体积影响;(2)温度对体积影响;(3)容量瓶至刻度线重复性对体积影响。合格的10mL容量瓶(A级)最大允差为±0.02mL[13]。假定为三角形分布,由容量瓶校准对体积影响引入的标准不确定度为0.02mL/=0.008 2mL;实验温控在20℃±5℃,又水膨胀系数0.00021L/℃,因此产生的体积变化为±(10×5×0.000 21)mL=±0.011mL,假定温度变化为矩形分布,则由温度对体积影响引入的标准不确定度为0.011mL/=0.006 4mL;通过多次充满10mL容量瓶至刻度并称量的实验,得出由充满容量瓶至刻度线重复性对体积影响引入的标准偏差为0.02mL。


4.1.3拟合标准曲线引入的不确定度
为了校准液相色谱仪,配制苋菜红系列标准工作溶液进行HPLC-DAD测定,以建立苋菜红组分校正曲线,经线性回归得到各自的线性方程,见表1。表中,A为峰面积;X为样品的质量浓度;R为线性相关系数;s为标准溶液峰面积残差的标准偏差;Sxx为标准溶液质量浓度的残差的平方和;Sa斜率标准偏差;Sb为截距标准偏差。
配制系列标准溶液涉及移取1mL、2mL和10mL的容量瓶的苋菜红溶液标准物质,用三次蒸馏水分别定容至10mL中,分别得到5mg/L、10mg/L、20mg/L、50 mg/L和100mg/L的工作标准溶液。计算5个工作标准溶液的引入的总不确定度为

表1 苋菜红组分的标准系列线性方程
葡萄酒的某个待测样品定容溶液进行了3次测定,由直线方程求得平均浓度,则X的标准不确定度为

由上述所得各参数,待测样品在标准曲线范围内,计算2个不同质量浓度样品在标准曲线引入的相对标准不确定度具体见表1,分别为0.24%和0.13%。
4.1.4样品制备过程引入的不确定度
样品制备的不确定度来源:(1)天平称量引入的不确定度;(2)样品定容体积引入的不确定度。
天平称量不确定度来源包括:天平称量最大允许误差;天平称量变动性;浮力影响。葡萄酒样品称量使用0.01 mg分度的分析天平,天平的变动性、检定误差等估计为0.05 mg,天平称量变动性及浮力影响(在常规状态下称重,此项可忽略)。纯品称重约5g,按矩形分布相对不确定度=(Δm/m)/= (0.05 mg/5 000 mg)/=0.002 9%。
定容体积不确定度来源包括:容量瓶校准对体积影响;温度对体积影响;容量瓶至刻度线重复性对体积影响。溶液配制定容体积为50mL,检定合格的50mL容量瓶最大允差为±0.02mL[13,14]。假定为三角形分布,此项标准不确定度为0.02mL/=0.008 2mL;本方法根据加入的3次水质量计算溶液体积,所以需要考虑温度对3次水体积的影响而引入的不确定度。实验温度控制在(25±5)℃,纯水膨胀系数为0.000 21 L/℃,因此产生的体积变化为(0.05 L×±5×0.000 21 L)× 1 000=±0.053mL,假定温度变化为矩形分布,则标准不确定度为0.053mL/=0.031mL;通过多次充满50mL容量瓶至刻度并称量的实验,得出标准偏差为0.02mL。综上所述,定容体积引入的相对合成不确定度为0.080%。
4.1.5样品测量重复性引入的不确定度
在不确定度评定过程中,A类不确定度主要体现为样品的测量重复性,对样品进行7次重复试验,用相对标准偏差来表示样品测量重复性引入的不确定度。葡萄酒中苋菜红质量浓度测定结果见表2。
4.1.6回收率引入的不确定度
前处理过程对样品回收率的影响所产生的不确定度,具体表现为7次测量样品回收率平均值的标准偏差S(ρRec)[15],基体加标回收试验中样品溶液各组分浓度均低于方法的报出限,其标准不确定度为


当t值大于或等于双边临界值t(95%,6)=2.45时,则与1有显著性差异,说明fR需要被使用以修正结果;若t值小于t(95%,6),则fR不需要使用。葡萄酒样品中苋菜红组分显著性差异结果见表2。根据t值得到苋菜红组分均无显著性差异,不需要修正测试结果。

表2 葡萄酒中苋菜红质量浓度与回收率测定结果
4.2合成标准不确定度
葡萄酒中苋菜红测量结果的不确定度来源很多,除了上述提及的不确定度分量,还有温度效应、玻璃膨胀系数等因素。由于这些分量引入的不确定度相对较小,本文中忽略不计。
根据上述分量,计算得到合成标准不确定度为

相对扩展不确定度为

两个样品质量浓度的相对扩展不确定度分别为2.6%和2.2%(k=2)。其中样品重复性测定和标准溶液配制是测定结果不确定度的重要来源。
5 结论
通过对葡萄酒样品中苋菜红组分测定过程的分析,测定结果的不确定度主要来源于标准物质、标准溶液配制、标准曲线拟合、样品制备、测量重复性和回收率6部分。本文对葡萄酒样品中苋菜红组分测定过程各步骤引入不确定度的采集和表述,可为胭脂红、山梨酸、安赛蜜等其它食品添加剂测量结果扩展不确定度计算提供借鉴。
[1]Souquet J M,Labarbe B,Guerneve C L,et al.Phenolic composition of grape stems[J].J Agric Food Chem,2000,48(4):1076-1080.
[2]Ryan J M,Revilla E.Anthocyanin composition of cabernet sauvignon and tempranillo grapes at different stages of ripening[J].J Agric Food Chem,2003,51 (11):3372-3378.
[3]国家质量监督检验检疫总局.GB 15037—2006,葡萄酒标准[S].
[4]中华人民共和国卫生部.GB 2760—2011,食品添加剂使用标准[S].
[5]中华人民共和国卫生部.GB 2758—2012,发酵酒及其配制酒卫生标准[S].
[6]谢娅黎,陈欣欣,冯勇,等.市售红葡萄酒中甜味剂以及人工合成色素使用情况分析[J].现代食品科技,2009,35(12):1482.
[7]Ma K,Wang H F,Zhao M,et al.Purity determination and uncertaintyevaluationoftheophyllinebymass balance method,high performance liquid chromatography and differential scanning calorimetry[J].Analytica Chimica Acta,2009,650(2):227-233.
[8]马康,赵敏,王海峰,等.茶碱标准物质的研制与定值[J].分析测试学报,2011,30(4):418-424.
[9]冯静,王海娇,何超君,等.高效液相色谱法测定地下水中苯并(a)芘的不确定度评定[J].岩矿测试,2011,30(5):617-622.
[10]国家质量技术监督局.JJG10 59.1—2011,测量不确定度评定与表示[S].
[11]ISO Guide35 2006Reference Materials-general and Statistical Principles for Certification[S].
[12]国家质量监督检验检疫总局.JJG 646—2006,移液器检定规程[S].
[13]国家质量监督检验检疫总局.JJG 196—2006,常用玻璃量器检定规程[S].
[14]马康,杨亚楠,刑金京,等.诱惑红溶液标准物质的研制及不确定度评定[J].分析测试学报,2012,31 (3):296-301.
[15]李松,饶竹.气相色谱法测定地下水中六六六结果的不确定度评定[J].岩矿测试,2008,27(4):295-298.
Uncertainty Evaluation for the Determination of Amaranthus Red in Wine Samples by High Performance Liquid Chromatography
MA Kang1,LI Xiao-Jia2,CUI Meng-meng3,MA Lian-di1
(1.National Institute of Metrology,Beijing 100029,China;2.School of Chemistry and Biological,Beijing University of Science and Technology,Beijing 100083,China;3.College of Chemistry,Beijing University of Chemical Technology,Beijing 100029,China)
Sources of measurement for amaranthus red in wine samples by high performance liquid chromatography are determined through studying the whole process of analytical results.The uncertainties of analytical result are evaluated by a metrological model of uncertainty.The standard uncertainty for analytical results for amaranthus red in wine samples is mainly consisted of uncertainty of solution reference material of amaranthus red,preparation of work standard solution,calibration curve using the least squares method,preparation for real wine sample,measured repeatability,method recovery and so on.Relative expanded uncertainties for two real wine sample with different content are evaluated and they are 2.6% and 2.2%(k=2).Evaluation of analytical results of two samples with different content indicated that main resource of uncertainty are measured repeatability and calibration curve.
Metrology;Amaranthus red;Wine;HPLC;Uncertainty
TB99
A
1000-1158(2015)01-0102-05
10.3969/j.issn.1000-1158.2015.01.22
2013-05-04;
2014-10-28
科技部公益性行业科研专项(2012104001);科技基础性工作专项(2008FY130200);中国计量科学研究院基础科研业务费(21-AKY1216)
马康(1973-),男,陕西宝鸡人,中国计量科学研究院副研究员,研究方向为食品添加剂的检测。makang@nim.ac.cn
