液相色谱—串联质谱法测定人血浆中氯吡格雷酸的浓度及意义
2015-10-21谭忆
谭忆
摘要:目的:探讨利用高效液相色谱-质谱联用法进行人血浆中氯吡格雷酸浓度测定的临床意义。方法:对血浆样品进行测定,首先在样品中加入内标物质美利曲辛,然后利用乙腈沉淀蛋白进行提取。并与健康男性受试者口服硫酸氢氯吡格雷受试制剂的血药浓度进行生物等效性比较。结果:利用高效液相色谱-质谱联用法测定人血浆中氯吡格雷酸,其回收率为97.2%-103.9%。结论:利用高效液相色谱-质谱联用法对人血浆中的吡格雷酸的浓度进行测定,具有较高的灵敏度,适用于临床上氯吡格雷片的药代动力学研究。
关键词: 氯吡格雷;高效液相色谱-质谱联用法;药代动力学
氯吡格雷是一种常用的抗血小板凝集及抗血栓药物,其主要成分为噻吩并吡嗪类衍生物。这是一种经过口服可在人体内快速吸收的药物,代谢速度较快,其在人体内的代谢产物主要是氯吡格雷酸[1]。氯吡格雷原型在人体内的浓度非常低,据相关文献报道,实验者在口服硫酸氢氯吡格雷75 mg 后对体内氯吡格雷酸的浓度进行测定,其在人体内地最大浓度(Cmax)仅为1010g[2]。国内外关于氯吡格雷血药浓度测定的相关文献较少,本文为了研究液相色谱-串联质谱法对人血浆中氯吡格雷酸的浓度测定的意义,具体研究如下:
1 仪器与试剂
本次试验选用的质谱仪为Agilent6410 型三重四极杆质谱仪,该类质谱仪配套有电喷雾离子源,另外选用的色谱仪为Agilent1200 型高效液相色谱仪。后期数据分析选用的软件为美国安捷伦公司生产的Agilent Mass Hunter Quatitative Analysis 。另外还有相关的分析天平(万分之一、FA2204N)、高速台式冷冻离心机(Happy-TL16)以及MTN-2800W 型氮吹浓缩仪[3]。(试剂:硫酸氢氯吡格雷对照品:USP LOT G1K326乙腈、醋酸铵:Dikma Technology(色谱纯);甲醇:天津市科密欧化学仪器试剂有限公司(色谱纯)[4]。
2 方法与结果
2.1 色谱/质谱条件:色谱柱为( 4. 6 mm × 100 mm,2. 7 μm、Dikma),流动相为浓度0.4%甲酸。甲酸与乙腈的比例为30比70,色谱柱的温度为30℃。进样量设定为50 μl,所采用的离子源为电喷离子源。干燥气流速度设定为12. 0 L /min,温度设定为350 ℃,雾化器压力为55 psig; 四极杆温度为100 ℃; 毛细管电压为4. 0 KV。
2.2溶液配制
对照品溶液:精密称取硫酸氢氯吡格雷13.54mg(换算成氯吡格雷为10.25mg),于100ml的量瓶中溶解,定容,摇匀,备用,甲醇最終制成浓度为102.5 μg/ml的氯吡格雷储备液。先后精密移取一定量的氯吡格雷储备液进行稀释,配制成一系不同浓度溶液,浓度先后为50. 4、151. 2、201. 6、1 008. 0、3 024. 0、4 032. 0、10 080. 0、30 240. 0、80 640. 0、1 00 800. 0 pg /ml。精密称取地西泮对照品10. 04 mg(相当与10.03mg的地西泮)置于100ml的量瓶中进行溶解,定容,充分混匀,备用。此为内标溶液。最终浓度为100. 3 μg /ml 的地西泮,需要进行低温保存,保存温度为4 ℃。精密移取1.0ml的地西泮内标储备液,置于50ml的量瓶中,定容,摇匀,此次选取的溶解液为甲醇–水( 1∶ 1) 溶液,充分混匀,此为地西泮内标溶液Ⅱ,浓度为2. 0 060 μg /ml。精密量取上述配比所得内标溶液Ⅱ2. 5 ml,置于100ml量瓶中,定容,摇匀,进行第三次稀释,所选取的稀释液仍旧为甲醇–水( 1∶ 1) 溶液,最终得到浓度50. 150 ng /ml 的内标溶液。
2.3血浆样品的处理
对于采取的血浆样品需要进行处理,首先需要量取空白血浆500μl,要进行精密量取。将空白血浆进行离心处理,血浆置于10ml的离心管,分别加入甲醇- 水( 1∶ 1) 溶液、内标溶液、50 mmol /L 醋酸铵溶液,剂量分别为50μl、50μl以及500μl。将以上混合液进行涡旋混合,再加入3ml的甲基叔丁基醚,进行充分震荡,时间8min左右,然后在5℃下进行离心,离心速度为1000转/分钟,时间6min。将有机层治愈离心管中,35℃水浴中进行吹干,大约留取200 μl 流动相溶液复溶,进行涡旋混合,精密称取50 μl 样本分析[5]。
2.4专属性试验:实验显示氯吡格雷和内标的保留时间分别为3. 7 和2. 7 min,说明血浆中的内源性物质不干扰氯吡格雷的测定。进行液相色谱-串联质谱法测定人血浆中氯吡格雷酸,其回收率为97.2%-103.9%。
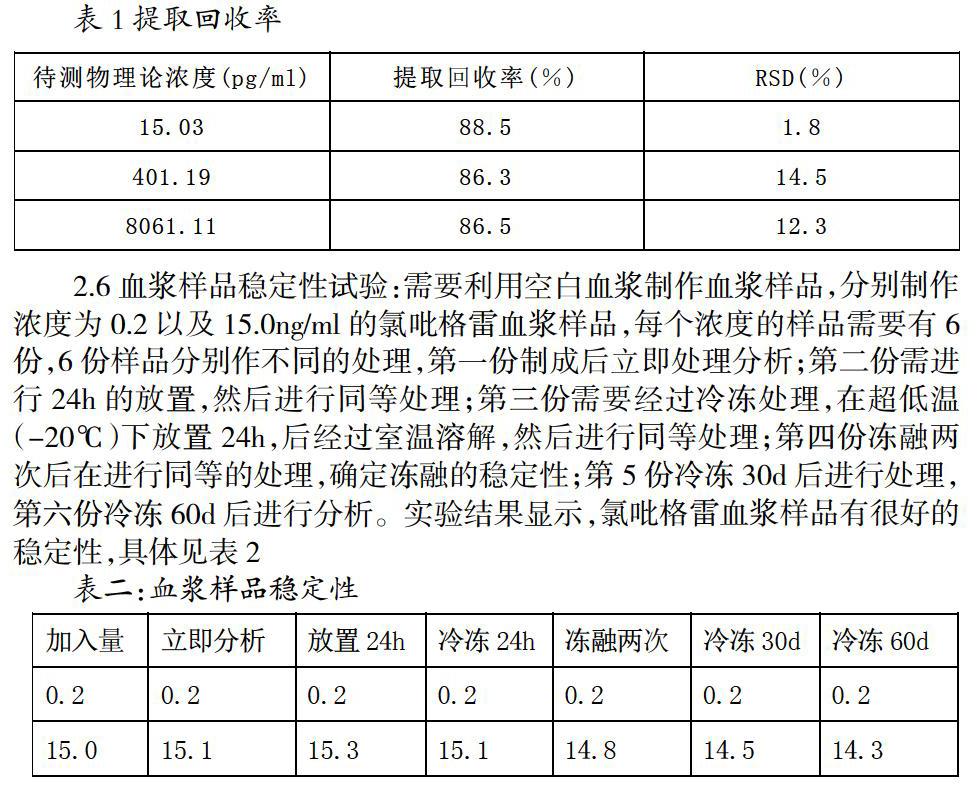
2.5提取回收率实验:需要精密量取氯吡格雷质控标准溶液以及内标溶液各50μl ,分别加入100μl流动相,进行充分混合,在混合均匀后提取50ul样本作相应研究,每个浓度有6份样本,得到未经提取的低、中、高3 个浓度的色谱峰面积( 6 次测定的平均值) ,计算每一浓度提取后样品( 即精密度及准确度试验样品) 与未经提取样品的色谱峰面积之比,得到的待测物和内标的提取回收率见表1,本方法待测物和内标的回收率均达到50% 以上,RSD小于15%,待测物低、中、高三个浓度的回收率相接近,内标回收率稳定,结果见表1。
表1提取回收率
2.6血浆样品稳定性试验:需要利用空白血浆制作血浆样品,分别制作浓度为0.2以及15.0ng/ml的氯吡格雷血浆样品,每个浓度的样品需要有6份,6份样品分别作不同的处理,第一份制成后立即处理分析;第二份需进行24h的放置,然后进行同等处理;第三份需要经过冷冻处理,在超低温(-20℃)下放置24h,后经过室温溶解,然后进行同等处理;第四份冻融两次后在进行同等的处理,确定冻融的稳定性;第5份冷冻30d后进行处理,第六份冷冻60d后进行分析。实验结果显示,氯吡格雷血浆样品有很好的稳定性,具体见表2
表二:血浆样品稳定性
3讨论
本文主要探讨利用液相色谱-串联质谱法进行人血浆中氯吡格雷酸浓度测定的临床意义。液相色谱-串联质谱法,以及乙醚提取处理法进行氯吡格雷酸浓度测定具有较高的灵敏度,其灵敏度为10 pg /ml。本次试验在此基础上,进行了实验条件的优化,选取了新的提取溶剂--甲基叔丁基醚。这种溶剂可以在很大程度上减少实验中的基质效应[6],促进了实验灵敏度的提升,是的灵敏度高达15pg /ml。本次试验所选取的测定方法可以有效的对硫酸氢氯吡格雷的药代动力学评价或生物等效性评价。
在实验过程中,本文对多个流动相的配比情况进行了观察与分析,分析中的乙腈比例会对实验的结果产生较大影响,会影响氯吡格雷的保留时间。乙腈的比例高低与氯吡格雷的保留时间成反比,当乙腈浓度的降低,氯吡格雷的保留时间会延长[7]。试验中选取0. 4%甲酸–乙腈( 40 ∶ 60) 作为流动相进行分析,在此条件下进行观察,氯吡格雷的保留时间较长,并且峰形较宽。实验如果选取0. 4% 甲酸- 乙腈( 25 ∶ 75) 作为流动相时,效果欠佳,因此流动相的选择最终确定为0. 4%甲酸水溶液-乙腈( 30 ∶ 70) 不但使氯吡格雷和内标物质得到很好的分离,同时也缩短了分析时间,有利于生物样品的分析。
综上所述:利用液相色谱-串联质谱法对人血浆中的吡格雷酸的浓度进行测定,具有较高的靈敏度,是临床上适用的氯吡格雷片的临床药代动力学研究的方法。
参考文献:
[1]陈敏纯,鹿成韬,贾艳艳,宋颖,李雪晴,杨静,丁莉坤,文爱东.液相色谱-串联质谱法测定人血浆氯吡格雷浓度及其生物等效性评价[J].中国医院药学杂志,2012,05(06):421-424.
[2]陈敏纯,李雪晴,贾艳艳,鹿成韬,宋颖,杨静,丁莉坤,周伦,冯智军,宋薇,文爱东.LC-MS/MS法测定人血浆氯吡格雷酸浓度及其生物等效性评价[J].中国新药杂志,2012,22(24):2924-2927+2935.
[3]商丹丹,邸欣,王鑫,张慧霞,封美慧,刘有平.液相色谱-串联质谱法同时测定人血浆中氯沙坦及其活性代谢物氯沙坦酸的浓度[J].中国新药与临床杂志,2013,11(12):975-980.
[4]慕杨娜,宋冬梅,于珊珊.液相色谱-串联质谱法测定人血浆中的氯吡格雷[J].沈阳医学院学报,2014,03(01):32-34+36.
[5]刘帅兵,王子腾,丁肖梁,许青青,郭哲宁,缪丽燕.液相色谱-质谱联用法测定人血浆氯吡格雷及其代谢产物药物浓度及应用[J].药物分析杂志,2015,12(01):56-63.
[6]高荧,乔亚楠,陆宇婷,宋敏,杭太俊,马鹏程.液相色谱-串联质谱法同时测定人血浆中氯沙坦、5-羧酸氯沙坦和氢氯噻嗪的浓度及药动学[J].中国新药与临床杂志,2014,15(12):884-889.
[7]张丹,王国才,黄建权,郑天雷,王涛,杨漫,王振龙,刘会臣.液相色谱-串联质谱法测定人血浆中二甲双胍的浓度[J].药物分析杂志,2011,09(02):317-321.
