液固压缩技术增溶制剂中的葛根总黄酮
2015-10-18李小芳罗丽佳冉茂莲李培培
罗 丹, 李小芳, 余 琳, 罗丽佳, 冉茂莲, 李 平, 李培培
(成都中医药大学药学院中药材标准化教育部重点实验室中药资源系统研究与开发利用省部共建国家重点实验室培育基地,四川 成都 610075)
液固压缩技术增溶制剂中的葛根总黄酮
罗 丹, 李小芳*, 余 琳, 罗丽佳, 冉茂莲, 李 平, 李培培
(成都中医药大学药学院中药材标准化教育部重点实验室中药资源系统研究与开发利用省部共建国家重点实验室培育基地,四川成都610075)
目的 运用液固压缩技术增加葛根总黄酮的溶出度,优选最佳处方。方法 筛选液体赋形剂和载体,制备药液比为1∶4,R值为20的葛根总黄酮液固压缩片,将其与原料药和市售片的溶出度进行比较,通过差示扫描量热分析考察药物的晶型转化。结果 液固压缩片较原料药和市售片的溶出度大幅度提高。优选的最佳处方LS-3,以吐温-80做液体赋形剂,微晶纤维素做载体,溶出50%时,仅需42.6s。差示扫描量热分析表明液固压缩片中主药的特征峰消失。结论 液固压缩技术可改善葛根总黄酮的溶出,快速释药,并将药物从结晶状态转化为分子或无定形状态。
液固压缩技术;葛根总黄酮;溶出度;差示扫描量热分析
液固压缩技术(Liquisolid technique)又名溶液粉末化技术,将难溶性药物悬浮或溶解在非挥发性液体赋形剂中,再与适宜的载体和涂层材料混合均匀转变为具有非黏性、良好流动性和可压性的干燥粉末[1]。目前,液固压缩技术已运用于法莫替丁、厄贝沙坦[2]、格列吡嗪[3]等西药,对α-细辛脑[4]、熊果酸[5]等中药难溶性有效成分液固压缩片的研究也相继有文献报道。
葛根总黄酮为葛根的主要成分,包括葛根素、羟基葛根素、甲氧基葛根素、大豆苷等,主要用于治疗心脑血管类疾病,如高血压、高血脂、偏头痛、冠心病、心肌梗塞、心绞痛、视网膜动脉阻塞、视网膜静脉阻塞和突发性耳聋等症[6]。然而,葛根总黄酮的主要成分葛根素的水溶性差,限制了其口服吸收,生物利用度低[7]。本实验拟制备葛根总黄酮液固压缩片,增加葛根总黄酮的溶出度,并探讨其增溶速释机制。
1 仪器与试药
1.1仪器 BP61型十万分之一电子天平(德国Satorius公司);DP-I型单冲压片机(上海中药机械厂);ZRS-8G智能溶出试验仪(天大天发科技有限公司),UV-6000型紫外可见分光光度计(上海美谱达仪器有限公司);SB-5200DT型超声仪(功率200W,工作频率40 kHz;宁波新芝生物科技股份有限公司);DSC差示扫描量热仪(北京恒久科学仪器厂)等。
1.2试药 葛根总黄酮(总黄酮纯度80.85%,西安飞达生物技术有限公司,批号FD20130912);葛根素对照品(纯度为98.0%,中国食品药品检定研究院,批号110752-200912);1,2-丙二醇(PG,成都市科龙化工试剂厂);聚乙二醇400(PEG400,成都市科龙化工试剂厂);吐温-80(成都市科龙化工试剂厂);微晶纤维素PH-101(MCC,成都市科龙化工试剂厂);乳糖(分析纯,成都市科龙化工试剂厂);可溶性淀粉(分析纯,成都市科龙化工试剂厂);微粉硅胶®200(成都市科龙化工试剂厂);羧甲基淀粉钠(成都市科龙化工试剂厂);蒸馏水等。
2 方法与结果
2.1液固压缩片的制备
2.1.1液固压缩系统的数学模型[8]通过R值和药液比两个参数可计算出液固压缩系统最佳的载体和涂层材料的用量,载体(Q)和涂层材料(q)能吸收一定的液体赋形剂,将载体材料(Q)吸收液体赋形剂(W)的最大量定义为液体负载因子(Lf)。载体材料和涂层材料的质量比称为R值,即:

φCA为载体对液体赋形剂的最大保留势能,φCO为涂层材料对液体赋形剂的最大保留势能,Lf又可由以下公式表示

φCA和φCO值为辅料的固有性质,本实验取PG、PEG400和吐温-80的φCA、φCO值分别为0.16、3.31、0.005、3.26、0.0741、1.958[9-10]。
2.1.2液固压缩片的处方 本实验取葛根总黄酮10 mg,液体赋形剂40 mg,微粉硅胶®200作为涂层材料,选择药液比为1∶4,R值为20,筛选不同的液体赋形剂和载体。根据公式(1~3)分别计算出各个处方的Lf、Q、q值及崩解剂的用量及片质量,结果见表1。
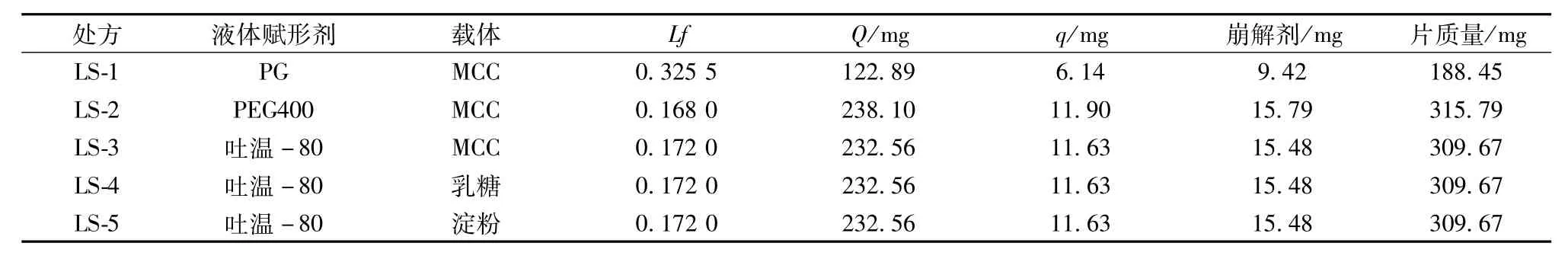
表1 葛根总黄酮液固压缩片的处方参数值Tab.1 Excipients in liquisolid tabletsw ith total flavone from Puerariae Radix
2.1.3液固压缩片的制备方法[11]精密称取表1中的处方量,将葛根总黄酮于60℃下磁力搅拌加入液体赋形剂中,待药物完全溶解在液体赋形剂中再连续加入载体,研钵研匀转化为湿颗粒,再加入微粉硅胶®200,研匀得干燥粉末,最后加入5%的羧甲基淀粉钠混匀,于干燥器中放置1 d,以单冲压片机,直接粉末压片,硬度控制在30~40 N。
2.2压缩前评价[12-13]粉末的流动性和可压性是影响液固粉末系统压片的重要因素,可通过休止角、卡尔指数和豪斯纳比对压缩前的粉末流动性进行评估。休止角体现粉末粒子间的摩擦和内聚的特性,而卡尔指数和豪斯纳比涉及粉末粒子间的摩擦,一般,休止角小于40°,卡尔指数小于25%,豪斯纳比小于1.25,说明粉末流动性好。
2.2.1休止角的测定 采用固定漏斗法,将漏斗固定于水平放置的绘图纸上方一定距离,漏斗下口距绘图纸高度为H,均速将粉末倒入漏斗中,直到漏斗下形成的圆锥体尖端接触到漏斗下口为止,测定圆锥体的直径2R。计算休止角θ,每个样品测3次,取平均值。
2.2.2卡尔指数和豪斯纳比的测定 分别测定每个处方粉末的松装密度ρa和振实密度ρp,根据公式(4)、(5)
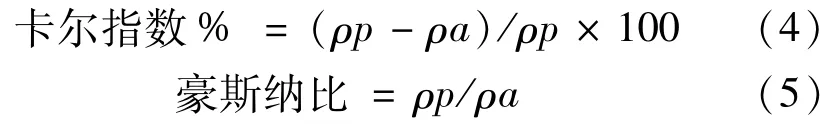
分别计算其卡尔指数和豪斯纳比,每个样品测3次,取平均值,结果见表2。
表2 葛根总黄酮液固粉末系统的流动性(±s)Tab.2 Fluidity of total flavone from Puerariae Radix liquisolid tablets(±s)
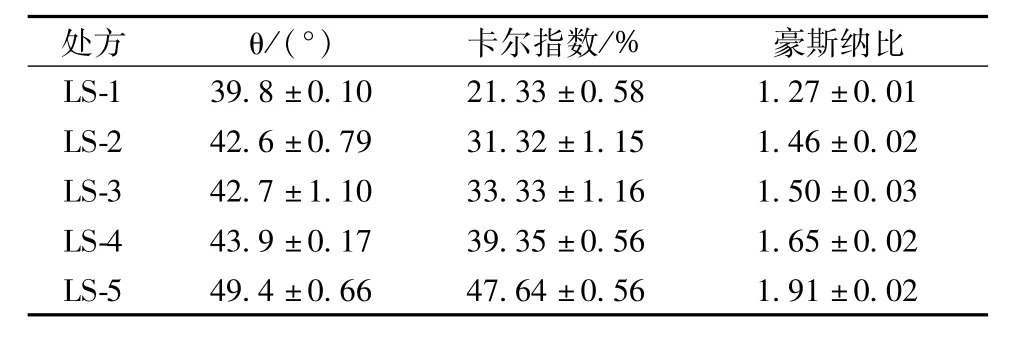
表2 葛根总黄酮液固粉末系统的流动性(±s)Tab.2 Fluidity of total flavone from Puerariae Radix liquisolid tablets(±s)
处方θ/(°)卡尔指数/%豪斯纳比LS-1 39.8±0.10 21.33±0.58 1.27±0.01 LS-2 42.6±0.79 31.32±1.15 1.46±0.02 LS-3 42.7±1.10 33.33±1.16 1.50±0.03 LS-4 43.9±0.17 39.35±0.56 1.65±0.02 LS-5 49.4±0.66 47.64±0.56 1.91±0.02
实验结果表明:LS-1、LS-2、LS-3相对于LS-4、LS-5的休止角、卡尔指数和豪斯纳比较小,为了得到流动性、可压性好的粉末,故选择MCC作载体。
2.3压缩后评价[5]
2.3.1片质量差异 根据《中国药典》2010年版附录ⅠD片剂[14]的方法进行测定。取各片剂20片,分别精密称定每片的质量。每片质量与标示片质量比较,标示片质量0.3 g以下的重量差异限度为±7.5%,0.3g以上限度为±5%,结果见表3。
2.3.2崩解时限 根据《中国药典》2010年版一部附录ⅫA崩解时限检查法[14]中的片剂方法进行测定。温度37℃,取药片6片分别置于吊篮的玻璃管内,启动崩解进行测定。结果见表3。
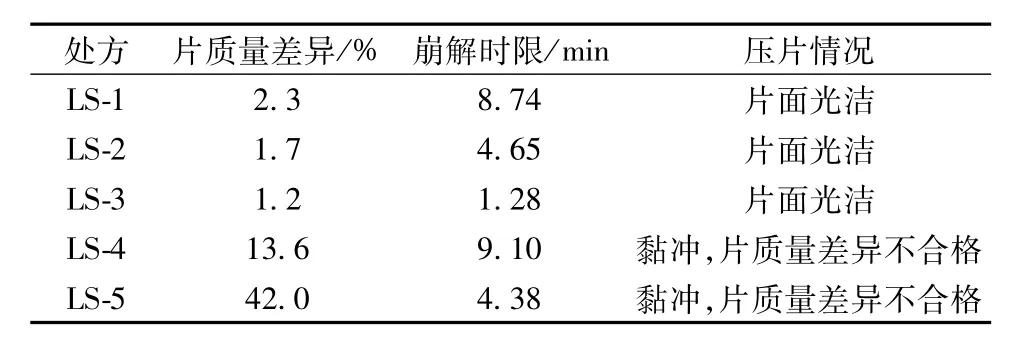
表3 葛根总黄酮液固压缩片的质量评价Tab.3 Quality evaluation on liquisolid tablets w ith total flavone from Puerariae Radix
实验结果表明:LS-4、LS-5黏冲,不利于压片,片质量差异不合格,而LS-1、LS-2、LS-3片质量差异合格,片面光洁,故选择MCC做载体。
2.4溶出度测定[15]
2.4.1对照品溶液的制备 取葛根素对照品适量,精密称定,加蒸馏水超声充分溶解,定容于50 mL量瓶中,制成每1 mL含0.245 4 mg葛根素的对照品溶液。
2.4.2标准曲线的制备 分别精密量取葛根素对照品溶液0.2、0.25、0.3、0.35、0.4、0.45、0.5 mL,置10 mL量瓶中,加蒸馏水定容,充分摇匀,在250 nm波长处测吸光度。以葛根素质量浓度(ρ)为横坐标,吸光度(A)为纵坐标绘制标准曲线,得线性方程A=0.075 4ρ-0.008 2,r=0.999 5。结果表明,葛根素在4.908~12.27 μg/mL内呈良好的线性关系。
2.4.3溶出度测定方法 采用《中国药典》2010年版二部附录ⅩC溶出度测定法[14]中的浆法对LS-1、LS-2、LS-3、原料药和市售片(愈风宁心片)的溶出度进行测定。转速为100 r/min,温度为37℃,以900 mL超声脱气蒸馏水作溶出介质。取片剂各6片投入溶出杯内,分别于1、3、5、10、20、30、60 min取样10 mL,经孔径0.8μm滤膜过滤,取续滤液,得样品溶液。同时补充等体积等温度的新鲜介质,操作在30 s内完成。根据“2.4.2”项下方法测定,结果见图1。将液固压缩片、原料药及市售片的溶出时间数据分别进行威布尔函数拟合,计算溶出参数Td和T50,结果见表4。
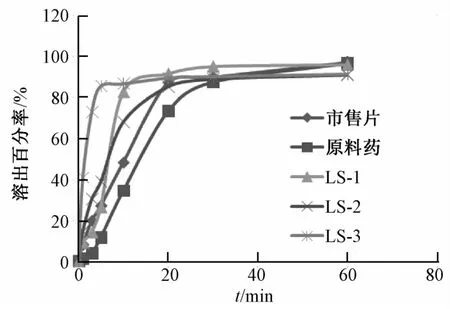
图1 药物的溶出曲线Fig.1 Drug's dissolution curve

表4 体外溶出W eibull函数拟合参数Tab.4 W eibu ll fitting of in vitro dissolution
实验结果表明,葛根总黄酮液固压缩片的溶出度明显优于原料药和市售片,其中液固压缩片LS-3的溶出度明显优于LS-1、LS-2,故选择吐温-80作液体赋形剂。
2.5差式扫描量热分析(DSC)[16]分别取葛根素、液固粉末系统、物理混合物和液固空白辅料为样品,以10℃/min的扫描速率,在扫描范围25~350℃温度内扫描,进样量分别为葛根素5.000 mg,液固粉末系统3.100 mg,物理混合物5.100 mg,液固空白辅料5.2 mg,结果见图2。
由图2A可知葛根素分别在209.2℃和230.5℃有两个尖锐的特征峰,表明葛根素以结晶的状态存在。图2B中在209.2℃和230.5℃处无特征峰,表明液固空白辅料对主药无干扰。图2C中受辅料量的影响,葛根素峰有所下降,但仍在209.2℃和230.5℃处有其特征峰,说明药物仍以结晶的状态存在。由图2D和图2A可知,在液固粉末系统中葛根素的特征峰消失,说明药物在液固压缩片中以分子或者无定形状态存在。
3 讨论
液固压缩技术是一种有前途的、能提高难溶性药物溶出度的新技术,可很好地提高葛根总黄酮的溶出度。优选的LS-3液固压缩片中,葛根总黄酮快速释放,溶出50%时,液固压缩片仅需42.6 s,而原料药和市售片需9.4 min和15.89 min。
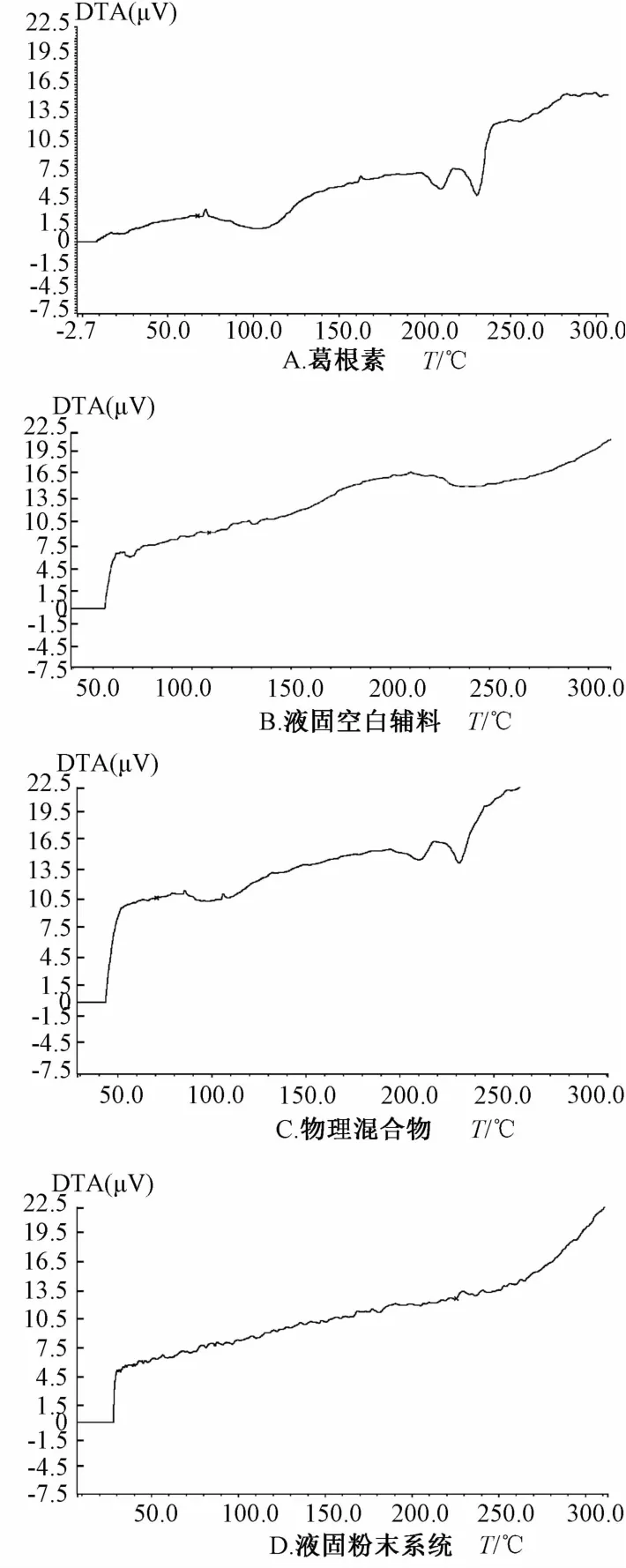
图2 差示扫描量热分析曲线Fig.2 Curves from differential scanning calorimeter
液固压缩技术增溶的机制可能是液体赋形剂增加了药物的溶解度。液固压缩片中所选的液体赋形剂均为良好的助溶剂,其中葛根总黄酮在吐温-80中的溶解度最大[17],能很好地降低表面张力,提高药物粒子的润湿性,使水分子借助毛细管作用深入到片剂的内部,使其快速崩解。
液固压缩技术增溶的机制也可能是载体和涂层材料增加了药物溶出有效表面积。由DSC图可知液固压缩技术能使药物从结晶状态转变为分子或者无定形状态。因为载体和涂层材料为多孔材料,具有很强的吸附性,能充分吸附呈分子分散于吐温-80中的药物。当液固压缩片崩解时,增大了溶出有效表面积,使得药物快速释放。
液固压缩技术增溶的机制还有可能是增加了药物粒子润湿性。由崩解时限结果可知,LS-3的崩解仅需要1.28 min,这可能与吐温-80改善药物粒子的润湿性有关。
[1] 李丽然,王成港,郭 红.液固压缩技术在药剂学中的应用[J].现代药物与临床床,2012,27(3):283-286.
[2] Rikisha B,Anuradha P,Hetal D,et al.Formulation and evalution of irbesartan liquisolid tablets[J].Int J Pharm Sci Reυ Res,2011,9(2):32-37.
[3] Patel V P,Patel N M.Dissolution enhancement of glipizide using liquisolid tablet technology[J].Indian Drugs,2008,45(4):318-323.
[4] 赵许杰,闫雪生,徐新刚,等.液固压缩技术速释α-细辛脑的机制探讨[J].中国实验方剂学杂志,2013,32(11):641-643.
[5] 赵许杰,闫雪生,徐新刚,等.液固压缩技术在熊果酸制剂工艺中的应用探讨[J].中成药,2013,35(10):2141-2143.
[6] 方士英,吴 虹,徐茂红,等.葛根黄酮对心脑血管系统作用及临床应用的研究进展[J].医学前沿,2011(23):193-194.
[7] 周 臻.葛根素分散片的处方筛选及其溶出度测定[J].广东药学院学报,2011,27(6):1-2.
[8] Kavitha K,Kotha L,Raju N S,Ganesh N S,et al.Effect of dissolution rate by liquisolid compact approach:An overview[J].Der Pharmacia Lett,2011,3(1):71-83.
[9] 赵许杰,闫雪生,袁 敏,等.液固压缩技术在水飞蓟素制剂方面的应用[J].药学研究,2013,79(1):262-269.
[10] Nokhodchia A,Aliakbara R,Desaia S,et al.Liquisolid compacts:The effect of cosolvent and HPMC on the ophylline release[J].Biointerfaces,2010,79(1):262-269.
[11] Bindu M B,Kusum B,David B,Novel strategies for poorly water soluble drugs.[J].Int J Pharm Sci ReυRes,2010,4(3):76-84.
[12] Rania F H,Mohammed K A.Enhancement of famotidine dissolution rate through liquisolid tablets formulation:Inυitro and inυiυo evaluation[J].Eur J Pharm Biopharm 2008,69(8):993-1003.
[13] 章 波,冯 怡,徐德生,等.粉体流动性的研究及其在中药制剂中的应用[J].中成药,2008,30(6):904-907.
[14] 国家药典委员会.中华人民共和国药典:2010年版一部[S].北京:中国医药科技出版社,2010:附录XC.
[15] 张嘉家,易荆丽,周毅生,等.葛根总黄酮分散片的处方工艺研究及溶出度测定[J].广东药学院学报,2012,28(6):2-5.
[16] 谢 捷,潘玲燕,朱兴一,等.磷脂和羟丙基—环糊精对葛根素溶解度的影响[J].中成药,2013,35(10):2130-2133.
[17] 崔升淼,赵春顺,何仲贵.葛根黄酮自微乳化软胶囊的制备和溶出度的考察[J].中成药,2007,29(7):993-996.
Liquisolid technique solubilizes the total flavone from Puerariae Radix preparations
LUO Dan, LIXiao-fang*, YU Lin, LUO Li-jia, RAN Mao-lian, LIPin, LIPei-pei
(School of Pharmacy,Chengdu Uniυersity of Traditional Chinese Medicine;Key Laboratory of the Ministry of Education for Standardization of Chinese Herbal Medicine;State Key Laboratory Breeding Base of Systematic Research,Deυelopment and Utilization of Chinese Medicine Resources,Chengdu 611137,China)
liquisolid technique;total flavone from Puerariae Radix;dissolution;differential scanning calorimeter
R944
A
1001-1528(2015)03-0522-04
10.3969/j.issn.1001-1528.2015.03.013
2014-05-24
四川省教育厅重点项目(12ZA042);成都中医药大学科技发展基金(ZRMS201240)
罗 丹(1989—),女,硕士生,研究方向为中药新剂型及新技术。Tel:13438024307,E-mail:929145900@qq.com
李小芳(1964—),女,教授,博士生导师,研究方向为中药新剂型及新技术。Tel:13808195110,E-mail:lixiaofang918 @163.com
