基于氮掺杂三维石墨烯/血红蛋白的丙烯酰胺电化学传感器制备及应用
2015-10-16林春水刘丛丛赵婷婷宋昕鸿
赵 丽, 林春水, 刘丛丛, 赵婷婷, 宋昕鸿, 陈 曦*
(1.厦门华厦学院,福建厦门 361024 2.厦门大学化学化工学院化学系,谱学分析与仪器教育部重点实验室,福建厦门 361005)
丙烯酰胺(AA)是一种强极性有机小分子化合物,它具有神经毒性、遗传毒性及可能的致癌性。AA在高温加热的淀粉类食物中具有较高的含量,且广泛存在于薯条、油条、烧烤等人们食用的食物中[1]。2002年,Stadle等[2]发现热加工食品中存在AA,并对其产生机理和生成条件进行了研究[2]。随后对AA的形成、分布、检测方法等的研究成为热点。目前,关于AA的检测方法已有许多报道,如色谱法[3]、毛细管电泳法[4]、荧光法[5]、酶联免疫分析法[6]及电化学方法[7]等。电化学方法具有分析速度快、操作简便易行、成本低及检测灵敏度高等优点。然而,单纯的裸电极对AA的检测没有选择性,需要借助其他的分离技术对其进行定量[8]。因此,寻找对AA具有特异性选择的电极修饰材料,是实现对AA直接检测的关键。
由生物分子制备的生物电化学传感器在检测小分子方面,具有简单、快速、选择性强等优点。研究发现,血红蛋白(Hb)可与AA发生加成反应[9 - 11]。因此,Hb可作为人体暴露在AA中的生物标记物。由于单一Hb与电极的电子传递能力不强[12],故需要寻找一种生物相容性好且电子传导能力强的材料与之共同修饰电极,以实现Hb与电极表面间良好的导电效果。石墨烯是一种严格的二维晶体材料,具有极高的力学性能和良好的导电性[13 - 15]。三维的还原型氧化石墨烯(3D RGO)是在二维石墨烯基础上发展起来的一类材料,它除了具有二维石墨烯优良的性能,三维立体结构也大大增加了它的比表面积,增强了其富集能力,而且增多了的三维结构使其传递电子的通道增多,增强了其电子传递能力。将有孤对电子的N原子掺杂在三维石墨烯(3D N-RGO)中,又使其导电性进一步增强[16]。
本研究构建了AA检测的电化学传感器,建立了一种AA的电化学检测方法。以3D N-RGO作为玻碳电极(GCE)上电子传递材料,以其疏松多孔、吸附能力强及电子传输通道多等优势,增强了AA与Hb的相互作用,实现对AA的快速检测。
1 实验部分
1.1 仪器与试剂
Biologic电化学工作站(法国);pH 510酸度计(Eutech,Singapore);S-4800扫描电子显微镜(SEM)(日本,日立)。实验采用三电极体系:修饰GCE(Φ=3 mm)为工作电极,Ag/AgCl电极为参比电极,Pt丝为对电极。电解池使用玻璃电解池,在使用前先用铬酸洗液浸泡,再用超纯水冲洗干净。
Hb购于宝生物工程(大连)有限公司;AA(>99.9%)购于Alfa Aesar公司(天津);3D N-RGO(含氮量为0.4%)由本课题组提供[17]。乙醇、HAc、NaAc、NaCl、NaOH、K4[Fe(CN)6]、ZnSO4、正己烷(用时重蒸),均购自国药集团化学试剂有限公司;5%Nafion购自Sigma-Aldrich化学公司(美国)。0.1 mmol/L Hb溶液是将Hb溶于200 mmol/L HAc-NaAc缓冲溶液(pH=4.9)制得,于冰箱4 ℃保存。5 mg/mL 3D N-RGO溶液是将3D N-RGO固体溶于超纯水,使用前超声3 h后使用。Carrez Ⅰ溶液为288 g/L K4[Fe(CN)6] 水溶液,Carrez Ⅱ溶液为577 g/L ZnSO4水溶液,0.5% Nafion溶液由乙醇稀释5% Nafion所得[9]。其它试剂均为分析纯。实验用水为超纯水。
薯片购自本地超市。
1.2 实验步骤
1.2.1Nafion/Hb/3DN-RGO/GCE的制备GCE先用1.0、0.3 μm的Al2O3依次进行抛光,然后用超纯水超声清洗,用N2吹干。电极修饰时每次取4 μL 5 mg/mL 3D N-RGO溶液滴加在GCE表面,室温下放置2 h 成膜后,滴加 4 μL 0.5% Nafion溶液,自然风干成膜。然后滴加 0.1 mmol/L Hb,于4 ℃过夜晾干,再滴加 4 μL 0.5% Nafion溶液4 ℃晾干成膜,以稳定Hb/3D N-RGO膜。修饰电极于4 ℃下保存。
1.2.2样品前处理样品粉粹,60 ℃下烘干。称取5.0 g样品于50 mL离心管中,加入10 mL重蒸正己烷脱脂,震荡,超声10 min后,放置10 min,过滤,再用10 mL正己烷加入到滤渣中,重复上述实验操作。向滤渣中加入10 mL水,超声10 min,离心分离(10 000 r/min,10 min),过滤,再向滤渣中加入10 mL水,重复上述操作,合并两次萃取液。向上述萃取液中依次加入0.5 mL Carrez Ⅰ和Carrez Ⅱ溶液[9],过滤上清液得到样品待测液。
1.2.2电化学测量循环伏安法(CV)和示差脉冲伏安法(DPV)检测电解质组成为:0.05 mol/L NaCl + 200 mmol/L HAc-NaAc缓冲溶液(pH=4.9)。所有的电化学测量采用三电极体系,所有的溶液在使用前均通N2除氧15 min。
CV测量在100 mV/s扫速下,扫描电位-0.6~+0.4 V。DPV检测在相同的电位条件下进行。修饰电极对不同浓度待测物响应情况,由峰电位下所测得的CV和DPV的电流值确定。
2 结果与讨论
2.1 材料表征

图1 3D N-RGO材料的扫描电镜(SEM)图Fig.1 SEM image of 3D N-RGO
实验对3D N-RGO材料进行SEM表征。如图1所示,3D N-RGO材料呈三维网状结构,疏松多孔的微结构,大大增加了材料的比表面积,增强了检测过程中对待测物的物理吸附作用,且为电子传递提供了多种通道。与二维结构相比,三维多空结构也使石墨烯层内部掺杂的N更易于与外部环境进行电子传递,N上的孤对电子增强了Hb与电极的电子传递能力。而AA的C=C结构,可以与RGO形成π-π键,使溶液中的AA有与电极表面靠近的倾向,对AA与Hb的键合起到促进作用[18]。
2.2 Nafion/Hb/3D N-RGO/GCE的循环伏安特性
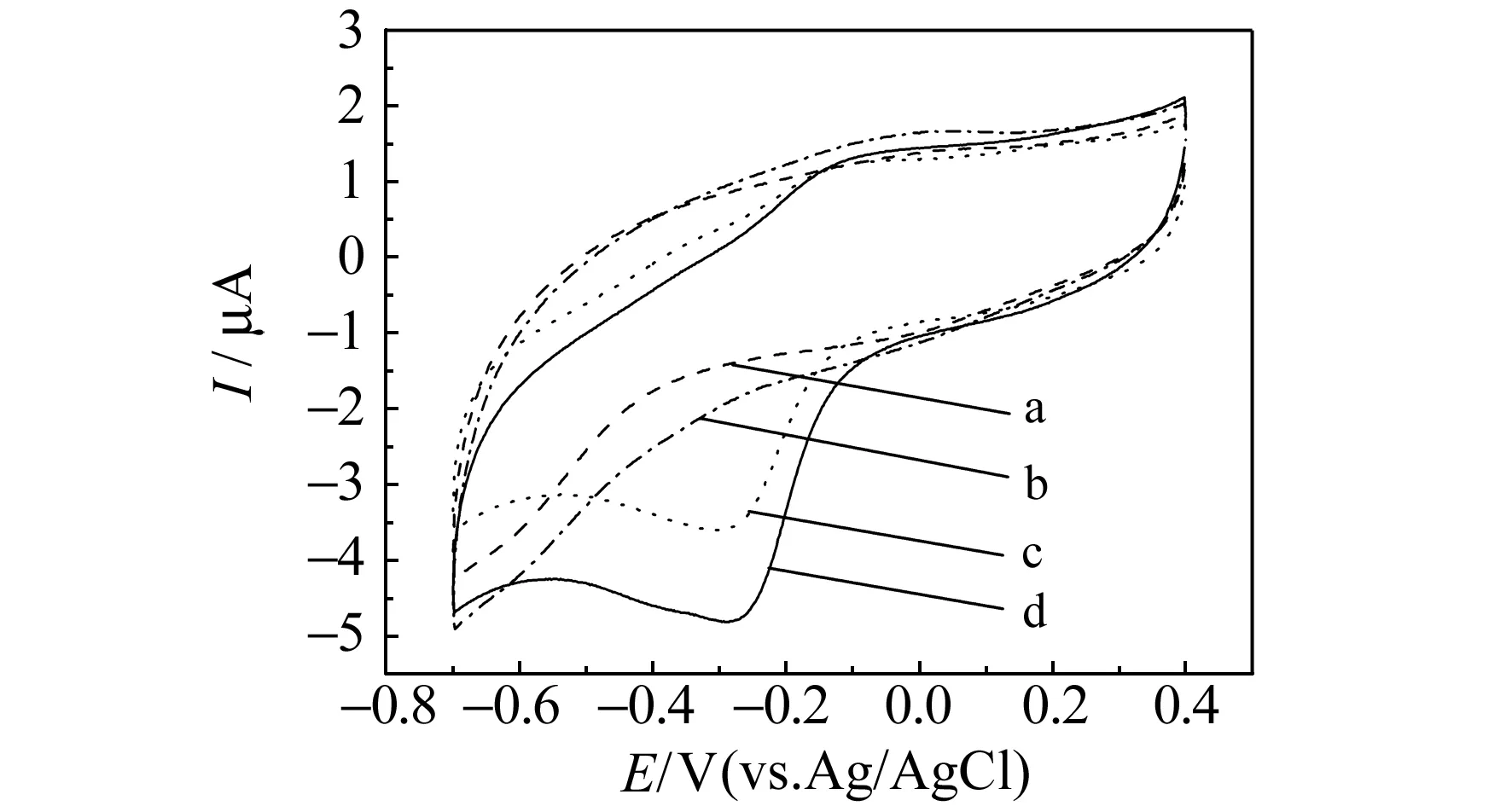
图2 不同修饰电极在电解质溶液中的循环伏安图Fig.2 CVs of different modifiedd electrodes in the electrolytic solution a:Nafion/GCE,b:Nafion/N-RGO/GCE,c:Nafion/Hb/GCE,d:Nafion/Hb/N-RGO/GCE.
电化学测量进行前,将三电极体系放入电解池,加入待测液,通N2除氧15 min,然后进行CV检测。为得到较稳定的曲线,每次扫描6个循环[19]。实验考察了不同材料修饰电极在无AA电解质溶液中的CV响应曲线。如图2曲线a、b所示,在-0.7~+0.4 V电位范围内,Nafion/GCE和Nafion/N-RGO/GCE无明显的电流峰出现,表明Nafion和N-RGO在此测量条件下不能在电极上发生电化学反应。图2曲线c所示,Nafion/Hb/GCE在-0.27 V电位时,出现明显的电流峰,为Hb的还原峰。图2曲线d所示Nafion/Hb/N-RGO/GCE,且N-RGO所具有的三维多空结构,增加了Hb与电极间的电子传递路径[20],而材料中所掺杂的N具有孤对电子,对电子传递也起到促进作用,使得Hb与GCE间电子传递能力增强,增加了Hb的还原峰电流值。结果表明,所使用的3D N-RGO材料对Hb的电子传递能力起到预期的增强效果,可作为电化学生物传感器的修饰材料,增强检测灵敏度。
将Nafion/Hb/N-RGO/GCE置于含有AA的支持电解质的三电极电解槽中,进行电位扫描,直到得到稳定的CV曲线。然后向电解质溶液中通N230 min,静置3 min后再进行电位扫描。如果与通N2前CV曲线一致,则向上述电解质溶液中加入一定量AA,再通N2搅拌15 min,以除去AA溶液中的O2,静置3 min后进行电位扫描,直到得到稳定的CV曲线,一般扫描6个循环。通过对不同浓度AA进行检测,发现修饰电极对不同浓度AA检测灵敏度较低。
2.3 丙烯酰胺的DPV法测定
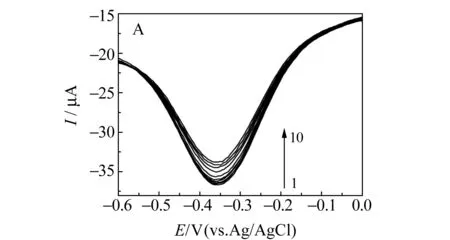
图3 不同浓度AA在Nafion/Hb/N-RGO/GCE上的DPV图Fig.3 DPVs of different concentrations of AA at Nafion/Hb/N-RGO/GCE from 1 to 10:(1)0,(2)1.4×10-12,(3)1.4×10-11,(4)1.4×10-10,(5)1.4×10-9,(6)1.4×10-8,(7)1.4×10-7,(8)1.4×10-6,(9)1.4×10-5,(10)1.4×10-4(mol/L).
实验进而利用DPV法考察Nafion/Hb/N-RGO/GCE对AA的电化学响应。DPV检测方法与上述相同,所测得氧化还原峰电位为-350 mV,对不同浓度AA溶液峰电位值基本稳定,峰电流值随AA浓度增大而逐渐减小(图3),且随着峰电流值的减小,峰电位值向负方向移动:△Ep=△Ep,0-△Ep,10=11±6 mV(三根电极平均值)。这是电化学体系的不可逆性增加引起的,这种不可逆性是由于随着反应的进行,Hb与AA在电极表面反应,生成了不可逆的加成产物。
实验结果表明,AA浓度在1.4×10-12~1.4×10-4mol/L范围内,峰电流强度(Ip)与AA浓度(c)呈现良好的线性关系,线性方程为:Ip=-0.9863c+88.56,相关系数R2=0.9799,最低检出浓度为1.0×10-12mol/L。
为了验证该AA电化学传感器的实用性,运用所制备的Nafion/Hb/N-RGO/GCE,选择常见的薯片作为检测对象,经过脱脂、萃取、除蛋白等前处理过程,得到薯片萃取液,用HAc和NaOH溶液调节pH为4.9,进行DPV检测。结果如表1所示,回收率范围为112.5%~126.0%,证明了所构建传感器可应用于实际样品中AA含量的测定。
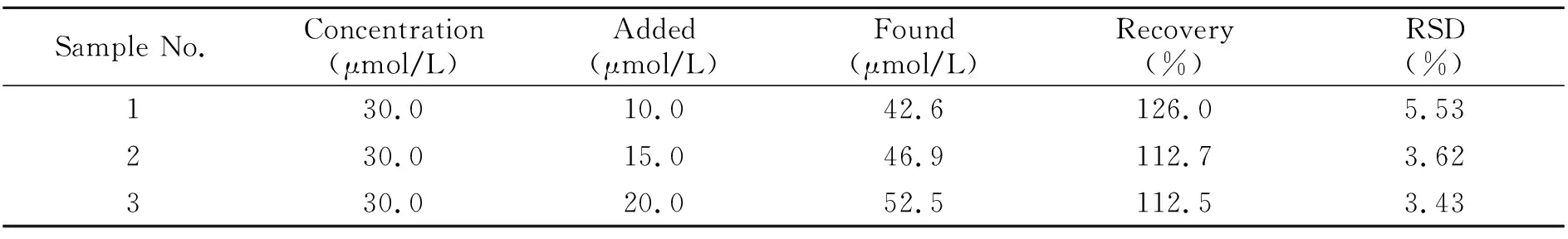
表1 实际样品中丙烯酰胺的检测与回收率(n=3)Table 1 Detection results for acrylamide and recovery of samples(n=3)
3 结论
利用3D N-RGO和Hb修饰玻碳电极,成功构建了一种基于Hb的AA电化学传感器。采用CV法比较了电极在不同材料修饰下的峰电流值,证明了3D N-RGO材料对Hb与电极的电子传递能力有较好的促进作用。利用DPV法成功实现了对不同浓度AA的定量检测,并成功利用该电化学传感器检测薯片中的AA,为AA的电化学检测方法提供了新思路。
