毛细管电泳-电化学发光/电化学检测法同时测定维生素B1和B1
2015-10-16樊子勉
崔 悦, 左 明, 樊子勉, 丁 敏
(重庆医科大学检验医学院,临床检验诊断学教育部重点实验室,重庆 400016)
维生素B1和B6(VB1、VB6)是复合维生素B(VB)片的重要组成成分。复合VB片可用于预防和治疗B族维生素缺乏所致的营养不良、厌食、脚气病、糙皮病等。《卫生部药品标准》采用重量法[1]对VB1进行含量测定,方法繁琐,且并未对VB6的含量进行控制。近年来,有报道用分光光度法[2]对VB1进行测定,用高效液相色谱法[3,4]对复合VB片进行分离检测。但前者所需样品量大且操作较为繁琐;后者的流动相多使用离子对试剂,且色谱仪昂贵,检测成本高。
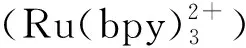
1 实验部分
1.1 仪器与试剂
MPI-B型多参数化学发光分析系统(西安瑞迈分析仪器有限公司);SB-3200D超声波清洗机(宁波新芝生物科技股份有限公司);pHS-2C型精密酸度计(上海精密科学仪器有限公司);CHI-852C电化学分析仪(上海辰华仪器有限公司);Millipore超纯水机(美国,Millipore公司);未涂层的熔融石英毛细管(50 cm×50 μm i.d.,河北永年锐丰色谱器件有限公司)。EC及ECL检测采用三电极系统:工作电极为直径500 μm的铂盘电极,参比电极为Ag/AgCl电极,辅助电极为铂电极。
二氯三联吡啶钌(Ru(bpy)3Cl2·6H2O,99.95%,美国Aldrich公司);维生素B1标准品(瑞士Adamas公司,编号:68429A),维生素B6标准品(美国Aldrich公司,编号:47862)。乙腈(色谱纯,美国 TEDIA公司);NaH2PO4和NaOH为国产分析纯。实验用水为超纯水。
复合维生素B片(福州海王福药制药有限公司,批号:1204050)。
1.2 溶液的配制
1.2.1标准品溶液的配制分别称取一定量维生素B1和B6标准品,用超纯水溶解配制成10.0 mg/mL的储备液,4 ℃下避光保存。
1.2.2供试品溶液的研制取20片复合维生素B片,碾碎并称重,取相当于30 mg维生素B1和2.0 mg维生素B6的重量,用超纯水溶解并定容至10.0 mL,过滤后,于4 ℃下避光保存。
1.3 实验方法
工作电极使用前用0.05 μm的Al2O3粉打磨至表面光滑,检测前在超纯水中对电极施加-0.5~0 V的循环电位,除去电极表面的氧化膜。工作电极与毛细管出口的距离设为80 μm。毛细管第一次使用前用1 mol/L NaOH溶液平衡12 h,每次实验前依次用0.1 mol/L NaOH溶液、超纯水和磷酸盐缓冲溶液(PBS)冲洗10 min。
2 结果与讨论
2.1 水解条件的考察
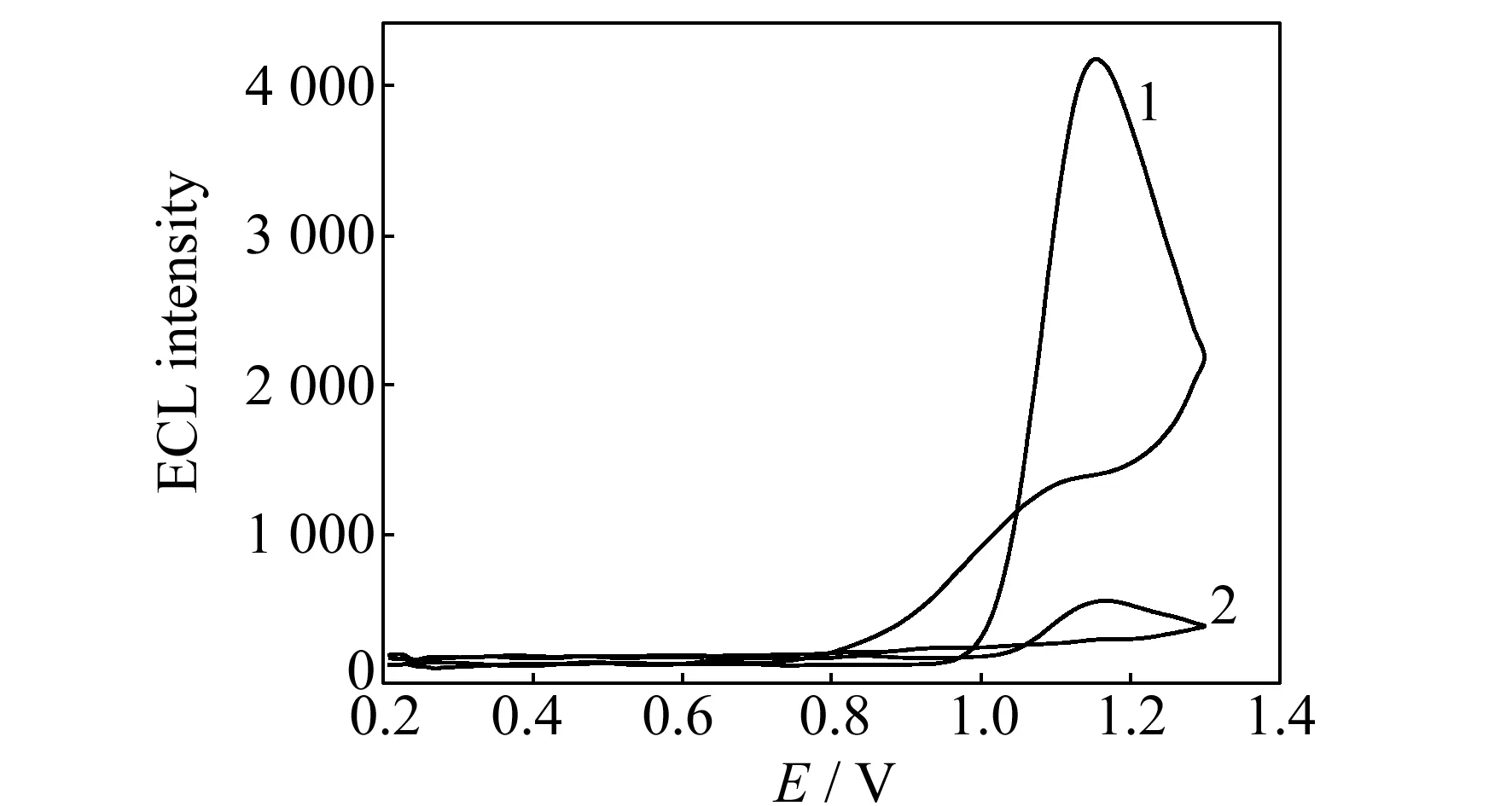
图1 维生素B1水解前后的电化学发光曲线Fig.1 ECL curve of vitamin B1 before and after the hydrolysis 1.after the hydrolysis of vitamin B1(3 mg/mL,pH=10.4);2.before the hydrolysis of vitamin B1(3 mg/mL,pH=5.0).
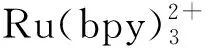
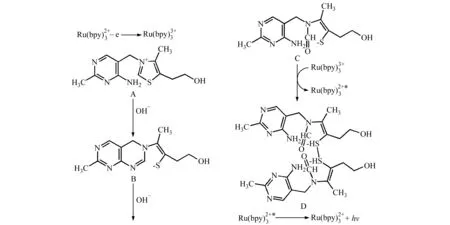
图2 碱性条件下维生素体系电化学发光的可能反应机理Fig.2 The possible principle of ECL of vitamin in alkaline conditions
为了考察碱性环境中水解后的VB1和VB6的稳定性,将VB1和VB6标准溶液与等体积不同pH值的PBS(0.2 mol/L)混合,进行ECL和EC分析,结果见图3。当PBS的pH值在7.5~11.0之间时,随着pH值的升高,VB1的ECL强度持续上升,pH值大于10.2后ECL强度趋于稳定。这表明利用碱性条件对VB1进行水解,pH为10.2时VB1已水解完全。而pH值在8.5~10.5之间,VB6的电流强度(μA)变化不大,表明VB6在此条件下保持稳定。本实验选择pH值10.4的PBS作为介质。
2.2 检测条件的考察
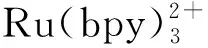
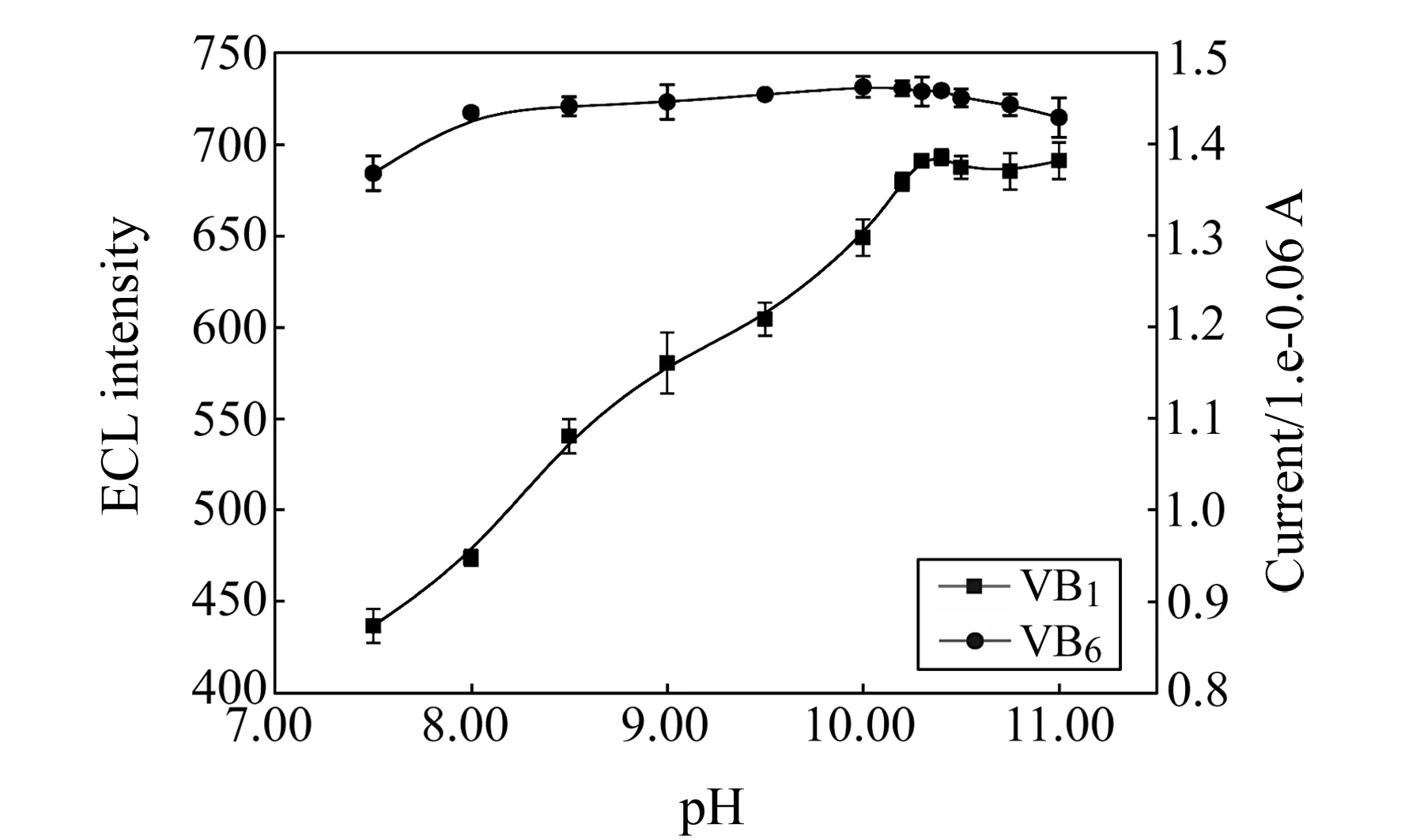
图3 缓冲溶液pH值对水解反应的影响Fig.3 Effect of buffer pH value on hydrolysis reaction Vitamin B1:0.4 mg/mL,using ECL intensity signal;Vitamin B6:0.3 mg/mL,using current signal.
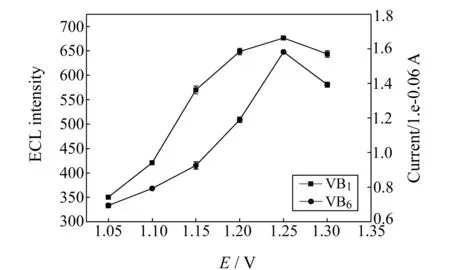
图4 检测电位对信号强度的影响Fig.4 Effect of detection potential on signal intensity Vitamin B1:0.4 mg/mL,using ECL intensity signal;Vitamin B6:0.3 mg/mL,using current signal.
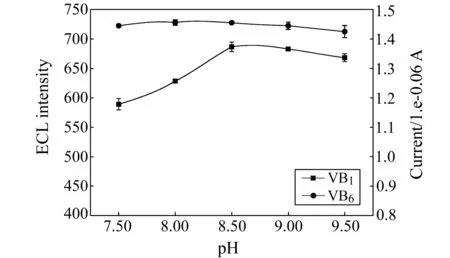
图5 检测池缓冲溶液pH值对信号强度的影响Fig.5 Effect of PBS pH value on signal intensity Vitamin B1:0.4 mg/mL,using ECL intensity signal;Vitamin B6:0.3 mg/mL,using current signal.
2.2.2检测池缓冲溶液pH的考察检测池缓冲溶液pH对物质的EC活性有较大影响,本实验考察了检测池PBS的pH对VB1和VB6信号强度的影响(图5)。PBS的pH在7.5~9.5变化时VB6的EC信号强度基本上不变,而VB1的ECL信号强度在pH为8.5时最大,故选择检测池PBS的pH为8.5。
2.3 CE分离条件的考察
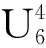
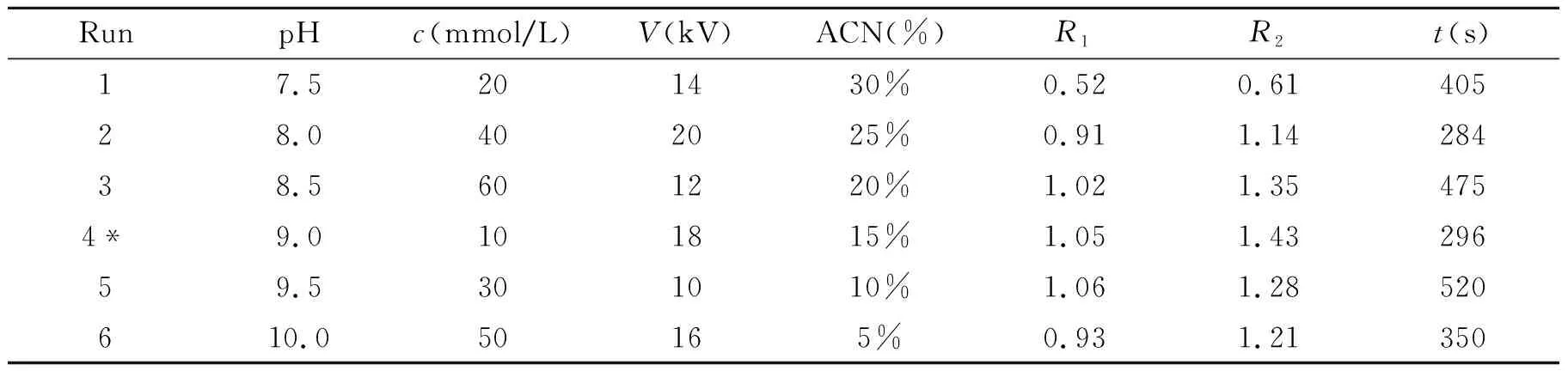
表1 第一次均匀设计及其结果Table 1 The first sequential uniform design and results
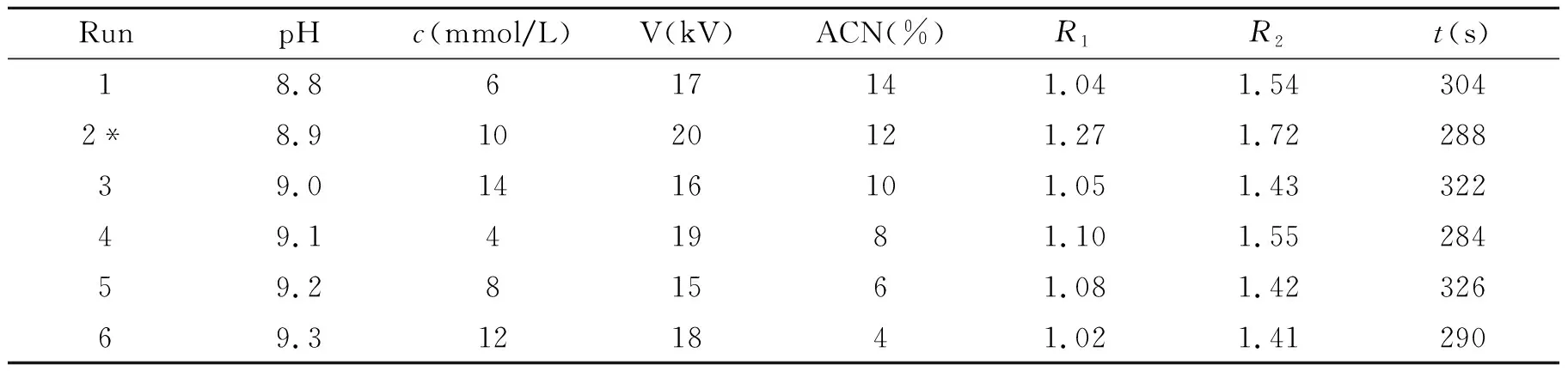
表2 第二次均匀设计及其结果Table 2 The second sequential uniform design and results
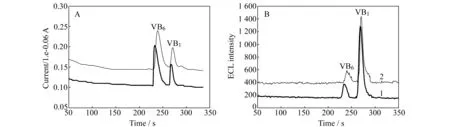
图6 维生素B1和B6的毛细管电泳图Fig.6 Capillary electrophoretograms of VB1 and VB6 solution A:EC detection;B:ECL detection;1:standard solution;2:sample solution.
2.4 标准曲线、线性范围及检测限
在最优实验条件下,测定系列VB1和VB6混合标准溶液,绘制标准曲线。VB1在5.0~5 000.0 μg/mL浓度范围与ECL强度呈线性关系,线性方程为:y=1.36x+184.0(r=0.997),检测限(S/N=3)为2.7 μg/mL;VB6在10.0~1 000.0 μg/mL浓度范围与电流强度呈线性关系,线性方程为:y=5.81×10-3x-0.23(r=0.998),检测限(S/N=3)为6.8 μg/mL。
2.5 回收率与精密度实验
对复合VB片样品溶液(含1.50 mg/mL维生素B1,0.10 mg/mL维生素B6)平行测定6次,VB1与VB6峰高与迁移时间的变异系数分别为1.7%、0.6%和2.3%、1.4%。将高、中、低浓度的VB1和VB6的标准品加入复合VB片样品溶液中,进行回收率实验,结果见表3。
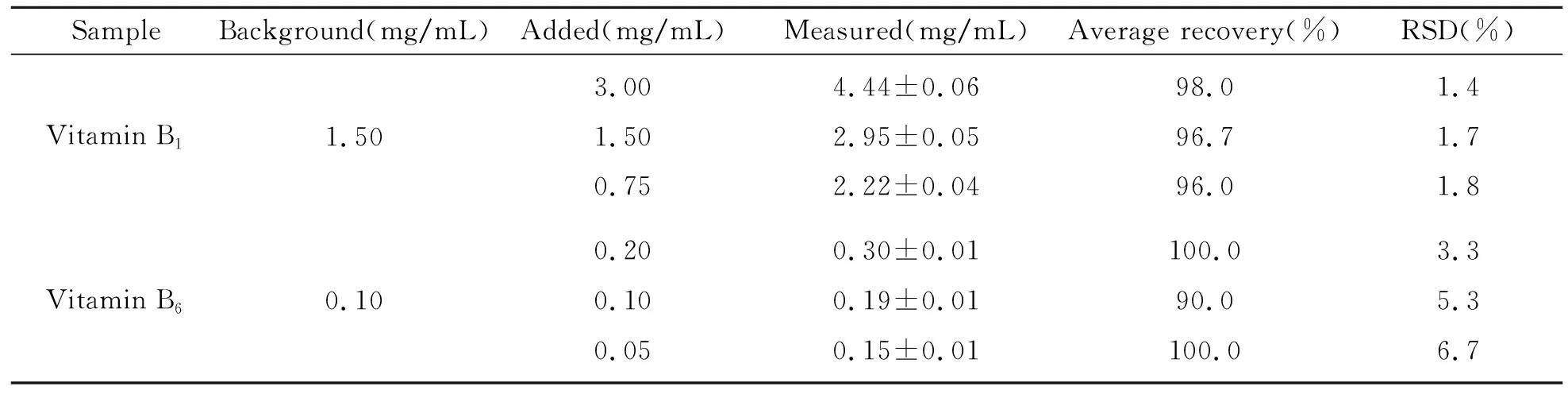
表3 维生素B1和维生素B6的加标回收率(n=3)Table 3 Spiked recoveries of vitamin B1 and B6 in vitamin B complex tables(n=3)
2.6 稳定性试验
将配制好的复合VB片溶液,按测定方法分别在5、15、30、45、60 min进行检测,结果测得VB1与VB6信号强度的RSD分别为1.38%和1.23%,表明碱性条件下复合VB片溶液在1 h内稳定。
2.7 样品测定
对复合VB片中VB1与VB6的含量进行测定,平行测定5次,结果分别为2.8±0.2 mg/tablet和0.20±0.01 mg/tablet,分别为标示量的93.0%和100.0%,符合药品质量检测的要求。
3 结论
本实验建立了CE-ECL/EC同时检测VB1和VB6的新方法。所建立方法具有快速、灵敏、准确、精密度高等特点,可用于复合VB片中VB1和VB6的含量分析,具有较好的应用前景。
