咖啡因分子印迹聚合物微球的制备及其吸附性能研究
2015-10-13蔡小玉李兆峰
董 雁,蔡小玉,李兆峰
咖啡因分子印迹聚合物微球的制备及其吸附性能研究
*董 雁,蔡小玉,李兆峰
(龙岩学院化学与材料学院,福建,龙岩 364012)
在水相中,将模板分子咖啡因、功能单体丙烯酰胺(MA)及乙二醇二甲基丙烯酸酯(EGDMA)采用悬浮聚合法合成咖啡因分子印迹聚合物(MIP),并对印迹聚合物微球进行吸附性能实验、吸附动力学实验、电镜和红外光谱的表征。结果表明:制备的印迹聚合物微球粒径均一,形貌较好,对咖啡因有较好的特异性选择吸附,吸附量为1009.5 μg/g,分离因子为2.37。
咖啡因;印迹聚合物微球;悬浮聚合
分子印迹聚合物(Molecularly Imprinted Polymer,MIP)是利用分子印迹技术,制备对模板分子有特异识别性的高分子聚合物,其原理是将模板分子与交联剂在功能单体溶液中进行聚合而得到模板分子、功能单体复合物,通过洗脱模板分子,在聚合物中留下与模板分子相匹配的“孔穴”,洗脱后的聚合物对模板分子具有选择吸附性。自德国的 Wulff 小组[1]提出分子印迹技术和分子印迹聚合物(MIPs)的概念后,分子印迹技术飞速发展,已被广泛应用于材料科学、传感器检测部件[2]、分离[3]、催化等领域,成为当今研究热点之一。
咖啡因是一种黄嘌呤生物碱化合物,具有兴奋中枢神经的作用,含咖啡因成分的咖啡、能量饮料及软饮料十分畅销,因此,咖啡因也是世界上最广泛使用的精神药品。如果长期摄取大剂量的咖啡因会使人成瘾,对人体造成损害,各国对咖啡因的使用都有严格的规定,因此,对咖啡因含量快速高效检测具有重要意义。制备咖啡因及其类似结构印迹微球聚合物已经有报道[4-7],大多采用的为沉淀聚合法。印迹聚合物微球制备的主要方法有:悬浮聚合法、多步溶胀聚合法、沉淀聚合法和乳液聚合法,不同的制备方法各有优缺点。悬浮聚合法是制备印迹聚合物微球的最简单且最常用的方法之一[8]。
本研究采用悬浮聚合法,以聚乙烯醇(PVA)作为分散剂,在水环境中制备对咖啡因具有识别功能的印迹聚合物微球,研究其结构及吸附性能,因而对从复杂环境检测咖啡因及富集高纯度的咖啡因具有重要意义。
1 实验
1.1 主要仪器和试剂
11.1 仪器
TU-1901双光束紫外可见分光光度计(北京普析通用仪器有限责任公司); S-3400N钨灯丝扫描电子显微镜(日本日立公司);IS10傅立叶红外光谱仪(Thermo Fisher Scientific)
1.1.2 试剂
咖啡因(CP);聚乙烯醇(AR,PVA);乙二醇二甲基丙烯酸酯(AR,EDGMA);偶氮二异丁腈(AR,AIBN);丙烯酰胺(AR,MA);三氯甲烷(AR)。
1.2 实验方法
1.2.1 印迹聚合物微球的制备
咖啡因分子印迹聚合物微球的制备:称取4.0 g的聚乙烯醇(PVA),在90~95 ℃的温度下将PVA溶解到150 mL蒸馏水中,倒入150 mL三口烧瓶中冷却至室温后加入咖啡因(2 mmol,先溶解在12 mL的三氯甲烷中)、功能单体(8 mmol)、交联剂乙二醇二甲基丙烯酸酯(EDGMA,40 mmol)、引发剂偶氮二异丁腈(AIBN,0.1 g),然后在25 ℃下超声脱气30 min,在氮气保护下60 ℃搅拌反应24 h,所得印迹聚合物微球(MIP)用蒸馏水洗涤至紫外可见分光光度计检测不出模板分子为止,将所得微球抽滤干燥保存备用。空白印迹聚合物(NIP)的制备除了不加咖啡因分子,其余步骤同上。
1.2.2 印迹聚合物微球的吸附性能的测定
分别配置浓度为0.1、0.2、0.3、0.4、0.5 g/L的咖啡因标准水溶液,取各浓度的标准水溶液25 mL用紫外可见分光光度计在272 nm下测定标准水溶液的吸光度值,以吸光度值对咖啡因标准水溶液制作线性回归图如图1所示,得到线性方程y = –0.0786 + 60.980x,相关系数= 0.99979。
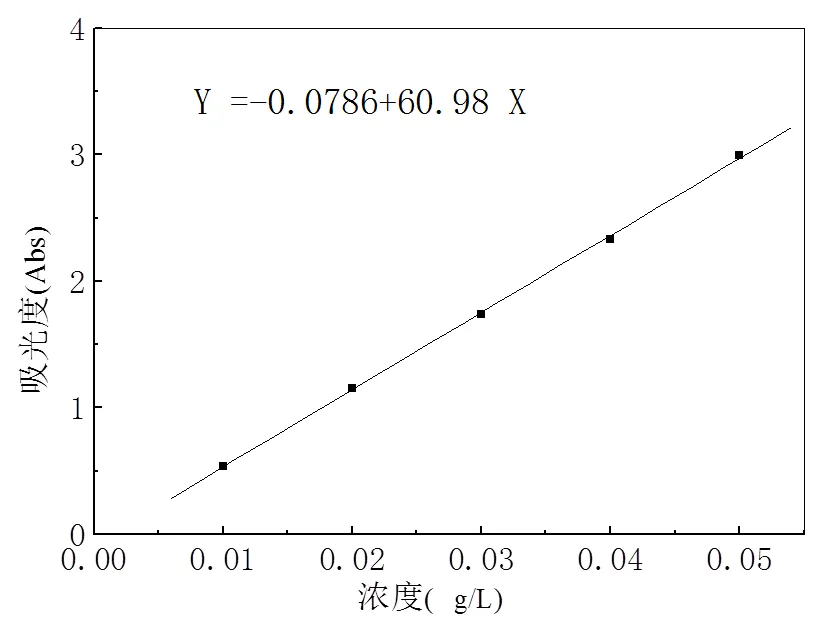
图1 咖啡因水溶液标准曲线
静态吸附法:称取若干份0.1 g的印迹聚合物微球MIP,分别放入到不同的锥形瓶中,分别加入25 mL不同浓度的咖啡因标准水溶液,于室温下振荡24 h,离心分离后,取上层清液于272 nm处测定其吸光度,利用咖啡因标准水溶液曲线计算水溶液中咖啡因浓度变化,得到印迹微球对不同浓度咖啡因的吸附量Q。
Q =(C0-C)V0/m (1)
式中:C0为咖啡因标准水溶液的初始浓度,μg/L;C为吸附后母液中咖啡因的浓度,μg/L;V0为咖啡因标准水溶液的体积,L;m为聚合物的质量,g。
1.2.3 印迹聚合物吸附速率测定
取若干份5.0 mL标准溶液,分别加入0.1 g聚合物后封口,每4 h测一份,计算相对吸附量,平行测定3次取平均值。
1.2.4 印迹聚合物微球的红外分析
取少量干燥的聚合物微球与干燥的KBr放入研钵中混合研细,在压片机上压制成圆形薄层样品,用IS10傅立叶红外光谱仪进行红外测量,测量范围4000~400 cm-1。
1.2.5 印迹聚合物微球的扫描电镜分析
将干燥的微球样品粘贴在双面胶上,真空中用离子溅射器对微球样品进行喷金,然后用S-3400 N扫描电子显微镜观察聚合物微球的形貌。
2 结果与讨论
2.1 MIP与NIP的吸附量
以MA为功能单体,在60 ℃下聚合反应所制得的微球的产量与吸附量如表1所示。

表1 印迹聚合物微球的产量及其吸附量
由表1可知,从聚合物产量考虑:以MA为功能单体时,NIP与MIP的产量差别不大,但是从吸附量的看出,MIP的对咖啡因的吸附量远高于NIP的吸附量,分离因子为2.37,这是因为MA与咖啡因分子发生反应,洗脱后留下与咖啡因分子空间构型相匹配的“孔穴”,有利于吸附咖啡因及其类似结构的物质,而NIP对咖啡因也一定的吸附作用,这可能是部分位于聚合物表面的单体与咖啡因产生了氢键作用的结果,属于非特异性吸附。
2.2 吸附性能的研究
测定聚合物微球对不同浓度的咖啡因标准水溶液的吸附量,即结合等温线,并针对不同功能单体制得的聚合物微球分别测定吸附量,不同功能单体制得的MIP和NIP对咖啡因分子的结合等温线如图2所示。

图2 聚合物微球的吸附等温线
由图2可知,随着咖啡因标准液浓度的增加,MIP与NIP对咖啡因的吸附量都在增加,在相同浓度下,MIP的吸附量远大于NIP,达到吸附平衡后,MIP的吸附量是NIP的2.4倍。这表明在印迹过程中MA与模板分子发生反应,MIP洗脱后,微球上留下与咖啡因分子空间构型相匹配的“孔穴”,产生特异性吸附。
2.3 吸附速率的研究
测定制得的MIP对一定浓度的咖啡因标准水溶液中吸附量随时间的变化曲线,如图3所示。
由图3可知,在吸附开始的阶段,吸附速率比较快,这一阶段是比较表面的浅空穴起了主要作用,当这些浅空穴吸附饱和后,便是MIP的深孔起主要的吸附作用,这对咖啡因的吸附有一定的位阻,使结合率下降,吸附速率降低,在24 h时基本上完成选择性吸附。
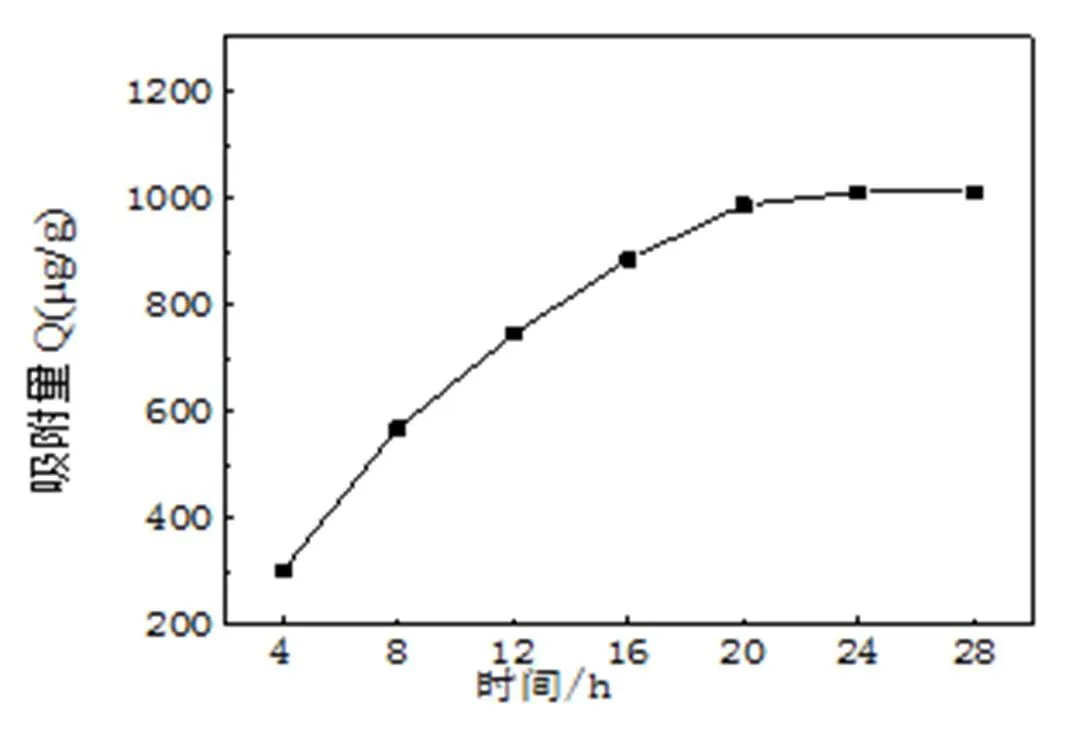
图3 印迹聚合物微球的吸附速率
2.4 印迹微球电镜扫描

图4 NIP(a)与MIP(b)的电镜扫描图
由图4可知,NIP与MIP的均呈现出大小均一的球形,MIP的微球粒径要略大于NIP的粒径,这是可能是聚合时,在模板分子周围形成了高度交联刚性聚合物,从而确保模板分子洗脱后所留下的“空穴”的形状和大小保持不变,导致了MIP的粒径略大[9]。
2.5 红外光谱测量分析
咖啡因印迹聚合物微球和空白聚合物微球,制得样品后进行红外光谱扫描,结果如图5所示。
由图5可知,两者都具有明显氨基、羰基的特征吸收峰,且峰形基本一致,但MIP的中没有出现咖啡因的特征吸收峰,表明咖啡因已洗脱干净。NIP:在3460.48 cm-1处是N-H伸缩振动峰,位于2997.60 cm-1是空白聚合物骨架上的C-H伸缩振动峰,1725.74 cm-1处则是C=O的伸缩振动峰,出现在1371.64 cm-1的是C-H弯曲振动峰。MIP:N-H的伸缩振动峰出现在3453.94 cm-1处,C-H的吸收峰为2991.08 cm-1(略有红移),这可能是因为模板分子与功能单体的氢键作用使电子云密度平均化的结果。C=O的特征吸收峰出现在1729.91cm-1处。MIP的各特征吸收峰的峰形较NIP更为尖锐,可能是咖啡因分子的酰胺基与氨基与MA中的氨基在聚合时通过氢键发生作用,MIP洗脱后,在其上留有“空穴”,使MIP的微环境可能保持了一种与咖啡因分子相匹配的特殊电子态势,能够产生特异性吸附[10]。
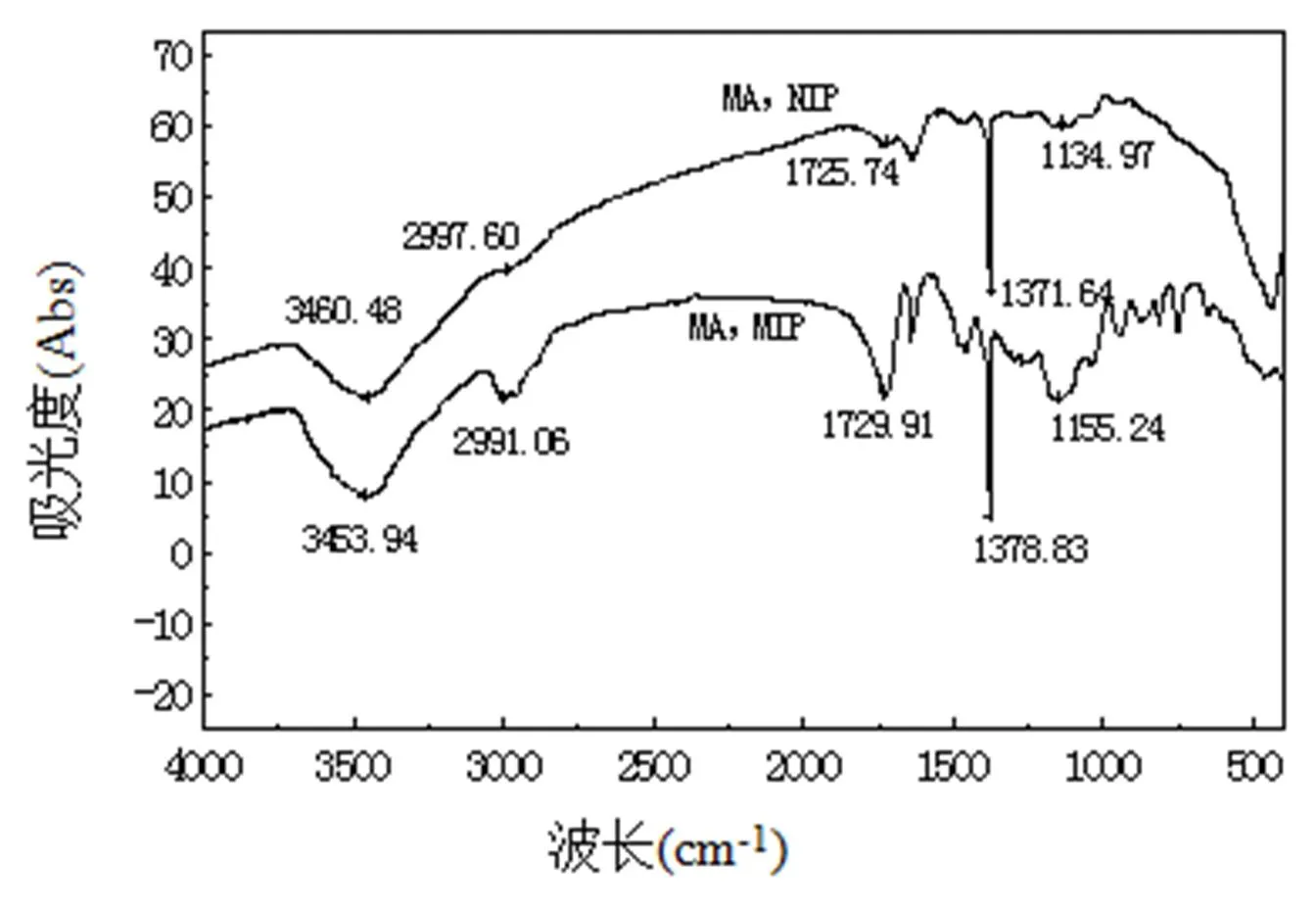
图5 NIP与MIP的红外光谱图
2.6 MIP的Scatchard分析
通过采用静态吸附法,在0~5.0 mmol·L-1测定咖啡因的等温吸附曲线,结果见图6。将图中的结合数据用Scatchard分析来评价聚合物的结合特性[11]。Scatchard方程为:
Q/C = (Qmax-Q)/Kd(2)
式中,Kd(mmol/L)是结合位点的平衡离解常数;Qmax(μmol·g-1)是结合位点的最大表观结合量;C(咖啡因,μmol·L-1)表示聚合物达到平衡时上清液中的平衡浓度。以Q/C对Q作图,得到MIP的Scatchard图(图7),由图7可知Q/C对Q呈现非线性关系,这说明MIP对咖啡因的结合位点是非均一的。
图7中的吸附量Q分别在0~3.4423 µmol·g-1和在3.4423~5.1900 μmol·g-1这两个范围内分别与Q/C呈线性关系,进行线性拟合,可得到两个拟合线性回归方程:y = 15.7322-3.98832x(= 0.9955);y = 5.50648-0.84243x(= 0.9899)。由线性回归方程的斜率k和截距可以计算出高亲和位点的离解常数为Kd1= 0.2507 mmol/L,最大表观结合量Qmax1=3.9446 μmol/g;低亲和位点的离解常数Kd2=1.1870 mmol/L,最大表观结合量Qmax2=6.5364 μmol/g。这表明在0~5.0 mmol·L-1范围内,印迹聚合物微球MIP对咖啡因存在有两类不等价的结合位点,具有非均一性[12],表明咖啡因分子印迹聚合物微球对咖啡因具有良好的再结合能力。可能是由于咖啡因结构中存在着酰胺基和氨基这两种不同类型的功能基,均能与功能单体MA中的氨基反应,可以形成两种不同的复合物,经聚合后形成两种具有不同性质的作用位点[10]。
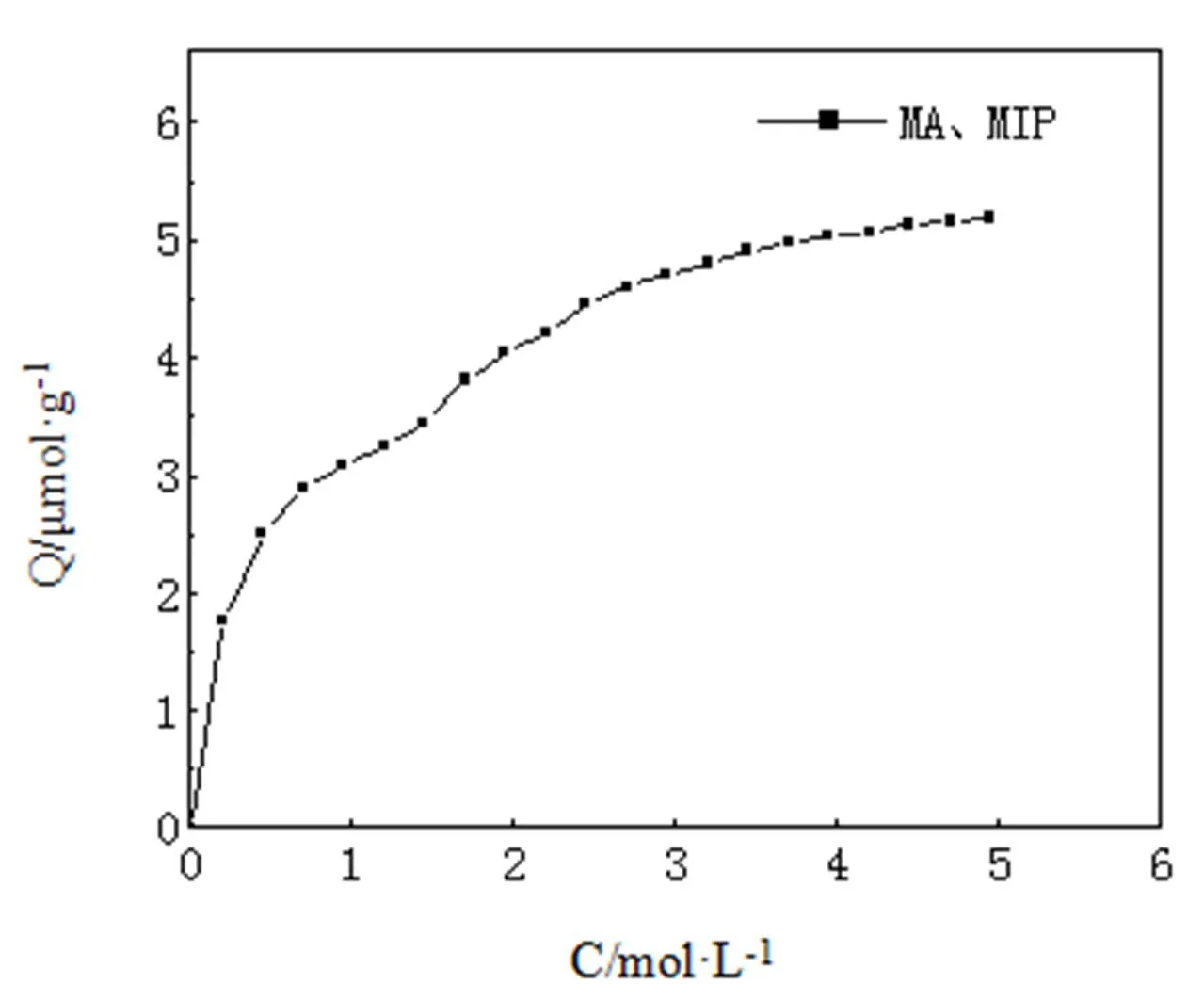
图6 MIP的结合等温线
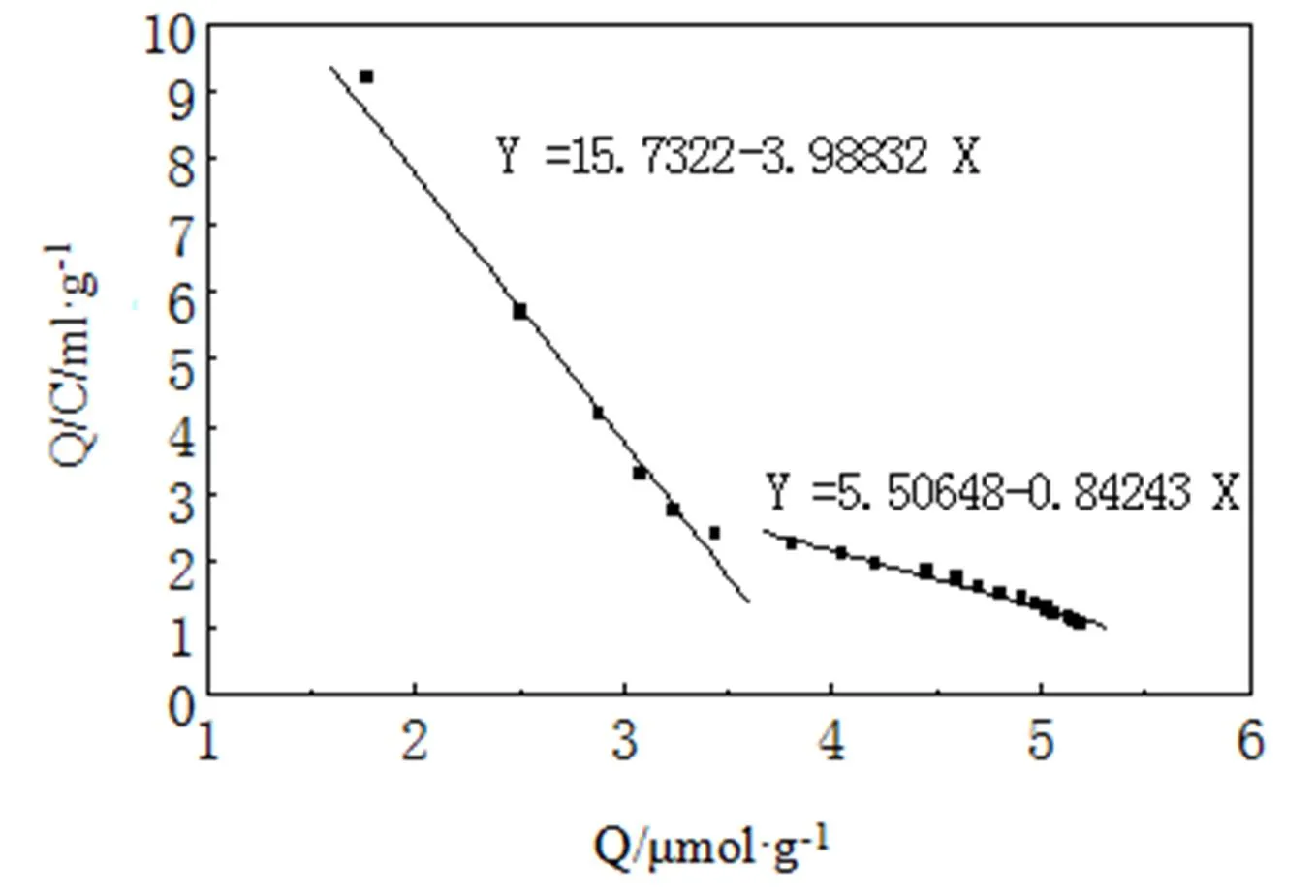
图7 印迹聚合物的Scatchard曲线
3 结论
本实验在水溶液中,采用经典配方即模板分子:功能单体:交联剂 = 1 : 4 : 20,用悬浮聚合法制备咖啡因分子印迹聚合物微球,所得的印迹聚合物微球形貌较好,粒径略大于非印迹聚合物,由傅里叶红外图谱及Scatchard分析可知,咖啡因分子与功能单体之间存在两种结合方式,可以形成两种不同的复合物。制备的印迹聚合物对咖啡因的最大吸附量为1009.5 μg/g,非印迹聚合物的吸附量为425.3 μg/g,分离因子为2.37,说明印迹微球对咖啡因有较好的选择吸附性,这种吸附属于特异性吸附,吸附大约在24 h后达到平衡。本实验为在复杂体系中咖啡因的识别、分离和提取提供了一定的研究基础。
参考文献:
[1] Wulff G, Sarhan A, Zabrocki K. Enzyme-analogue built polymers and their use for the resolution of racemates[J]. Tetrahedron Letters, 1973, 14(44): 4329-4332.
[2] Guan G, Liu B, Wang Z, et al. Imprinting of molecular recognition sites on nanostructures and its applications in chemosensors[J]. Sensors, 2008, 8(12): 8291-8320.
[3] Ye L, Haupt K. Molecularly imprinted polymers as antibody and receptor mimics for assays, sensors and drug discovery[J]. Analytical and bioanalytical chemistry, 2004, 378(8): 1887-1897.
[4] Kempe M, Mosbach K. Separation of amino acids, peptides and proteins on molecularly imprinted stationary phases[J]. Journal of Chromatography A, 1995, 691(1): 317-323.
[5] 蒋旭红,吴嫦秋,刘展眉.茶碱分子印迹聚合物微球的合成及其性能研究[J].中草药,2013,44(15): 2055-2058.
[6] 苏博,宫建龙,罗来盛,等.双酚A分子印迹聚合物的制备及其在水相中的吸附性能[J].化工环保,2011,31(2): 167-171.
[7] 姚伟,高志贤,房彦军,等.沉淀聚合法制备咖啡因分子印迹聚合物微球[J].化工进展,2007,26(6): 869-872,877.
[8] 姜忠义,吴洪.分子印迹技术[M].北京:化学工业出版社,2003.
[9] 文峰球,潘浪胜.领苯二甲酸二丁酯分子印迹聚合物的制备及性能研究[J].应用化工,2013,42(8): 1451-1453.
[10] 董雁,何立芳,章汝平,等.咖啡因分子印迹聚合物微球的沉淀聚合法制备及其性能研究[J].泉州师范学院学报,2014,32(6):49-54.
[11] 杨卫海,严守雷,卫晨,等.沉淀聚合法制备三聚氰胺分子印迹聚合物微球[J].高分子学报,2010(10):1163-1169.
[12] 苏立强,陈超男,韩爽,等.乙酰水杨酸分子印迹聚合物微球的制备及性能研究[J].化学试剂,2014,36(1):18-22.
SYNTHESIS AND ADSORPTION PROPERTIES OF CAFFEINE MOLECULARLY IMPRINTED POLYMER MICROSPHERES
*DONG Yan, CAI Xiao-yu, LI Zhao-feng
(College of Chemistry and Materials Science, Longyan University, Longyan, Fujian 364012, China)
Molecularly imprinted polymers (MIP) were prepared by suspension polymerization in water utilizing caffeineas imprinted molecules, acrylamide(AM)as functional monomer and ethylene glycol dimethacrylate (EGDMA) as crosslinker. Imprinted polymers were characterized by adsorption properties tests, sorption kinetics tests, FT-IR spectra and SEM images. The results showed that adsorptive capacity of imprinted polymer on caffeine was 1009.5 μg/g, and separation factor was 2.37. In conclusion, micro-spheres with uniform size and preferred shapehave selective adsorption of caffeine with good specificity.
caffeine; imprinted polymer microspheres; suspension polymerization
1674-8085(2015)06-0041-05
TQ317
A
10.3969/j.issn.1674-8085.2015.06.009
2015-06-06;修改日期:2015-08-20
福建省大学生创新创业训练计划项目(201511312051);龙岩学院“百名青年教师攀登项目”(LQ2013020)
*董 雁(1982-),女,福建长汀人,讲师,硕士,主要从事功能高分子材料研究(E-mail:dyfz0591@126.com);
蔡小玉(1994-),女,福建漳州人,龙岩学院化学与材料学院化学教育专业2013级本科生(E-mail:1298424606@qq.com);
李兆峰(1991-),女,福建上杭人,龙岩学院化学与材料学院材料科学与工程专业2011级本科生(E-mail:2274140160@qq.com).
